名校
1 . 海水是巨大的资源宝库,以下是人类从海水中提取某些重要化工原料的简单流程示意图。下列说法错误的是
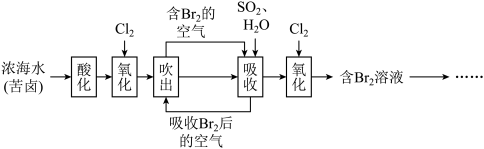
| A.“吹出”时,常采用热空气吹出溴,利用了溴单质的易挥发性 |
B.用 水溶液吸收 水溶液吸收 的离子方程式为 的离子方程式为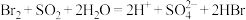 |
| C.流程中氧化→吸收→氧化的目的是富集溴单质 |
D.工业上也可用 溶液代替二氧化硫吸收 溶液代替二氧化硫吸收 ,会生成无色无味气体和 ,会生成无色无味气体和 ,则反应的化学方程式为 ,则反应的化学方程式为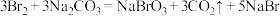 |
您最近一年使用:0次
2024-06-17更新
|
66次组卷
|
2卷引用:河南省名校联盟2023-2024学年高一下学期5月联考化学试题
名校
2 . 如图所示装置制备亚氯酸钠( )(已知:
)(已知: 与
与 在酸性条件下反应生成
在酸性条件下反应生成 )。回答下列问题。
)。回答下列问题。___________ 。
(2)写出A中的化学反应方程式___________ 。
(3)B中离子反应离子方程式为___________ 。
(4)某学习小组设计了如图所示装置来验证二氧化硫的化学性质。
方案I;向第一份溶液中加入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
方案II:向第二份溶液中加入品红溶液,红色褪去。
方案III:向第三份溶液中加入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
上述方案合理的是___________ (填“I”“II”或“III”);试管b中发生的离子方程式为___________ 。
②将气体X和 同时通入盛有
同时通入盛有 溶液的洗气瓶中,下列气体可能产生白色沉淀的是
溶液的洗气瓶中,下列气体可能产生白色沉淀的是___________ (填序号)。
① ②
② ③
③ ④
④
 )(已知:
)(已知: 与
与 在酸性条件下反应生成
在酸性条件下反应生成 )。回答下列问题。
)。回答下列问题。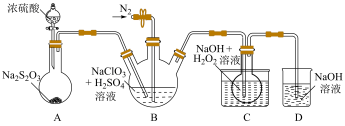
(2)写出A中的化学反应方程式
(3)B中离子反应离子方程式为
(4)某学习小组设计了如图所示装置来验证二氧化硫的化学性质。
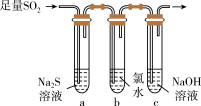
方案I;向第一份溶液中加入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。方案II:向第二份溶液中加入品红溶液,红色褪去。
方案III:向第三份溶液中加入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。上述方案合理的是
②将气体X和
 同时通入盛有
同时通入盛有 溶液的洗气瓶中,下列气体可能产生白色沉淀的是
溶液的洗气瓶中,下列气体可能产生白色沉淀的是①
 ②
② ③
③ ④
④
您最近一年使用:0次
名校
3 .  既是一种重要的能源,也是一种重要的化工原料。
既是一种重要的能源,也是一种重要的化工原料。
(1)已知8.0g 完全燃烧生成液体水放出444.8kJ热量。则
完全燃烧生成液体水放出444.8kJ热量。则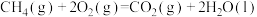 △H=
△H=___________  。若8.0g
。若8.0g 完全燃烧生成气态水,则放出的热量
完全燃烧生成气态水,则放出的热量___________ 444.8kJ。(填“>”、“<”或“=”)
(2)以 为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为
为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为___________ ,通入b气体的电极反应式为___________ 。(质子交换膜只允许 通过)
通过) 与
与 可直接转化成乙酸,这是实现“减排”的一种研究方向。
可直接转化成乙酸,这是实现“减排”的一种研究方向。
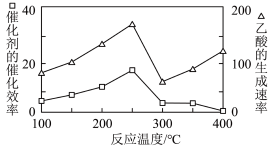
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在___________ 左右。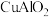 ,难溶物),其中铜元素化合价为
,难溶物),其中铜元素化合价为___________ 。将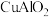 溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为
溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为___________ 。
(4) 还原法是处理
还原法是处理 气体的一种方法。已知一定条件下
气体的一种方法。已知一定条件下 与
与 反应转化为
反应转化为 和
和 ,若标准状况下8.96L
,若标准状况下8.96L 可处理22.4L
可处理22.4L ,则x值为
,则x值为___________ 。
 既是一种重要的能源,也是一种重要的化工原料。
既是一种重要的能源,也是一种重要的化工原料。(1)已知8.0g
 完全燃烧生成液体水放出444.8kJ热量。则
完全燃烧生成液体水放出444.8kJ热量。则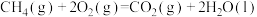 △H=
△H= 。若8.0g
。若8.0g 完全燃烧生成气态水,则放出的热量
完全燃烧生成气态水,则放出的热量(2)以
 为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为
为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为 通过)
通过)
 与
与 可直接转化成乙酸,这是实现“减排”的一种研究方向。
可直接转化成乙酸,这是实现“减排”的一种研究方向。①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在
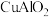 ,难溶物),其中铜元素化合价为
,难溶物),其中铜元素化合价为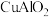 溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为
溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为(4)
 还原法是处理
还原法是处理 气体的一种方法。已知一定条件下
气体的一种方法。已知一定条件下 与
与 反应转化为
反应转化为 和
和 ,若标准状况下8.96L
,若标准状况下8.96L 可处理22.4L
可处理22.4L ,则x值为
,则x值为
您最近一年使用:0次
名校
4 . FeOOH在生产生活中有广泛应用。
I.用硫酸渣(主要成分为 、
、 )制备铁基颜料铁黄(FeOOH)的一种工艺流程如下图。
)制备铁基颜料铁黄(FeOOH)的一种工艺流程如下图。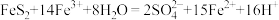 ;
; 、
、 均与
均与 不反应。
不反应。
(1)基态 价层电子排布式为
价层电子排布式为___________ 。
(2)“还原”时还原产物与氧化产物的物质的量之比为___________ 。
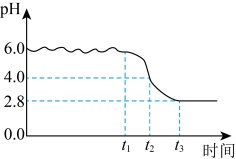
(3)“氧化”时,当滴加氨水至pH为6.0时,停止滴加氨水,开始通空气,生成铁黄。通入空气过程中,记录溶液pH变化如图所示。 完全沉淀的
完全沉淀的 。
。 时段发生的反应为
时段发生的反应为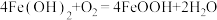 ;
; 时段,溶液pH明显降低,请解释原因:
时段,溶液pH明显降低,请解释原因:___________ 。
II. 在环境保护等领域有广泛应用。
在环境保护等领域有广泛应用。
(4)在80℃下,向 溶液中边搅拌边分批加入
溶液中边搅拌边分批加入 固体,同时滴加
固体,同时滴加 溶液,使溶液pH控制在4~4.5之间。一段时间后,过滤、洗涤得
溶液,使溶液pH控制在4~4.5之间。一段时间后,过滤、洗涤得 固体。
固体。
①制备1mol 理论上需要
理论上需要 的物质的量为
的物质的量为___________ mol;实际生产过程中所加 低于理论用量的原因是
低于理论用量的原因是___________ 。
②为检验 已被完全氧化,某同学向过滤所得滤液中滴加酸性
已被完全氧化,某同学向过滤所得滤液中滴加酸性 溶液,该设计方案不合理的理由是
溶液,该设计方案不合理的理由是___________ 。
(5) 可用于脱除烟气中的
可用于脱除烟气中的 。脱硫、再生过程中可能的物种变化如图1所示。生成的
。脱硫、再生过程中可能的物种变化如图1所示。生成的 结构如图2所示。
结构如图2所示。 分子中的共价键的物质的量为
分子中的共价键的物质的量为___________ mol。
②写出反应II的化学方程式:___________ 。
I.用硫酸渣(主要成分为
 、
、 )制备铁基颜料铁黄(FeOOH)的一种工艺流程如下图。
)制备铁基颜料铁黄(FeOOH)的一种工艺流程如下图。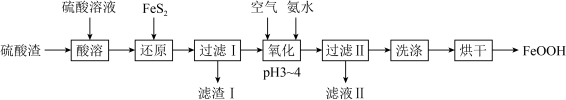
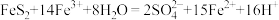 ;
; 、
、 均与
均与 不反应。
不反应。(1)基态
 价层电子排布式为
价层电子排布式为(2)“还原”时还原产物与氧化产物的物质的量之比为
(3)“氧化”时,当滴加氨水至pH为6.0时,停止滴加氨水,开始通空气,生成铁黄。通入空气过程中,记录溶液pH变化如图所示。
 完全沉淀的
完全沉淀的 。
。 时段发生的反应为
时段发生的反应为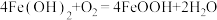 ;
; 时段,溶液pH明显降低,请解释原因:
时段,溶液pH明显降低,请解释原因:II.
 在环境保护等领域有广泛应用。
在环境保护等领域有广泛应用。(4)在80℃下,向
 溶液中边搅拌边分批加入
溶液中边搅拌边分批加入 固体,同时滴加
固体,同时滴加 溶液,使溶液pH控制在4~4.5之间。一段时间后,过滤、洗涤得
溶液,使溶液pH控制在4~4.5之间。一段时间后,过滤、洗涤得 固体。
固体。①制备1mol
 理论上需要
理论上需要 的物质的量为
的物质的量为 低于理论用量的原因是
低于理论用量的原因是②为检验
 已被完全氧化,某同学向过滤所得滤液中滴加酸性
已被完全氧化,某同学向过滤所得滤液中滴加酸性 溶液,该设计方案不合理的理由是
溶液,该设计方案不合理的理由是(5)
 可用于脱除烟气中的
可用于脱除烟气中的 。脱硫、再生过程中可能的物种变化如图1所示。生成的
。脱硫、再生过程中可能的物种变化如图1所示。生成的 结构如图2所示。
结构如图2所示。
 分子中的共价键的物质的量为
分子中的共价键的物质的量为②写出反应II的化学方程式:
您最近一年使用:0次
2024-06-16更新
|
62次组卷
|
2卷引用:江苏省南通市海安高级中学2023-2024学年高一下学期期中考试化学试题
名校
5 . 近几年来关于氮污染的治理倍受关注。
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的 、
、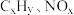 三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。___________ ,X的化学式为___________ 。
②钡元素在周期表中的位置是___________ 。
(2)SCR技术可使 与
与 直接反应,实现无害转化。当
直接反应,实现无害转化。当 与
与 的物质的最之比为2:1时,写出发生反应的化学方程式:
的物质的最之比为2:1时,写出发生反应的化学方程式:___________ 。
(3)利用 氧化氮氧化物反应过程如下:
氧化氮氧化物反应过程如下: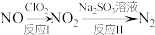 反应I的化学方程式是
反应I的化学方程式是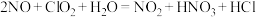 ,反应II的离子方程式是
,反应II的离子方程式是_______________ 。
(4)加入过量次氯酸钠可使废水中 完全转化为
完全转化为 ,而本身被还原为
,而本身被还原为 。检验废水中是否存在
。检验废水中是否存在 的方法是
的方法是___________ 。
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的
 、
、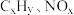 三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。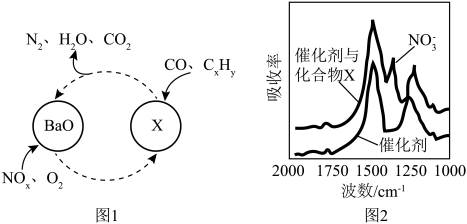
②钡元素在周期表中的位置是
(2)SCR技术可使
 与
与 直接反应,实现无害转化。当
直接反应,实现无害转化。当 与
与 的物质的最之比为2:1时,写出发生反应的化学方程式:
的物质的最之比为2:1时,写出发生反应的化学方程式:(3)利用
 氧化氮氧化物反应过程如下:
氧化氮氧化物反应过程如下: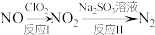 反应I的化学方程式是
反应I的化学方程式是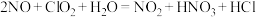 ,反应II的离子方程式是
,反应II的离子方程式是(4)加入过量次氯酸钠可使废水中
 完全转化为
完全转化为 ,而本身被还原为
,而本身被还原为 。检验废水中是否存在
。检验废水中是否存在 的方法是
的方法是
您最近一年使用:0次
名校
6 . 以铝土矿(主要成分为 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如下:
等杂质)为原料制备铝的一种工艺流程如下: 在“碱溶”时转化为铝硅酸钠沉淀
在“碱溶”时转化为铝硅酸钠沉淀
②电解时,阳极发生氧化反应
下列说法正确的是
 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如下:
等杂质)为原料制备铝的一种工艺流程如下: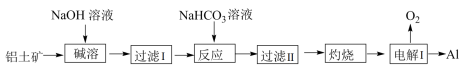
 在“碱溶”时转化为铝硅酸钠沉淀
在“碱溶”时转化为铝硅酸钠沉淀②电解时,阳极发生氧化反应
下列说法正确的是
A.“碱溶”时生成偏铝酸钠的离子方程式为 |
B.“过滤Ⅰ”的滤渣成分为 |
C.“反应”中加入 溶液的作用同于通入 溶液的作用同于通入 |
| D.“电解Ⅰ”中作阳极的石墨易消枆,阳极反应中失电子物质主要是石墨 |
您最近一年使用:0次
名校
7 . 电池在人们的生产生活中起着重要的作用,请回答下列问题:
(1)碱性锌锰电池适合需要大电流供电的设备使用如照相机、野外摄像机、无线电控制的航模与海模、电动工具、电动玩具、收录机等,其结构如图所示,放电时的总反应为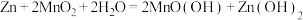 。该电池的正极为
。该电池的正极为 ,其电极反应式为:
,其电极反应式为:___________ 。___________ ;
②写出a电极上发生的电极反应___________ 。
(3)钴酸锂电池的正极采用钴酸锂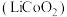 ,负极采用金属锂和碳的复合材料,该电池充放电时的总反应式:
,负极采用金属锂和碳的复合材料,该电池充放电时的总反应式: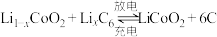 ,写出放电时负极的电极反应
,写出放电时负极的电极反应___________ 。
(4)利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下:
①烧渣是LiCl、 和
和 的混合物,则500℃焙烧反应的氧化产物与还原产物的物质的量之比为
的混合物,则500℃焙烧反应的氧化产物与还原产物的物质的量之比为___________ ;
②“滤饼2”的主要成分是___________ ,常温下, 的溶解度比LiOH
的溶解度比LiOH___________ (填“大”或“小”);
③“850℃煅烧”时的化学方程式为:___________ ;
④在实验室检查滤饼2是否洗涤干净的具体操作是:___________ 。
(1)碱性锌锰电池适合需要大电流供电的设备使用如照相机、野外摄像机、无线电控制的航模与海模、电动工具、电动玩具、收录机等,其结构如图所示,放电时的总反应为
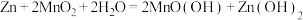 。该电池的正极为
。该电池的正极为 ,其电极反应式为:
,其电极反应式为: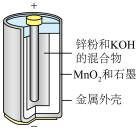
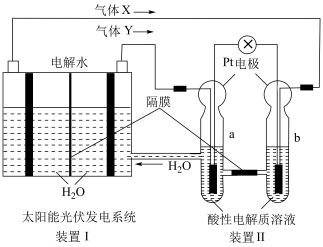
②写出a电极上发生的电极反应
(3)钴酸锂电池的正极采用钴酸锂
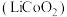 ,负极采用金属锂和碳的复合材料,该电池充放电时的总反应式:
,负极采用金属锂和碳的复合材料,该电池充放电时的总反应式: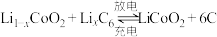 ,写出放电时负极的电极反应
,写出放电时负极的电极反应(4)利用
 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下: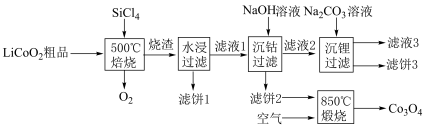
①烧渣是LiCl、
 和
和 的混合物,则500℃焙烧反应的氧化产物与还原产物的物质的量之比为
的混合物,则500℃焙烧反应的氧化产物与还原产物的物质的量之比为②“滤饼2”的主要成分是
 的溶解度比LiOH
的溶解度比LiOH③“850℃煅烧”时的化学方程式为:
④在实验室检查滤饼2是否洗涤干净的具体操作是:
您最近一年使用:0次
名校
解题方法
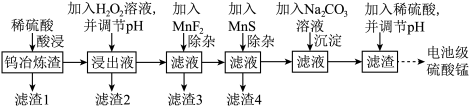
8 . 钨在自然界的储量只有620万吨,江西独占有520万吨。江西每年产生大量的钨冶炼渣(主要含SiO2、MnO2、Al2O3、CaO、MgO、FeO、Fe2O3以及少量重金属氧化物等),以钨冶炼渣为原料,提炼制备电池级硫酸锰的工艺流程如下: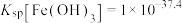 ,
, 。
。
(1)“酸浸”时,为提高锰的浸出率,可采取的措施是_______ (写一种即可),滤渣1的主要成分为SiO2、_______ (填化学式)。
(2)酸浸后所得浸出液中金属阳离子包括Mn2+,写出生成Mn2+的离子方程式_______ 。
(3)若要使 和
和 沉淀完全,则需调节溶液的pH最小值为
沉淀完全,则需调节溶液的pH最小值为_______ 。
(4)滤渣3的主要成分是CaF2和_______ 。
(5)加MnS的目的是_______ 。
(6)如图为MnSO4溶解度曲线。从MnSO4溶液中提取MnSO4晶体的操作为_______ , _______ ,洗涤,干燥,碾磨,即得到了电池级硫酸锰。
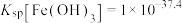 ,
, 。
。(1)“酸浸”时,为提高锰的浸出率,可采取的措施是
(2)酸浸后所得浸出液中金属阳离子包括Mn2+,写出生成Mn2+的离子方程式
(3)若要使
 和
和 沉淀完全,则需调节溶液的pH最小值为
沉淀完全,则需调节溶液的pH最小值为(4)滤渣3的主要成分是CaF2和
(5)加MnS的目的是
(6)如图为MnSO4溶解度曲线。从MnSO4溶液中提取MnSO4晶体的操作为

您最近一年使用:0次
名校
9 .  (亚硝酸钙)广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂。
(亚硝酸钙)广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂。
(1)用石灰乳吸收硝酸工业尾气中 、
、 ,既能获得
,既能获得 ,亦能净化尾气。
,亦能净化尾气。
① 和
和 与石灰乳生成
与石灰乳生成 的化学方程式为
的化学方程式为_______ 。
②下列措施能提高尾气中 和
和 去除率的有
去除率的有_______ (填字母)
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量石灰乳
③吸收后经处理得到 晶体,该晶体的主要杂质是
晶体,该晶体的主要杂质是_______ (填化学式);吸收后排放的尾气含量较高的氮氧化物是_______ (填化学式)。
(2)实验室可用反应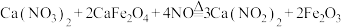 制备
制备 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为_______ 。对于 硫酸和硝酸的混合溶液,若硫酸和硝酸的物质的量浓度存在如下关系:
硫酸和硝酸的混合溶液,若硫酸和硝酸的物质的量浓度存在如下关系: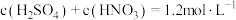 ,则理论上最多能溶解的铜的物质的量为
,则理论上最多能溶解的铜的物质的量为_______  .
.
 (亚硝酸钙)广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂。
(亚硝酸钙)广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂。(1)用石灰乳吸收硝酸工业尾气中
 、
、 ,既能获得
,既能获得 ,亦能净化尾气。
,亦能净化尾气。①
 和
和 与石灰乳生成
与石灰乳生成 的化学方程式为
的化学方程式为②下列措施能提高尾气中
 和
和 去除率的有
去除率的有A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量石灰乳
③吸收后经处理得到
 晶体,该晶体的主要杂质是
晶体,该晶体的主要杂质是(2)实验室可用反应
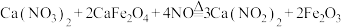 制备
制备 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为 硫酸和硝酸的混合溶液,若硫酸和硝酸的物质的量浓度存在如下关系:
硫酸和硝酸的混合溶液,若硫酸和硝酸的物质的量浓度存在如下关系: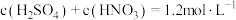 ,则理论上最多能溶解的铜的物质的量为
,则理论上最多能溶解的铜的物质的量为 .
.
您最近一年使用:0次
名校
10 . 下列过程中的化学反应,相应的离子方程式正确的是
A.用淀粉 溶液和醋酸检验加碘盐中的 溶液和醋酸检验加碘盐中的 : : |
B. 溶液中通入少量 溶液中通入少量 : :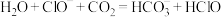 |
C.氯化亚铁溶液中加入酸性的 溶液: 溶液: |
D. 固体与氢碘酸反应: 固体与氢碘酸反应: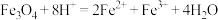 |
您最近一年使用:0次
2024-06-11更新
|
453次组卷
|
2卷引用:福建省部分优质高中2023-2024 学年高一第二学期期末模拟考试化学试卷



