名校
解题方法
1 . 向仅含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知:b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法错误的是
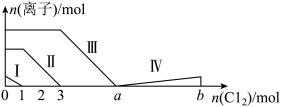
| A.线段Ⅰ、Ⅱ、Ⅲ、Ⅳ分别代表I-、Fe2+、Br-、HIO3的变化情况 |
| B.Fe2+、I-和Br-的物质的量之比为1∶2∶3 |
| C.根据图像可计算b=11 |
| D.线段Ⅳ对应的反应中氧化剂和还原剂的物质的量之比是5∶1 |
您最近一年使用:0次
2023-08-14更新
|
519次组卷
|
4卷引用:浙江省宁波市鄞州中学(宁波鄞州蓝青高级中学)2023-2024学年高一上学期12月月考化学学科试题
浙江省宁波市鄞州中学(宁波鄞州蓝青高级中学)2023-2024学年高一上学期12月月考化学学科试题河北省迁安市第一中学2022-2023学年高三上学期期中考试化学试题 山东省日照市五莲县第一中学2024届高三上学期阶段性测试化学试题(已下线)第04讲 氧化还原反应的基本概念和规律(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
2023高三·全国·专题练习
解题方法
2 . 亚氯酸钠(NaClO2)和ClO2都是重要的漂白剂。
(1)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原NaClO3,可较安全地生成ClO2,反应的离子方程式为_______ 。
(2)自来水用ClO2处理后,有少量ClO2残留在水中,可用碘量法做如下检测(已知ClO2存在于pH为4~6的溶液中,ClO 存在于中性溶液中):
存在于中性溶液中):
①取0.50 L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。写出ClO2与碘化钾反应的化学方程式:_______ 。
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4 mol·L-1的Na2S2O3溶液至恰好反应,消耗Na2S2O3溶液20.00 mL。该水样中ClO2的浓度是_______ mg·L-1。
(3)某学习小组设计如下装置制取亚氯酸钠(NaClO2)。
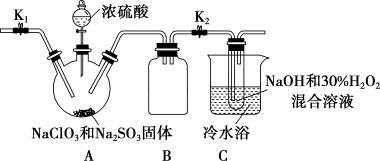
①装置A中产生的ClO2气体,在装置C中反应生成NaClO2,写出生成NaClO2的化学方程式:_______ 。
②将NaClO2溶液在一定条件下处理即可得到NaClO2晶体。装置B的作用是_______ 。
(1)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原NaClO3,可较安全地生成ClO2,反应的离子方程式为
(2)自来水用ClO2处理后,有少量ClO2残留在水中,可用碘量法做如下检测(已知ClO2存在于pH为4~6的溶液中,ClO
 存在于中性溶液中):
存在于中性溶液中):①取0.50 L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。写出ClO2与碘化钾反应的化学方程式:
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4 mol·L-1的Na2S2O3溶液至恰好反应,消耗Na2S2O3溶液20.00 mL。该水样中ClO2的浓度是
(3)某学习小组设计如下装置制取亚氯酸钠(NaClO2)。

①装置A中产生的ClO2气体,在装置C中反应生成NaClO2,写出生成NaClO2的化学方程式:
②将NaClO2溶液在一定条件下处理即可得到NaClO2晶体。装置B的作用是
您最近一年使用:0次
名校
3 . 以高硫铝土矿(主要成分为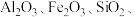 少量
少量 )为原料,生产
)为原料,生产 的部分工艺流程如下:
的部分工艺流程如下: 是一种难溶于水的酸性氧化物,
是一种难溶于水的酸性氧化物, 酸性比碳酸弱,难溶于水。下列说法
酸性比碳酸弱,难溶于水。下列说法不正确 的是
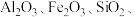 少量
少量 )为原料,生产
)为原料,生产 的部分工艺流程如下:
的部分工艺流程如下: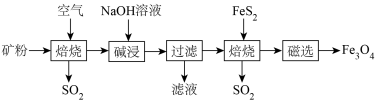
 是一种难溶于水的酸性氧化物,
是一种难溶于水的酸性氧化物, 酸性比碳酸弱,难溶于水。下列说法
酸性比碳酸弱,难溶于水。下列说法| A.高硫铝土矿加工成粉状,可以加快焙烧速率,又能提高原料利用率 |
B.碱浸过程 发生的反应: 发生的反应: |
C.向过滤后得到的滤液中通入过量 ,得到的沉淀为 ,得到的沉淀为 |
D.若由 与 与 在无氧条件下焙烧制得 在无氧条件下焙烧制得 ,则两者物质的量之比为 ,则两者物质的量之比为 |
您最近一年使用:0次
2023-06-27更新
|
618次组卷
|
4卷引用:江苏省连云港市2022-2023学年高一下学期6月期末考试化学试题
江苏省连云港市2022-2023学年高一下学期6月期末考试化学试题(已下线)重难点05 铁及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)河南省新乡市原阳县第一高级中学2023-2024学年高一下学期5月月考化学试题江西省赣州市全南中学2023-2024学年高二上学期开学考试化学试题
名校
解题方法
4 . 过多的 、
、 排放,往往会产生污染。
排放,往往会产生污染。
(Ⅰ) 过多排放是形成硝酸型酸雨的主要原因。某研究性小组探究
过多排放是形成硝酸型酸雨的主要原因。某研究性小组探究 与炽热的铜粉反应,设计如下:
与炽热的铜粉反应,设计如下: 能被酸性高锰酸钾溶液氧化成
能被酸性高锰酸钾溶液氧化成 。
。
(1)直角导管d的作用为______ ;装有 的U形管的作用为
的U形管的作用为_______ ;
(2)选择正确的实验步骤,并排序______________ (操作可重复使用);
①向装置中装好药品,连接好装置,检验装置气密性;②连接好装置,检验装置气密性;③点燃D处酒精灯;④通 ;⑤熄灭酒精灯。
;⑤熄灭酒精灯。
(3)预测D装置中反应后的产物可能为_________ ;
A. 和
和 B.
B. 和
和 C.
C. 和
和
写出可能发生的一个反应的化学方程式,并用单线桥表示其电子转移方向及数目:_____ 。
(Ⅱ)燃煤的烟气中含有,为了治理雾䨪天气,工厂采用多种方法实现烟气脱硫。
(4)“湿式吸收法”利用吸收剂与 发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是
发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是_____ (填字母序号);
a.石灰乳 b. 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液
(5)某工厂利用烟气处理含 的酸性废水,在脱硫的同时制备
的酸性废水,在脱硫的同时制备 产品。具体流程如下:
产品。具体流程如下: 形式存在,则其中发生反应的离子方程式为
形式存在,则其中发生反应的离子方程式为__________________ ;
②中和池中的反应除生成 沉淀外,还会产生某种气体,该气体的化学式为
沉淀外,还会产生某种气体,该气体的化学式为___________ 。
 、
、 排放,往往会产生污染。
排放,往往会产生污染。(Ⅰ)
 过多排放是形成硝酸型酸雨的主要原因。某研究性小组探究
过多排放是形成硝酸型酸雨的主要原因。某研究性小组探究 与炽热的铜粉反应,设计如下:
与炽热的铜粉反应,设计如下:
 能被酸性高锰酸钾溶液氧化成
能被酸性高锰酸钾溶液氧化成 。
。(1)直角导管d的作用为
 的U形管的作用为
的U形管的作用为(2)选择正确的实验步骤,并排序
①向装置中装好药品,连接好装置,检验装置气密性;②连接好装置,检验装置气密性;③点燃D处酒精灯;④通
 ;⑤熄灭酒精灯。
;⑤熄灭酒精灯。(3)预测D装置中反应后的产物可能为
A.
 和
和 B.
B. 和
和 C.
C. 和
和
写出可能发生的一个反应的化学方程式,并用单线桥表示其电子转移方向及数目:
(Ⅱ)燃煤的烟气中含有,为了治理雾䨪天气,工厂采用多种方法实现烟气脱硫。
(4)“湿式吸收法”利用吸收剂与
 发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是
发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是a.石灰乳 b.
 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液(5)某工厂利用烟气处理含
 的酸性废水,在脱硫的同时制备
的酸性废水,在脱硫的同时制备 产品。具体流程如下:
产品。具体流程如下:
 形式存在,则其中发生反应的离子方程式为
形式存在,则其中发生反应的离子方程式为②中和池中的反应除生成
 沉淀外,还会产生某种气体,该气体的化学式为
沉淀外,还会产生某种气体,该气体的化学式为
您最近一年使用:0次
解题方法
5 . 电解金属锰阳极渣(主要成分MnO2,杂质为PbCO3、Fe2O3、CuO)和黄铁矿(FeS2)为原料可制备Mn3O4,其流程如图所示:
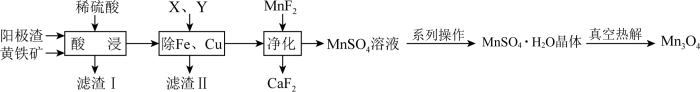
已知:部分阳离子以氢氧化物形式完全沉淀时的pH如下:Fe3+ 3.7,Fe2+ 9.7,Cu2+ 7.4,Mn2+ 9.8
回答下列问题:
(1)“酸浸”过程中,滤渣Ⅰ的主要成分为S、______ (填化学式)。
(2)“酸浸”过程中Fe2+、Fe3+的质量浓度、Mn浸出率与时间的关系如图1所示。
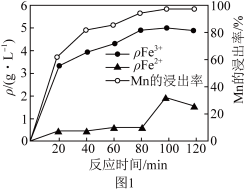
20~80min,浸出Mn元素的主要离子方程式为______ 。80~100min时,Fe2+浓度上升的原因可能是______ 。
(3)“除Fe、Cu”过程中依次加入的试剂X、Y为______ (填序号)。
A.NH3•H2O、H2O2 B.H2O2、CaCO3 C.SO2、MnCO3
(4)硫酸锰晶体的溶解度曲线如图2,由MnSO4溶液获得MnSO4•H2O晶体的系列操作为______ 、洗涤、干燥。
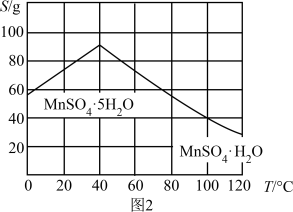
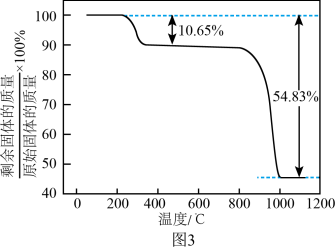
(5)“真空热解”过程中,测得固体的质量随温度变化如图3所示。需控制的温度为______ 。
(6)由MnSO4溶液制取Mn3O4的另一种方案是:向MnSO4溶液中加入氨水,产生Mn(OH)2沉淀和少量Mn2(OH)2SO4,滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得Mn3O4。沉淀加热通空气过程中,7小时之前,溶液的pH=6,7小时之后迅速下降,原因是______ 。

已知:部分阳离子以氢氧化物形式完全沉淀时的pH如下:Fe3+ 3.7,Fe2+ 9.7,Cu2+ 7.4,Mn2+ 9.8
回答下列问题:
(1)“酸浸”过程中,滤渣Ⅰ的主要成分为S、
(2)“酸浸”过程中Fe2+、Fe3+的质量浓度、Mn浸出率与时间的关系如图1所示。

20~80min,浸出Mn元素的主要离子方程式为
(3)“除Fe、Cu”过程中依次加入的试剂X、Y为
A.NH3•H2O、H2O2 B.H2O2、CaCO3 C.SO2、MnCO3
(4)硫酸锰晶体的溶解度曲线如图2,由MnSO4溶液获得MnSO4•H2O晶体的系列操作为

(5)“真空热解”过程中,测得固体的质量随温度变化如图3所示。需控制的温度为

(6)由MnSO4溶液制取Mn3O4的另一种方案是:向MnSO4溶液中加入氨水,产生Mn(OH)2沉淀和少量Mn2(OH)2SO4,滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得Mn3O4。沉淀加热通空气过程中,7小时之前,溶液的pH=6,7小时之后迅速下降,原因是
您最近一年使用:0次
2023-04-27更新
|
878次组卷
|
2卷引用:山东新高考2022-2023学年高一上学期质量测评模拟演练化学试题
22-23高一下·四川·期中
名校
6 . 以黄铁矿(主要成分为FeS2)为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如下图所示。___________ 。
(2)“氧化”时,反应的化学方程式为___________ 。
(3)工业上,吸收SO3时宜选用的试剂X为___________ 。
(4)因为Na2S2O5在保存过程中发生___________ (填“氧化”或“还原”)反应,导致商品Na2S2O5中不可避免地存在Na2SO4.欲检验是否变质,可取少量样品溶于水中,___________ ,说明含有 。
。
(5)Na2S2O5可用于葡萄酒的抗氧化剂。用碘标准液可测定葡萄酒中Na2S2O5的残留量,请配平该反应的方程式:___________ 。
________S2O +________I2+_______H2O=______
+________I2+_______H2O=______ +_______I-+_______H+
+_______I-+_______H+
(6)某同学以如图所示装置用电化学原理模拟生产硫酸:________ (填“正”或“负”)极。写出通入O2的电极的电极反应式________ 。
②若此过程中转移了0.4mol电子,则理论上可以得到硫酸的质量为_____ ;溶液中的H+_____ (填“从左向右”或“从右向左”)移动。
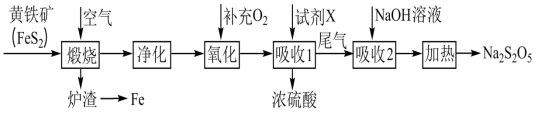
(2)“氧化”时,反应的化学方程式为
(3)工业上,吸收SO3时宜选用的试剂X为
(4)因为Na2S2O5在保存过程中发生
 。
。(5)Na2S2O5可用于葡萄酒的抗氧化剂。用碘标准液可测定葡萄酒中Na2S2O5的残留量,请配平该反应的方程式:
________S2O
 +________I2+_______H2O=______
+________I2+_______H2O=______ +_______I-+_______H+
+_______I-+_______H+(6)某同学以如图所示装置用电化学原理模拟生产硫酸:

②若此过程中转移了0.4mol电子,则理论上可以得到硫酸的质量为
您最近一年使用:0次
名校
解题方法
7 . 下列反应的离子方程式书写正确的是
A. 溶液中加入过量醋酸溶液: 溶液中加入过量醋酸溶液: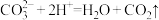 |
B. 溶液中通入过量 溶液中通入过量 : :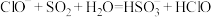 |
C. 溶液中加入 溶液中加入 溶液: 溶液: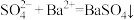 |
D.酸性高锰酸钾溶液中滴加KI溶液: |
您最近一年使用:0次
2023-02-10更新
|
990次组卷
|
2卷引用:山东省潍坊市2022-2023学年高一上学期期末考试化学试题
名校
8 . 以红土镍矿(主要含有Fe2O3、FeO、NiO、SiO2等)为原料,获取净水剂黄钠铁矾[NaFe3(SO4)2(OH)6]和纳米镍粉的部分工艺流程如图:
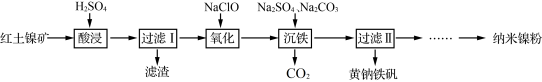
已知:
①Fe3+在pH约为3.7时可完全转化为Fe(OH)3,Fe2+在pH约为9时可完全转化为Fe(OH)2;
②SiO2为不溶于水的酸性氧化物,常温下和硫酸不反应,但可以溶于强碱溶液。
下列说法不正确的是

已知:
①Fe3+在pH约为3.7时可完全转化为Fe(OH)3,Fe2+在pH约为9时可完全转化为Fe(OH)2;
②SiO2为不溶于水的酸性氧化物,常温下和硫酸不反应,但可以溶于强碱溶液。
下列说法不正确的是
| A.“滤渣”的主要成分是SiO2 |
| B.为提高“酸浸”速率,可将稀硫酸更换为浓硫酸 |
| C.“氧化”过程发生的离子方程式为:2H++2Fe2++ClO-=2Fe3++Cl-+H2O |
| D.“沉铁”过程中加入碳酸钠的作用是调节溶液的酸碱度,应将pH控制在3.7~9 |
您最近一年使用:0次
2023-01-14更新
|
376次组卷
|
2卷引用:山东师范大学附属中学 2022-2023 学年高一上学期学科水平自我诊断化学试题
名校
9 . 氯气可用于制取漂白剂和自来水消毒。
(1)下图是实验室制备氯气的制备和除杂装置
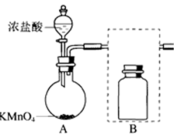
①A为氯气发生装置。A中反应方程式是_______ (锰被还原为 )。
)。
②将除杂装置B补充完整并标明所用试剂_______ 。
(2)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入NaOH溶液中,反应的离子方程式为_______ 。
(3)同学们探究“84”消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液稀释100倍,测得稀释后溶液的 ;
;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用 溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计)。
溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计)。
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
已知,溶液中 、HClO和
、HClO和 物质的量分数
物质的量分数 随溶液pH变化的关系如下图所示:
随溶液pH变化的关系如下图所示:
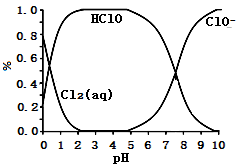
①由实验现象可得以下结论:溶液pH在4~10范围内,pH越大,红纸褪色_______ 。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是_______ 。
(4)由于氯气会与自来水中的有机物发生反应生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如 气体就是一种新型高效含氯消毒剂。
气体就是一种新型高效含氯消毒剂。
①一种制备 的方法是用
的方法是用 通入硫酸酸化的
通入硫酸酸化的 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为_______ 。
②另一种制备 的方法是用
的方法是用 与盐酸反应,同时有
与盐酸反应,同时有 生成,产物中
生成,产物中 体积约占
体积约占 ,每生成
,每生成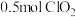 ,转移
,转移_______  。
。
③ 在杀菌消毒过程中会产生副产物亚氯酸盐
在杀菌消毒过程中会产生副产物亚氯酸盐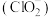 ,需将其转化为
,需将其转化为 除去。下列试剂中,可将
除去。下列试剂中,可将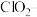 转化为
转化为 的是
的是_______ (填字母序号)。
a. b.
b. c.
c. d.KI
d.KI
(1)下图是实验室制备氯气的制备和除杂装置

①A为氯气发生装置。A中反应方程式是
 )。
)。②将除杂装置B补充完整并标明所用试剂
(2)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入NaOH溶液中,反应的离子方程式为
(3)同学们探究“84”消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液稀释100倍,测得稀释后溶液的
 ;
;步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用
 溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计)。
溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计)。步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
| 烧杯 | 溶液的pH | 现象 |
| a | 10 | 10min后,红纸基本不褪色;4h后红纸褪色 |
| b | 7 | 10min后,红纸颜色变浅;4h后红纸褪色 |
| c | 4 | 10min后,红纸颜色变得更浅;4h后红纸褪色 |
 、HClO和
、HClO和 物质的量分数
物质的量分数 随溶液pH变化的关系如下图所示:
随溶液pH变化的关系如下图所示:
①由实验现象可得以下结论:溶液pH在4~10范围内,pH越大,红纸褪色
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是
(4)由于氯气会与自来水中的有机物发生反应生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如
 气体就是一种新型高效含氯消毒剂。
气体就是一种新型高效含氯消毒剂。①一种制备
 的方法是用
的方法是用 通入硫酸酸化的
通入硫酸酸化的 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为②另一种制备
 的方法是用
的方法是用 与盐酸反应,同时有
与盐酸反应,同时有 生成,产物中
生成,产物中 体积约占
体积约占 ,每生成
,每生成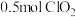 ,转移
,转移 。
。③
 在杀菌消毒过程中会产生副产物亚氯酸盐
在杀菌消毒过程中会产生副产物亚氯酸盐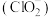 ,需将其转化为
,需将其转化为 除去。下列试剂中,可将
除去。下列试剂中,可将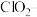 转化为
转化为 的是
的是a.
 b.
b. c.
c. d.KI
d.KI
您最近一年使用:0次
2023-01-07更新
|
450次组卷
|
2卷引用:北京市第八中学2022-2023学年高一上学期期末考试化学试题
名校
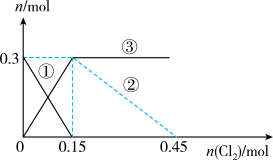
10 . 向100mL
 溶液中逐渐通入
溶液中逐渐通入 ,其中
,其中 、
、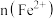 、
、 随通入
随通入 的物质的量
的物质的量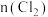 变化如图所示,下列说法错误的是
变化如图所示,下列说法错误的是

 溶液中逐渐通入
溶液中逐渐通入 ,其中
,其中 、
、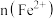 、
、 随通入
随通入 的物质的量
的物质的量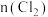 变化如图所示,下列说法错误的是
变化如图所示,下列说法错误的是
A.②代表 ,③代表 ,③代表 |
B.还原性强弱: |
C. 时,溶液中 时,溶液中 |
D.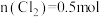 时,总的离子方程式为: 时,总的离子方程式为: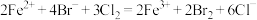 |
您最近一年使用:0次
2023-01-04更新
|
402次组卷
|
2卷引用:湖北省荆州市八县市2022-2023学年高一上学期期末联考化学试题



