名校
解题方法
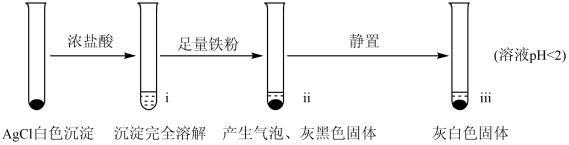
1 . 工业上用铁粉还原AgCl制取银,某小组探究其过程和影响因素。
【实验A】在试管中加入NaCl溶液,然后滴入AgNO3溶液,产生白色沉淀。滤出白色沉淀,继续实验如图:
【资料】 ;②Fe3++4Cl−⇌FeCl
;②Fe3++4Cl−⇌FeCl
(1)检验ⅱ中产物
①取ⅱ中上层清液,滴加K3[Fe(CN)6]溶液,有_______ (填现象),说明溶液中含有Fe2+。
②取ⅱ中少量灰黑色固体,洗涤后将固体等分两份。取其中一份,加入_______ (填试剂)溶解,再加入NaCl溶液生成白色沉淀,证明灰黑色固体中含有Ag。向另一份加入KI溶液,无明显现象。
(2)检验ⅲ中产物。
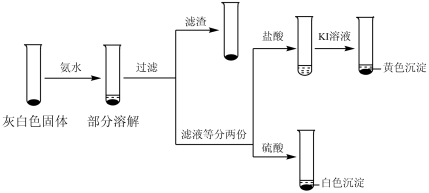
①取ⅲ中灰白色固体,洗涤。进行如图实验,确认灰白色固体中含AgCl:_______ 。
②取iii中上层溶液,加几滴KSCN溶液。取样时间与溶液颜色如表。
用离子方程式表示溶液变红的原因_______ ,Fe3++3SCN−⇌Fe(SCN)3。
(3)小组同学认为不能排除O2直接氧化Ag继而生成AgCl,对此设计实验:_______ 。结果发现,该实验产生AgCl所需的时间更长。说明AgCl的产生主要与Fe3+有关。
(4)实验A中的i~iii中,i中AgCl溶解,iii中又生成AgCl,试解释iii中生成AgCl的原因:_______ 。
实验反思:铁粉还原AgCl制取银时应控制铁粉、盐酸的浓度和浸泡时间等因素。
【实验A】在试管中加入NaCl溶液,然后滴入AgNO3溶液,产生白色沉淀。滤出白色沉淀,继续实验如图:
【资料】
 ;②Fe3++4Cl−⇌FeCl
;②Fe3++4Cl−⇌FeCl
(1)检验ⅱ中产物
①取ⅱ中上层清液,滴加K3[Fe(CN)6]溶液,有
②取ⅱ中少量灰黑色固体,洗涤后将固体等分两份。取其中一份,加入
(2)检验ⅲ中产物。
①取ⅲ中灰白色固体,洗涤。进行如图实验,确认灰白色固体中含AgCl:
②取iii中上层溶液,加几滴KSCN溶液。取样时间与溶液颜色如表。
| 取样时间 | 10分钟 | 12小时 | 24小时 |
| 溶液颜色 | 浅红色 | 红色 | 深红色 |
(3)小组同学认为不能排除O2直接氧化Ag继而生成AgCl,对此设计实验:
(4)实验A中的i~iii中,i中AgCl溶解,iii中又生成AgCl,试解释iii中生成AgCl的原因:
实验反思:铁粉还原AgCl制取银时应控制铁粉、盐酸的浓度和浸泡时间等因素。
您最近一年使用:0次
解题方法
2 . 含砷废水常见于采矿、半导体等工业,部分砷的化合物有毒,因此需除去废水中的砷。
Ⅰ.天然水体中砷元素主要以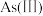 和
和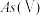 存在。在
存在。在 水溶液中,各种微粒的物质的量分数与溶液
水溶液中,各种微粒的物质的量分数与溶液 的关系如图1所示。
的关系如图1所示。
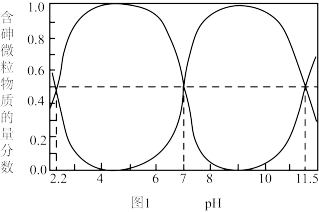
(1)当天然水体的 为4时,水体中所含
为4时,水体中所含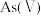 的主要微粒是
的主要微粒是_______ 。
(2)将 溶液滴入
溶液滴入 溶液中,当
溶液中,当 达到8时,所发生反应的离子方程式为
达到8时,所发生反应的离子方程式为_______ 。此时,溶液中含砷离子浓度由大到小的顺序为_______ 。
(3) 时,向
时,向 溶液中加入
溶液中加入 溶液至中性,此时溶液中
溶液至中性,此时溶液中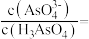
_______ 。
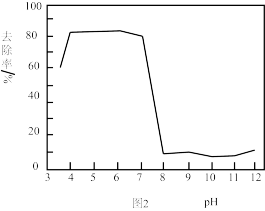
Ⅱ.利用高铁酸盐处理含砷废水。在一定 范围内,高铁酸盐被还原成胶体,而吸附含砷化合物。不同
范围内,高铁酸盐被还原成胶体,而吸附含砷化合物。不同 对
对 除砷影响如图2所示。
除砷影响如图2所示。
已知:溶液的 对胶体粒子表面所带电荷有影响。
对胶体粒子表面所带电荷有影响。 时,胶体粒子表面带正电荷,
时,胶体粒子表面带正电荷, 越低,表面所带正电荷越多。
越低,表面所带正电荷越多。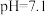 时,胶体粒子表面不带电荷;
时,胶体粒子表面不带电荷;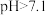 时,胶体粒子表面带负电荷,
时,胶体粒子表面带负电荷, 越高,表面所带负电荷越多。
越高,表面所带负电荷越多。
(4)结合图1和图2分析,除砷过程中控制废水 约为
约为_______ 适宜, 过低或过高,砷的去除率都会下降。
过低或过高,砷的去除率都会下降。 过低,主要以
过低,主要以 形式存在,不易形成
形式存在,不易形成 胶体。
胶体。 过高,一是
过高,一是 氧化性减弱,产生
氧化性减弱,产生 胶体的量少;二是
胶体的量少;二是_______ ;三是 过高,生成
过高,生成 沉淀而不是
沉淀而不是 胶体。
胶体。
(5)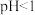 时,
时, 氧化
氧化 的离子方程式为
的离子方程式为_______ 。
Ⅰ.天然水体中砷元素主要以
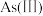 和
和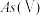 存在。在
存在。在 水溶液中,各种微粒的物质的量分数与溶液
水溶液中,各种微粒的物质的量分数与溶液 的关系如图1所示。
的关系如图1所示。
(1)当天然水体的
 为4时,水体中所含
为4时,水体中所含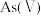 的主要微粒是
的主要微粒是(2)将
 溶液滴入
溶液滴入 溶液中,当
溶液中,当 达到8时,所发生反应的离子方程式为
达到8时,所发生反应的离子方程式为(3)
 时,向
时,向 溶液中加入
溶液中加入 溶液至中性,此时溶液中
溶液至中性,此时溶液中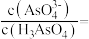
Ⅱ.利用高铁酸盐处理含砷废水。在一定
 范围内,高铁酸盐被还原成胶体,而吸附含砷化合物。不同
范围内,高铁酸盐被还原成胶体,而吸附含砷化合物。不同 对
对 除砷影响如图2所示。
除砷影响如图2所示。
已知:溶液的
 对胶体粒子表面所带电荷有影响。
对胶体粒子表面所带电荷有影响。 时,胶体粒子表面带正电荷,
时,胶体粒子表面带正电荷, 越低,表面所带正电荷越多。
越低,表面所带正电荷越多。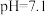 时,胶体粒子表面不带电荷;
时,胶体粒子表面不带电荷; 时,胶体粒子表面带负电荷,
时,胶体粒子表面带负电荷, 越高,表面所带负电荷越多。
越高,表面所带负电荷越多。(4)结合图1和图2分析,除砷过程中控制废水
 约为
约为 过低或过高,砷的去除率都会下降。
过低或过高,砷的去除率都会下降。 过低,主要以
过低,主要以 形式存在,不易形成
形式存在,不易形成 胶体。
胶体。 过高,一是
过高,一是 氧化性减弱,产生
氧化性减弱,产生 胶体的量少;二是
胶体的量少;二是 过高,生成
过高,生成 沉淀而不是
沉淀而不是 胶体。
胶体。(5)
 时,
时, 氧化
氧化 的离子方程式为
的离子方程式为
您最近一年使用:0次
2022-01-25更新
|
224次组卷
|
2卷引用:山东省威海市2021-2022学年高二上学期期末考试化学试题
19-20高三·江苏苏州·期末
名校
3 . 铁及其化合物在处理工业废水、废气过程中发挥着重要作用。
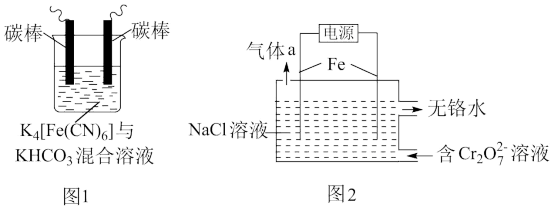
(1)用铁的化合物除硫化氢:2[Fe(CN)6]3-+ 2 +HS- =2[Fe(CN)6]4-+ 2
+HS- =2[Fe(CN)6]4-+ 2 +S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为
+S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为_______ ;电解过程中阴极区溶液的pH_______ (填“变大”、 “变小”或“不变")。
(2)以铁为电极电解除铬,如图2
已知: + H2O=2
+ H2O=2 +2H+
+2H+
氧化性: >
>
①电解过程中主要反应之一: +6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是
+6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是_______ 。
②电解过程中,不同pH时,通电时间与Cr元素的去除率关系如图3所示,pH=10相比pH=4,Cr元素的去除率偏低的原因可能是_______ 。
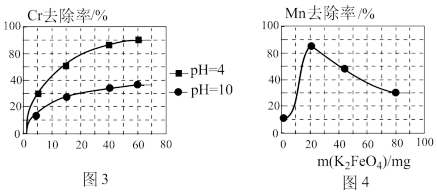
(3)高铁酸钾(K2FeO4)除锰
已知:K2FeO4具有强氧化性,极易溶于水
①在酸性条件下,能与废水中的Mn2+反应生成Fe(OH)3和MnO2沉淀来除锰,该反应的离子方程式_______ 。
②用K2FeO4处理1L 50 mg/L的含Mn2+废水,Mn元素的去除率与K2FeO4量的关系如图4所示,当K2FeO4超过20 mg时,Mn元素的去除率下降的原因可能是_______ 。

(1)用铁的化合物除硫化氢:2[Fe(CN)6]3-+ 2
 +HS- =2[Fe(CN)6]4-+ 2
+HS- =2[Fe(CN)6]4-+ 2 +S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为
+S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为(2)以铁为电极电解除铬,如图2
已知:
 + H2O=2
+ H2O=2 +2H+
+2H+氧化性:
 >
>
①电解过程中主要反应之一:
 +6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是
+6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是②电解过程中,不同pH时,通电时间与Cr元素的去除率关系如图3所示,pH=10相比pH=4,Cr元素的去除率偏低的原因可能是

(3)高铁酸钾(K2FeO4)除锰
已知:K2FeO4具有强氧化性,极易溶于水
①在酸性条件下,能与废水中的Mn2+反应生成Fe(OH)3和MnO2沉淀来除锰,该反应的离子方程式
②用K2FeO4处理1L 50 mg/L的含Mn2+废水,Mn元素的去除率与K2FeO4量的关系如图4所示,当K2FeO4超过20 mg时,Mn元素的去除率下降的原因可能是
您最近一年使用:0次
2021-03-25更新
|
453次组卷
|
5卷引用:【苏州新东方】化学试卷
(已下线)【苏州新东方】化学试卷(已下线)2.3.1 浓度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)湖北省武汉市蔡甸区汉阳一中2021-2022学年高二上学期12月月考化学试题湖北省武汉市部分重点中学2021-2022学年高二上学期12月联考化学试题江苏省常州市第一中学2023-2024学年高二上学期11月期中考试化学试题
4 . 制备高铁酸钾[K2FeO4]并用其除去土壤和废水中的有机砷(HAPA)与无机砷[+3价砷表示As(Ⅲ)]的流程如图所示:
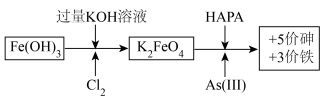
已知:酸性越强,K2FeO4越容易发生反应生成O2。
回答下列问题:
(1)生成K2FeO4的化学方程式为___ 。
(2)K2FeO4去除砷污染时作__ (填“氧化剂”或“还原剂”)。若污染物中的砷全部以Na3AsO3计,则去除全部污染时Na3AsO3与K2FeO4的物质的量之比为__ 。
(3)氢离子浓度、高铁酸钾的用量对HAPA和As(Ⅲ)去除效果的影响如图所示。
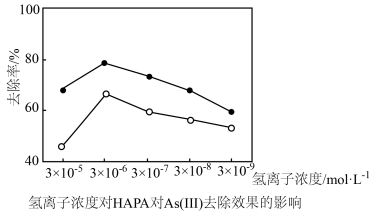
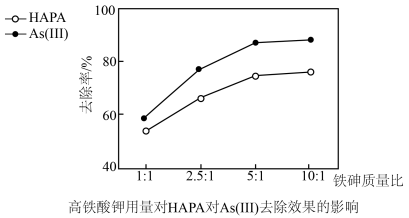
①氢离子浓度为3×10-5mol•L-1时去除率低,原因是(用离子方程式表示)__ 。
②最佳铁砷质量比为___ ,理由是__ 。

已知:酸性越强,K2FeO4越容易发生反应生成O2。
回答下列问题:
(1)生成K2FeO4的化学方程式为
(2)K2FeO4去除砷污染时作
(3)氢离子浓度、高铁酸钾的用量对HAPA和As(Ⅲ)去除效果的影响如图所示。


①氢离子浓度为3×10-5mol•L-1时去除率低,原因是(用离子方程式表示)
②最佳铁砷质量比为
您最近一年使用:0次
2021-01-28更新
|
722次组卷
|
4卷引用:山东省潍坊市2020-2021学年高一上学期期末统考化学试题
山东省潍坊市2020-2021学年高一上学期期末统考化学试题(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练山东省高密市第一中学2023-2024学年高一上学期1月冬学竞赛化学试题
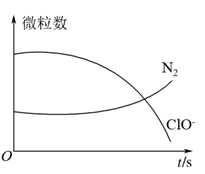
5 . 某离子反应涉及H2O、ClO-、 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
| A.该反应中Cl-为氧化产物 |
| B.消耗1个还原剂微粒,转移6e- |
C. 被ClO-氧化成N2 被ClO-氧化成N2 |
| D.反应后溶液的酸性减弱 |
您最近一年使用:0次
2020-10-02更新
|
1134次组卷
|
8卷引用:广东省深圳市高级中学2018-2019学年高一上学期期末考试化学试题
真题
名校
6 . 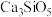 是硅酸盐水泥的重要成分之一,其相关性质的说法
是硅酸盐水泥的重要成分之一,其相关性质的说法不正确 的是
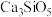 是硅酸盐水泥的重要成分之一,其相关性质的说法
是硅酸盐水泥的重要成分之一,其相关性质的说法A.可发生反应: |
| B.具有吸水性,需要密封保存 |
C.能与 ,反应生成新盐 ,反应生成新盐 |
D.与足量盐酸作用,所得固体产物主要为 |
您最近一年使用:0次
2020-07-11更新
|
5371次组卷
|
31卷引用:北京市昌平区2022-2023学年高三上学期期末质量检测化学试题
北京市昌平区2022-2023学年高三上学期期末质量检测化学试题2020年浙江省高考化学试卷(7月选考)(已下线)专题05 元素及其化合物-2020年高考真题和模拟题化学分项汇编(已下线)第9讲 硅及其化合物-2021年高考化学一轮复习名师精讲练(已下线)第13讲 碳、硅及无机非金属材料(精讲)——2021年高考化学一轮复习讲练测(已下线)小题必刷08 氧化还原反应的规律及应用——2021年高考化学一轮复习小题必刷(通用版)(已下线)小题必刷17 碳、硅与无机非金属材料——2021年高考化学一轮复习小题必刷(通用版)(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练天津市实验中学滨海学校2021届高三上学期第一次月考化学试题(已下线)课时20 碳、硅与无机非金属材料-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考向05 氧化还原反应-备战2022年高考化学一轮复习考点微专题(已下线)考点10 碳、硅及其无机非金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点10 碳、硅及其无机非金属材料-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)第9讲 无机非金属材料 (讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向10 碳、硅及其化合物-备战2022年高考化学一轮复习考点微专题(已下线)专题05.元素及其化合物-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)专题07 常见非金属及其化合物-备战2022年高考化学学霸纠错(全国通用)重庆市第七中学校2021-2022学年高一下学期3月月考化学试题(已下线)考点12 硅及其无机非金属材料-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第11讲 碳、硅及无机非金属材料(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第14练 无机非金属材料-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第09讲 无机非金属材料(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第09讲 无机非金属材料(讲)-2023年高考化学一轮复习讲练测(新教材新高考)第四章 非金属及其化合物 第17讲 无机非金属材料(已下线)第10讲 硅及其化合物(已下线)第7讲 碳、硅及无机非金属材料(已下线)考点13 硅及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)浙江省杭州市西湖高级中学2023-2024学年高一下学期4月期中考试化学试题湖北省武汉市第三中学2023-2024学年高一下学期3月月考化学试卷(已下线)第05讲 氧化还原反应方程式的配平、书写及计算(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
7 . 三氯氧磷(POCl3)广泛用于农药、医药等生产。工业制备三氯氧磷的过程中会产生副产品亚磷酸(H3PO3)。回答下列问题:
(1)三氯氧磷可由三氯化磷、水、氯气加热反应生成,反应的化学方程式为_______
(2)已知亚磷酸(H3PO3)为二元弱酸,则Na2HPO3溶液中,各离子浓度的大小关系为_______
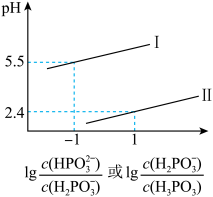
(3)常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示lg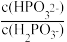 的是曲线
的是曲线_____ (填“Ⅰ”或“Ⅱ”),亚磷酸(H3PO3)的Ka1=_____ ,反应HPO32-+H2O H2PO3-+OH-的平衡常数的值是
H2PO3-+OH-的平衡常数的值是_____ 。
(4)工业上生产三氯氧磷的同时会产生含磷废水(主要成分为H3PO4、H3PO3)。向废水中先加入适量漂白粉,再加入生石灰调节pH,将磷元素转化为磷酸的钙盐沉淀并回收。若处理后的废水中c(Ca2+)=5×10-6 mol·L-1,则溶液中c(PO43-)=_____ mol·L-1。(已知Ksp[Ca3(PO4)2]=2×10-29)
(1)三氯氧磷可由三氯化磷、水、氯气加热反应生成,反应的化学方程式为
(2)已知亚磷酸(H3PO3)为二元弱酸,则Na2HPO3溶液中,各离子浓度的大小关系为
(3)常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示lg
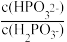 的是曲线
的是曲线 H2PO3-+OH-的平衡常数的值是
H2PO3-+OH-的平衡常数的值是
(4)工业上生产三氯氧磷的同时会产生含磷废水(主要成分为H3PO4、H3PO3)。向废水中先加入适量漂白粉,再加入生石灰调节pH,将磷元素转化为磷酸的钙盐沉淀并回收。若处理后的废水中c(Ca2+)=5×10-6 mol·L-1,则溶液中c(PO43-)=

您最近一年使用:0次
2020-04-03更新
|
792次组卷
|
4卷引用:湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题19 大题综合训练
8 . 硝酸是一种重要的化工原料,用来制取一系列硝酸盐类氮肥,如硝酸铵、硝酸钾等;也用来制取含硝基的炸药等。试回答下列问题:
(1)某同学对铁与稀硝酸的反应进行探究,若HNO3只被还原成NO,则:
①写出铁与过量稀硝酸反应的离子方程式:__ 。
②写出过量铁与稀硝酸反应的离子方程式:__ 。
③若28g铁与含1.6mol硝酸的稀硝酸恰好完全反应,则生成的Fe3+和Fe2+的物质的量之比为__ 。上述反应结束后,向反应后的溶液中加足量氢氧化钠溶液,滤出沉淀洗涤后,在空气中灼烧至质量不变,最终得到的固体质量为__ g。
(2)饮用水中NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO3-还原为N2。
①配平方程式:__ Al+__ NO3-+__ OH-+__ =__ [Al(OH)4]-+__ N2↑。
②上述反应中,还原剂与还原产物的物质的量之比是__ ,反应中转移电子0.3mol,生成__ mL(标准状况下)N2。
(1)某同学对铁与稀硝酸的反应进行探究,若HNO3只被还原成NO,则:
①写出铁与过量稀硝酸反应的离子方程式:
②写出过量铁与稀硝酸反应的离子方程式:
③若28g铁与含1.6mol硝酸的稀硝酸恰好完全反应,则生成的Fe3+和Fe2+的物质的量之比为
(2)饮用水中NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO3-还原为N2。
①配平方程式:
②上述反应中,还原剂与还原产物的物质的量之比是
您最近一年使用:0次
2019-12-05更新
|
617次组卷
|
5卷引用:云南省广南县二中2019-2020学年高一上学期期末考试化学试题
云南省广南县二中2019-2020学年高一上学期期末考试化学试题云南省贡山县第三中学2017-2018学年高一上学期期末考试化学试题贵州省独山县第四中学2019-2020学年高一上学期期末考试化学试题鲁科版必修一2019—2020学年第三章检测试题(已下线)第三单元 物质的性质与转化(能力提升)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)
名校
9 . 某离子反应涉及到 H2O、ClO-、NH4+、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,下列说法不正确 的是
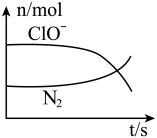

| A.该反应中Cl-为还原产物 |
| B.氧化剂与还原剂物质的量比为3:2 |
| C.消耗1 mol还原剂,转移6 mol电子 |
| D.氧化性:ClO-比 N2强 |
您最近一年使用:0次
2019-07-02更新
|
974次组卷
|
11卷引用:福建省宁德博雅培文学校2022-2023学年高一上学期线上期末考试化学试题
福建省宁德博雅培文学校2022-2023学年高一上学期线上期末考试化学试题福建省莆田第六中学2018-2019学年高一(实验班)下学期期中考试化学试题福建省莆田第六中学2018-2019学年高一下学期期中考试化学试题(已下线)2019年10月6日《每日一题》必修1 —— 每周一测甘肃省兰州第一中学2019-2020学年高一上学期期中考试化学试题上海市格致中学2020届高三上学期开学考试化学试题鲁科版(2019)高一必修第一册第二章B 素养拓展区 过素养 学科素养拓展训练高一必修第一册(苏教2019版)专题3 B 素养拓展区 过素养 学科素养拓展训练甘肃省嘉峪关市第一中学2021届高三上学期一模考试化学试卷辽宁省沈阳市东北育才学校2020届高三上学期第一次模拟考试化学试题湖北省十堰市第二中学2021-2022学年高一上学期12月考试化学试题
10 . CuS、Cu2S用于处理酸性废水中的Cr2O72-反应如下。
反应I:CuS+Cr2O72-+H+→Cu2++SO42-+Cr3++H2O(未配平)
反应Ⅱ:Cu2S+Cr2O72-+H+→Cu2++SO42-+Cr3++H2O(未配平)
下列有关说法正确的是
反应I:CuS+Cr2O72-+H+→Cu2++SO42-+Cr3++H2O(未配平)
反应Ⅱ:Cu2S+Cr2O72-+H+→Cu2++SO42-+Cr3++H2O(未配平)
下列有关说法正确的是
| A.反应I和Ⅱ中各有2种元素的化合价发生变化 |
| B.处理1molCr2O72-时反应I、Ⅱ中消耗H+的物质的量相等 |
| C.反应Ⅱ中还原剂与氧化剂的物质的量之比为3:5 |
| D.质量相同时,Cu2S能去除更多的Cr2O72- |
您最近一年使用:0次
2019-02-25更新
|
543次组卷
|
4卷引用:【市级联考】山东省济南市2019届高三上学期期末考试化学试题
【市级联考】山东省济南市2019届高三上学期期末考试化学试题(已下线)专题2.2 离子反应 离子共存及检验(练)-《2020年高考一轮复习讲练测》(已下线)专题2.3 氧化还原反应(练)-《2020年高考一轮复习讲练测》沪科版高中化学拓展课程第4章《离子互换反应和氧化还原反应》检测题3



