解题方法
1 . 以下是有关铝的实验探究,请回答相关问题:
(1)用铝粉和 做铝热反应实验,需要的试剂还有___________。
做铝热反应实验,需要的试剂还有___________。
(2)镁能发生和铝类似的“镁热反应”,写出镁在高温下和 反应的化学方程式
反应的化学方程式___________ 。
(3)向集满 的铝制易拉罐中加入过量
的铝制易拉罐中加入过量 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:___________ 。
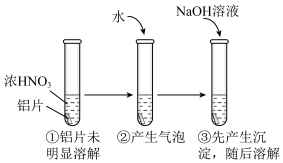
(4)用打磨过的铝片进行如下实验,下列分析不合理的是___________
(5)某铝土矿的主要成分为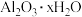 ,还含有
,还含有 和
和 杂质(已知
杂质(已知 难溶于水,且与稀硫酸及其它成分均不反应)。称取
难溶于水,且与稀硫酸及其它成分均不反应)。称取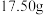 铝土矿样品,加入
铝土矿样品,加入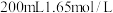 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。
①该试样中 的物质的量为
的物质的量为___________  。
。
②样品中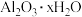 的
的
___________ 。
(1)用铝粉和
 做铝热反应实验,需要的试剂还有___________。
做铝热反应实验,需要的试剂还有___________。A. | B. | C. | D. |
(2)镁能发生和铝类似的“镁热反应”,写出镁在高温下和
 反应的化学方程式
反应的化学方程式(3)向集满
 的铝制易拉罐中加入过量
的铝制易拉罐中加入过量 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:(4)用打磨过的铝片进行如下实验,下列分析不合理的是___________

| A.①中铝片发生了钝化 |
| B.②中产生的气泡是氮氧化合物,不是氢气 |
C.③中沉淀溶解的离子方程式是 |
| D.②中加水稀释过程中,仅发生了氧化还原反应 |
(5)某铝土矿的主要成分为
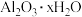 ,还含有
,还含有 和
和 杂质(已知
杂质(已知 难溶于水,且与稀硫酸及其它成分均不反应)。称取
难溶于水,且与稀硫酸及其它成分均不反应)。称取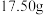 铝土矿样品,加入
铝土矿样品,加入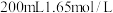 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。①该试样中
 的物质的量为
的物质的量为 。
。②样品中
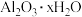 的
的
您最近一年使用:0次
解题方法
2 . 硫化钠主要用于皮革、毛纺、高档纸张、染料等行业。回答下列问题:
Ⅰ、工业生产硫化钠大多采用无水芒硝( )-炭粉还原法,其流程示意图如下:
)-炭粉还原法,其流程示意图如下:
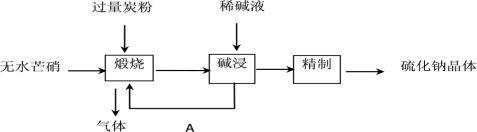
(1)上述流程中“碱浸”后,物质A必须经过___________ (填写操作名称)处理后,方可“煅烧”;若煅烧所得气体为等物质的量的CO和 ,写出煅烧时发生的总的化学反应方程式为
,写出煅烧时发生的总的化学反应方程式为___________ 。
(2)上述流程中采用稀碱液比用热水更好,理由是___________ 。
Ⅱ、工业生产的硫化钠粗品中常含有一定量的煤灰及重金属硫化物等杂质。硫化钠易溶于热乙醇,重金属硫化物难溶于乙醇。实验室中常用95%乙醇重结晶纯化硫化钠粗品。
(3)溶解回流装置如图所示,回流前无需加入沸石,其原因是___________ ,回流时,烧瓶内气雾上升高度不宜超过冷凝管高度的 ,若气雾上升过高,可采取的措施是
,若气雾上升过高,可采取的措施是___________ 。
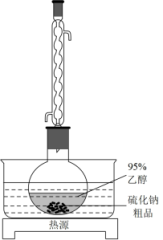
(4)回流时间不宜过长,原因是___________ ;回流结束后,需进行的操作有①停止加热 ②关闭冷凝水 ③移去水浴,正确的顺序为___________ (填标号)。
a.①②③ b.③①② c.②①③ d.①③②
(5)该实验热过滤操作时,过滤除去的杂质为___________ ,若滤纸上析出大量晶体,则可能的原因是___________ 。
Ⅰ、工业生产硫化钠大多采用无水芒硝(
 )-炭粉还原法,其流程示意图如下:
)-炭粉还原法,其流程示意图如下:
(1)上述流程中“碱浸”后,物质A必须经过
 ,写出煅烧时发生的总的化学反应方程式为
,写出煅烧时发生的总的化学反应方程式为(2)上述流程中采用稀碱液比用热水更好,理由是
Ⅱ、工业生产的硫化钠粗品中常含有一定量的煤灰及重金属硫化物等杂质。硫化钠易溶于热乙醇,重金属硫化物难溶于乙醇。实验室中常用95%乙醇重结晶纯化硫化钠粗品。
(3)溶解回流装置如图所示,回流前无需加入沸石,其原因是
 ,若气雾上升过高,可采取的措施是
,若气雾上升过高,可采取的措施是
(4)回流时间不宜过长,原因是
a.①②③ b.③①② c.②①③ d.①③②
(5)该实验热过滤操作时,过滤除去的杂质为
您最近一年使用:0次
名校
解题方法
3 . 某小组为探究含硫化合物(NH4)2S2O8的性质,设计如下实验探究(NH4)2S2O8的氧化性。实验操作:向小试管中加入2mL0.2mol/LKI溶液,并滴入两滴淀粉溶液,无明显变化,再加入少量0.2mol/L(NH4)2S2O8溶液,试管中溶液立即变蓝。取上层清液检验,证明溶液中存在 。
。
(1)(NH4)2S2O8与KI反应的离子方程式为___________ 。
已知:I2可与S2O 发生反应:2S2O
发生反应:2S2O +I2=S4O
+I2=S4O +2I-。为了进一步探究S2O
+2I-。为了进一步探究S2O 与KI的反应速率,小组同学设计下表实验:
与KI的反应速率,小组同学设计下表实验:
(2)上述实验Ⅱ中的V1=___________ ;V2=___________ 。
加入Na2S2O3溶液后溶液变蓝的时间明显增长,小组同学对此提出两种猜想:
猜想1:(NH4)2S2O8与KI反应的速率远低于I2与Na2S2O3反应的速率;
猜想2:(NH4)2S2O8先与Na2S2O3反应,Na2S2O3消耗完后才与I-反应。
为验证上述猜想,小组同学补充下表实验:
(3)验证猜想1的实验设计为___________ (填“实验Ⅲ”或“实验Ⅳ”下同)。
(4)实验Ⅲ中下层溶液显浅紫色的原因为___________ 。
(5)由上述实验可知___________ (填“猜想1”或“猜想2”)成立。
 。
。(1)(NH4)2S2O8与KI反应的离子方程式为
已知:I2可与S2O
 发生反应:2S2O
发生反应:2S2O +I2=S4O
+I2=S4O +2I-。为了进一步探究S2O
+2I-。为了进一步探究S2O 与KI的反应速率,小组同学设计下表实验:
与KI的反应速率,小组同学设计下表实验:| 试验编号 | 0.2mol/LKI溶液/mL | 0.01mol/LNa2S2O3溶液/mL | 蒸馏水/mL | 0.4%的淀粉溶液/滴 | 0.2mol/L(NH4)2S2O8溶液/mL | 变色时间/s |
| Ⅰ | 4.0 | 0 | 4.0 | 2 | 2.0 | 立即 |
| Ⅱ | 4.0 | 1.0 | V1 | 2 | V2 | 30 |
加入Na2S2O3溶液后溶液变蓝的时间明显增长,小组同学对此提出两种猜想:
猜想1:(NH4)2S2O8与KI反应的速率远低于I2与Na2S2O3反应的速率;
猜想2:(NH4)2S2O8先与Na2S2O3反应,Na2S2O3消耗完后才与I-反应。
为验证上述猜想,小组同学补充下表实验:
| 试验编号 | 0.2mol/LKI溶液/mL | 0.001mol/L碘水/mL | 0.01mol/LNa2S2O3溶液/mL | CCl4/mL | 0.4%的淀粉溶液/滴 | 0.2mol/L(NH4)2S2O8溶液/mL | 实验现象 |
| Ⅲ | 2 | 0 | 20 | 10 | 0 | 0.2 | 下层溶液显浅紫色 |
| Ⅳ | 0 | 5 | 20 | 0 | 2 | 20 | 溶液先变蓝,后迅速褪色,一段时间后又变蓝 |
(4)实验Ⅲ中下层溶液显浅紫色的原因为
(5)由上述实验可知
您最近一年使用:0次
4 . 已知在碱性溶液中可发生如下反应:2R(OH)3+3ClO﹣+4OH﹣=2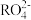 +3Cl﹣+5H2O。则
+3Cl﹣+5H2O。则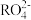 中R 的化合价是
中R 的化合价是
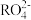 +3Cl﹣+5H2O。则
+3Cl﹣+5H2O。则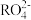 中R 的化合价是
中R 的化合价是| A.+3 | B.+4 | C.+6 | D.+5 |
您最近一年使用:0次
5 . 高锰酸钾生产过程中产生的废锰渣(主要成分为MnO2、KOH、MgO和Fe2O3)可用于制备MnSO4晶体,工艺流程如下:
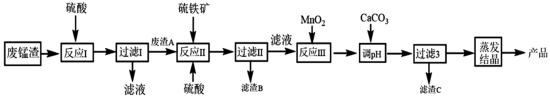
该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:
回答以下问题:
(1)MnSO4中阴离子的空间构型为___________ 、阳离子的价电子排布式为___________ 。
(2)提高“反应I”速率可采取的措施是___________ (除“加热”外,任写一种),滤渣A的主要成分为___________ (填化学式)。
(3)“反应II”中硫铁矿(FeS2)的作用为___________ 。
(4)“反应III”的离子方程式为___________ 。
(5)“调pH”步骤中,应调节pH不低于___________ 。

该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀pH | 2.10 | 7.45 | 9 27 27 | 9.60 |
| 完全沉淀pH | 3.20 | 8.95 | 10.87 | 11.13 |
(1)MnSO4中阴离子的空间构型为
(2)提高“反应I”速率可采取的措施是
(3)“反应II”中硫铁矿(FeS2)的作用为
(4)“反应III”的离子方程式为
(5)“调pH”步骤中,应调节pH不低于
您最近一年使用:0次
解题方法
6 . 锶(Sr)为第五周期IIA族元素,工业上常以天青石(主要成分为 ,含少量
,含少量 )为原料制备六水氯化锶(
)为原料制备六水氯化锶( ),生产流程如图所示(已知:“高温焙烧”时,
),生产流程如图所示(已知:“高温焙烧”时, 转化为SrS、BaS):
转化为SrS、BaS):

已知:25 ℃时, 的
的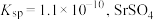 的
的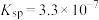 ;溶液中离子浓度小于或等于
;溶液中离子浓度小于或等于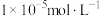 时,认为沉淀完全。
时,认为沉淀完全。
下列说法错误的是
 ,含少量
,含少量 )为原料制备六水氯化锶(
)为原料制备六水氯化锶( ),生产流程如图所示(已知:“高温焙烧”时,
),生产流程如图所示(已知:“高温焙烧”时, 转化为SrS、BaS):
转化为SrS、BaS):
已知:25 ℃时,
 的
的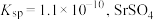 的
的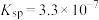 ;溶液中离子浓度小于或等于
;溶液中离子浓度小于或等于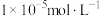 时,认为沉淀完全。
时,认为沉淀完全。下列说法错误的是
A.“高温焙烧”时 转化为SrS的化学方程式为 转化为SrS的化学方程式为 |
| B.“操作1”是蒸发浓缩、冷却结晶 |
C.为除去“溶液”中的 ,提高原料利用率,“滤液”中 ,提高原料利用率,“滤液”中 的浓度应小于 的浓度应小于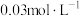 |
D.制取无水 时,一定要在无水氯化氢气流中加热 时,一定要在无水氯化氢气流中加热 至恒重 至恒重 |
您最近一年使用:0次
7 . 某反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3(不溶于水)、H2O、H2O2,已知该反应中H2O2只发生如下过程H2O2→O2.
(1)写出该反应的化学方程式:_____ 。
(2)该反应中氧化剂是_____ ,氧化产物是_____ 。
(3)产生1个O2,转移的电子的个数为_____ 个。
(4)用单线桥标出该反应中电子转移情况:_____ 。
(1)写出该反应的化学方程式:
(2)该反应中氧化剂是
(3)产生1个O2,转移的电子的个数为
(4)用单线桥标出该反应中电子转移情况:
您最近一年使用:0次
解题方法
8 . 某离子反应涉及H2O、ClO-、 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是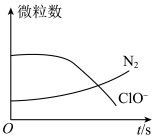
| A.该反应中Cl-为氧化产物 | B.消耗1mol还原剂微粒,转移6mol电子 |
C. 被ClO-氧化成N2 被ClO-氧化成N2 | D.该反应为非氧化还原反应 |
您最近一年使用:0次
2024-04-05更新
|
61次组卷
|
2卷引用:江苏省徐州市睢宁县第一中学2023-2024学年高一下学期5月月考化学试卷
名校
解题方法
9 . 控制、治理氮氧化物对大气的污染是改善大气质量的证要方面。
(1)火力发电厂的燃煤排烟中含大量的氮氧化物( ),可利用甲烷和
),可利用甲烷和 在一条件下反应消除其污染,那么
在一条件下反应消除其污染,那么 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
(2)在一密闭容器中发生反应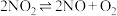 ,反应过程中
,反应过程中 的浓度随时间变化的情况如以下图所示。请回答:
的浓度随时间变化的情况如以下图所示。请回答:
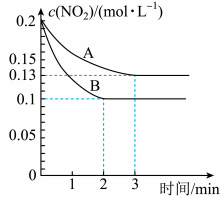
①依曲线A,反应在前3min内氧气的平均反应速率为___________ 。(保留三位有效数字)
②假设曲线A、B分别表示的是该反应在某不同条件下的反应情况,那么此条件是___________ 。(填“浓度”、“压强”、“温度”或“催化剂”)
③曲线A、B分别对应的反应平衡常数的大小关系是
___________  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(3)一定温度下,密闭容器中 可发生以下反应:
可发生以下反应:
 I
I
 Ⅱ
Ⅱ
那么反应I的平衡常数表达式为___________ 。假设达平衡时, ,
,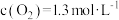 ,那么反应Ⅱ中
,那么反应Ⅱ中 的转化率为
的转化率为___________ , (g)的起始浓度不低于
(g)的起始浓度不低于___________  。
。
(1)火力发电厂的燃煤排烟中含大量的氮氧化物(
 ),可利用甲烷和
),可利用甲烷和 在一条件下反应消除其污染,那么
在一条件下反应消除其污染,那么 与
与 反应的化学方程式为
反应的化学方程式为(2)在一密闭容器中发生反应
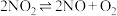 ,反应过程中
,反应过程中 的浓度随时间变化的情况如以下图所示。请回答:
的浓度随时间变化的情况如以下图所示。请回答:
①依曲线A,反应在前3min内氧气的平均反应速率为
②假设曲线A、B分别表示的是该反应在某不同条件下的反应情况,那么此条件是
③曲线A、B分别对应的反应平衡常数的大小关系是

 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)(3)一定温度下,密闭容器中
 可发生以下反应:
可发生以下反应: I
I Ⅱ
Ⅱ那么反应I的平衡常数表达式为
 ,
,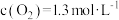 ,那么反应Ⅱ中
,那么反应Ⅱ中 的转化率为
的转化率为 (g)的起始浓度不低于
(g)的起始浓度不低于 。
。
您最近一年使用:0次
2024-04-05更新
|
69次组卷
|
2卷引用:湖南省常德市汉寿县第一中学2023-2024学年高三下学期3月月考化学试题
解题方法
10 . 废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备ZnSO4·7H2O和CuSO4·5H2O的部分实验步骤如下:
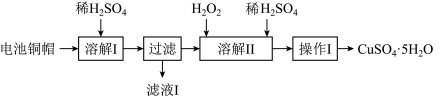
(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是_______ (任写一种方法)。
(2)从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为_______ 、_______ 、过滤、冰水洗涤、低温干燥。
(3)仔细分析流程,在“溶解II”步骤中,发生反应的化学方程式为_______ (用双线桥标出电子转移的方向和数目)。
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol/LNa2S2O3标准溶液至滴定终点,消耗Na2S2O3溶液25.00mL。
已知:2CuSO4+4KI=2CuI(白色)+I2+2K2SO4;2Na2S2O3+I2=2NaI+Na2S4O6
请依据实验数据计算样品中CuSO4·5H2O的质量分数_______ (写出计算过程,结果用百分数表示,小数点后保留1位有效数字)。

(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是
(2)从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为
(3)仔细分析流程,在“溶解II”步骤中,发生反应的化学方程式为
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol/LNa2S2O3标准溶液至滴定终点,消耗Na2S2O3溶液25.00mL。
已知:2CuSO4+4KI=2CuI(白色)+I2+2K2SO4;2Na2S2O3+I2=2NaI+Na2S4O6
请依据实验数据计算样品中CuSO4·5H2O的质量分数
您最近一年使用:0次



