名校
解题方法
1 . LiMn2O4作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO3,含有少量Si、Fe、Ni、Al等元素)制备LiMn2O4的流程如图:

已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为________ 。为提高溶矿速率,可采取的措施________ (举1例)。
(2)加入少量MnO2的作用是________ 。不宜使用H2O2替代MnO2,原因是________ 。
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=________ mol•L-1;用石灰乳调节至pH≈7,除去的金属离子是________ 。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有________ 。
(5)煅烧窑中,生成LiMn2O4反应的化学方程式是________ 。

已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为
(2)加入少量MnO2的作用是
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有
(5)煅烧窑中,生成LiMn2O4反应的化学方程式是
您最近一年使用:0次
2023-09-15更新
|
231次组卷
|
5卷引用:黑龙江省七台河市勃利县高级中学2023-2024学年高三上学期9月月考化学试题
名校
解题方法
2 . 科学、安全、有效和合理地开发自然资源,对生产、生活有重要价值。请回答下列问题:
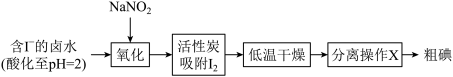
(1)活性炭吸附法是工业提取碘的方法之一,其流程如下:
已知: 时,Ⅰ.
时,Ⅰ. 溶液只能将
溶液只能将 氧化为
氧化为 ,同时生成NO
,同时生成NO
Ⅱ.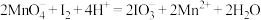
①氧化过程的离子方程式为___________ 。
②根据 的特性,分离操作X为
的特性,分离操作X为___________ ,冷凝得到粗碘。
③酸性 是常用的强氧化剂,但该方法中却选择了价格较高的
是常用的强氧化剂,但该方法中却选择了价格较高的 ,原因是
,原因是___________ 。
④活性炭上吸附的 还能用浓
还能用浓 溶液吸收,每吸收
溶液吸收,每吸收 转移5mol电子,该反应的离子方程式是
转移5mol电子,该反应的离子方程式是___________ 。
(2)以金红石(主要成分为 )为原料,制取Ti的工艺流程如图所示:
)为原料,制取Ti的工艺流程如图所示:
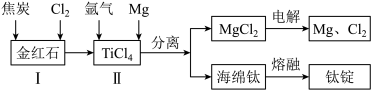
①Ⅰ在高温条件下进行,产物中有一种可燃性无色气体。Ⅰ中反应的化学方程式为___________ 。
②Ⅱ中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为___________ ℃。

③Ⅱ中氩气的作用是___________ 。
④海绵钛除杂时得到的 可以循环使用,在上述工艺流程中可循环使用的物质还有
可以循环使用,在上述工艺流程中可循环使用的物质还有___________ (填化学式)。
(1)活性炭吸附法是工业提取碘的方法之一,其流程如下:

已知:
 时,Ⅰ.
时,Ⅰ. 溶液只能将
溶液只能将 氧化为
氧化为 ,同时生成NO
,同时生成NOⅡ.
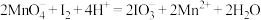
①氧化过程的离子方程式为
②根据
 的特性,分离操作X为
的特性,分离操作X为③酸性
 是常用的强氧化剂,但该方法中却选择了价格较高的
是常用的强氧化剂,但该方法中却选择了价格较高的 ,原因是
,原因是④活性炭上吸附的
 还能用浓
还能用浓 溶液吸收,每吸收
溶液吸收,每吸收 转移5mol电子,该反应的离子方程式是
转移5mol电子,该反应的离子方程式是(2)以金红石(主要成分为
 )为原料,制取Ti的工艺流程如图所示:
)为原料,制取Ti的工艺流程如图所示:
①Ⅰ在高温条件下进行,产物中有一种可燃性无色气体。Ⅰ中反应的化学方程式为
②Ⅱ中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为

③Ⅱ中氩气的作用是
④海绵钛除杂时得到的
 可以循环使用,在上述工艺流程中可循环使用的物质还有
可以循环使用,在上述工艺流程中可循环使用的物质还有
您最近一年使用:0次
2023-05-23更新
|
660次组卷
|
3卷引用:黑龙江省勃利县高级中学2022-2023学年高一下学期5月月考化学试题
名校
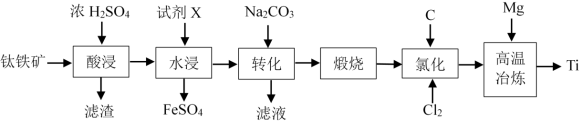
3 . 金属钛(Ti)广泛应用于航空、军工、医疗等领域。以钛铁矿(主要含有FeTiO3及少量SiO2、FeO、Fe2O3、CaO)制备金属Ti的工艺流程如下:
(1)“酸浸”前钛铁矿需要粉碎研磨,其目的是_______ 。
(2)FeTiO3中Ti的化合价为_______ ,“滤渣”中主要含有SiO2和_______ (填化学式)。
(3)“酸浸”中发生主要反应的化学方程式为_______ 。
(4)试剂X为_______ (填化学式),其作用是_______ 。
(5)“高温冶炼”过程需在氩气气氛中进行,其原因是_______ 。
(1)“酸浸”前钛铁矿需要粉碎研磨,其目的是
(2)FeTiO3中Ti的化合价为
(3)“酸浸”中发生主要反应的化学方程式为
(4)试剂X为
(5)“高温冶炼”过程需在氩气气氛中进行,其原因是
您最近一年使用:0次
2023-05-05更新
|
602次组卷
|
3卷引用:黑龙江省七台河市勃利县高级中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
4 . 工业上常用添加Fe2+EDTA的溶液处理氮氧化物。某实验小组欲探究60 ℃下,20 mmol·L-1 Fe2+EDTA溶液脱除NO的能力
Ⅰ.NO的吸收。取250 mL 20 mmol·L-1 Fe2+EDTA溶液于三颈烧瓶中,按如图所示连接仪器。

(1)装置A中盛放浓硝酸的仪器名称为___________ ,导管m的作用为___________
(2)滴加浓硝酸前,需要先打开K,通入一段时间氮气,目的为___________
(3)对C装置采用的合适加热方式是___________
(4)装置D中酸性KMnO4溶液可将NO氧化为NO ,发生反应的离子方程式为
,发生反应的离子方程式为___________
Ⅱ.NO吸收效果的检测。实验步骤如下:
a.取装置C中的吸收液100 mL,加入H2O2溶液,将Fe2+EDTA吸收液络合的NO及Fe2+氧化为NO 及Fe3+,微热使剩余的H2O2完全分解
及Fe3+,微热使剩余的H2O2完全分解
b.在酸性环境下,向其中加入V1 mL物质的量浓度为c1 mol·L-1的Fe2+(足量),将NO 转化为NO
转化为NO
c.用c2 mol·L-1K2Cr2O7标准液滴定b中溶液至终点,消耗标准液V2 mL
(5)Fe2+EDTA吸收液的吸收能力为___________ g(用含字母的代数式表示)NO/100 mL吸收液
(6)若步骤c滴定终点时俯视读数,则测定结果将___________ (填“偏高”“偏低”或“不变”)
Ⅰ.NO的吸收。取250 mL 20 mmol·L-1 Fe2+EDTA溶液于三颈烧瓶中,按如图所示连接仪器。

(1)装置A中盛放浓硝酸的仪器名称为
(2)滴加浓硝酸前,需要先打开K,通入一段时间氮气,目的为
(3)对C装置采用的合适加热方式是
(4)装置D中酸性KMnO4溶液可将NO氧化为NO
 ,发生反应的离子方程式为
,发生反应的离子方程式为Ⅱ.NO吸收效果的检测。实验步骤如下:
a.取装置C中的吸收液100 mL,加入H2O2溶液,将Fe2+EDTA吸收液络合的NO及Fe2+氧化为NO
 及Fe3+,微热使剩余的H2O2完全分解
及Fe3+,微热使剩余的H2O2完全分解b.在酸性环境下,向其中加入V1 mL物质的量浓度为c1 mol·L-1的Fe2+(足量),将NO
 转化为NO
转化为NOc.用c2 mol·L-1K2Cr2O7标准液滴定b中溶液至终点,消耗标准液V2 mL
(5)Fe2+EDTA吸收液的吸收能力为
(6)若步骤c滴定终点时俯视读数,则测定结果将
您最近一年使用:0次



