解题方法
1 . 某化学小组探究硫酸铁铵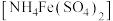 与
与 、
、 的反应。
的反应。
已知: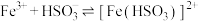 (棕红)
(棕红)
(1)①实验Ⅰ中产生红褐色沉淀与气泡的离子方程式为___________ 。
②由实验Ⅰ可得出与 结合的能力:
结合的能力:
___________  (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。
(2)资料显示, 可以氧化
可以氧化 。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。
。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。
①实验Ⅲ中 与
与 反应生成
反应生成 的离子方程式为
的离子方程式为___________ 。
②结合化学反应原理解释实验Ⅱ、Ⅳ中现象存在差异的可能原因___________ 。
(3)针对实验Ⅲ、Ⅳ的现象差异,小组同学提出猜想:pH影响了 的氧化性或
的氧化性或 的还原性,并实施实验。
的还原性,并实施实验。
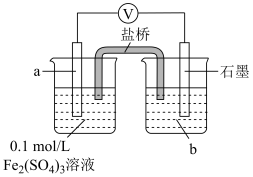
①a、b分别是___________ 。
②结合电极反应解释步骤3中电压表示数减小的原因___________ 。
③补充实验Ⅵ:向实验Ⅱ得到的棕红色液体中加入3滴10%稀硫酸,棕红色迅速变黄,检测到 。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因
。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因___________ 。
(4)综合以上实验,盐溶液间反应的多样性与___________ 有关。
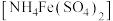 与
与 、
、 的反应。
的反应。| 实验 | 操作 | 现象 |
| Ⅰ | 向2mL 溶液(pH=2.03)中逐滴加入 溶液(pH=2.03)中逐滴加入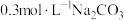 溶液 溶液 | 迅速产生大量红褐色沉淀和大量气泡;继续滴加,当气泡量明显减少时,试管口的湿润红色石蕊试纸开始逐渐变蓝 |
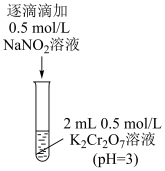
| Ⅱ | 向2mL 溶液(pH=2.03)中逐滴加入 溶液(pH=2.03)中逐滴加入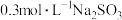 溶液 溶液 | 溶液立即变棕红(无丁达尔现象),继续滴加 溶液至过量,溶液依然为棕红色,放置两天无明显变化 溶液至过量,溶液依然为棕红色,放置两天无明显变化 |
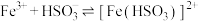 (棕红)
(棕红)(1)①实验Ⅰ中产生红褐色沉淀与气泡的离子方程式为
②由实验Ⅰ可得出与
 结合的能力:
结合的能力:
 (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。(2)资料显示,
 可以氧化
可以氧化 。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。
。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。| 实验 | 操作 | 现象 |
| Ⅲ | 向2mL 溶液(pH=1.78)中加入0.5mL 溶液(pH=1.78)中加入0.5mL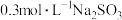 溶液 溶液 | 溶液立即变棕红色,约2小时后,棕红色变为黄色,检测到 |
| Ⅳ | 向2mL 溶液(pH=2.03)中加入0.5mL 溶液(pH=2.03)中加入0.5mL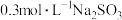 溶液 溶液 | 溶液立即变棕红色,约5小时后,棕红色变为黄色,检测到 |
 与
与 反应生成
反应生成 的离子方程式为
的离子方程式为②结合化学反应原理解释实验Ⅱ、Ⅳ中现象存在差异的可能原因
(3)针对实验Ⅲ、Ⅳ的现象差异,小组同学提出猜想:pH影响了
 的氧化性或
的氧化性或 的还原性,并实施实验。
的还原性,并实施实验。| 实验 | 实验装置 | 实验步骤及现象 |
| Ⅴ |
| 1.按如图搭好装置,接通电路,电压表读数为0.6V; 2.向a电极附近滴加3滴10%稀硫酸,电压表读数不变; 3.向石墨电极附近滴加3滴10%稀硫酸,电压表读数变为0.5V。 |
②结合电极反应解释步骤3中电压表示数减小的原因
③补充实验Ⅵ:向实验Ⅱ得到的棕红色液体中加入3滴10%稀硫酸,棕红色迅速变黄,检测到
 。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因
。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因(4)综合以上实验,盐溶液间反应的多样性与
您最近半年使用:0次
解题方法
2 . 从某工厂铜电解车间产生的难溶副产物黑铜泥(主要成分为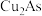 和
和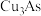 )和废水车间产生的含砷废渣(主要成分为
)和废水车间产生的含砷废渣(主要成分为 )中回收铜和砷的一种流程示意图如下。
)中回收铜和砷的一种流程示意图如下。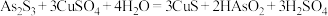 ;
;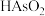 易分解生成微溶于水的
易分解生成微溶于水的 ;随着硫酸浓度的增大,
;随着硫酸浓度的增大, 在硫酸溶液中的溶解度变小。
在硫酸溶液中的溶解度变小。
(1)升温能加快氧化浸出的速率。温度过高时,浸出速率反而会下降,原因是___________ 。
(2)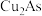 和
和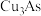 被氧化为
被氧化为 和
和 。
。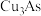 被氧化的离子方程式为
被氧化的离子方程式为___________ 。
(3)沉铜前,需要对氧化浸出液进行稀释。稀释倍数对沉铜的影响如下图所示。___________ 。
(4)上述流程中可循环使用的物质是___________ 。
(5)粗三氧化二砷中砷含量的测定。
ⅰ.取0.1g样品于锥形瓶中,加入NaOH溶液,使样品完全溶解;
ⅱ.加入适量乙酸铅溶液,消除-2价硫的干扰;
ⅲ.用稀硫酸调pH=8,加入3g碳酸氢钠和少量淀粉溶液;
ⅳ.用 碘标准溶液(溶质按
碘标准溶液(溶质按 计)滴定,将砷氧化至最高价态。到达滴定终点时,消耗碘标准溶液VmL。
计)滴定,将砷氧化至最高价态。到达滴定终点时,消耗碘标准溶液VmL。
已知:样品中砷只以+3价的形式存在。
①若样品中有-2价硫,没有步骤ⅱ,测定结果将___________ (填“偏大”“偏小”或“不变”)。
②样品中砷的质量分数为___________ 。
③步骤ⅲ中加入碳酸氢钠,能保持滴定过程中溶液pH基本稳定,结合化学用语解释原因___________ 。
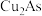 和
和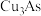 )和废水车间产生的含砷废渣(主要成分为
)和废水车间产生的含砷废渣(主要成分为 )中回收铜和砷的一种流程示意图如下。
)中回收铜和砷的一种流程示意图如下。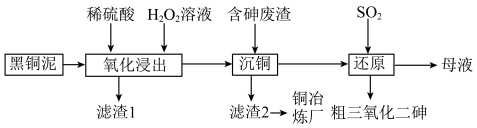
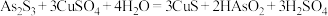 ;
;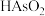 易分解生成微溶于水的
易分解生成微溶于水的 ;随着硫酸浓度的增大,
;随着硫酸浓度的增大, 在硫酸溶液中的溶解度变小。
在硫酸溶液中的溶解度变小。(1)升温能加快氧化浸出的速率。温度过高时,浸出速率反而会下降,原因是
(2)
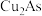 和
和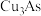 被氧化为
被氧化为 和
和 。
。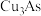 被氧化的离子方程式为
被氧化的离子方程式为(3)沉铜前,需要对氧化浸出液进行稀释。稀释倍数对沉铜的影响如下图所示。
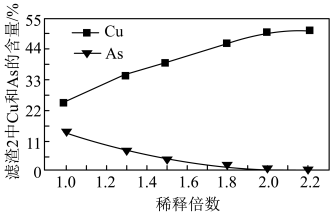
(4)上述流程中可循环使用的物质是
(5)粗三氧化二砷中砷含量的测定。
ⅰ.取0.1g样品于锥形瓶中,加入NaOH溶液,使样品完全溶解;
ⅱ.加入适量乙酸铅溶液,消除-2价硫的干扰;
ⅲ.用稀硫酸调pH=8,加入3g碳酸氢钠和少量淀粉溶液;
ⅳ.用
 碘标准溶液(溶质按
碘标准溶液(溶质按 计)滴定,将砷氧化至最高价态。到达滴定终点时,消耗碘标准溶液VmL。
计)滴定,将砷氧化至最高价态。到达滴定终点时,消耗碘标准溶液VmL。已知:样品中砷只以+3价的形式存在。
①若样品中有-2价硫,没有步骤ⅱ,测定结果将
②样品中砷的质量分数为
③步骤ⅲ中加入碳酸氢钠,能保持滴定过程中溶液pH基本稳定,结合化学用语解释原因
您最近半年使用:0次
名校
解题方法
3 . 将足量SO2通入AgNO3溶液中,产生沉淀。探究反应原理及沉淀成分,装置如下(加热,夹持等装置略)。
资料:i.Ag2SO4微溶于水;Ag2SO3难溶于水。
ii.Ag2SO4、Ag2SO3均溶于氨水。___________ 。
②B的作用是___________ 。
(2)探究沉淀成分。实验发现,沉淀的颜色与取样时间有关,对比实验记录如下:
推测白色沉淀(t1)可能为Ag2SO4、Ag2SO3或混合物。探究如下:
①试剂a是___________ 。
②产生白色沉淀Y的原因是___________ 。
(3)推测灰黑色沉淀(t2)含Ag。探究如下:
取灰黑色沉淀,加入氨水,部分沉淀溶解,过滤,洗涤。向洗净的沉淀中加入浓HNO3,证实沉淀含Ag。现象是___________ 。
(4)通过检测 探究产生Ag的原因。
探究产生Ag的原因。
①实验:___________ 。(用化学方程式表示)
②t1时,C中产生白色沉淀的离子方程式是___________ 。
综上可知,化学反应的产物与反应速率有关。
资料:i.Ag2SO4微溶于水;Ag2SO3难溶于水。
ii.Ag2SO4、Ag2SO3均溶于氨水。
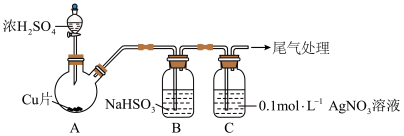
②B的作用是
(2)探究沉淀成分。实验发现,沉淀的颜色与取样时间有关,对比实验记录如下:
| 时间 | 反应开始时(t1) | 一段时间后(t2) | 较长时间后(t3) |
| 颜色 | 白色 | 灰黑色 | 灰黑色加深 |

①试剂a是
②产生白色沉淀Y的原因是
(3)推测灰黑色沉淀(t2)含Ag。探究如下:
取灰黑色沉淀,加入氨水,部分沉淀溶解,过滤,洗涤。向洗净的沉淀中加入浓HNO3,证实沉淀含Ag。现象是
(4)通过检测
 探究产生Ag的原因。
探究产生Ag的原因。①实验:
 (已排除O2的影响)
(已排除O2的影响)
②t1时,C中产生白色沉淀的离子方程式是
综上可知,化学反应的产物与反应速率有关。
您最近半年使用:0次
解题方法
4 . 处理废旧铅酸电池中的含铅浆液(主要含 、
、 )的一种流程示意图如下。
)的一种流程示意图如下。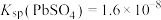 ,
,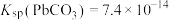 ,
,
ii. 和
和 均为可溶于水的强电解质。
均为可溶于水的强电解质。
(1)向含铅浆液中加入过量的 实现转化脱硫。
实现转化脱硫。
①结合离子方程式说明 溶液显碱性的原因:
溶液显碱性的原因:________ 。
②转化脱硫反应的离子方程式是________ 。
③检验 ,证明固体a已洗涤干净,操作和现象是
,证明固体a已洗涤干净,操作和现象是________ 。
(2)受热时, 分解产生
分解产生 ,最终生成PbO。
,最终生成PbO。
将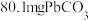 样品置于氩气中加热,316℃时,剩余固体的质量为713mg,此时固体中
样品置于氩气中加热,316℃时,剩余固体的质量为713mg,此时固体中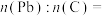
________ 。[ 、
、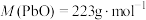 ]
]
(3)“还原”时加入 溶液,反应的化学方程式是
溶液,反应的化学方程式是________ 。
(4)“浸出”反应的离子方程式是________ 。
(5)以惰性电极电解 溶液制得Pb,溶液b中可循环利用的物质是
溶液制得Pb,溶液b中可循环利用的物质是________ 。
 、
、 )的一种流程示意图如下。
)的一种流程示意图如下。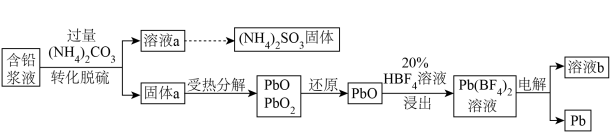
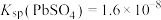 ,
,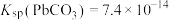 ,
,ii.
 和
和 均为可溶于水的强电解质。
均为可溶于水的强电解质。(1)向含铅浆液中加入过量的
 实现转化脱硫。
实现转化脱硫。①结合离子方程式说明
 溶液显碱性的原因:
溶液显碱性的原因:②转化脱硫反应的离子方程式是
③检验
 ,证明固体a已洗涤干净,操作和现象是
,证明固体a已洗涤干净,操作和现象是(2)受热时,
 分解产生
分解产生 ,最终生成PbO。
,最终生成PbO。将
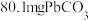 样品置于氩气中加热,316℃时,剩余固体的质量为713mg,此时固体中
样品置于氩气中加热,316℃时,剩余固体的质量为713mg,此时固体中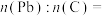
 、
、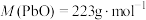 ]
](3)“还原”时加入
 溶液,反应的化学方程式是
溶液,反应的化学方程式是(4)“浸出”反应的离子方程式是
(5)以惰性电极电解
 溶液制得Pb,溶液b中可循环利用的物质是
溶液制得Pb,溶液b中可循环利用的物质是
您最近半年使用:0次
解题方法
5 . 废电池中含磷酸铁锂,提锂后的废渣主要含 、
、 和金属铝等,以废渣为原料制备电池级
和金属铝等,以废渣为原料制备电池级 的一种工艺流程如下。
的一种工艺流程如下。 、
、 均难溶于水。
均难溶于水。
ii.将 转化为
转化为 有利于更彻底除去
有利于更彻底除去 。
。
(1)酸浸前,将废渣粉碎的目的是________ 。
(2)从平衡移动的角度解释加入硝酸溶解 的原因:
的原因:________ 。
(3)在酸浸液中加入 进行电解,电解原理的示意图如下图所示,电解过程中
进行电解,电解原理的示意图如下图所示,电解过程中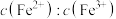 不断增大。结合电极反应说明
不断增大。结合电极反应说明 在电解中的作用:
在电解中的作用:________ 。 。向“氧化”后的溶液中加入HCHO,加热,产生NO和
。向“氧化”后的溶液中加入HCHO,加热,产生NO和 ,当液面上方不再产生红棕色气体时,静置一段时间,产生
,当液面上方不再产生红棕色气体时,静置一段时间,产生 沉淀。阐述此过程中HCHO的作用:
沉淀。阐述此过程中HCHO的作用:________ 。
(5)过滤得到电池级 后,滤液中主要的金属阳离子有
后,滤液中主要的金属阳离子有________ 。
(6)磷酸铁锂-石墨电池的总反应: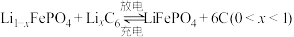 。
。
①高温条件下, 、葡萄糖(
、葡萄糖( )和
)和 可制备电极材料
可制备电极材料 ,同时生成CO和
,同时生成CO和 ,反应的化学方程式是
,反应的化学方程式是________ 。
②放电时负极的电极反应式是________ 。
 、
、 和金属铝等,以废渣为原料制备电池级
和金属铝等,以废渣为原料制备电池级 的一种工艺流程如下。
的一种工艺流程如下。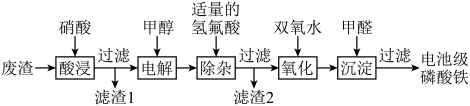
 、
、 均难溶于水。
均难溶于水。ii.将
 转化为
转化为 有利于更彻底除去
有利于更彻底除去 。
。(1)酸浸前,将废渣粉碎的目的是
(2)从平衡移动的角度解释加入硝酸溶解
 的原因:
的原因:(3)在酸浸液中加入
 进行电解,电解原理的示意图如下图所示,电解过程中
进行电解,电解原理的示意图如下图所示,电解过程中 不断增大。结合电极反应说明
不断增大。结合电极反应说明 在电解中的作用:
在电解中的作用: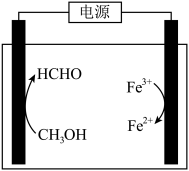
 。向“氧化”后的溶液中加入HCHO,加热,产生NO和
。向“氧化”后的溶液中加入HCHO,加热,产生NO和 ,当液面上方不再产生红棕色气体时,静置一段时间,产生
,当液面上方不再产生红棕色气体时,静置一段时间,产生 沉淀。阐述此过程中HCHO的作用:
沉淀。阐述此过程中HCHO的作用:(5)过滤得到电池级
 后,滤液中主要的金属阳离子有
后,滤液中主要的金属阳离子有(6)磷酸铁锂-石墨电池的总反应:
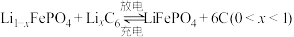 。
。①高温条件下,
 、葡萄糖(
、葡萄糖( )和
)和 可制备电极材料
可制备电极材料 ,同时生成CO和
,同时生成CO和 ,反应的化学方程式是
,反应的化学方程式是②放电时负极的电极反应式是
您最近半年使用:0次
6 . 某小组探究 的制备。
的制备。
已知:i. (绿色,不溶于水)、
(绿色,不溶于水)、 (绿色)、
(绿色)、 (灰绿色,不溶于水)、
(灰绿色,不溶于水)、
 (玫瑰红色)、
(玫瑰红色)、 (橙色)、
(橙色)、 (黄色)
(黄色)
ii. 是一种弱酸,易分解:
是一种弱酸,易分解: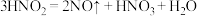
将 固体和
固体和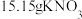 固体(物质的量之比为1:3)与过量的
固体(物质的量之比为1:3)与过量的 固体混合,高温煅烧得含
固体混合,高温煅烧得含 的黄色固体,反应如下:
的黄色固体,反应如下:
 。
。
(1) 受热分解转化为
受热分解转化为 ,反应的化学方程式是
,反应的化学方程式是________ 。
(2) 转化为
转化为 ,进行实验Ⅰ:
,进行实验Ⅰ: ,
, 转化为
转化为 反应的离子方程式是
反应的离子方程式是________ 。
②无色气泡中的气体有________ 。
③资料显示溶液变为棕黑色是 与
与 混合所致。设计实验:取少量棕黑色溶液于试管中,逐滴加入NaOH溶液,生成灰绿色沉淀,溶液变为黄色,至不再生成沉淀时,静置,取上清液
混合所致。设计实验:取少量棕黑色溶液于试管中,逐滴加入NaOH溶液,生成灰绿色沉淀,溶液变为黄色,至不再生成沉淀时,静置,取上清液________ (填操作和现象),证实溶液中存在 与
与 。
。
(3)探究 的来源
的来源
来源1:……
来源2:酸性环境中, 与
与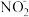 发生氧化还原反应生成
发生氧化还原反应生成 。
。
①来源1:________ 。
②进行实验Ⅱ证实来源2成立,实验操作及现象如下:
溶液由橙色变为绿色、绿色变为玫瑰红色的反应的离子方程式:________ 、________ 。
从平衡移动的角度解释溶液由玫瑰红色变为绿色的原因:________ 。
(4)为避免 转化为
转化为 的过程中产生
的过程中产生 ,进行实验Ⅲ。
,进行实验Ⅲ。
将煅烧后的黄色固体浸泡于100mL水中,过滤后向滤液中加入醋酸溶液,调至pH=5,溶液变为橙色。
实验Ⅲ中溶液的颜色与实验Ⅰ中的不同的原因可能是________ 。
 的制备。
的制备。已知:i.
 (绿色,不溶于水)、
(绿色,不溶于水)、 (绿色)、
(绿色)、 (灰绿色,不溶于水)、
(灰绿色,不溶于水)、 (玫瑰红色)、
(玫瑰红色)、 (橙色)、
(橙色)、 (黄色)
(黄色)ii.
 是一种弱酸,易分解:
是一种弱酸,易分解: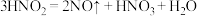
将
 固体和
固体和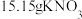 固体(物质的量之比为1:3)与过量的
固体(物质的量之比为1:3)与过量的 固体混合,高温煅烧得含
固体混合,高温煅烧得含 的黄色固体,反应如下:
的黄色固体,反应如下: 。
。(1)
 受热分解转化为
受热分解转化为 ,反应的化学方程式是
,反应的化学方程式是(2)
 转化为
转化为 ,进行实验Ⅰ:
,进行实验Ⅰ: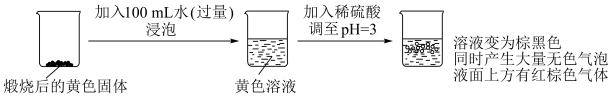
 ,
, 转化为
转化为 反应的离子方程式是
反应的离子方程式是②无色气泡中的气体有
③资料显示溶液变为棕黑色是
 与
与 混合所致。设计实验:取少量棕黑色溶液于试管中,逐滴加入NaOH溶液,生成灰绿色沉淀,溶液变为黄色,至不再生成沉淀时,静置,取上清液
混合所致。设计实验:取少量棕黑色溶液于试管中,逐滴加入NaOH溶液,生成灰绿色沉淀,溶液变为黄色,至不再生成沉淀时,静置,取上清液 与
与 。
。(3)探究
 的来源
的来源来源1:……
来源2:酸性环境中,
 与
与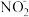 发生氧化还原反应生成
发生氧化还原反应生成 。
。①来源1:
②进行实验Ⅱ证实来源2成立,实验操作及现象如下:
实验操作 | 实验现象 |
| 溶液由橙色逐渐变为棕黑色,进而变为绿色,过程中无红棕色气体产生。 继续加入  溶液,溶液变为玫瑰红色,加入 溶液,溶液变为玫瑰红色,加入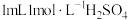 溶液后,溶液恢复绿色。 溶液后,溶液恢复绿色。 |
从平衡移动的角度解释溶液由玫瑰红色变为绿色的原因:
(4)为避免
 转化为
转化为 的过程中产生
的过程中产生 ,进行实验Ⅲ。
,进行实验Ⅲ。将煅烧后的黄色固体浸泡于100mL水中,过滤后向滤液中加入醋酸溶液,调至pH=5,溶液变为橙色。
实验Ⅲ中溶液的颜色与实验Ⅰ中的不同的原因可能是
您最近半年使用:0次
名校
7 . 实验室研究从医用废感光胶片中回收银的方法。
(1)银的浸出 溶液与
溶液与 溶液直接混合能发生氧化还原反应:
溶液直接混合能发生氧化还原反应:
ii. 。
。
① 溶液将胶片上的单质银转化为
溶液将胶片上的单质银转化为 ,其离子方程式是
,其离子方程式是___________ 。
② 溶液能溶解
溶液能溶解 并得到含
并得到含 的浸出液。结合平衡移动原理解释
的浸出液。结合平衡移动原理解释 溶解的原因:
溶解的原因:___________ 。
Ⅱ.一步法:用水溶解 和乙二胺四乙酸二钠(用
和乙二胺四乙酸二钠(用 表示)的混合固体,调节
表示)的混合固体,调节 形成
形成 溶液,再加入一定量
溶液,再加入一定量 ,配成浸取液。将废感光胶片浸入浸取液中,发生反应:
,配成浸取液。将废感光胶片浸入浸取液中,发生反应:
 。
。
③从物质氧化性或还原性的角度分析加入 的作用:
的作用:___________ 。
(2)银的还原
调节(1)所得浸出液 ,向其中加入
,向其中加入 溶液(B的化合价为
溶液(B的化合价为 )至不再产生黑色沉淀,过滤得到粗银:滤液中的
)至不再产生黑色沉淀,过滤得到粗银:滤液中的 可以循环使用。补全离子方程式:
可以循环使用。补全离子方程式:___________ 。

(3)银浸出率的测定
称取 洗净干燥的原胶片,灼烧灰化后用
洗净干燥的原胶片,灼烧灰化后用 溶解,过滤。滤液用
溶解,过滤。滤液用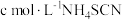 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液 。另取
。另取 洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗
洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗 标准溶液
标准溶液 。(已知:
。(已知: )
)
银的浸出率
___________ (列出计算表达式)。
(1)银的浸出
I、两步法:
 溶液与
溶液与 溶液直接混合能发生氧化还原反应:
溶液直接混合能发生氧化还原反应:ii.
 。
。①
 溶液将胶片上的单质银转化为
溶液将胶片上的单质银转化为 ,其离子方程式是
,其离子方程式是②
 溶液能溶解
溶液能溶解 并得到含
并得到含 的浸出液。结合平衡移动原理解释
的浸出液。结合平衡移动原理解释 溶解的原因:
溶解的原因:Ⅱ.一步法:用水溶解
 和乙二胺四乙酸二钠(用
和乙二胺四乙酸二钠(用 表示)的混合固体,调节
表示)的混合固体,调节 形成
形成 溶液,再加入一定量
溶液,再加入一定量 ,配成浸取液。将废感光胶片浸入浸取液中,发生反应:
,配成浸取液。将废感光胶片浸入浸取液中,发生反应: 。
。③从物质氧化性或还原性的角度分析加入
 的作用:
的作用:(2)银的还原
调节(1)所得浸出液
 ,向其中加入
,向其中加入 溶液(B的化合价为
溶液(B的化合价为 )至不再产生黑色沉淀,过滤得到粗银:滤液中的
)至不再产生黑色沉淀,过滤得到粗银:滤液中的 可以循环使用。补全离子方程式:
可以循环使用。补全离子方程式:
(3)银浸出率的测定
称取
 洗净干燥的原胶片,灼烧灰化后用
洗净干燥的原胶片,灼烧灰化后用 溶解,过滤。滤液用
溶解,过滤。滤液用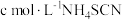 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液 。另取
。另取 洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗
洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗 标准溶液
标准溶液 。(已知:
。(已知: )
)银的浸出率

您最近半年使用:0次
名校
解题方法
8 . 将足量SO2通入AgNO3溶液中,产生沉淀。探究反应原理及沉淀成分,装置如下(加热、夹持等装置略)。
资料:ⅰ.Ag2SO4微溶于水;Ag2SO3难溶于水。
ⅱ.Ag2SO4、Ag2SO3均溶于氨水。___________ 。
②用NaOH溶液吸收尾气中的SO2,产物是___________ 。
(2)探究沉淀成分。实验发现,沉淀的颜色与取样时间有关,对比实验记录如下:
推测白色沉淀(t1)可能为Ag2SO4、Ag2SO3或二者混合物。探究如下:
①t1时,C中产生白色沉淀的离子方程式是___________ 。
②试剂a是___________ 。
③产生白色沉淀Y的原因是___________ 。
(3)推测灰黑色沉淀(t2)含Ag。探究如下:
取灰黑色沉淀,加入氨水,部分沉淀溶解,过滤。向滤出的沉淀中加入浓HNO3,证实沉淀含Ag。现象是___________ 。
(4)通过检测SO 探究产生Ag的原因。
探究产生Ag的原因。___________ 。(用化学方程式表示)
综上可知,化学反应的产物与反应速率和限度有关。
资料:ⅰ.Ag2SO4微溶于水;Ag2SO3难溶于水。
ⅱ.Ag2SO4、Ag2SO3均溶于氨水。

②用NaOH溶液吸收尾气中的SO2,产物是
(2)探究沉淀成分。实验发现,沉淀的颜色与取样时间有关,对比实验记录如下:
| 时间 | 反应开始时(t1) | 一段时间后(t2) | 较长时间后(t3) |
| 颜色 | 白色 | 灰黑色 | 灰黑色加深 |

①t1时,C中产生白色沉淀的离子方程式是
②试剂a是
③产生白色沉淀Y的原因是
(3)推测灰黑色沉淀(t2)含Ag。探究如下:
取灰黑色沉淀,加入氨水,部分沉淀溶解,过滤。向滤出的沉淀中加入浓HNO3,证实沉淀含Ag。现象是
(4)通过检测SO
 探究产生Ag的原因。
探究产生Ag的原因。实验: (已排除O2的影响)
(已排除O2的影响)
综上可知,化学反应的产物与反应速率和限度有关。
您最近半年使用:0次
解题方法
9 .  是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。
【 的制备】
的制备】
(1)用下图装置制备 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是___________ 。 ;
;___________ 。
【 的性质探究】
的性质探究】
资料:i. 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成
,在近中性条件下被还原成 。
。
ii.单质硫可溶于 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。
某小组研究 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。
(3)①甲同学取实验Ⅰ中少量溶液进行实验,检测有 ,得出
,得出 被氧化成
被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是___________ 。
②同学讨论后,设计了如下实验,证实该条件下 的确可以将
的确可以将 氧化成
氧化成 。
。___________ 。
b.连通后电流计指针偏转,一段时间后,___________ (填操作和现象)。
(4)实验I的现象与资料i不相符,其原因是新生成的产物( )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是___________ 。
(5)实验II的现象与资料也不完全相符,丙同学猜想原因与(4)中所述原因相似,其原因是___________ ,请设计验证此猜想的实验方案___________ 。
(6)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与___________ 等因素有关。
 是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。【
 的制备】
的制备】(1)用下图装置制备
 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是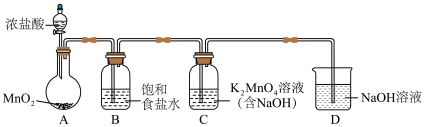
 ;
;【
 的性质探究】
的性质探究】资料:i.
 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成
,在近中性条件下被还原成 。
。ii.单质硫可溶于
 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。某小组研究
 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。| 实验序号 | 实验过程 | 实验现象 |
| Ⅰ |
| 紫色变浅( ),生成棕褐色沉淀( ),生成棕褐色沉淀( ) ) |
| Ⅱ |
| 溶液呈淡黄色( ),生成浅粉色沉淀(MnS) ),生成浅粉色沉淀(MnS) |
(3)①甲同学取实验Ⅰ中少量溶液进行实验,检测有
 ,得出
,得出 被氧化成
被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是②同学讨论后,设计了如下实验,证实该条件下
 的确可以将
的确可以将 氧化成
氧化成 。
。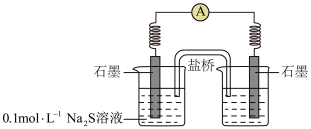
b.连通后电流计指针偏转,一段时间后,
(4)实验I的现象与资料i不相符,其原因是新生成的产物(
 )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是(5)实验II的现象与资料也不完全相符,丙同学猜想原因与(4)中所述原因相似,其原因是
(6)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与
您最近半年使用:0次
2024·北京·模拟预测
10 . 四氧化三锰( )是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含
)是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含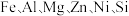 等元素)为原料制备高纯
等元素)为原料制备高纯 的工艺流程如下图所示。
的工艺流程如下图所示。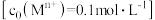 形成氢氧化物沉淀的
形成氢氧化物沉淀的 范围如下表:
范围如下表:
回答下列问题:
(1)“氧化”中添加适量的 的作用是
的作用是___________ 。(用离子方程式表示)
(2)“滤渣2”中主要有___________ ,“调 ”时溶液的
”时溶液的 范围应调节为
范围应调节为___________ ~6.2之间。
(3)“除杂2”的目的是生成 ,沉淀除去
,沉淀除去 。若溶液酸度过高,会导致
。若溶液酸度过高,会导致___________ 。
(4)常温下,利用表格中的数据,计算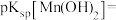
___________ 。(已知 )
)
(5) 和氨水混合在
和氨水混合在 下得到的
下得到的 的产率最高。若继续升高温度,会导致产率降低,原因可能是
的产率最高。若继续升高温度,会导致产率降低,原因可能是___________ 。
(6)在“沉锰”时,可用尿素 代替
代替 ,同时控制温度在
,同时控制温度在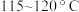 ,写出尿素“沉锰”反应的离子方程式:
,写出尿素“沉锰”反应的离子方程式:___________ 。
 )是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含
)是一种可用于生产锂离子电池正极材料的原料。以天然二氧化锰粉与硫化锰矿(还含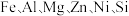 等元素)为原料制备高纯
等元素)为原料制备高纯 的工艺流程如下图所示。
的工艺流程如下图所示。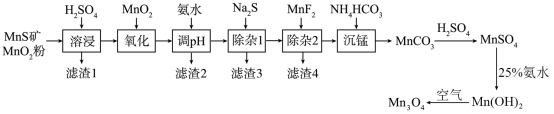
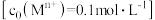 形成氢氧化物沉淀的
形成氢氧化物沉淀的 范围如下表:
范围如下表:| 金属离子 |  |  |  |  |  |  |  |
开始沉淀的 | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的 | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“氧化”中添加适量的
 的作用是
的作用是(2)“滤渣2”中主要有
 ”时溶液的
”时溶液的 范围应调节为
范围应调节为(3)“除杂2”的目的是生成
 ,沉淀除去
,沉淀除去 。若溶液酸度过高,会导致
。若溶液酸度过高,会导致(4)常温下,利用表格中的数据,计算
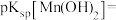
 )
)(5)
 和氨水混合在
和氨水混合在 下得到的
下得到的 的产率最高。若继续升高温度,会导致产率降低,原因可能是
的产率最高。若继续升高温度,会导致产率降低,原因可能是(6)在“沉锰”时,可用尿素
 代替
代替 ,同时控制温度在
,同时控制温度在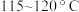 ,写出尿素“沉锰”反应的离子方程式:
,写出尿素“沉锰”反应的离子方程式:
您最近半年使用:0次