1 . 在研究前18号元素时发现,随原子序数递增可以将它们排成如图所示的蜗牛形状。图中每个点代表一种元素,其中①代表氢元素。___________ 键(填“离子”或“共价”);
(2)写出由元素①、②、③形成的化合物的电子式___________ 。
(3)Li和元素③在同一族,现代航天工业中选择用 做供氧剂的原因是
做供氧剂的原因是___________ 。
(4)元素④在元素周期表中的位置是___________ 。
(5)自然界磷元素只存在一种稳定的核素 。约里奧-居里夫妇在核反应中用α粒子轰击
。约里奧-居里夫妇在核反应中用α粒子轰击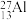 ,得到另一种核素
,得到另一种核素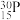 。
。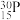 与
与 的关系是
的关系是___________ 。
(6)请设计实验验证元素④的非金属性弱于元素⑤的非金属性___________ (用离子方程式表示)。
(7)向由元素②、③、⑤按原子个数比1∶1∶1组成的化合物水溶液中滴入石蕊试液,溶液变成蓝色,一段时间后溶液颜色褪去,请解释原因___________ 。

(2)写出由元素①、②、③形成的化合物的电子式
(3)Li和元素③在同一族,现代航天工业中选择用
 做供氧剂的原因是
做供氧剂的原因是(4)元素④在元素周期表中的位置是
(5)自然界磷元素只存在一种稳定的核素
 。约里奧-居里夫妇在核反应中用α粒子轰击
。约里奧-居里夫妇在核反应中用α粒子轰击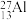 ,得到另一种核素
,得到另一种核素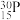 。
。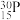 与
与 的关系是
的关系是(6)请设计实验验证元素④的非金属性弱于元素⑤的非金属性
(7)向由元素②、③、⑤按原子个数比1∶1∶1组成的化合物水溶液中滴入石蕊试液,溶液变成蓝色,一段时间后溶液颜色褪去,请解释原因
您最近一年使用:0次
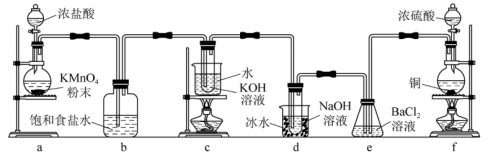
2 . 实验室里可用如下图所示的装置制取氯酸钾、次氯酸钠,并验证氯水的性质。 的发生装置。
的发生装置。
(1)装置a中,为了使浓盐酸在反应中顺利滴入,应采取的措施是___________ 。
(2)比较制取氯酸钾和次氯酸钠的条件,你得出的结论是___________ 。
(3)将d中余气与f中产生的气体通入e中,产生的现象是___________ ,请用离子方程式表示产生此现象的原因:___________ 、___________ 。
(4)写出装置c中发生反应的化学方程式___________ 。
(5)工业上为了变废为宝,可用多种方式处理硫酸工业排出的尾气(主要含 ),其中之一便是用
),其中之一便是用 浆液吸收。溶液中
浆液吸收。溶液中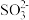 吸收
吸收 的离子方程式为
的离子方程式为___________ (已知20℃时 的溶解度为0.57g)。
的溶解度为0.57g)。
 的发生装置。
的发生装置。(1)装置a中,为了使浓盐酸在反应中顺利滴入,应采取的措施是
(2)比较制取氯酸钾和次氯酸钠的条件,你得出的结论是
(3)将d中余气与f中产生的气体通入e中,产生的现象是
(4)写出装置c中发生反应的化学方程式
(5)工业上为了变废为宝,可用多种方式处理硫酸工业排出的尾气(主要含
 ),其中之一便是用
),其中之一便是用 浆液吸收。溶液中
浆液吸收。溶液中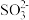 吸收
吸收 的离子方程式为
的离子方程式为 的溶解度为0.57g)。
的溶解度为0.57g)。
您最近一年使用:0次
解题方法
3 . 废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备 和
和 的部分实验步骤如下:
的部分实验步骤如下: ”步骤中,为加快溶解速率,可采取的措施是
”步骤中,为加快溶解速率,可采取的措施是___________ 。(任写一种方法)。
(2)从“滤液 ”中提取
”中提取 的实验步骤依次为
的实验步骤依次为___________ 、过滤、冰水洗涤、低温干燥,其中冰水洗涤晶体的目的是___________ 。
(3)在“溶解 ”步骤中,发生反应的化学方程式为
”步骤中,发生反应的化学方程式为___________ 。
(4)为测定产品中 的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
 溶液至刚好完全反应,消耗
溶液至刚好完全反应,消耗 溶液25.00mL。
溶液25.00mL。
已知: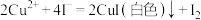 ,
, 。请依据实验数据计算样品中
。请依据实验数据计算样品中 的质量分数
的质量分数___________ (写出计算过程,结果保留2位小数)。
 和
和 的部分实验步骤如下:
的部分实验步骤如下: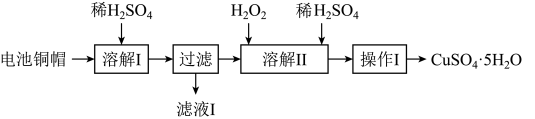
 ”步骤中,为加快溶解速率,可采取的措施是
”步骤中,为加快溶解速率,可采取的措施是(2)从“滤液
 ”中提取
”中提取 的实验步骤依次为
的实验步骤依次为(3)在“溶解
 ”步骤中,发生反应的化学方程式为
”步骤中,发生反应的化学方程式为(4)为测定产品中
 的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
 溶液至刚好完全反应,消耗
溶液至刚好完全反应,消耗 溶液25.00mL。
溶液25.00mL。已知:
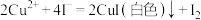 ,
, 。请依据实验数据计算样品中
。请依据实验数据计算样品中 的质量分数
的质量分数
您最近一年使用:0次
解题方法
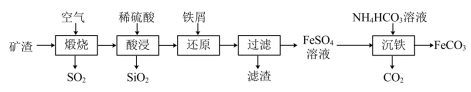
4 . 利用金属矿渣(含有FeS2、SiO2及Cu2O)制备FeCO3的实验流程如下。已知煅烧过程中FeS2和Cu2O转化为Fe2O3和CuO。 的反应外,还发生反应的
的反应外,还发生反应的离子方程式 有___________ 、___________ 。
(2)检验Fe3+是否完全被还原的实验操作是___________ 。
(3)FeSO4溶液浓度的测定。取制得的FeSO4溶液25.00mL,置于锥形瓶中,加入一定量的酸溶液,用0.1000mol/L的KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液19.50mL。计算FeSO4溶液的物质的是浓度___________ 。(写出计算过程)
(4)制备 FeCO3.写出“沉铁”步骤发生反应的离子方程式 :___________ 。
 的反应外,还发生反应的
的反应外,还发生反应的(2)检验Fe3+是否完全被还原的实验操作是
(3)FeSO4溶液浓度的测定。取制得的FeSO4溶液25.00mL,置于锥形瓶中,加入一定量的酸溶液,用0.1000mol/L的KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液19.50mL。计算FeSO4溶液的物质的是浓度
(4)制备 FeCO3.写出“沉铁”步骤发生反应的
您最近一年使用:0次
解题方法
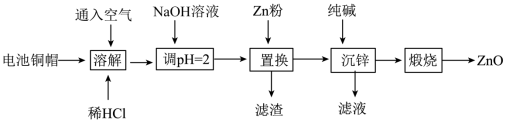
5 . 实验室利用废弃旧电池的铜帽(主要成分为Zn和Cu)回收Cu并制备ZnO的实验流程如下:___________ 。
(2)“溶解”可适当升高温度以加快反应速率,但温度不宜过高。温度不宜过高的原因是___________ 。
(3)用NaOH溶液调节pH=2的目的是___________ 。
(4)滤渣中的主要物质是___________ (填化学式)。
(5)“沉锌”时生成碱式碳酸锌[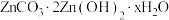 ],碱式碳酸锌在空气中加热可转化为ZnO,过程中固体质量随温度的变化关系如下图所示。已知:
],碱式碳酸锌在空气中加热可转化为ZnO,过程中固体质量随温度的变化关系如下图所示。已知: 加热至125℃、
加热至125℃、 加热至350℃均分解成ZnO,该碱式碳酸锌失去结晶水的温度与
加热至350℃均分解成ZnO,该碱式碳酸锌失去结晶水的温度与 的分解温度接近。
的分解温度接近。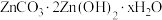 中x的值为
中x的值为___________ (写出计算过程)。
(2)“溶解”可适当升高温度以加快反应速率,但温度不宜过高。温度不宜过高的原因是
(3)用NaOH溶液调节pH=2的目的是
(4)滤渣中的主要物质是
(5)“沉锌”时生成碱式碳酸锌[
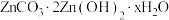 ],碱式碳酸锌在空气中加热可转化为ZnO,过程中固体质量随温度的变化关系如下图所示。已知:
],碱式碳酸锌在空气中加热可转化为ZnO,过程中固体质量随温度的变化关系如下图所示。已知: 加热至125℃、
加热至125℃、 加热至350℃均分解成ZnO,该碱式碳酸锌失去结晶水的温度与
加热至350℃均分解成ZnO,该碱式碳酸锌失去结晶水的温度与 的分解温度接近。
的分解温度接近。
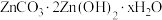 中x的值为
中x的值为
您最近一年使用:0次
解题方法
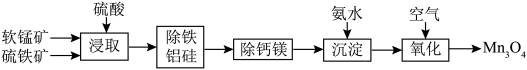
6 . 以软锰矿(主要成分为 ,还含少量Fe、Si、Al、Ca、Mg等的氧化物)和硫铁矿(主要成分
,还含少量Fe、Si、Al、Ca、Mg等的氧化物)和硫铁矿(主要成分 )为原料,两矿联合浸取可制备大颗粒的电池用
)为原料,两矿联合浸取可制备大颗粒的电池用 。
。 和
和 颗粒构成两个原电池反应,其原理如图1所示(部分产物未标出)。
颗粒构成两个原电池反应,其原理如图1所示(部分产物未标出)。 的电子排布式为:
的电子排布式为:___________ 。
②若 原电池中生成单质S,其电池总反应的离子方程式为
原电池中生成单质S,其电池总反应的离子方程式为___________ 。
③随硫铁矿的增加,锰的浸出率降低,可能的原因是___________ 。
(2)除钙镁:向已除去Fe、Al、Si元素的 溶液中(pH约为5)加入
溶液中(pH约为5)加入 溶液,将
溶液,将 、
、 转化为氟化物沉淀。则
转化为氟化物沉淀。则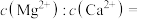
___________ 。
[已知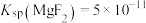 ,
,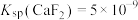 ]
]
(3)氧化:将“沉淀”步骤所得含少量 的
的 固体滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得
固体滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得 。
。
①写出由 反应得到
反应得到 的化学方程式
的化学方程式___________ 。
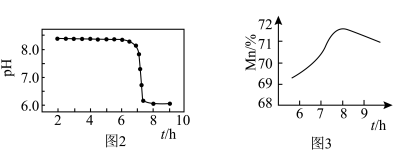
②沉淀加热通空气过程中溶液pH随时间变化如图2所示,其中pH先基本不变后迅速下降的原因是___________ 。___________ 。
 ,还含少量Fe、Si、Al、Ca、Mg等的氧化物)和硫铁矿(主要成分
,还含少量Fe、Si、Al、Ca、Mg等的氧化物)和硫铁矿(主要成分 )为原料,两矿联合浸取可制备大颗粒的电池用
)为原料,两矿联合浸取可制备大颗粒的电池用 。
。
 和
和 颗粒构成两个原电池反应,其原理如图1所示(部分产物未标出)。
颗粒构成两个原电池反应,其原理如图1所示(部分产物未标出)。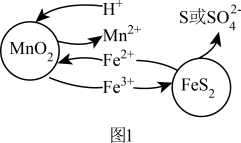
 的电子排布式为:
的电子排布式为:②若
 原电池中生成单质S,其电池总反应的离子方程式为
原电池中生成单质S,其电池总反应的离子方程式为③随硫铁矿的增加,锰的浸出率降低,可能的原因是
(2)除钙镁:向已除去Fe、Al、Si元素的
 溶液中(pH约为5)加入
溶液中(pH约为5)加入 溶液,将
溶液,将 、
、 转化为氟化物沉淀。则
转化为氟化物沉淀。则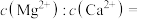
[已知
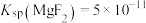 ,
,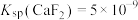 ]
](3)氧化:将“沉淀”步骤所得含少量
 的
的 固体滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得
固体滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得 。
。①写出由
 反应得到
反应得到 的化学方程式
的化学方程式②沉淀加热通空气过程中溶液pH随时间变化如图2所示,其中pH先基本不变后迅速下降的原因是
您最近一年使用:0次
解题方法
7 . 利用硫酸烧渣(主要含Fe2O3、FeO,还含有SiO2和CuO等)来制取FeSO4溶液。
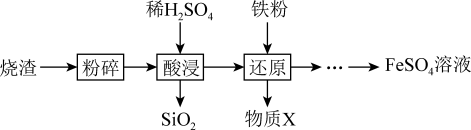
(1)“酸浸”时,Fe2O3发生反应的离子方程式是_______ 。
(2)“还原”时,铁粉将Fe3+、Cu2+还原为Fe2+和Cu。检验Fe3+是否已全部被还原,所选用试剂的化学式是______ 。
(3)实验室测定FeSO4溶液的浓度,常用K2Cr2O7标准溶液进行滴定。现称量2.940gK2Cr2O7(M=294g•mol-1)固体,配制成0.0100mol•L-1K2Cr2O7标准溶液。
①称量时,需用到的仪器有_______ 。
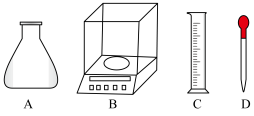
②根据计算,选用的容量瓶规格应为______ 。
A.100mL B.250mL C.500mL D.1000mL
(4)将(2)得到的FeSO4溶液进行下列操作,测定其物质的量浓度:
步骤一:取10.00mLFeSO4溶液,将其稀释成100.00mL溶液。
步骤二:取25.00mL稀释后的溶液,向其中加入0.100mol•L-1酸性KMnO4溶液。恰好反应时,记下消耗KMnO4溶液的体积。
步骤三:重复上述实验3次,平均消耗KMnO4溶液20.00mL。
已知:MnO +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O
①“步骤一”中稀释时所用的水需先进行加热煮沸,其目的是_______ 。
②试通过计算,求原FeSO4溶液的物质的量浓度是多少_______ ?(写出计算过程)

(1)“酸浸”时,Fe2O3发生反应的离子方程式是
(2)“还原”时,铁粉将Fe3+、Cu2+还原为Fe2+和Cu。检验Fe3+是否已全部被还原,所选用试剂的化学式是
(3)实验室测定FeSO4溶液的浓度,常用K2Cr2O7标准溶液进行滴定。现称量2.940gK2Cr2O7(M=294g•mol-1)固体,配制成0.0100mol•L-1K2Cr2O7标准溶液。
①称量时,需用到的仪器有

②根据计算,选用的容量瓶规格应为
A.100mL B.250mL C.500mL D.1000mL
(4)将(2)得到的FeSO4溶液进行下列操作,测定其物质的量浓度:
步骤一:取10.00mLFeSO4溶液,将其稀释成100.00mL溶液。
步骤二:取25.00mL稀释后的溶液,向其中加入0.100mol•L-1酸性KMnO4溶液。恰好反应时,记下消耗KMnO4溶液的体积。
步骤三:重复上述实验3次,平均消耗KMnO4溶液20.00mL。
已知:MnO
 +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O①“步骤一”中稀释时所用的水需先进行加热煮沸,其目的是
②试通过计算,求原FeSO4溶液的物质的量浓度是多少
您最近一年使用:0次
解题方法
8 . 废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备ZnSO4·7H2O和CuSO4·5H2O的部分实验步骤如下:
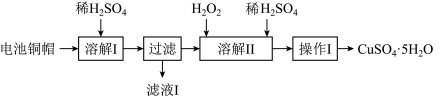
(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是_______ (任写一种方法)。
(2)从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为_______ 、_______ 、过滤、冰水洗涤、低温干燥。
(3)仔细分析流程,在“溶解II”步骤中,发生反应的化学方程式为_______ (用双线桥标出电子转移的方向和数目)。
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol/LNa2S2O3标准溶液至滴定终点,消耗Na2S2O3溶液25.00mL。
已知:2CuSO4+4KI=2CuI(白色)+I2+2K2SO4;2Na2S2O3+I2=2NaI+Na2S4O6
请依据实验数据计算样品中CuSO4·5H2O的质量分数_______ (写出计算过程,结果用百分数表示,小数点后保留1位有效数字)。

(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是
(2)从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为
(3)仔细分析流程,在“溶解II”步骤中,发生反应的化学方程式为
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol/LNa2S2O3标准溶液至滴定终点,消耗Na2S2O3溶液25.00mL。
已知:2CuSO4+4KI=2CuI(白色)+I2+2K2SO4;2Na2S2O3+I2=2NaI+Na2S4O6
请依据实验数据计算样品中CuSO4·5H2O的质量分数
您最近一年使用:0次
解题方法
9 . 已知海水中溴元素主要以 形式存在,工业上从海水中提取溴的流程如下:
形式存在,工业上从海水中提取溴的流程如下:
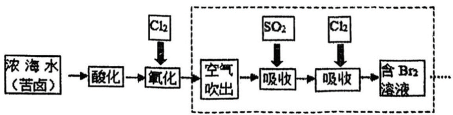
资料:溴单质容易挥发。
(1)写出“氧化”时的离子方程式____________ 。
(2)写出第1步“吸收”时的离子方程式____________________ ,该反应体现了 的
的____________ 性。
(3)得到的“含 溶液”通过以下不同操作,都可得到溴单质:
溶液”通过以下不同操作,都可得到溴单质:
①直接蒸馏得到溴单质,该操作利用的是溴的何种性质:________________ ;
②加入四氯化碳萃取,将得到的溴的四氯化碳溶液蒸馏得到溴单质。可以用四氯化碳对溴溶液进行萃取利用的是溴的何种性质:________________ 。
(4)工业可用 溶液代替二氧化硫的水溶液吸收
溶液代替二氧化硫的水溶液吸收 ,完成下列化学反应方程式:
,完成下列化学反应方程式:_____ 。
_________ _________
_________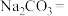 _________
_________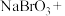 _________
_________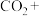 _________
_________
若有480g溴完全反应,转移电子的物质的量为_________  。
。
 形式存在,工业上从海水中提取溴的流程如下:
形式存在,工业上从海水中提取溴的流程如下:
资料:溴单质容易挥发。
(1)写出“氧化”时的离子方程式
(2)写出第1步“吸收”时的离子方程式
 的
的(3)得到的“含
 溶液”通过以下不同操作,都可得到溴单质:
溶液”通过以下不同操作,都可得到溴单质:①直接蒸馏得到溴单质,该操作利用的是溴的何种性质:
②加入四氯化碳萃取,将得到的溴的四氯化碳溶液蒸馏得到溴单质。可以用四氯化碳对溴溶液进行萃取利用的是溴的何种性质:
(4)工业可用
 溶液代替二氧化硫的水溶液吸收
溶液代替二氧化硫的水溶液吸收 ,完成下列化学反应方程式:
,完成下列化学反应方程式:_________
 _________
_________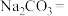 _________
_________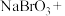 _________
_________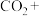 _________
_________若有480g溴完全反应,转移电子的物质的量为
 。
。
您最近一年使用:0次
名校
10 . 工业或机动车尾气中的 会造成环境问题,可用多种方法脱除。
会造成环境问题,可用多种方法脱除。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含 ),获得副产品。
),获得副产品。
①等物质的量NO与 被NaOH溶液吸收,产物只有一种盐,反应的离子方程式为
被NaOH溶液吸收,产物只有一种盐,反应的离子方程式为_______ 。
②若吸收时NO与 比例控制不当,则吸收液经浓缩结晶、过滤得到
比例控制不当,则吸收液经浓缩结晶、过滤得到 晶体中最有可能混有的杂质是
晶体中最有可能混有的杂质是_______ (填化学式)。排放的尾气中含量较高的氮氧化物是_______ (填化学式)。
(2)还原法:尿素水溶液热解产生的 可去除尾气中的
可去除尾气中的 ,流程如下:
,流程如下:
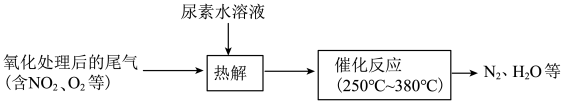
①尿素 中氮元素的化合价为
中氮元素的化合价为_______ 。
②写出“催化反应”过程中 还原
还原 的化学方程式
的化学方程式_______ 。
③若氧化处理后的尾气中混有 ,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低
,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低 的去除率。试分析硫酸盐的产生过程
的去除率。试分析硫酸盐的产生过程_______ 。
④“催化反应”过程中需控制温度在250℃~380℃之间,温度过高, 的去除率下降,其原因可能是温度过高催化剂的活性降低和
的去除率下降,其原因可能是温度过高催化剂的活性降低和_______ 。
 会造成环境问题,可用多种方法脱除。
会造成环境问题,可用多种方法脱除。(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含
 ),获得副产品。
),获得副产品。①等物质的量NO与
 被NaOH溶液吸收,产物只有一种盐,反应的离子方程式为
被NaOH溶液吸收,产物只有一种盐,反应的离子方程式为②若吸收时NO与
 比例控制不当,则吸收液经浓缩结晶、过滤得到
比例控制不当,则吸收液经浓缩结晶、过滤得到 晶体中最有可能混有的杂质是
晶体中最有可能混有的杂质是(2)还原法:尿素水溶液热解产生的
 可去除尾气中的
可去除尾气中的 ,流程如下:
,流程如下:
①尿素
 中氮元素的化合价为
中氮元素的化合价为②写出“催化反应”过程中
 还原
还原 的化学方程式
的化学方程式③若氧化处理后的尾气中混有
 ,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低
,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低 的去除率。试分析硫酸盐的产生过程
的去除率。试分析硫酸盐的产生过程④“催化反应”过程中需控制温度在250℃~380℃之间,温度过高,
 的去除率下降,其原因可能是温度过高催化剂的活性降低和
的去除率下降,其原因可能是温度过高催化剂的活性降低和
您最近一年使用:0次
2024-04-03更新
|
364次组卷
|
2卷引用:12 2024苏州太仓明德高级中学高一3月月考



