名校
1 . SO2、NOx为常见的空气污染物,会引起酸雨、光化学烟雾等污染问题。研究者以多种方法进行“脱硫”“脱硝”。
(1)利用工业废碱渣(主要成分为Na2CO3)来吸收含SO2的烟气,同时得到Na2SO3粗品。其流程如图所示:___________ ;
②SO2被Na2CO3溶液吸收时,会释放出一种无色无味气体,该反应的离子方程式为___________ 。
(2)利用含有SO2的烟气制备NaClO2。其流程如图所示:___________ 。
②反应b中的氧化剂和还原剂的物质的量之比为___________ 。
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”“脱硝”。控制溶液的pH=5.5,一定时间内,温度对SO2、NO脱除率的影响如图所示: 、NO
、NO 。
。
①NO在吸收过程中,反应的离子方程式是___________ 。
②50℃时,吸收液中烟气转化生成的Cl‒和NO 的物质的量之比为
的物质的量之比为___________ 。
③烟气中NOx含量的测定:将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO ,加水稀释至100mL。量取25mL该溶液,加入V1mLc1mol·L‒1FeSO4溶液(过量),充分反应后,用c2mol·L‒1K2Cr2O7溶液和剩余的Fe2+恰好反应(该反应的还原产物为Cr3+),消耗V2mL。气样中NOx折合成NO的含量为
,加水稀释至100mL。量取25mL该溶液,加入V1mLc1mol·L‒1FeSO4溶液(过量),充分反应后,用c2mol·L‒1K2Cr2O7溶液和剩余的Fe2+恰好反应(该反应的还原产物为Cr3+),消耗V2mL。气样中NOx折合成NO的含量为___________ mg·L‒1。
(1)利用工业废碱渣(主要成分为Na2CO3)来吸收含SO2的烟气,同时得到Na2SO3粗品。其流程如图所示:
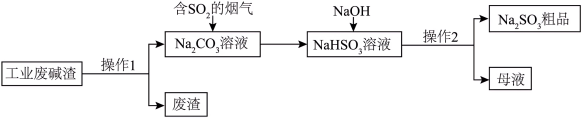
②SO2被Na2CO3溶液吸收时,会释放出一种无色无味气体,该反应的离子方程式为
(2)利用含有SO2的烟气制备NaClO2。其流程如图所示:
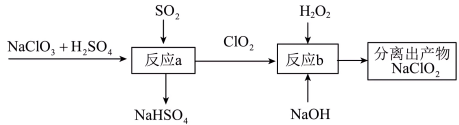
②反应b中的氧化剂和还原剂的物质的量之比为
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”“脱硝”。控制溶液的pH=5.5,一定时间内,温度对SO2、NO脱除率的影响如图所示:
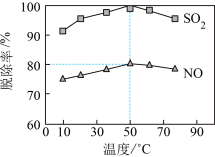
 、NO
、NO 。
。①NO在吸收过程中,反应的离子方程式是
②50℃时,吸收液中烟气转化生成的Cl‒和NO
 的物质的量之比为
的物质的量之比为③烟气中NOx含量的测定:将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO
 ,加水稀释至100mL。量取25mL该溶液,加入V1mLc1mol·L‒1FeSO4溶液(过量),充分反应后,用c2mol·L‒1K2Cr2O7溶液和剩余的Fe2+恰好反应(该反应的还原产物为Cr3+),消耗V2mL。气样中NOx折合成NO的含量为
,加水稀释至100mL。量取25mL该溶液,加入V1mLc1mol·L‒1FeSO4溶液(过量),充分反应后,用c2mol·L‒1K2Cr2O7溶液和剩余的Fe2+恰好反应(该反应的还原产物为Cr3+),消耗V2mL。气样中NOx折合成NO的含量为
您最近一年使用:0次
2024-05-27更新
|
252次组卷
|
2卷引用:北师大附属实验中学2023-2024学年度第二学期期中试卷
名校
解题方法
2 . 下列离子方程式书写正确的是
A.酸化的FeSO4溶液长时间存放变黄:4H++2Fe2++SO =2Fe3++SO2↑+2H2O =2Fe3++SO2↑+2H2O |
B.向(NH4)2SO4溶液中滴加Ba(OH)2溶液:NH +SO +SO +Ba2++OH−=NH3·H2O+BaSO4↓ +Ba2++OH−=NH3·H2O+BaSO4↓ |
C.向FeCl3溶液中通入SO2,黄色溶液变为浅绿色:SO2+2Fe3++2H2O=SO +2Fe2++4H+ +2Fe2++4H+ |
D.过量铁粉与稀硝酸反应,产生无色气体:Fe+NO +4H+=Fe3++NO↑+2H2O +4H+=Fe3++NO↑+2H2O |
您最近一年使用:0次
2024-05-27更新
|
189次组卷
|
2卷引用:北师大附属实验中学2023-2024学年度第二学期期中试卷
3 . 室温下,将充满某气体的试管倒立在水中(如下图)。下列对实验现象描述不正确的是
| 实验装置 | 选项 | 气体 | 实验现象 |
| A | Cl2 | 试管中液面上升,取试管中溶液滴加紫色石蕊溶液,溶液先变红后褪色 |
| B | SO2 | 试管中液面上升,取试管中溶液滴加紫色石蕊溶液,溶液先变红后褪色 | |
| C | NO2 | 试管中液面逐渐上升,停止后,向试管中再缓缓通入一定量的O2,试管中的液面会继续上升 | |
| D | NO | 试管中液面无明显上升,取出试管正立,试管口有红棕色气体出现 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-27更新
|
116次组卷
|
2卷引用:北师大附属实验中学2023-2024学年度第二学期期中试卷
4 . 下列有关物质的用途不正确的是
| A.液氨可用作制冷剂 | B.SO2可用于纸浆漂白 |
| C.NH4HCO3可用作化肥 | D.晶体硅可用作光导纤维 |
您最近一年使用:0次
2024-05-27更新
|
85次组卷
|
2卷引用:北师大附属实验中学2023-2024学年度第二学期期中试卷
名校
解题方法
5 . 现有一份雨水样品,每隔一段时间测定该雨水样品的pH,所得数据如下:
分析数据,回答下列问题:
①雨水样品的pH变化的原因是(结合离子方程式解释):___________ 。
②如果将刚取样的上述雨水和自来水相结合,pH将___________ (填“变大”、“变小”“不变”),原因是(用化学方程式表示):___________ 。
测试时间 | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
①雨水样品的pH变化的原因是(结合离子方程式解释):
②如果将刚取样的上述雨水和自来水相结合,pH将
您最近一年使用:0次
名校
6 .  是重要的大气污染物,会导致“酸雨”。
是重要的大气污染物,会导致“酸雨”。
1. 产生硫酸型酸雨有两条途径:途径一是
产生硫酸型酸雨有两条途径:途径一是 ;另一途径是:
;另一途径是:
___________ 。
2.将装有 的试管倒立在水槽中,可观察到
的试管倒立在水槽中,可观察到___________ 。取出试管中的溶液,分别进行如下实验:滴加品红溶液,振荡,观察到红色褪去,说明 具有性。滴加
具有性。滴加 溶液,无明显现象,再滴入氨水后出现白色沉淀。出现白色沉淀的原因
溶液,无明显现象,再滴入氨水后出现白色沉淀。出现白色沉淀的原因___________ 。
 是重要的大气污染物,会导致“酸雨”。
是重要的大气污染物,会导致“酸雨”。1.
 产生硫酸型酸雨有两条途径:途径一是
产生硫酸型酸雨有两条途径:途径一是 ;另一途径是:
;另一途径是:
2.将装有
 的试管倒立在水槽中,可观察到
的试管倒立在水槽中,可观察到 具有性。滴加
具有性。滴加 溶液,无明显现象,再滴入氨水后出现白色沉淀。出现白色沉淀的原因
溶液,无明显现象,再滴入氨水后出现白色沉淀。出现白色沉淀的原因
您最近一年使用:0次
名校
解题方法
7 . 为消除燃煤烟气中含有的: 、
、 ,研究者提出若干烟气“脱硫”、“脱硝”的方法。
,研究者提出若干烟气“脱硫”、“脱硝”的方法。
Ⅰ。合成氨催化氧化制硝酸的流程示意图:
(1)结合上表数据进行估算,当1 mol 完全参与反应转化成
完全参与反应转化成 时,反应总共
时,反应总共___________ (填“放出”或“吸收”)___________ kJ热量。
(2)氧化炉中的反应化学方程式___________ 。
(3)吸收塔中若不通入氧气,只用水吸收, 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为___________ 。
Ⅱ。工业上广泛使用以溶液作为吸收剂进行一体化“脱硫”、“脱硝”。
(4)下列物质中,能吸收 的有
的有___________ (填序号)。
a.氨水 b.酸性 溶液 c.
溶液 c. 溶液 d.NaOH溶液
溶液 d.NaOH溶液
(5)用NaClO溶液作吸收剂,控制溶液的 ,可将烟气中的NO转化为
,可将烟气中的NO转化为 。写出NaClO溶液吸收烟气中NO的离子方程式是
。写出NaClO溶液吸收烟气中NO的离子方程式是___________ 。
 、
、 ,研究者提出若干烟气“脱硫”、“脱硝”的方法。
,研究者提出若干烟气“脱硫”、“脱硝”的方法。Ⅰ。合成氨催化氧化制硝酸的流程示意图:

| 共价键 |  |  |  |
| 断开1 mol共价键所需能量(kJ) | 946 | 436 | 391 |
(1)结合上表数据进行估算,当1 mol
 完全参与反应转化成
完全参与反应转化成 时,反应总共
时,反应总共(2)氧化炉中的反应化学方程式
(3)吸收塔中若不通入氧气,只用水吸收,
 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为Ⅱ。工业上广泛使用以溶液作为吸收剂进行一体化“脱硫”、“脱硝”。
(4)下列物质中,能吸收
 的有
的有a.氨水 b.酸性
 溶液 c.
溶液 c. 溶液 d.NaOH溶液
溶液 d.NaOH溶液(5)用NaClO溶液作吸收剂,控制溶液的
 ,可将烟气中的NO转化为
,可将烟气中的NO转化为 。写出NaClO溶液吸收烟气中NO的离子方程式是
。写出NaClO溶液吸收烟气中NO的离子方程式是
您最近一年使用:0次
名校
解题方法
8 .  .某实验小组利用以下装置制取氨气并探究氨气的性质:
.某实验小组利用以下装置制取氨气并探究氨气的性质:___________ 。
(2)装置B中的干燥剂是___________ (填名称)。
(3)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___________ 。
(4)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置是___________ (填“E”、“F”、“G”或“H”)。
 .探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
②反应前I装置中CuO质量为8g,反应后I装置中红色固体质量为6.8g,通过计算,写出I装置中发生反应的总方程式为___________ 。
(6)如图所示,若从a处通入 ,
, 溶液中产生白色沉淀,其化学式为
溶液中产生白色沉淀,其化学式为___________ 。若向a处分别通入___________ (填选项),也会产生白色沉淀,其化学式为___________ 。 B.
B. C.
C. D.
D.
 .某实验小组利用以下装置制取氨气并探究氨气的性质:
.某实验小组利用以下装置制取氨气并探究氨气的性质: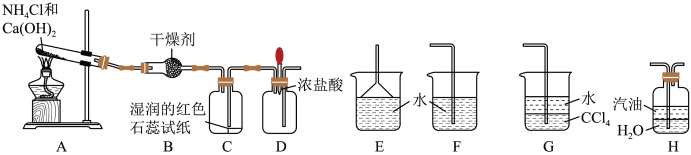
(2)装置B中的干燥剂是
(3)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(4)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置是
 .探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。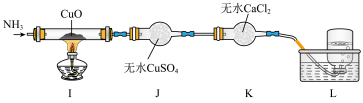
| 序号 | 实验现象 | 实验结论 |
| i | I装置中黑色CuO固体全部变红 | 反应生成了 或 或 |
| ii | J装置中无水 变蓝 变蓝 | 反应生成了 |
| iii | L装置中收集到无色无味气体 | 反应生成了 |
(6)如图所示,若从a处通入
 ,
, 溶液中产生白色沉淀,其化学式为
溶液中产生白色沉淀,其化学式为
 B.
B. C.
C. D.
D.
您最近一年使用:0次
名校
9 . 标准状况下,将SO2和Cl2组成的混合气体amol通入200mL Fe2(SO4)3溶液中,充分反应后,气体被完全吸收,溶液的棕黄色变浅。向反应后的溶液中加入足量的BaCl2溶液,将所得沉淀过滤、洗涤、干燥后称重,其质量为23.3g。则a的数值可能是
Fe2(SO4)3溶液中,充分反应后,气体被完全吸收,溶液的棕黄色变浅。向反应后的溶液中加入足量的BaCl2溶液,将所得沉淀过滤、洗涤、干燥后称重,其质量为23.3g。则a的数值可能是
 Fe2(SO4)3溶液中,充分反应后,气体被完全吸收,溶液的棕黄色变浅。向反应后的溶液中加入足量的BaCl2溶液,将所得沉淀过滤、洗涤、干燥后称重,其质量为23.3g。则a的数值可能是
Fe2(SO4)3溶液中,充分反应后,气体被完全吸收,溶液的棕黄色变浅。向反应后的溶液中加入足量的BaCl2溶液,将所得沉淀过滤、洗涤、干燥后称重,其质量为23.3g。则a的数值可能是| A.0.06 | B.0.07 | C.0.08 | D.0.09 |
您最近一年使用:0次
名校
解题方法
10 . 下列关于含硫元素的物质的表述正确的是
| A.S单质在化学反应中只能表现出还原性 |
| B.SO2具有漂白性,因此可使酸性KMnO4溶液褪色 |
| C.用浓硫酸在纸上书写的字迹变黑,体现了浓硫酸的氧化性 |
| D.浓硫酸具有吸水性,可用来干燥SO2气体 |
您最近一年使用:0次