1 . 计算
(1)在标准状况下,10.2gH2S 与标况下_______ LNH3含有相同的H原子。
(2)实验室中有一瓶碳酸氢钠固体,因受热而部分变质(杂质为Na2CO3,假设杂质分布均匀)。为测定其组成,称取4.420g样品溶于水,配成500mL溶液。取出50.00mL该溶液,加入0. 1000 mol/L Ba(OH)2溶液至50.00mL时沉淀量达到最大。请计算:
①25°C时,0.1000 mol/L Ba(OH)2溶液中的氢氧根离子浓度是_______ mol/L。
②样品中n(NaHCO3):n(Na2CO3)=_______ 。
(1)在标准状况下,10.2gH2S 与标况下
(2)实验室中有一瓶碳酸氢钠固体,因受热而部分变质(杂质为Na2CO3,假设杂质分布均匀)。为测定其组成,称取4.420g样品溶于水,配成500mL溶液。取出50.00mL该溶液,加入0. 1000 mol/L Ba(OH)2溶液至50.00mL时沉淀量达到最大。请计算:
①25°C时,0.1000 mol/L Ba(OH)2溶液中的氢氧根离子浓度是
②样品中n(NaHCO3):n(Na2CO3)=
您最近一年使用:0次
解题方法
2 . 工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量的NaCl,现欲测定某碳酸钠样品中Na2CO3的质量分数,某探究性学习小组设计以下两种方案。
Ⅰ.取样品bg,设计如下实验方案,操作步骤如下:
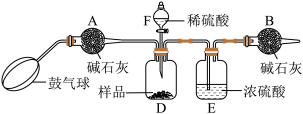
①如图连接装置(除B外)并加入所需药品。
②称量并记录B的质量(a1g)。
③按动鼓气球,持续约1分钟。
④连接上B。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(a2g)。
⑧计算
(1)操作③中,鼓入空气的作用是_______ ;操作⑥中,鼓入空气的作用是_______ ;
(2)根据题干所给的数据列出样品中Na2CO3的质量分数表达式_______ 。
(3)经实验发现最终所得的 Na2CO3的质量分数超过100%,其可能的原因是_______ 。
Ⅱ.现有碳酸钠和氯化钠的混合物样品25g,将其放入干净的烧杯中,加入一定量的水,使其完全溶解得到200mL溶液。向所得溶液中慢慢加入4mol•L-1的盐酸,烧杯中溶液的质量与加入盐酸的体积关系曲线如图所示。请回答下列问题。
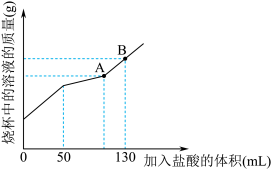
(4)加入50mL盐酸时,写出反应的离子反应方程式_______ 。
(5)在这个样品中,含碳酸钠的质量分数为_______ 。
(6)A点时,溶液溶质是_______ ,所得溶质质量分数为_______ 。(忽略体积的微小变化,结果保留小数点后两位)。
Ⅰ.取样品bg,设计如下实验方案,操作步骤如下:

①如图连接装置(除B外)并加入所需药品。
②称量并记录B的质量(a1g)。
③按动鼓气球,持续约1分钟。
④连接上B。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(a2g)。
⑧计算
(1)操作③中,鼓入空气的作用是
(2)根据题干所给的数据列出样品中Na2CO3的质量分数表达式
(3)经实验发现最终所得的 Na2CO3的质量分数超过100%,其可能的原因是
Ⅱ.现有碳酸钠和氯化钠的混合物样品25g,将其放入干净的烧杯中,加入一定量的水,使其完全溶解得到200mL溶液。向所得溶液中慢慢加入4mol•L-1的盐酸,烧杯中溶液的质量与加入盐酸的体积关系曲线如图所示。请回答下列问题。

(4)加入50mL盐酸时,写出反应的离子反应方程式
(5)在这个样品中,含碳酸钠的质量分数为
(6)A点时,溶液溶质是
您最近一年使用:0次
解题方法
3 . I.某双原子分子构成的气体,其摩尔质量为Mg/mol,该气体的质量为mg。设阿伏加德罗常数的值为 ,则:
,则:
(1)该气体在标准状况下的体积为_______ L;
(2)该气体在标准状况下的密度为_______ g/L;
(3)该气体所含的原子总数为_______ ;
(4)一个该气体分子的质量为_______ g;
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_______  。
。
II.实验室需要0.1mol/LNaOH溶液480mL。根据溶液的配制情况回答下列问题。
(6)由NaOH固体配制溶液,在如图所示仪器中,配制上述溶液肯定不需要的是_______ (填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是_______ 。
A. B.
B. C.
C. D.
D. E.
E.
(7)下列操作会导致所配溶液浓度偏高的是_______ (填字母)。
A.配制氢氧化钠溶液时,称量时间过长
B.转移溶液前容量瓶中存在少量蒸馏水
C.定容前未洗涤烧杯和玻璃棒
D.配制氢氧化钠溶液时,将称量好的氢氧化钠固体在小烧杯中溶解后,未冷却立即转移到容量瓶中并定容
E.定容时俯视容量瓶刻度线
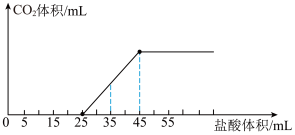
(8)取配制好的NaOH溶液100mL,然后向其通入一定量的 气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的
气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的 气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。A溶液中溶质及物质的量之比为
气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。A溶液中溶质及物质的量之比为_______ 。
 ,则:
,则:(1)该气体在标准状况下的体积为
(2)该气体在标准状况下的密度为
(3)该气体所含的原子总数为
(4)一个该气体分子的质量为
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为
 。
。II.实验室需要0.1mol/LNaOH溶液480mL。根据溶液的配制情况回答下列问题。
(6)由NaOH固体配制溶液,在如图所示仪器中,配制上述溶液肯定不需要的是
A.
 B.
B. C.
C. D.
D. E.
E.
(7)下列操作会导致所配溶液浓度偏高的是
A.配制氢氧化钠溶液时,称量时间过长
B.转移溶液前容量瓶中存在少量蒸馏水
C.定容前未洗涤烧杯和玻璃棒
D.配制氢氧化钠溶液时,将称量好的氢氧化钠固体在小烧杯中溶解后,未冷却立即转移到容量瓶中并定容
E.定容时俯视容量瓶刻度线
(8)取配制好的NaOH溶液100mL,然后向其通入一定量的
 气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的
气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的 气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。A溶液中溶质及物质的量之比为
气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。A溶液中溶质及物质的量之比为
您最近一年使用:0次
4 . 一定条件下,向10mL 和NaOH的混合溶液中缓慢通入足量的
和NaOH的混合溶液中缓慢通入足量的 气体,生成沉淀的质量(m)与通入
气体,生成沉淀的质量(m)与通入 气体的体积(V)(已折算成标准状况)的关系如下图所示。
气体的体积(V)(已折算成标准状况)的关系如下图所示。

回答下列问题:
(1)①A点前发生反应的离子方程式是___________ ;
②B→C发生反应的离子方程式是___________ 。
(2)A点对应生成沉淀的质量为___________ ;C点对应的 的体积是
的体积是___________ 。
(3)向A点和B点间的P点所对应的溶液中逐滴滴加盐酸,滴加盐酸的体积与产生气体的物质的量之间所对应的图像可能是___________ (填字母)。

(4)混合稀溶液中 和NaOH的物质的量浓度之比为
和NaOH的物质的量浓度之比为___________ 。
(5)若取2L该混合溶液,通入一定体积的 ,结果生成了5g沉淀,则通入
,结果生成了5g沉淀,则通入 气体的体积(标准状况)可能是
气体的体积(标准状况)可能是___________ 。
 和NaOH的混合溶液中缓慢通入足量的
和NaOH的混合溶液中缓慢通入足量的 气体,生成沉淀的质量(m)与通入
气体,生成沉淀的质量(m)与通入 气体的体积(V)(已折算成标准状况)的关系如下图所示。
气体的体积(V)(已折算成标准状况)的关系如下图所示。
回答下列问题:
(1)①A点前发生反应的离子方程式是
②B→C发生反应的离子方程式是
(2)A点对应生成沉淀的质量为
 的体积是
的体积是(3)向A点和B点间的P点所对应的溶液中逐滴滴加盐酸,滴加盐酸的体积与产生气体的物质的量之间所对应的图像可能是

(4)混合稀溶液中
 和NaOH的物质的量浓度之比为
和NaOH的物质的量浓度之比为(5)若取2L该混合溶液,通入一定体积的
 ,结果生成了5g沉淀,则通入
,结果生成了5g沉淀,则通入 气体的体积(标准状况)可能是
气体的体积(标准状况)可能是
您最近一年使用:0次
5 . 有氯化钠、碳酸钠、碳酸氢钠的固体混合物共4克,加热到质量不再减少为止。此时剩余固体质量为3.38克,在残留的固体中加入足量盐酸,将产生的气体通过干燥管后,通入澄清石灰水中,生成2g固体。
(1)原混合物中碳酸氢钠的物质的量是___________ 。
(2)原混合物中碳酸钠的质量是多少?(写出具体计算过程)___________
(1)原混合物中碳酸氢钠的物质的量是
(2)原混合物中碳酸钠的质量是多少?(写出具体计算过程)
您最近一年使用:0次
解题方法
6 . 加热5.00克碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物的质量减小了0.31克,写出发生反应方程式_______ ,则原混合物中碳酸钠的质量分数是_______ 。
您最近一年使用:0次
7 . 把13.7gNa2CO3和NaHCO3的混合物加热到质量不再变化时,得到10.6g残留固体。试求:
(1)原混合物中无水碳酸钠的质量是_______ 。
(2)在原混合物中NaHCO3的质量分数是_______ 。
(3)若把10.6g残留固体全部溶于水,配成500mL的溶液,则所得溶液中溶质的物质的量浓度是_______ 。
(1)原混合物中无水碳酸钠的质量是
(2)在原混合物中NaHCO3的质量分数是
(3)若把10.6g残留固体全部溶于水,配成500mL的溶液,则所得溶液中溶质的物质的量浓度是
您最近一年使用:0次
解题方法
8 . 碳酸钠和碳酸氢钠是用途广泛的化合物。在实验室中,充分加热碳酸钠和碳酸氢钠的混合物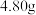 ,完全反应后称得剩余固体质量为
,完全反应后称得剩余固体质量为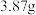 ,求混合物中碳酸氢钠的质量分数
,求混合物中碳酸氢钠的质量分数_______ 。
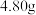 ,完全反应后称得剩余固体质量为
,完全反应后称得剩余固体质量为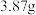 ,求混合物中碳酸氢钠的质量分数
,求混合物中碳酸氢钠的质量分数
您最近一年使用:0次
名校
解题方法
9 . 将某碳酸钠和碳酸氢钠混合物2.43g加热到质量不再变化时,剩余物质的质量为2.12g,求:
(1)写出加热过程中发生反应的化学方程式_______ 。
(2)碳酸氢钠的质量为_______ 克?
(3)碳酸钠的质量分数为_______ (保留三位有效数字)?
(1)写出加热过程中发生反应的化学方程式
(2)碳酸氢钠的质量为
(3)碳酸钠的质量分数为
您最近一年使用:0次
2022-11-19更新
|
292次组卷
|
3卷引用:浙江省杭州市S9联盟2022-2023学年高一上学期期中联考化学试题
10 . 取一定物质的量浓度的NaOH溶液100mL,然后向其中通入一定量的 气体,得到溶液A,向A中逐滴缓慢加入
气体,得到溶液A,向A中逐滴缓慢加入 的HCl溶液,产生的
的HCl溶液,产生的 气体体积(标准状况)与所加HC1溶液的体积之间关系如图所示。
气体体积(标准状况)与所加HC1溶液的体积之间关系如图所示。

(1)溶液A中的溶质为_______ 。
(2)滴加盐酸过程中,最终产生标况下 体积为
体积为_______ mL。
 气体,得到溶液A,向A中逐滴缓慢加入
气体,得到溶液A,向A中逐滴缓慢加入 的HCl溶液,产生的
的HCl溶液,产生的 气体体积(标准状况)与所加HC1溶液的体积之间关系如图所示。
气体体积(标准状况)与所加HC1溶液的体积之间关系如图所示。
(1)溶液A中的溶质为
(2)滴加盐酸过程中,最终产生标况下
 体积为
体积为
您最近一年使用:0次



