13-14高三上·江苏扬州·阶段练习
名校
1 . 硼镁矿属于硼酸盐,可用来制备硼酸(H3BO3)和MgO,方法如下:硼镁矿粉与(NH4)2SO4溶液混合后加热,反应生成H3BO3晶体和MgSO4溶液,同时放出NH3;再向MgSO4溶液中通入NH3与CO2,得到MgCO3沉淀和滤液,沉淀经洗涤、煅烧后得MgO,滤液则循环使用。回答下列问题:
(1)与硅酸盐类似,硼酸盐结构也比较复杂,如硬硼钙石化学式为Ca2B6O11·5H2O,将其改写为氧化物的形式_____________________________ 。
(2)上述制备过程中,检验沉淀洗涤是否完全的方法是_______________________ 。
(3)写出MgSO4溶液中通入NH3与CO2反应的化学方程式_______________________ 。
(4)若准确称取1.68 g硼镁矿,完全反应后得H3BO3晶体1.24 g,MgO 0.8 g,计算该硼酸盐的组成。(写出计算过程)___________________
(1)与硅酸盐类似,硼酸盐结构也比较复杂,如硬硼钙石化学式为Ca2B6O11·5H2O,将其改写为氧化物的形式
(2)上述制备过程中,检验沉淀洗涤是否完全的方法是
(3)写出MgSO4溶液中通入NH3与CO2反应的化学方程式
(4)若准确称取1.68 g硼镁矿,完全反应后得H3BO3晶体1.24 g,MgO 0.8 g,计算该硼酸盐的组成。(写出计算过程)
您最近一年使用:0次
2016-12-09更新
|
502次组卷
|
3卷引用:2013届江苏省扬州市高三第一学期检测试题化学试卷
2 . 在AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液直至过量,理论上,加入NaOH的体积和所得沉淀的物质的量的示意图如下,b处NaOH的体积为1L,则下列判断正确的是
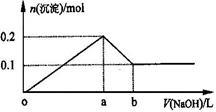

| A.混合溶液中Al3+的物质的量为0.2mol |
| B.NaOH的浓度为0.5 mol/L |
| C.在b点处溶液中的溶质只有NaAlO2 |
| D.图中线段oa:ab=5:1 |
您最近一年使用:0次
2016-12-09更新
|
470次组卷
|
3卷引用:重庆市朝阳中学2019-2020学年高一12月月考化学试题
重庆市朝阳中学2019-2020学年高一12月月考化学试题黑龙江省鹤岗市第一中学2016-2017学年高二下学期期末考试化学试题(已下线)小题必刷13 镁及其化合物——2021年高考化学一轮复习小题必刷(通用版)
3 . 有无色溶液,加入Na2O2时有无色无味气体放出,并有白色沉淀生成,加入Na2O2的量与生成白色沉淀的量如图所示。该无色溶液中含有的物质是
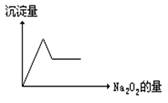

| A.CaCl2和MgCl2、 | B.Al2 (SO4)3 | C.Al2(SO4)3和MgSO4 | D.Na2SO4和MgSO4 |
您最近一年使用:0次
11-12高一上·河北衡水·阶段练习
4 . 向Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量w和加入NaOH体积v之间的关系如图所示.则混合溶液中 Al2(SO4)3和MgSO4的物质的量之比为


| A.1: 1 | B.1:2 | C.2:1 | D.1:3 |
您最近一年使用:0次
5 . 向x的溶液中,加入Y试剂,产生的沉淀示意图如图所示的是(注意线段的斜率)
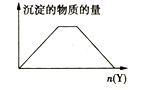

| A.向NaOH和Ca(OH)2的混合液中通入CO2 |
| B.向HCl和A1C13的混合液中滴加NaOH溶液 |
| C.向NH4A1(SO4)2溶液中滴加NaOH溶液 |
| D.向NH4C1和MgCl2的混合液中滴加NaOH溶液 |
您最近一年使用:0次
10-11高一下·湖北黄冈·阶段练习
6 . 由短周期元素组成的A、B、C、D、E、F六种微粒,其中只有C、D是分子,其余四种均为阳离子或阴离子,且每个微粒中都含有10个电子。已知A、E是由非金属元素组成的阳离子,六种微粒间有下列关系:
①A++B- C+D, B-+E+=2D;
C+D, B-+E+=2D;
②通常情况下,C是一种无色刺激性气味的气体,且可使湿润的红色石蕊试纸变蓝;
③向含F离子的溶液中加入C的水溶液,可生成白色沉淀W,C溶液过量沉淀也不消失。再加入含大量B离子或大量E离子的溶液时,沉淀W在其中一种情况下溶解,另一种情况下不溶解。
请回答下列问题:
(1)微粒A的名称及化学式分别为_____________ 、_________________ 。
(2)C的水溶液中存在的分子总数至少有___________ 种。
(3)写出微粒F与过量C的水溶液反应的离子方程式:__________________________ 。
(4)向含有0.1mol F离子的50mL溶液中,加入含1.5mol/L B离子的200mL强碱溶液,结果有白色沉淀产生,再向该混合物中加入含1mol/L E离子的强酸溶液,若要使沉淀恰好溶解,则最后加入的溶液的体积至少为___________ mL。
①A++B-
 C+D, B-+E+=2D;
C+D, B-+E+=2D;②通常情况下,C是一种无色刺激性气味的气体,且可使湿润的红色石蕊试纸变蓝;
③向含F离子的溶液中加入C的水溶液,可生成白色沉淀W,C溶液过量沉淀也不消失。再加入含大量B离子或大量E离子的溶液时,沉淀W在其中一种情况下溶解,另一种情况下不溶解。
请回答下列问题:
(1)微粒A的名称及化学式分别为
(2)C的水溶液中存在的分子总数至少有
(3)写出微粒F与过量C的水溶液反应的离子方程式:
(4)向含有0.1mol F离子的50mL溶液中,加入含1.5mol/L B离子的200mL强碱溶液,结果有白色沉淀产生,再向该混合物中加入含1mol/L E离子的强酸溶液,若要使沉淀恰好溶解,则最后加入的溶液的体积至少为
您最近一年使用:0次
7 . 把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1mol/LNaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示。
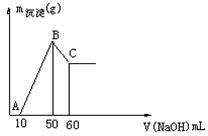
求:(1)合金中镁、铝各自的质量_______ 、_________ 。
(2)盐酸的物质的量浓度______________ 。

求:(1)合金中镁、铝各自的质量
(2)盐酸的物质的量浓度
您最近一年使用:0次
8 . 某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
向2支盛有1 mL 1 mol·L-1的MgCl2溶液中各加入10滴2 mol·L-1NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
(1)从沉淀溶解平衡的角度解释实验Ⅰ的反应过程_____________ 。
(2)测得实验Ⅱ中所用NH4Cl溶液显酸性(pH约为4.5),用离子方程式解释其显酸性的原因___________ 。
(3)甲同学认为应补充一个实验:向同样的Mg(OH)2沉淀中加4 mL蒸馏水,观察到沉淀不溶解。该实验的目的是_________ 。
(4)同学们猜测实验Ⅱ中沉淀溶解的原因有两种:一是NH4Cl溶液显酸性,溶液中的H+可以结合OH- ,进而使沉淀溶解;二是____________ 。
(5)乙同学继续进行实验:向4 mL 2 mol·L-1 NH4Cl溶液中滴加2滴浓氨水,得到pH约为8的混合溶液,向同样的Mg(OH)2沉淀中加入该混合溶液,观察现象。
①实验结果证明(4)中的第二种猜测是成立的,乙同学获得的实验现象是___________ 。
③乙同学这样配制混合溶液的理由是___________ 。
向2支盛有1 mL 1 mol·L-1的MgCl2溶液中各加入10滴2 mol·L-1NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
| 实验序号 | 加入试剂 | 实验现象 |
| Ⅰ | 4 mL 2 mol·L-1HCl 溶液 | 沉淀溶解 |
| Ⅱ | 4 mL 2 mol·L-1NH4Cl 溶液 | 沉淀溶解 |
(1)从沉淀溶解平衡的角度解释实验Ⅰ的反应过程
(2)测得实验Ⅱ中所用NH4Cl溶液显酸性(pH约为4.5),用离子方程式解释其显酸性的原因
(3)甲同学认为应补充一个实验:向同样的Mg(OH)2沉淀中加4 mL蒸馏水,观察到沉淀不溶解。该实验的目的是
(4)同学们猜测实验Ⅱ中沉淀溶解的原因有两种:一是NH4Cl溶液显酸性,溶液中的H+可以结合OH- ,进而使沉淀溶解;二是
(5)乙同学继续进行实验:向4 mL 2 mol·L-1 NH4Cl溶液中滴加2滴浓氨水,得到pH约为8的混合溶液,向同样的Mg(OH)2沉淀中加入该混合溶液,观察现象。
①实验结果证明(4)中的第二种猜测是成立的,乙同学获得的实验现象是
③乙同学这样配制混合溶液的理由是
您最近一年使用:0次
2016-12-08更新
|
1509次组卷
|
6卷引用:上海杨浦高级中学2018-2019学年高三上学期第一次月考化学试题
10-11高三上·河南鹤壁·阶段练习
9 . (1)“绿色试剂”双氧水可作为矿业废液消毒剂,如消除采矿业废液中的氰化物(如KCN),反应的化学方程式为;KCN+H2O2+H2O=A+NH3↑
回答下列问题:
①生成物A的化学式为______ 。
②在标准状况下若有0.448L氨气生成,则转移的电子数为______ 。
③反应中被氧化的元素为______ 。
(2)在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量和所得沉淀的物质的量的关系如下图所示。则:
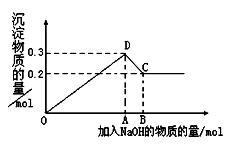
①原溶液中c(Mg2+)∶c(Al3+)为______ 。
②图中C点表示当加入______ mol NaOH时,Al3+已经转化为______ ,Mg2+已经转化为______ 。
③图中线段OA∶AB=______ 。
回答下列问题:
①生成物A的化学式为
②在标准状况下若有0.448L氨气生成,则转移的电子数为
③反应中被氧化的元素为
(2)在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量和所得沉淀的物质的量的关系如下图所示。则:

①原溶液中c(Mg2+)∶c(Al3+)为
②图中C点表示当加入
③图中线段OA∶AB=
您最近一年使用:0次
名校
10 . 生活中碰到的某些问题,常涉及到化学知识,下列分析不正确的是
| A.Mg(OH)2和Al(OH)3热分解生成的气态水可覆盖火焰、驱逐O2、稀释可燃气体,分解产物MgO和Al2O3能较快地与塑料燃烧过程中产生的酸性及腐蚀性气体反应,所以它们可以作为未来发展方向的无机阻燃剂 |
| B.用灼烧并闻气味的方法区别纯棉织物和纯毛织物 |
| C.某雨水样品采集后放置一段时间,pH值由4.68变为4.28,是因为水中溶解了较多的CO2 |
| D.蒙古牧民喜欢用银器盛放鲜牛奶有其科学道理:用银器盛放鲜牛奶,溶入的极微量的银离子,可杀死牛奶中的细菌,防止牛奶变质 |
您最近一年使用:0次
2016-11-15更新
|
200次组卷
|
5卷引用:2017届辽宁省铁岭市高三上学期第一次联考化学试卷



