1 . 在如图的物质转化关系中,A是红棕色固体,B存在于人体胃液中,C是一种气体单质F常用于配制农药波尔多液。图中“→”表示反应的方向,“—”表示连线两端的物质能发生反应;另外,部分反应物、生成物在图中省略。
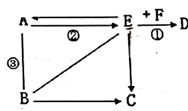
(1)B的化学式为___________
(2)反应①的基本反应类型是___________ 反应②的条件是___________
(3)反应③的化学方程式是___________ 其在生产生活中可用于___________

(1)B的化学式为
(2)反应①的基本反应类型是
(3)反应③的化学方程式是
您最近一年使用:0次
2 . A、B、C为中学常见单质,其中一种为金属,通常情况下,A为固体,B为黄绿色气体,C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体。它们之间的转化关系如图所示(其中某些反应条件和部分反应物已略去)。
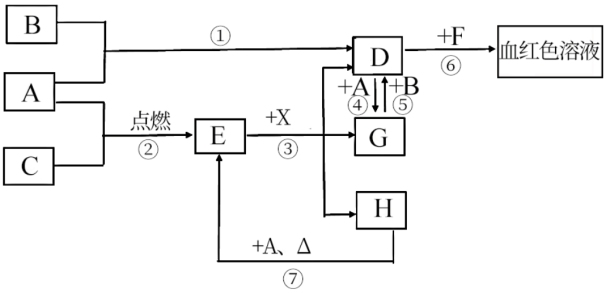
请回答下列问题:
(1)写出下列物质的化学式:D_______ 、X_______ 。
(2)在反应①~⑦中,不属于氧化还原反应的是_______ 。
(3)反应④的离子方程式是_______ ;
(4)反应⑦的化学方程式是:_______ ;该反应中每消耗0.3mol的A,可转移电子_______ mol。
(5)除去D溶液中混有的少量G的方法是_______ 。
(6)检验G溶液中阳离子的方法是_______ 。

请回答下列问题:
(1)写出下列物质的化学式:D
(2)在反应①~⑦中,不属于氧化还原反应的是
(3)反应④的离子方程式是
(4)反应⑦的化学方程式是:
(5)除去D溶液中混有的少量G的方法是
(6)检验G溶液中阳离子的方法是
您最近一年使用:0次
名校
解题方法
3 . 常温下, 与水并不反应,但在高温下,
与水并不反应,但在高温下, 与水蒸气可发生反应应用下图装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“
与水蒸气可发生反应应用下图装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“ 与水蒸气的反应实验”(部分夹持装置已略去),请回答下列问题:
与水蒸气的反应实验”(部分夹持装置已略去),请回答下列问题:
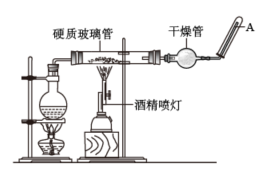
(1)写出该反应的化学方程式_______ 。
(2)硬质玻璃管中石棉绒的作用是__ ,圆底烧瓶中盛装水,且应事先放置___ ,其作用是___ 。
(3)该同学欲确定反应后硬质玻璃管中固体物质的成分,设计了如下实验方案:
①待硬质玻璃管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B,向其中滴加KSCN溶液,若溶液变红色,则说明硬质玻璃管中固体物质的成分是___ ,若溶液未变红色,则说明硬质玻璃管中固体物质的成分是___ 。
(4)该同学按上述实验方案进行了实验,结果溶液未变红色。
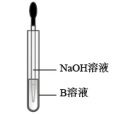
(5)该同学马上另取少童溶液B,使其与NaOH溶液反应。若按下图所示的操作,可观察到生成白色沉淀,在空气中迅速变成灰绿色,最后变成红褐色,请写出与沉淀颜色变化相关的反应的化学方程式____ 。
(6)段时间后,该同学发现(4)中未变红的溶液变成红色,说明 具有
具有___ 性。由此可知,实验室中含 的盐溶液需要现用现配,并且配制含
的盐溶液需要现用现配,并且配制含 的盐溶液时应加入少量
的盐溶液时应加入少量___ 。
 与水并不反应,但在高温下,
与水并不反应,但在高温下, 与水蒸气可发生反应应用下图装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“
与水蒸气可发生反应应用下图装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“ 与水蒸气的反应实验”(部分夹持装置已略去),请回答下列问题:
与水蒸气的反应实验”(部分夹持装置已略去),请回答下列问题:
(1)写出该反应的化学方程式
(2)硬质玻璃管中石棉绒的作用是
(3)该同学欲确定反应后硬质玻璃管中固体物质的成分,设计了如下实验方案:
①待硬质玻璃管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B,向其中滴加KSCN溶液,若溶液变红色,则说明硬质玻璃管中固体物质的成分是
(4)该同学按上述实验方案进行了实验,结果溶液未变红色。
(5)该同学马上另取少童溶液B,使其与NaOH溶液反应。若按下图所示的操作,可观察到生成白色沉淀,在空气中迅速变成灰绿色,最后变成红褐色,请写出与沉淀颜色变化相关的反应的化学方程式

(6)段时间后,该同学发现(4)中未变红的溶液变成红色,说明
 具有
具有 的盐溶液需要现用现配,并且配制含
的盐溶液需要现用现配,并且配制含 的盐溶液时应加入少量
的盐溶液时应加入少量
您最近一年使用:0次
解题方法
4 . 同学们在实验室中进行了铁粉与水蒸气的反应。
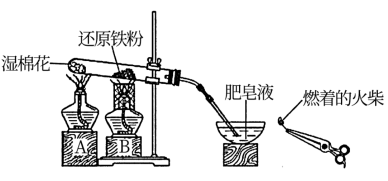
(1)铁粉与水蒸气反应的化学方程式是_______ 。
(2)B处酒精灯上网罩的作用是_______ 。
(3)实验开始时,应先点燃_______ (填“A”或“B”)处的酒精灯。实验开始后,用燃着的火柴点燃肥皂泡时的现象是_______ 。
(4)同学们对反应后黑色固体的成分展开了探究:将黑色固体用足量的FeCl3溶液浸泡,除去未反应的铁,有关反应的离子方程式是_______ 。然后过滤,将滤渣洗涤、干燥后,用磁铁吸引,观察到_______ ,证明黑色固体中含有Fe3O4。

(1)铁粉与水蒸气反应的化学方程式是
(2)B处酒精灯上网罩的作用是
(3)实验开始时,应先点燃
(4)同学们对反应后黑色固体的成分展开了探究:将黑色固体用足量的FeCl3溶液浸泡,除去未反应的铁,有关反应的离子方程式是
您最近一年使用:0次
名校
解题方法
5 . 在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物,该氧化物又被 H2还原,生成颗粒很细的铁粉,这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称"引火铁"。回答下列问题∶
I.利用图1所示装置(加热装置省略)制取铁的氧化物
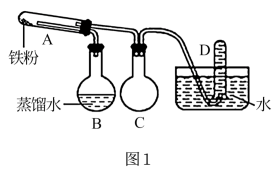
(1)试管 A中发生反应的化学方程式是___________ ,该反应的氧化剂是___________ 。
(2)烧瓶 B的作用是___________ 。
II.利用图2所示装置制取"引火铁"
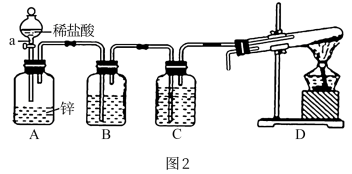
(1)仪器 a的名称是___________ 。
(2)装置 B的作用是___________ ;装置C中盛放的试剂是___________ ,其作用是___________ 。
(3)为了安全,在试管中的反应发生前,在导管出口处必须___________ 。
I.利用图1所示装置(加热装置省略)制取铁的氧化物

(1)试管 A中发生反应的化学方程式是
(2)烧瓶 B的作用是
II.利用图2所示装置制取"引火铁"

(1)仪器 a的名称是
(2)装置 B的作用是
(3)为了安全,在试管中的反应发生前,在导管出口处必须
您最近一年使用:0次
2021-01-09更新
|
275次组卷
|
5卷引用:山西省运城市高中联合体2020-2021学年高一上学期12月阶段性测试化学试题
10-11高三上·福建福州·阶段练习
名校
解题方法
6 . 已知A是单质,A与盐酸反应得到B溶液和气体,且有以下物质相互转化。

试回答:
(1)写出B的化学式______ D的化学式______ 。
(2)写出由E转变成F的化学方程式______ 。
(3)写出用KSCN鉴别G溶液的离子方程式______ ;向G溶液加入A的有关离子反应方程式______ 。

试回答:
(1)写出B的化学式
(2)写出由E转变成F的化学方程式
(3)写出用KSCN鉴别G溶液的离子方程式
您最近一年使用:0次
2021-01-07更新
|
247次组卷
|
16卷引用:山西省晋中市平遥县第二中学2020届高三10月月考化学试题
山西省晋中市平遥县第二中学2020届高三10月月考化学试题山西省运城市景胜中学2020-2021学年高一9月月考化学试题(已下线)2011届福建省福州金桥高级中学高三12月月考化学试卷(已下线)2012届吉林省汪清县第六中学高三第一次月考化学试卷2015-2016学年山东省淄博市高青一中高一下收心考试化学试卷云南省中央民大附中芒市国际学校2017-2018学年高一下学期期末考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第5讲 无机框图题的解答策略【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第5讲 无机框图题的解答策略【押题专练】【全国百强校】湖北省沙市中学2018-2019学年高一上学期12月月考化学试题黑龙江省大庆市第四中学2018-2019学年高二下学期第二次月考化学试题江西省抚州市南城县第二中学2019-2020学年高一上学期第二次月考化学试题内蒙古通辽市科左后旗甘旗卡第二高级中学2019-2020学年高一下学期期末考试化学试题(已下线)第03章 铁 金属材料(B卷能力提高篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)(已下线)【浙江新东方】双师(39).黑龙江省漠河市高级中学2020-2021学年高一上学期期末考试化学试题甘肃省兰州市教育局第四片区2021-2022学年高一上学期期末考试化学试题
名校
解题方法
7 . 在一定条件下,用普通铁粉和水蒸气反应,可以得到铁的氧化物,该氧化物又可以经此反应的逆反应,生成颗粒很细的铁粉。某校化学小组利用下图所列装置进行铁与水反应的实验,并利用产物进一步与四氧化三铁反应制取铁粉。(装置中的铁架台、铁夹等必要的夹持仪器在图中均已略去)
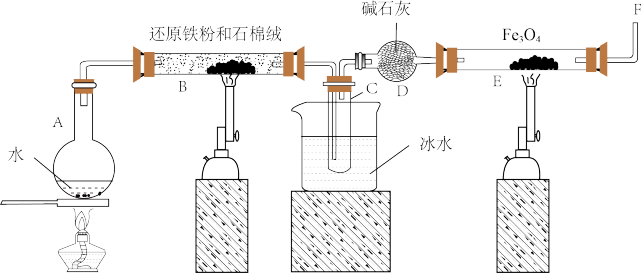
(1)烧瓶A中常加入碎瓷片,其作用是___________________ ,小试管C的作用是______________________________ 。
(2)为了安全,在E管中的反应发生前,在F出口处必须_________________ ,E管中的反应开始后,在F出口处应______________________ 。
(3)反应3Fe+4H2O(g) Fe3O4+4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释
Fe3O4+4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释_____________________ 。
(4)停止反应,待B管冷却后,取其中固体加入过量稀盐酸,充分反应后过滤。简述证明滤液中含有Fe3+的实验操作及现象______________________ 。
(5)若E管中反应按以下两步进行:Fe3O4+H2 3FeO+H2O,FeO+H2
3FeO+H2O,FeO+H2 Fe+H2O,假设实验开始时E管中的Fe3O4为23.2 g,反应一段时间后停止实验,冷却后取出其中固体干燥后称量,其质量变为20 g。通过计算分析其组成可能为
Fe+H2O,假设实验开始时E管中的Fe3O4为23.2 g,反应一段时间后停止实验,冷却后取出其中固体干燥后称量,其质量变为20 g。通过计算分析其组成可能为________ (填序号)
①Fe ②Fe和Fe3O4 ③FeO和Fe3O4④Fe和FeO ⑤Fe、FeO和Fe3O4
用此20 g固体与铝粉在一定条件下进行铝热反应,最多可消耗铝粉________ g。(不考虑空气中的成分参与反应)

(1)烧瓶A中常加入碎瓷片,其作用是
(2)为了安全,在E管中的反应发生前,在F出口处必须
(3)反应3Fe+4H2O(g)
 Fe3O4+4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释
Fe3O4+4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释(4)停止反应,待B管冷却后,取其中固体加入过量稀盐酸,充分反应后过滤。简述证明滤液中含有Fe3+的实验操作及现象
(5)若E管中反应按以下两步进行:Fe3O4+H2
 3FeO+H2O,FeO+H2
3FeO+H2O,FeO+H2 Fe+H2O,假设实验开始时E管中的Fe3O4为23.2 g,反应一段时间后停止实验,冷却后取出其中固体干燥后称量,其质量变为20 g。通过计算分析其组成可能为
Fe+H2O,假设实验开始时E管中的Fe3O4为23.2 g,反应一段时间后停止实验,冷却后取出其中固体干燥后称量,其质量变为20 g。通过计算分析其组成可能为①Fe ②Fe和Fe3O4 ③FeO和Fe3O4④Fe和FeO ⑤Fe、FeO和Fe3O4
用此20 g固体与铝粉在一定条件下进行铝热反应,最多可消耗铝粉
您最近一年使用:0次
解题方法
8 . X、Y、Z、W、Q五种元素的原子序数依次增大,X原子的半径最小;Y的单质在空气中含量最大;元素Z的焰色在浓雾中最具穿透性;含元素W的化合物很多具有漂白性;Q是最常见金属,位于周期表过渡区。回答问题:
(1)X与Z的化合物 与水反应转移的电子数为
与水反应转移的电子数为____________ 。
(2)用Y的某化合物可检查输送液态W单质的管道是否泄漏,其化学方程式为____________ 。
(3)检查某常见固体物质为 的操作为
的操作为_______________ 。
(4)Q位于周期表的第_________ 周期第________ 族,其单质 溶于
溶于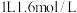 稀硝酸中(只被还原为
稀硝酸中(只被还原为 )的化学方程式为
)的化学方程式为______________ 。
(1)X与Z的化合物
 与水反应转移的电子数为
与水反应转移的电子数为(2)用Y的某化合物可检查输送液态W单质的管道是否泄漏,其化学方程式为
(3)检查某常见固体物质为
 的操作为
的操作为(4)Q位于周期表的第
 溶于
溶于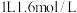 稀硝酸中(只被还原为
稀硝酸中(只被还原为 )的化学方程式为
)的化学方程式为
您最近一年使用:0次
解题方法
9 . 喷泉是一种常见的现象,其产生的原理是存在压强差。

试回答下列问题:
(1)实验室制取氨气的化学方程式为________ 。
①用图A装置进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是_______ 。
②利用图B装置引发喷泉的操作是___________ 。
(2)利用图C装置,在锥形瓶中分别加入足量的下列物质,反应后可能产生喷泉的有______ 。
A. 与稀盐酸 B.
与稀盐酸 B. 与稀硫酸
与稀硫酸
C. 与稀硝酸 D.
与稀硝酸 D. 溶液与
溶液与 溶液
溶液
(3)在图D装置的锥形瓶中加入乙醇,瓶外放一水槽,水槽中加入冷水后,再加入足量的下列物质,结果也形成了喷泉,水槽中加入的物质可能是_____ 。
A 浓硫酸 B 食盐 C 硝酸钾 D 硫酸铜
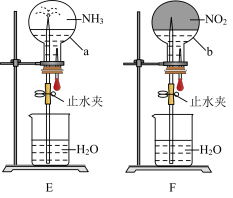
(4)同温同压下,两个等体积的干燥圆底烧瓶中分别充满 和
和 ,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有
,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有 体积的液体,则两烧瓶内溶质的物质的量浓度的关系是
体积的液体,则两烧瓶内溶质的物质的量浓度的关系是_______ 。
A.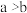 B.
B. C.
C. D.不能确定
D.不能确定

试回答下列问题:
(1)实验室制取氨气的化学方程式为
①用图A装置进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是
②利用图B装置引发喷泉的操作是
(2)利用图C装置,在锥形瓶中分别加入足量的下列物质,反应后可能产生喷泉的有
A.
 与稀盐酸 B.
与稀盐酸 B. 与稀硫酸
与稀硫酸C.
 与稀硝酸 D.
与稀硝酸 D. 溶液与
溶液与 溶液
溶液(3)在图D装置的锥形瓶中加入乙醇,瓶外放一水槽,水槽中加入冷水后,再加入足量的下列物质,结果也形成了喷泉,水槽中加入的物质可能是
A 浓硫酸 B 食盐 C 硝酸钾 D 硫酸铜
(4)同温同压下,两个等体积的干燥圆底烧瓶中分别充满
 和
和 ,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有
,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有 体积的液体,则两烧瓶内溶质的物质的量浓度的关系是
体积的液体,则两烧瓶内溶质的物质的量浓度的关系是
A.
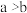 B.
B. C.
C. D.不能确定
D.不能确定
您最近一年使用:0次
2020-09-16更新
|
325次组卷
|
2卷引用:山西省运城市2019-2020学年高一上学期期末调研测试化学试题
名校
解题方法
10 . 工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是___ 。
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用___ (选填序号)。
a.KSCN溶液和氯水 b.K3Fe(CN)6溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的体积分数为___ 。分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和Q气体(Q不考虑水蒸气)。为此设计了下列探究实验装置(图中夹持仪器省略)。
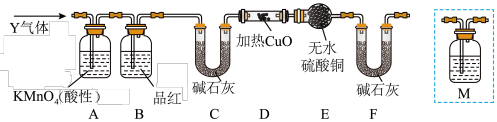
(3)装置B中试剂的作用是___ 。
(4)如果气体Y中含有H2,预计实验现象应是___ 。
(5)认为气体Y中还含有Q的理由是___ (用化学方程式表示)。
(6)为确认Q的存在,需在装置中添加M于___ (选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用
a.KSCN溶液和氯水 b.K3Fe(CN)6溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的体积分数为

(3)装置B中试剂的作用是
(4)如果气体Y中含有H2,预计实验现象应是
(5)认为气体Y中还含有Q的理由是
(6)为确认Q的存在,需在装置中添加M于
a.A之前 b.A-B间 c.B-C间 d.C-D间
您最近一年使用:0次



