1 . 氯气是一种重要的化工原料,在生产和生活中的应用十分广泛,可用于制漂白剂等。
Ⅰ.制新型灭菌消毒剂ClO2.在通常状况下,ClO2能溶于水,在水中的杀菌、消毒能力比Cl2强,且ClO2、Cl2在杀菌、消毒时均被还原为Cl-;浓的ClO2受热时易爆炸。
(1)制备ClO2反应为Cl2+2NaClO2=2NaCl+2ClO2,实验装置如下图所示:
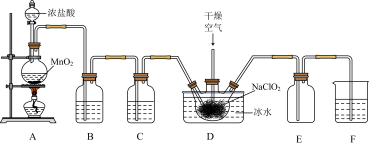
①装置A中发生反应的化学方程式为___________ ,装置B中盛放的试剂为___________ 。
②装置D中将三颈烧瓶置于冰水浴中并向其中通入干燥空气的目的是___________ 。
(2)等物质的量的ClO2和Cl2相比,ClO2的杀菌、消毒能力强于Cl2的原因是___________ 。
Ⅱ.制优良的饮用水消毒剂Na2FeO4.Na2FeO4具有很强的氧化性,能有效地杀灭水中的病菌和病毒,同时自身被还原成新生态的Fe(OH)3。
(3)制备方法如下:Fe(NO3)3+NaOH+Cl2—Na2FeO4+NaNO3+NaCl+H2O(未配平)。
①Na2FeO4中铁元素的化合价是___________ ,Na2FeO4属于___________ (填序号)。
A.酸 B.碱 C.盐 D.氧化物
②Na2FeO4作饮用水消毒剂的同时也能够起到净水作用的原因是___________ 。
Ⅰ.制新型灭菌消毒剂ClO2.在通常状况下,ClO2能溶于水,在水中的杀菌、消毒能力比Cl2强,且ClO2、Cl2在杀菌、消毒时均被还原为Cl-;浓的ClO2受热时易爆炸。
(1)制备ClO2反应为Cl2+2NaClO2=2NaCl+2ClO2,实验装置如下图所示:

①装置A中发生反应的化学方程式为
②装置D中将三颈烧瓶置于冰水浴中并向其中通入干燥空气的目的是
(2)等物质的量的ClO2和Cl2相比,ClO2的杀菌、消毒能力强于Cl2的原因是
Ⅱ.制优良的饮用水消毒剂Na2FeO4.Na2FeO4具有很强的氧化性,能有效地杀灭水中的病菌和病毒,同时自身被还原成新生态的Fe(OH)3。
(3)制备方法如下:Fe(NO3)3+NaOH+Cl2—Na2FeO4+NaNO3+NaCl+H2O(未配平)。
①Na2FeO4中铁元素的化合价是
A.酸 B.碱 C.盐 D.氧化物
②Na2FeO4作饮用水消毒剂的同时也能够起到净水作用的原因是
您最近一年使用:0次
名校
解题方法
2 . 将1.12g铁粉加入25mL2mol∙L-1的FeCl3溶液中,充分反应后,其结果正确的是
| A.铁粉有剩余,溶液呈浅绿色,Cl-的量保持不变 |
| B.往溶液中滴入KSCN溶液,溶液不显红色 |
| C.Fe2+和Fe3+的物质的量之比为1:6 |
| D.氧化产物和还原产物的物质的量之比为1:2 |
您最近一年使用:0次
名校
解题方法
3 . 下列反应的离子方程式正确的是
A.溴与冷的NaOH溶液反应: |
B.少量 通入 通入 溶液中: 溶液中: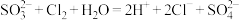 |
C.向血红色 溶液中加入过量铁粉至溶液褪色: 溶液中加入过量铁粉至溶液褪色: |
D.向含氯化铁的氯化镁溶液中加入氧化镁: |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
4 . 以硫酸渣(含Fe2O3、SiO2等)为原料制备铁黄(FeOOH)的一种工艺流程如图:
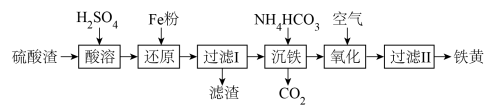
(1)“酸溶”中加快溶解的方法为_______ (任意写出一种)。
(2)“还原”过程中的离子方程式为_______ 。
(3)写出“滤渣”中主要成分的化学式:_______ 。
(4)①“沉铁”过程中生成Fe(OH)2的化学方程式为_______ 。
②若用CaCO3“沉铁”,则生成FeCO3沉淀。当反应完成时,溶液中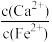 =
=_______ 。[已知Ksp(CaCO3)=2.8×10-9,Ksp(FeCO3)=2×10-11]
(5)“氧化”时,用NaNO2浓溶液代替空气氧化Fe(OH)2浆液,能缩短氧化时间,但缺点是_______ 。

(1)“酸溶”中加快溶解的方法为
(2)“还原”过程中的离子方程式为
(3)写出“滤渣”中主要成分的化学式:
(4)①“沉铁”过程中生成Fe(OH)2的化学方程式为
②若用CaCO3“沉铁”,则生成FeCO3沉淀。当反应完成时,溶液中
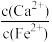 =
=(5)“氧化”时,用NaNO2浓溶液代替空气氧化Fe(OH)2浆液,能缩短氧化时间,但缺点是
您最近一年使用:0次
解题方法
5 . 认识物质的转化关系能更好地制备物质。某化学学习小组研究发现在合适条件下有多种元素及其化合物的转化符合如图所示的转化关系,下列说法错误的是


| A.若化合物甲具有特殊香味,X为氧气,则甲与丙反应可生成有香味的液体 |
| B.若甲为常见非金属单质,丙的浓溶液能与铜发生氧化还原反应,则甲一定是氮气 |
| C.若甲是常见的简单氢化物,丙与水反应后溶液显酸性,则乙可能是氧化物 |
| D.若甲为黄绿色气体,则2mol乙与足量X反应可生成3mol丙 |
您最近一年使用:0次
6 . 甲、乙、丙三种物质间通过一步反应能实现如图转化,下列选项中符合转化关系的是


A.甲为 ,乙为 ,乙为 ,丙为 ,丙为 |
B.甲为 ,乙为 ,乙为 ,丙为 ,丙为 |
C.甲为 ,乙为 ,乙为 ,丙为 ,丙为 |
D.甲为 ,乙为 ,乙为 ,丙为 ,丙为 |
您最近一年使用:0次
名校
7 . 向稀硫酸和稀硝酸的混合溶液200 mL中逐渐加入铁粉,产生气体的量随铁粉质量的变化如图所示(已知硝酸只被还原为NO气体)。下列分析错误的是
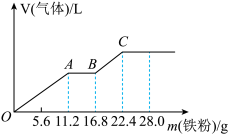

A.OA段产生的是NO,AB段的反应为 |
B.A点溶液中的溶质为 和 和 |
C.原混合酸中 的物质的量浓度为2mol·L 的物质的量浓度为2mol·L |
D.原混合酸中 和 和 物质的量之比为2∶1 物质的量之比为2∶1 |
您最近一年使用:0次
8 . 乳酸亚铁晶体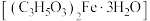 是一种吸收效果很好的食品铁强化剂,易溶于水,难溶于乙醇。某兴趣小组用废铁屑(部分被氧化)制备
是一种吸收效果很好的食品铁强化剂,易溶于水,难溶于乙醇。某兴趣小组用废铁屑(部分被氧化)制备 ,再与乳酸反应制得乳酸亚铁晶体。
,再与乳酸反应制得乳酸亚铁晶体。
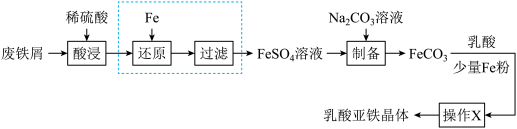
(1)“酸浸”时, 单质发生反应的离子方程式有
单质发生反应的离子方程式有___________ 。
(2)向酸浸液中滴加___________ (填化学式)溶液可判断是否要进行“还原”、“过滤”操作;在实验室中进行过滤操作需要的玻璃仪器有___________ 。
(3)制备过程中将 溶液加入
溶液加入 溶液中制得
溶液中制得 。
。
①该反应的离子方程式为___________ 。
②若 置于空气中时间过长,表面生成
置于空气中时间过长,表面生成 ,其原因是
,其原因是___________ (用化学方程式表示)。
(4) 与乳酸反应过程中加入少量铁粉的目的是
与乳酸反应过程中加入少量铁粉的目的是___________ 。
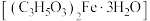 是一种吸收效果很好的食品铁强化剂,易溶于水,难溶于乙醇。某兴趣小组用废铁屑(部分被氧化)制备
是一种吸收效果很好的食品铁强化剂,易溶于水,难溶于乙醇。某兴趣小组用废铁屑(部分被氧化)制备 ,再与乳酸反应制得乳酸亚铁晶体。
,再与乳酸反应制得乳酸亚铁晶体。
(1)“酸浸”时,
 单质发生反应的离子方程式有
单质发生反应的离子方程式有(2)向酸浸液中滴加
(3)制备过程中将
 溶液加入
溶液加入 溶液中制得
溶液中制得 。
。①该反应的离子方程式为
②若
 置于空气中时间过长,表面生成
置于空气中时间过长,表面生成 ,其原因是
,其原因是(4)
 与乳酸反应过程中加入少量铁粉的目的是
与乳酸反应过程中加入少量铁粉的目的是
您最近一年使用:0次
名校
9 . 一种以钛铁矿( ,含
,含 、CaO、
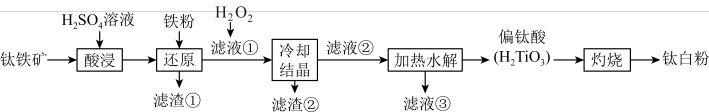
、CaO、 等杂质)为主要原料制备钛白粉(
等杂质)为主要原料制备钛白粉( )的工艺流程如图所示。
)的工艺流程如图所示。
已知:
① 不溶于水和稀酸;
不溶于水和稀酸;
②“酸浸”后钛元素主要以 形式存在;
形式存在;
③ 在pH=1.8时生成沉淀,pH=4.1时沉淀完全。
在pH=1.8时生成沉淀,pH=4.1时沉淀完全。
回答下列问题:
(1)“酸浸”时,常将钛铁矿粉碎,并进行搅拌,其目的是_____ 。
(2)“酸浸”时, 发生反应的化学方程式为
发生反应的化学方程式为_____ 。
(3)滤渣①的主要成分是_____ 、_____ (填化学式)和 。
。
(4)流程中加入铁粉的目的是还原体系中的 ,反应的离子方程式为
,反应的离子方程式为_____ 。为探究最佳反应条件,某化学兴趣小组在保持反应时间相同的情况下进行探究得到结果如下图所示。
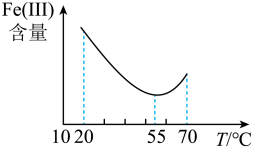
保持其它反应条件不变,还原体系中Fe(Ⅲ)含量随温度变化如图所示。由图可知,还原体系中Fe(Ⅲ)的最佳反应温度为_____ ℃。
(5)经处理后,流程中可循环利用的物质除Fe外,还有_____ (填化学式)。
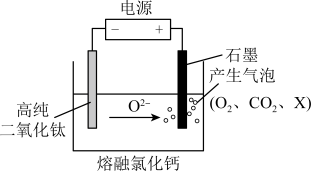
(6)如图为EFC剑桥法用固体二氧化钛( )生产海绵钛的装置示意图,其原理是在较低的阴极电位下,
)生产海绵钛的装置示意图,其原理是在较低的阴极电位下, (阴极)中的氧解离进入熔盐,阴极最后只剩下纯钛。阴极的电极反应式为
(阴极)中的氧解离进入熔盐,阴极最后只剩下纯钛。阴极的电极反应式为__________ ,产生的气体中X的化学式为_____ 。
 ,含
,含 、CaO、
、CaO、 等杂质)为主要原料制备钛白粉(
等杂质)为主要原料制备钛白粉( )的工艺流程如图所示。
)的工艺流程如图所示。
已知:
①
 不溶于水和稀酸;
不溶于水和稀酸;②“酸浸”后钛元素主要以
 形式存在;
形式存在;③
 在pH=1.8时生成沉淀,pH=4.1时沉淀完全。
在pH=1.8时生成沉淀,pH=4.1时沉淀完全。回答下列问题:
(1)“酸浸”时,常将钛铁矿粉碎,并进行搅拌,其目的是
(2)“酸浸”时,
 发生反应的化学方程式为
发生反应的化学方程式为(3)滤渣①的主要成分是
 。
。(4)流程中加入铁粉的目的是还原体系中的
 ,反应的离子方程式为
,反应的离子方程式为
保持其它反应条件不变,还原体系中Fe(Ⅲ)含量随温度变化如图所示。由图可知,还原体系中Fe(Ⅲ)的最佳反应温度为
(5)经处理后,流程中可循环利用的物质除Fe外,还有
(6)如图为EFC剑桥法用固体二氧化钛(
 )生产海绵钛的装置示意图,其原理是在较低的阴极电位下,
)生产海绵钛的装置示意图,其原理是在较低的阴极电位下, (阴极)中的氧解离进入熔盐,阴极最后只剩下纯钛。阴极的电极反应式为
(阴极)中的氧解离进入熔盐,阴极最后只剩下纯钛。阴极的电极反应式为
您最近一年使用:0次
名校
10 . 向一定质量 和
和 的混合溶液中逐渐加入足量的锌粒,下列图像能正确反映对应关系的是
的混合溶液中逐渐加入足量的锌粒,下列图像能正确反映对应关系的是
 和
和 的混合溶液中逐渐加入足量的锌粒,下列图像能正确反映对应关系的是
的混合溶液中逐渐加入足量的锌粒,下列图像能正确反映对应关系的是A.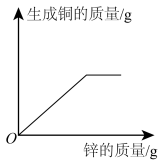 | B.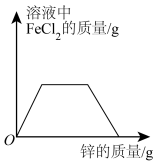 |
C.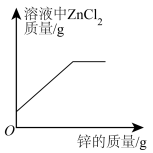 | D.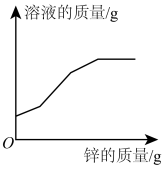 |
您最近一年使用:0次
2023-09-28更新
|
207次组卷
|
4卷引用:安徽省九师联盟2023-2024学年高三上学期9月月考化学试题



