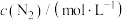名校
解题方法
1 . I.我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
a)CH4(g)+CO2(g) 2CO(g)+2H2(g) ∆H1
2CO(g)+2H2(g) ∆H1
b)CO2(g)+H2(g) CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2
c)CH4(g) C(s)+2H2(g) ∆H3
C(s)+2H2(g) ∆H3
d)2CO(g) CO2(g)+C(s) ∆H4
CO2(g)+C(s) ∆H4
e)CO(g)+H2(g) H2O(g)+C(s) ∆H5
H2O(g)+C(s) ∆H5
(1)根据盖斯定律,反应a的∆H1=___________ (写出一个代数式即可)。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
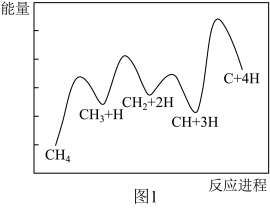
(3)一定条件下,CH4分解形成碳的反应历程如图1所示。该历程分___________ 步进行,其中,第___________ 步的正反应活化能最大。
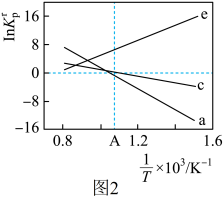
(4)设 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(kPa)除以p0(p0=100kPa)。反应a、c、e的
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(kPa)除以p0(p0=100kPa)。反应a、c、e的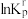 随
随 (温度的倒数)的变化如图2所示。
(温度的倒数)的变化如图2所示。
①反应a、c、e中,属于吸热反应的有___________ (填字母)。
②反应c的相对压力平衡常数表达式为 =
=___________ 。
③在图2中A点对应温度下、原料组成为n(CO2):n(CH4)=1:1、初始总压为100kPa的恒容密闭容器中进行反应,体系达到平衡时H2的分压为40kPa。则CH4的平衡转化率为___________ 。
a)CH4(g)+CO2(g)
 2CO(g)+2H2(g) ∆H1
2CO(g)+2H2(g) ∆H1b)CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2c)CH4(g)
 C(s)+2H2(g) ∆H3
C(s)+2H2(g) ∆H3d)2CO(g)
 CO2(g)+C(s) ∆H4
CO2(g)+C(s) ∆H4e)CO(g)+H2(g)
 H2O(g)+C(s) ∆H5
H2O(g)+C(s) ∆H5(1)根据盖斯定律,反应a的∆H1=
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
| A.增大CO2与CH4的浓度,反应a、b、c的正反应速率都增加 |
| B.移去部分C(s),反应c、d、e的平衡均向右移动 |
| C.加入反应a的催化剂,可提高CH4的平衡转化率 |
| D.降低反应温度,反应a~e的正、逆反应速率都减小 |


(4)设
 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(kPa)除以p0(p0=100kPa)。反应a、c、e的
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(kPa)除以p0(p0=100kPa)。反应a、c、e的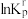 随
随 (温度的倒数)的变化如图2所示。
(温度的倒数)的变化如图2所示。①反应a、c、e中,属于吸热反应的有
②反应c的相对压力平衡常数表达式为
 =
=③在图2中A点对应温度下、原料组成为n(CO2):n(CH4)=1:1、初始总压为100kPa的恒容密闭容器中进行反应,体系达到平衡时H2的分压为40kPa。则CH4的平衡转化率为
您最近一年使用:0次
2021-10-18更新
|
561次组卷
|
3卷引用:福建省莆田第一中学2022-2023学年高二上学期第一学段考试化学试题
2 . 研究氮氧化物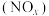 还原处理方法是环保领域的主要方向之一。上海复兴路的“生态马路”运用了“光触媒”技术,即在路面上涂了一层光催化剂涂料,可将汽车尾气中部分NO和
还原处理方法是环保领域的主要方向之一。上海复兴路的“生态马路”运用了“光触媒”技术,即在路面上涂了一层光催化剂涂料,可将汽车尾气中部分NO和 转化为
转化为 和
和 。
。
(1)在密闭容器中发生该反应,氮气浓度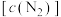 随温度
随温度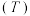 、时间
、时间 的变化关系如下表。
的变化关系如下表。
据此判断:
①
___________  (填“>”或“<”)。
(填“>”或“<”)。
② 时,
时, 内的
内的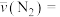
___________  。
。
(2)在绝热、恒容的密闭体系中充入一定量的 和
和 气体,反应达到平衡的标志是_______。
气体,反应达到平衡的标志是_______。
(3)计算机模拟 还原
还原 的反应经历以下3个步骤:
的反应经历以下3个步骤:
I: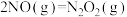
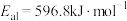
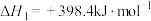
II:
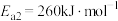
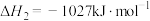
III :
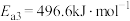
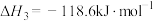
①反应过程的决速步骤是___________ (填“I”“II”或“III”)。
②总反应的热化学方程式为___________ 。
(4)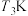 时,在刚性密闭容器中充入物质的量之比为
时,在刚性密闭容器中充入物质的量之比为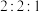 的
的 、
、 和
和 的混合气体,起始气体总压强为
的混合气体,起始气体总压强为 ,达到平衡时气体总压强为
,达到平衡时气体总压强为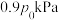 。实验测得:
。实验测得: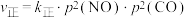 ,
,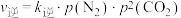 ,其中
,其中 、
、 分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=总压×物质的量分数)。
分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=总压×物质的量分数)。
①平衡后升高温度, 增大的倍数比
增大的倍数比 的
的___________ (填“大”或“小”)。
② 的平衡转化率为
的平衡转化率为___________ 。
③
___________ (用含 的代数式表示)。
的代数式表示)。
(5)该反应的某种催化剂的催化效率与NO的消耗速率随温度的变化关系如图所示。300~350℃之间,NO的消耗速率加快的原因是___________ 。

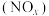 还原处理方法是环保领域的主要方向之一。上海复兴路的“生态马路”运用了“光触媒”技术,即在路面上涂了一层光催化剂涂料,可将汽车尾气中部分NO和
还原处理方法是环保领域的主要方向之一。上海复兴路的“生态马路”运用了“光触媒”技术,即在路面上涂了一层光催化剂涂料,可将汽车尾气中部分NO和 转化为
转化为 和
和 。
。(1)在密闭容器中发生该反应,氮气浓度
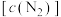 随温度
随温度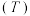 、时间
、时间 的变化关系如下表。
的变化关系如下表。
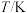 | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
 | 0 | 0.10 | 0.18 | 0.25 | 0.25 | 0.25 | 0.25 |
 | 0 | 0.08 | 0.15 | 0.21 | 0.26 | 0.29 | 0.29 |
①

 (填“>”或“<”)。
(填“>”或“<”)。②
 时,
时, 内的
内的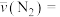
 。
。(2)在绝热、恒容的密闭体系中充入一定量的
 和
和 气体,反应达到平衡的标志是_______。
气体,反应达到平衡的标志是_______。| A.体系温度不变 | B. |
C. 的体积分数不变 的体积分数不变 | D. |
 还原
还原 的反应经历以下3个步骤:
的反应经历以下3个步骤:I:
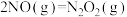
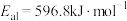
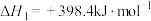
II:

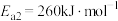
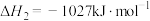
III :

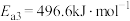
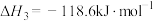
①反应过程的决速步骤是
②总反应的热化学方程式为
(4)
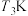 时,在刚性密闭容器中充入物质的量之比为
时,在刚性密闭容器中充入物质的量之比为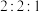 的
的 、
、 和
和 的混合气体,起始气体总压强为
的混合气体,起始气体总压强为 ,达到平衡时气体总压强为
,达到平衡时气体总压强为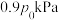 。实验测得:
。实验测得: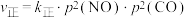 ,
,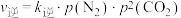 ,其中
,其中 、
、 分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=总压×物质的量分数)。
分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=总压×物质的量分数)。①平衡后升高温度,
 增大的倍数比
增大的倍数比 的
的②
 的平衡转化率为
的平衡转化率为③

 的代数式表示)。
的代数式表示)。(5)该反应的某种催化剂的催化效率与NO的消耗速率随温度的变化关系如图所示。300~350℃之间,NO的消耗速率加快的原因是

您最近一年使用:0次
3 . 镁和卤素单质( )反应的相对能量变化如图所示,下列说法正确的是
)反应的相对能量变化如图所示,下列说法正确的是
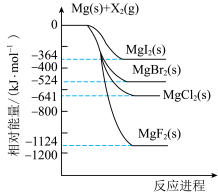
 )反应的相对能量变化如图所示,下列说法正确的是
)反应的相对能量变化如图所示,下列说法正确的是
A.热稳定性: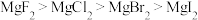 |
| B.1mol碘晶体与足量的Mg充分反应,放热364kJ |
C.工业上常用电解 溶液的方法冶炼金属Mg 溶液的方法冶炼金属Mg |
D.由图可知, 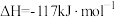 |
您最近一年使用:0次
2023-10-28更新
|
226次组卷
|
2卷引用:福建省漳州市东山县2023-2024学年高二上学期期中考试化学试题
4 . N2H4(肼)常用作火箭推进剂。
已知:①N2(g)+2O2(g)=2NO2(g) ΔH1=+67.2kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(l) ΔH2=-534kJ/mol,
请写出气态N2H4(肼)在NO2气体中燃烧,生成N2、液态H2O反应的热化学方程式___________ 。
已知:①N2(g)+2O2(g)=2NO2(g) ΔH1=+67.2kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(l) ΔH2=-534kJ/mol,
请写出气态N2H4(肼)在NO2气体中燃烧,生成N2、液态H2O反应的热化学方程式
您最近一年使用:0次
解题方法
5 . 甲醇是重要的化工原料。回答下列问题:
(1)以Na2CO3固体为催化剂,甲醇脱氢可制得甲醛。反应机理如下:
(i)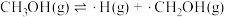 ;
;
(ii)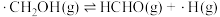 ;
;
(iii)
①(i)中反应物的总能量___________ (填“>”“=”或“<”)生成物的总能量。
②某温度时反应(i)、(ii)、(iii)的平衡常数依次为K1、K2、K3,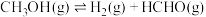 的平衡常数为K,则K=
的平衡常数为K,则K=___________ (用含K1、K2、K3的代数式表示)。
(2)向体积为1L恒容反应器中加入2mlCH3OH及适量催化剂,发生反应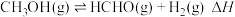 ,在T1、T2(T1<T2)时,CH3OH转化率与时间关系如图所示。
,在T1、T2(T1<T2)时,CH3OH转化率与时间关系如图所示。
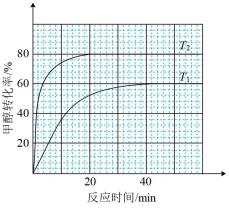
①T2温度下,20min时甲醇的体积分数为___________ %(保留三位有效数字),前20min平均反应速率v(HCHO)=___________  。
。
②T1温度下该反应的平衡常数Kp=___________ kPa(用平衡分压代替平衡浓度计算,分压=总压 物质的量分数,反应器内的初始压强为1
物质的量分数,反应器内的初始压强为1 103kPa)。
103kPa)。
(3)固体氧化物甲醇燃料电池是能效高、环境友好地转化成电能的全固态电源,工作原理如图所示。
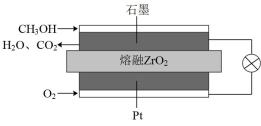
①石墨极上的反应式为___________ 。
②若通过用电器的电子的物质的量为1.2mol,则消耗标准状况下O2的体积为___________ L。
(1)以Na2CO3固体为催化剂,甲醇脱氢可制得甲醛。反应机理如下:
(i)
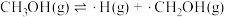 ;
;(ii)
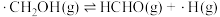 ;
;(iii)

①(i)中反应物的总能量
②某温度时反应(i)、(ii)、(iii)的平衡常数依次为K1、K2、K3,
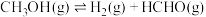 的平衡常数为K,则K=
的平衡常数为K,则K=(2)向体积为1L恒容反应器中加入2mlCH3OH及适量催化剂,发生反应
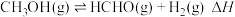 ,在T1、T2(T1<T2)时,CH3OH转化率与时间关系如图所示。
,在T1、T2(T1<T2)时,CH3OH转化率与时间关系如图所示。
①T2温度下,20min时甲醇的体积分数为
 。
。②T1温度下该反应的平衡常数Kp=
 物质的量分数,反应器内的初始压强为1
物质的量分数,反应器内的初始压强为1 103kPa)。
103kPa)。(3)固体氧化物甲醇燃料电池是能效高、环境友好地转化成电能的全固态电源,工作原理如图所示。

①石墨极上的反应式为
②若通过用电器的电子的物质的量为1.2mol,则消耗标准状况下O2的体积为
您最近一年使用:0次
名校
6 . 火箭推进器中装有还原剂液态肼(N2H4)和氧化剂过氧化氢(H2O2),当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65kJ的热量。回答下列问题:
(1)过氧化氢的电子式是___________ 。
(2)该反应的热化学方程式为___________ 。
(3)实验室可用次氯酸钠溶液与氨气反应制备液态肼,已知生成物之一是常见的盐,则反应的化学方程式为___________ 。
(4)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
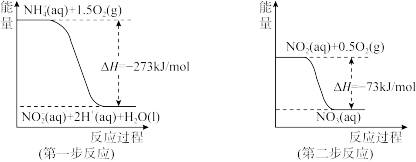
①第一步反应是___________ (填“放热”或“吸热”)反应,判断依据是___________ 。
②1 mol NH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的反应热ΔH是
(aq)的反应热ΔH是___________ 。
(5)已知: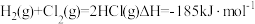 ,几种化学键的键能如下表所示,则a=
,几种化学键的键能如下表所示,则a=___________ 。
(1)过氧化氢的电子式是
(2)该反应的热化学方程式为
(3)实验室可用次氯酸钠溶液与氨气反应制备液态肼,已知生成物之一是常见的盐,则反应的化学方程式为
(4)在微生物作用的条件下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
①第一步反应是
②1 mol NH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的反应热ΔH是
(aq)的反应热ΔH是(5)已知:
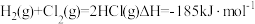 ,几种化学键的键能如下表所示,则a=
,几种化学键的键能如下表所示,则a=| 共价键 | H-H | Cl-Cl | H-Cl |
键能/( ) ) | 436 | 247 | a |
您最近一年使用:0次
2023-10-24更新
|
206次组卷
|
2卷引用:福建省漳州市东山县2023-2024学年高二上学期期中考试化学试题
7 . 化学家发现物质的能量变化与其反应路径无关。依据图示关系,下列说法错误的是


| A.石墨燃烧是放热反应 |
B.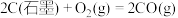 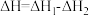 |
C.化学反应的 ,只与反应体系的始态和终态有关,与反应途径无关 ,只与反应体系的始态和终态有关,与反应途径无关 |
D.1 mol C(石墨)和1mol CO分别在足量 中燃烧,全部转化为 中燃烧,全部转化为 ,前者放热多 ,前者放热多 |
您最近一年使用:0次
8 . HCl(g)溶于大量水的过程放热,循环关系如图所示:下列说法不正确的是
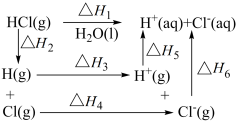

A.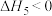 , ,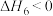 |
B.若将循环图中 元素改成 元素改成 元素,相应的 元素,相应的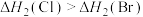 |
C.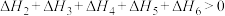 |
D.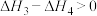 |
您最近一年使用:0次
2023-04-21更新
|
216次组卷
|
4卷引用:福建省南安市华侨中学2023-2024学年高二上学期8月月考化学试题
名校
解题方法
9 . 黑火药爆炸的热化学方程式为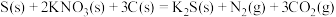
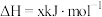
已知: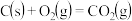

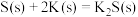
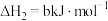
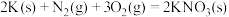
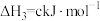 则
则 为
为
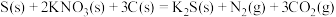
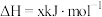
已知:
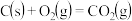

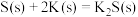
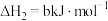
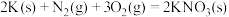
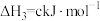 则
则 为
为A.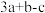 | B.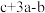 | C.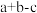 | D.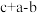 |
您最近一年使用:0次
名校
10 . 回答下列问题:
(1)在25℃、101 kPa下,1 g液态甲醇(CH3OH)燃烧生成CO2和液态水时放热22.7 kJ,则该反应的热化学方程式应为_______ 。
(2)由氢气和氧气反应生成1 mol液态水时放热285.8 kJ,写出该反应的热化学方程式_______ ;若1g水蒸气转化成液态水放热2.4 kJ,则反应2H2(g) + O2(g) = 2H2O(g)的△H=_______ 。
(3)已知:① Cs+O2g=CO2g; H=-393.5 kJ·mol1
② 2COg+O2g=2CO2g; H=-566 kJ·mol1
③ TiO2s+2Cl2g=TiCl4s+O2g; H=+141 kJ·mol1
则TiO2s+2Cl2g+2Cs=TiCl4s+2COg的H=_______ 。
(4)把煤作为燃料可通过下列两种途径:
途径Ⅰ C(s)+O2(g)=CO2(g);ΔH1<0 ①
途径Ⅱ 先制成水煤气:
C(s)+H2O(g)=CO(g)+H2(g);ΔH2>0 ②
再燃烧水煤气:
2CO(g)+O2(g)=2CO2(g);ΔH3<0 ③
2H2(g)+O2(g)=2H2O(g); ΔH4<0 ④
请回答下列问题:
①途径Ⅰ放出的热量理论上_______ (填“大于”“等于”或“小于”)途径Ⅱ放出的热量。
②ΔH1、ΔH2、ΔH3、ΔH4的数学关系式是_______ 。
(1)在25℃、101 kPa下,1 g液态甲醇(CH3OH)燃烧生成CO2和液态水时放热22.7 kJ,则该反应的热化学方程式应为
(2)由氢气和氧气反应生成1 mol液态水时放热285.8 kJ,写出该反应的热化学方程式
(3)已知:① Cs+O2g=CO2g; H=-393.5 kJ·mol1
② 2COg+O2g=2CO2g; H=-566 kJ·mol1
③ TiO2s+2Cl2g=TiCl4s+O2g; H=+141 kJ·mol1
则TiO2s+2Cl2g+2Cs=TiCl4s+2COg的H=
(4)把煤作为燃料可通过下列两种途径:
途径Ⅰ C(s)+O2(g)=CO2(g);ΔH1<0 ①
途径Ⅱ 先制成水煤气:
C(s)+H2O(g)=CO(g)+H2(g);ΔH2>0 ②
再燃烧水煤气:
2CO(g)+O2(g)=2CO2(g);ΔH3<0 ③
2H2(g)+O2(g)=2H2O(g); ΔH4<0 ④
请回答下列问题:
①途径Ⅰ放出的热量理论上
②ΔH1、ΔH2、ΔH3、ΔH4的数学关系式是
您最近一年使用:0次