名校
解题方法
1 . 研究碳及其化合物的资源化利用具有重要的意义。回答下列问题:
(1)已知下列热化学方程式:
反应I:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH1=-164.9kJ/mol。
CH4(g)+2H2O(g) ΔH1=-164.9kJ/mol。
反应II:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41.2kJ/mol
CO(g)+H2O(g) ΔH2=+41.2kJ/mol
则反应CH4(g)+H2O(g) CO(g)+3H2(g)的ΔH3=
CO(g)+3H2(g)的ΔH3=_______ kJ/mol。
(2)在T°C时,将1molCO2和3molH2加入容积不变的密闭容器中,发生反应I:CO2(g)+4H2(g) CH4(g)+2H2O(g),实验测得CO2的体积分数φ(CO2)如表所示:
CH4(g)+2H2O(g),实验测得CO2的体积分数φ(CO2)如表所示:
①能判断反应CO2(g)+4H2(g) CH4(g)+2H2O(g)达到平衡的是
CH4(g)+2H2O(g)达到平衡的是_______ (填标号)。
A.CO2的消耗速率和CH4的生成速率相等
B.混合气体的密度不再发生变化
C.容器内气体压强不再发生变化
D.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO2的转化率为_______ %(结果保留三位有效数字)。
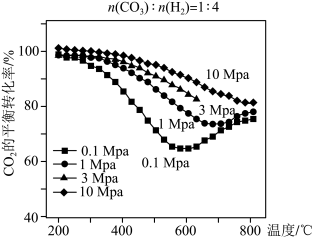
(3)将n(CO2):n(H2)=1:4的混合气体充入密闭容器中发生上述反应I、II,在不同温度和压强时,CO2的平衡转化率如图。0.1MPa时,CO2的转化率在600°C之后,随温度升高而增大的主要原因是_______ 。
(4)在T°C时,向容积为2L的恒容密闭容器中充入1molCO2和一定量的H2发生反应:CO2(g)+2H2(g) =HCHO(g)+H2O(g)。达到平衡时,HCHO的分压与起始
=HCHO(g)+H2O(g)。达到平衡时,HCHO的分压与起始 的关系如图所示:(分压=总压×物质的量分数)
的关系如图所示:(分压=总压×物质的量分数)

①起始时容器内气体的总压强为1.2pkPa,若5min时反应到达c点,v(H2)=_______ mol/(L·min)。
②b点时反应的平衡常数Kp=_______ (kPa)-1(以分压表示)。
③c点时,再加入CO2(g)和H2O(g),使二者分压均增大0.05pkPa,则H2的转化率_______ (填“增大”“不变”或减小”)。
(1)已知下列热化学方程式:
反应I:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH1=-164.9kJ/mol。
CH4(g)+2H2O(g) ΔH1=-164.9kJ/mol。反应II:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41.2kJ/mol
CO(g)+H2O(g) ΔH2=+41.2kJ/mol则反应CH4(g)+H2O(g)
 CO(g)+3H2(g)的ΔH3=
CO(g)+3H2(g)的ΔH3=(2)在T°C时,将1molCO2和3molH2加入容积不变的密闭容器中,发生反应I:CO2(g)+4H2(g)
 CH4(g)+2H2O(g),实验测得CO2的体积分数φ(CO2)如表所示:
CH4(g)+2H2O(g),实验测得CO2的体积分数φ(CO2)如表所示:| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| φ(CO2) | 0.25 | 0.23 | 0.214 | 0.202 | 0.200 | 0.200 |
 CH4(g)+2H2O(g)达到平衡的是
CH4(g)+2H2O(g)达到平衡的是A.CO2的消耗速率和CH4的生成速率相等
B.混合气体的密度不再发生变化
C.容器内气体压强不再发生变化
D.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO2的转化率为
(3)将n(CO2):n(H2)=1:4的混合气体充入密闭容器中发生上述反应I、II,在不同温度和压强时,CO2的平衡转化率如图。0.1MPa时,CO2的转化率在600°C之后,随温度升高而增大的主要原因是

(4)在T°C时,向容积为2L的恒容密闭容器中充入1molCO2和一定量的H2发生反应:CO2(g)+2H2(g)
 =HCHO(g)+H2O(g)。达到平衡时,HCHO的分压与起始
=HCHO(g)+H2O(g)。达到平衡时,HCHO的分压与起始 的关系如图所示:(分压=总压×物质的量分数)
的关系如图所示:(分压=总压×物质的量分数)
①起始时容器内气体的总压强为1.2pkPa,若5min时反应到达c点,v(H2)=
②b点时反应的平衡常数Kp=
③c点时,再加入CO2(g)和H2O(g),使二者分压均增大0.05pkPa,则H2的转化率
您最近一年使用:0次
2022-03-10更新
|
425次组卷
|
5卷引用:湖北省七市(州)2021-2022学年高三下学期3月联合统一调研测试化学试题
湖北省七市(州)2021-2022学年高三下学期3月联合统一调研测试化学试题福建省漳州市七校(厦大附中、龙海一中、南靖一中、平和一中、诏安一中、长泰一中、龙海二中)2021-2022学年高三下学期毕业班4月诊断性联考化学试题江西省南昌市第十中学2021-2022学年高三下学期第一次月考理科综合化学试题(已下线)押新高考卷17题 化学反应原理综合题-备战2022年高考化学临考题号押题(新高考通版)湖南省平江县第一中学2023届高三下学期适应性考试(二)化学试题
2 . 北京冬奥会火炬“飞扬”在研制的过程中,解决了火焰颜色与稳定性、高压储氢、氢能安全利用等多项技术难题。中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水来制备氢气,其主要过程如图所示。

已知:几种物质中化学键的键能如表所示。
(1)写出水蒸气光催化反应的热化学方程式_______ 。
(2)过程Ⅲ属于_______ 反应(填“吸热”或“放热”)。
(3)分解产生的 可以与
可以与 反应合成甲醇,制备甲醇的过程可能涉及的反应如下:
反应合成甲醇,制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
则:
①反应Ⅲ的
_______  。
。
②对于反应Ⅰ,不同温度对 的转化率及催化剂的催化效率影响如下图甲所示,下列有关说法不正确的是
的转化率及催化剂的催化效率影响如下图甲所示,下列有关说法不正确的是_______ 。
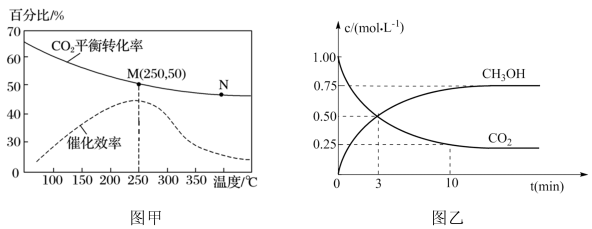
A.其他条件不变,若不使用催化剂,则 时
时 的平衡转化率可能位于N点
的平衡转化率可能位于N点
B.M点时对应平衡常数比N点时对应平衡常数大
C.温度低于 时,随温度升高甲醇的平衡产率增大
时,随温度升高甲醇的平衡产率增大
D.实际反应时既要考虑较高的催化效率,也要兼顾较高的 的平衡转化率
的平衡转化率
③对于反应Ⅰ,一定条件下在 的密闭容器,起始物
的密闭容器,起始物 时发生反应测得
时发生反应测得 和
和 的浓度随时间变化如上图乙所示。从
的浓度随时间变化如上图乙所示。从 到
到 ,
,
_______  ;该条件下
;该条件下 的平衡转化率为
的平衡转化率为_______ 。该反应的化学平衡常数为_______ 。

已知:几种物质中化学键的键能如表所示。
| 化学键 |  键 键 |  键 键 |  键 键 |  键 键 |
键能 | 463 | 496 | 436 | 138 |
(2)过程Ⅲ属于
(3)分解产生的
 可以与
可以与 反应合成甲醇,制备甲醇的过程可能涉及的反应如下:
反应合成甲醇,制备甲醇的过程可能涉及的反应如下:反应Ⅰ:

反应Ⅱ:

反应Ⅲ:

则:
①反应Ⅲ的

 。
。②对于反应Ⅰ,不同温度对
 的转化率及催化剂的催化效率影响如下图甲所示,下列有关说法不正确的是
的转化率及催化剂的催化效率影响如下图甲所示,下列有关说法不正确的是
A.其他条件不变,若不使用催化剂,则
 时
时 的平衡转化率可能位于N点
的平衡转化率可能位于N点B.M点时对应平衡常数比N点时对应平衡常数大
C.温度低于
 时,随温度升高甲醇的平衡产率增大
时,随温度升高甲醇的平衡产率增大D.实际反应时既要考虑较高的催化效率,也要兼顾较高的
 的平衡转化率
的平衡转化率③对于反应Ⅰ,一定条件下在
 的密闭容器,起始物
的密闭容器,起始物 时发生反应测得
时发生反应测得 和
和 的浓度随时间变化如上图乙所示。从
的浓度随时间变化如上图乙所示。从 到
到 ,
,
 ;该条件下
;该条件下 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
3 . N2O是《联合国气候变化框架公约》所列六种温室气体之一。目前,直接催化分解法是消除N2O的主要方法,该过程中发生的反应如下:
i.2N2O(g) 2N2(g)+O2(g) △H1
2N2(g)+O2(g) △H1
ii.2N2O(g) N2(g)+2NO(g) △H2
N2(g)+2NO(g) △H2
iii.4N2O(g) 3N2(g)+2NO2(g) △H3
3N2(g)+2NO2(g) △H3
回答下列问题:
(1)根据盖斯定律,反应2NO(g)+O2(g) 2NO2(g)的△H=
2NO2(g)的△H=___ (写出代数式即可)。
(2)已知反应i在任意温度下均能自发进行,则反应i为___ (填“吸热”或“放热”)反应。
(3)反应i的势能曲线示意图如图(…表示吸附作用,A表示催化剂,TS表示过渡态分子):
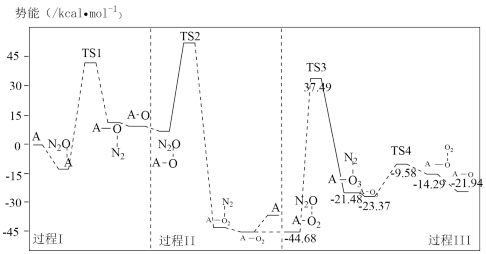
①过程Ⅲ中最大势能垒(活化能)为___ kcal·mol-1。
②下列有关反应i的说法不正确的是___ (填标号)。
A.过程Ⅰ中有极性键断裂
B.过程Ⅰ、Ⅱ、Ⅲ中都有N2生成
C.该反应中只有两种物质能够吸附N2O分子
D.过程Ⅱ中间体A—O2可释放O2也可吸附N2O分子
(4)模拟废气中N2O直接催化分解过程。
①515℃时,将模拟废气(N2O体积分数为40%)以6000m3·h-1的速度通过催化剂,测得N2O的转化率为40%,则平均反应速率v(N2O)为____ m3·h-1。欲提高N2O的转化率,可采取的措施为____ (任写一条)。
②T℃和P0kPa时,在恒压密闭容器中进行模拟实验。各组分的相关信息如表:
其中x=____ ,N2O的平衡转化率为____ (保留三位有效数字);该温度下,反应2N2O(g) 2N2(g)+O2(g)的压强平衡常数Kp=
2N2(g)+O2(g)的压强平衡常数Kp=___ kPa(以分压表示,分压=总压×物质的量分数)。
i.2N2O(g)
 2N2(g)+O2(g) △H1
2N2(g)+O2(g) △H1ii.2N2O(g)
 N2(g)+2NO(g) △H2
N2(g)+2NO(g) △H2iii.4N2O(g)
 3N2(g)+2NO2(g) △H3
3N2(g)+2NO2(g) △H3回答下列问题:
(1)根据盖斯定律,反应2NO(g)+O2(g)
 2NO2(g)的△H=
2NO2(g)的△H=(2)已知反应i在任意温度下均能自发进行,则反应i为
(3)反应i的势能曲线示意图如图(…表示吸附作用,A表示催化剂,TS表示过渡态分子):

①过程Ⅲ中最大势能垒(活化能)为
②下列有关反应i的说法不正确的是
A.过程Ⅰ中有极性键断裂
B.过程Ⅰ、Ⅱ、Ⅲ中都有N2生成
C.该反应中只有两种物质能够吸附N2O分子
D.过程Ⅱ中间体A—O2可释放O2也可吸附N2O分子
(4)模拟废气中N2O直接催化分解过程。
①515℃时,将模拟废气(N2O体积分数为40%)以6000m3·h-1的速度通过催化剂,测得N2O的转化率为40%,则平均反应速率v(N2O)为
| 物质 | N2 | N2O | O2 | CO2 | NO | NO2 |
| n(投料)/mol | 19 | 34 | 6.5 | 25 | 0 | 0 |
| n(平衡)/mol | 50 | x | 20 | 25 | 2 | 2 |
其中x=
 2N2(g)+O2(g)的压强平衡常数Kp=
2N2(g)+O2(g)的压强平衡常数Kp=
您最近一年使用:0次
2022-02-26更新
|
1310次组卷
|
6卷引用:湖北省十堰市郧阳中学、恩施高中、随州二中、襄阳三中2022-2023学年高二下学期5月联考化学试题
湖北省十堰市郧阳中学、恩施高中、随州二中、襄阳三中2022-2023学年高二下学期5月联考化学试题广东省深圳市普通高中2022届高三下学期第一次调研考试化学试题(已下线)【直击双一流】07-备战2022年高考化学名校进阶模拟卷(通用版)(已下线)专项16 化学反应原理综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)湖南省常宁市第一中学2021-2022学年高三下学期期中考试化学试题(已下线)押江苏卷第18题 化学反应原理综合题 -备战2022年高考化学临考题号押题(江苏卷)
名校
解题方法
4 . “绿水青山就是金山银山”,运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。甲醇是一种可再生能源,具有广泛的开发和应用前景:工业上一般以CO和 为原料合成甲醇,该反应的热化学方程式为:
为原料合成甲醇,该反应的热化学方程式为:

(1)已知: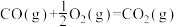



则表示1mol气态甲醇完全燃烧生成 和水蒸气时的热化学方程式为
和水蒸气时的热化学方程式为___________ 。
(2)下列措施中有利于增大反应: 的反应速率且利于反应正向进行的是___________。
的反应速率且利于反应正向进行的是___________。
(3)恒温条件下,可逆反应: 在体积固定的密闭容器中进行,达到平衡状态的标志的是
在体积固定的密闭容器中进行,达到平衡状态的标志的是______ 。
A.单位时间内生成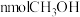 的同时生成
的同时生成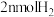
B.混合气体的密度不再改变的状态
C.混合气体的压强不再改变的状态
D.混合气体的平均摩尔质量不再改变的状态
E.CO、 、
、 浓度之比为1∶2∶1的状态。
浓度之比为1∶2∶1的状态。
(4)一定条件下向2L的密闭容器中充入1molCO和2mol 发生反应:
发生反应: ,CO的平衡转化率与温度、压强的关系如图所示:
,CO的平衡转化率与温度、压强的关系如图所示:
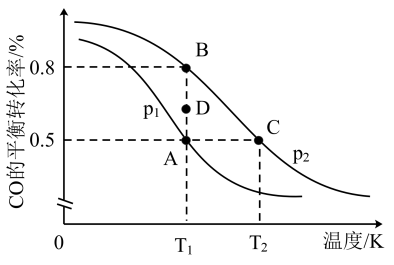
①A、B、C三点平衡常数KA、KB、KC的大小关系是______ ;
②压强p1______ p2(填“>”“<”或“=”),若 ,则B点的
,则B点的 =
=______  (
( 为以分压表示的平衡常数;分压=总压×物质的量分数)
为以分压表示的平衡常数;分压=总压×物质的量分数)
③在T1和p1条件下,由D点到A点过程中,正、逆反应速率之间的关系:
______ 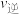 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
 为原料合成甲醇,该反应的热化学方程式为:
为原料合成甲醇,该反应的热化学方程式为:

(1)已知:
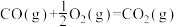



则表示1mol气态甲醇完全燃烧生成
 和水蒸气时的热化学方程式为
和水蒸气时的热化学方程式为(2)下列措施中有利于增大反应:
 的反应速率且利于反应正向进行的是___________。
的反应速率且利于反应正向进行的是___________。A.随时将 与反应混合物分离 与反应混合物分离 | B.降低反应温度 |
| C.增大体系压强 | D.使用高效催化剂 |
 在体积固定的密闭容器中进行,达到平衡状态的标志的是
在体积固定的密闭容器中进行,达到平衡状态的标志的是A.单位时间内生成
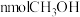 的同时生成
的同时生成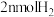
B.混合气体的密度不再改变的状态
C.混合气体的压强不再改变的状态
D.混合气体的平均摩尔质量不再改变的状态
E.CO、
 、
、 浓度之比为1∶2∶1的状态。
浓度之比为1∶2∶1的状态。(4)一定条件下向2L的密闭容器中充入1molCO和2mol
 发生反应:
发生反应: ,CO的平衡转化率与温度、压强的关系如图所示:
,CO的平衡转化率与温度、压强的关系如图所示:
①A、B、C三点平衡常数KA、KB、KC的大小关系是
②压强p1
 ,则B点的
,则B点的 =
= (
( 为以分压表示的平衡常数;分压=总压×物质的量分数)
为以分压表示的平衡常数;分压=总压×物质的量分数)③在T1和p1条件下,由D点到A点过程中,正、逆反应速率之间的关系:

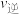 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
2022-02-18更新
|
79次组卷
|
2卷引用:湖北省南漳县第一中学2021-2022学年高二下学期3月月考化学试题
21-22高三上·广东广州·期末
名校
解题方法
5 . 甲醇是重要的化工原料,研究甲醇的制备及用途在工业上有重要的意义。
(1)一种重要的工业制备甲醇的反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H
CH3OH(g)+H2O(g)△H
已知:①CO(g)+H2O(g) CO2(g)+H2(g)△H1=-40.9kJ·mol-1
CO2(g)+H2(g)△H1=-40.9kJ·mol-1
②CO(g)+2H2(g) CH3OH(g)△H2=-90.4kJ·mol-1
CH3OH(g)△H2=-90.4kJ·mol-1
试计算制备反应的△H=___ 。
(2)对于反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),v正=k正p(CO2)p3(H2),v逆=k逆p(CH3OH)p(H2O)。其中k正、k逆分别为正、逆反应速率常数,p为气体分压(分压=物质的量分数×总压)。
CH3OH(g)+H2O(g),v正=k正p(CO2)p3(H2),v逆=k逆p(CH3OH)p(H2O)。其中k正、k逆分别为正、逆反应速率常数,p为气体分压(分压=物质的量分数×总压)。
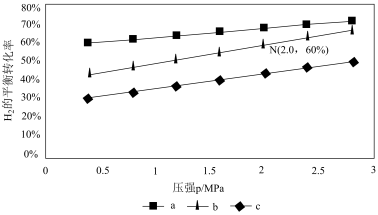
在540K下,按初始投料比n(CO2):n(H2)=3:1、n(CO2):n(H2)=1:1、n(CO2):n(H2)=1:3,得到不同压强条件下H2的平衡转化率关系图:____ (用字母表示)。
②点N在线b上,计算540K的压强平衡常数Kp=___ (用平衡分压代替平衡浓度计算)。
③540K条件下,某容器测得某时刻p(CO2)=0.2MPa,p(CH3OH)=p(H2O)=0.1MPa,p(H2)=0.4MPa,此时v正:v逆=___ 。
(3)甲醇催化可制取丙烯,反应为:3CH3OH(g) C3H6(g)+3H2O(g),反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为Rlnk=-
C3H6(g)+3H2O(g),反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为Rlnk=- +C(Ea为活化能,k为速率常数,R和C为常数)。
+C(Ea为活化能,k为速率常数,R和C为常数)。
①该反应的活化能Ea=___ kJ·mol-1。
②当使用更高效催化剂时,在图中画出Rlnk与 关系的示意图
关系的示意图___ 。____ 。
(1)一种重要的工业制备甲醇的反应为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H
CH3OH(g)+H2O(g)△H已知:①CO(g)+H2O(g)
 CO2(g)+H2(g)△H1=-40.9kJ·mol-1
CO2(g)+H2(g)△H1=-40.9kJ·mol-1②CO(g)+2H2(g)
 CH3OH(g)△H2=-90.4kJ·mol-1
CH3OH(g)△H2=-90.4kJ·mol-1试计算制备反应的△H=
(2)对于反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),v正=k正p(CO2)p3(H2),v逆=k逆p(CH3OH)p(H2O)。其中k正、k逆分别为正、逆反应速率常数,p为气体分压(分压=物质的量分数×总压)。
CH3OH(g)+H2O(g),v正=k正p(CO2)p3(H2),v逆=k逆p(CH3OH)p(H2O)。其中k正、k逆分别为正、逆反应速率常数,p为气体分压(分压=物质的量分数×总压)。在540K下,按初始投料比n(CO2):n(H2)=3:1、n(CO2):n(H2)=1:1、n(CO2):n(H2)=1:3,得到不同压强条件下H2的平衡转化率关系图:
②点N在线b上,计算540K的压强平衡常数Kp=
③540K条件下,某容器测得某时刻p(CO2)=0.2MPa,p(CH3OH)=p(H2O)=0.1MPa,p(H2)=0.4MPa,此时v正:v逆=
(3)甲醇催化可制取丙烯,反应为:3CH3OH(g)
 C3H6(g)+3H2O(g),反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为Rlnk=-
C3H6(g)+3H2O(g),反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为Rlnk=- +C(Ea为活化能,k为速率常数,R和C为常数)。
+C(Ea为活化能,k为速率常数,R和C为常数)。①该反应的活化能Ea=
②当使用更高效催化剂时,在图中画出Rlnk与
 关系的示意图
关系的示意图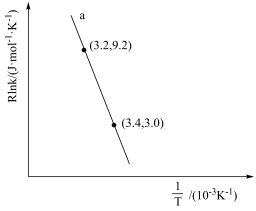
您最近一年使用:0次
2022-01-23更新
|
751次组卷
|
4卷引用:八省八校(T8联考湖北版)2021-2022学年高三下学期第二次联考化学试题
八省八校(T8联考湖北版)2021-2022学年高三下学期第二次联考化学试题 (已下线)广东省华师附中、实验中学、深圳中学、广雅中学四校2021-2022学年高三上学期期末联考化学试题广东名校2021-2022学年高三下学期开学测试化学试题湖南省岳阳市2024届高三下学期考情信息卷化学试题
解题方法
6 . 用 转化为乙醇可实现碳循环。近年来,随着全球变暖及能源枯竭的加剧,由
转化为乙醇可实现碳循环。近年来,随着全球变暖及能源枯竭的加剧,由 制乙醇又再次成为各国的研究热点。
制乙醇又再次成为各国的研究热点。
Ⅰ. 转化为乙醇的一种途径如下:
转化为乙醇的一种途径如下:
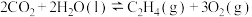
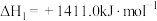
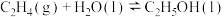
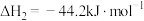
(1)则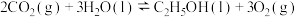

___________  。
。
Ⅱ.已知 催化加氢制乙醇原理为
催化加氢制乙醇原理为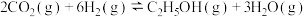 ,回答下列问题:
,回答下列问题:
(2)在恒温恒容的密闭容器中,对 催化加氢制乙醇反应体系说法错误的是
催化加氢制乙醇反应体系说法错误的是___________ 。(填序号)
A.增大原料气中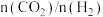 的比例,有利于提高
的比例,有利于提高 的转化率
的转化率
B.若混合气体的密度保持不变,说明反应体系已达平衡
C.体系达平衡后,若压缩容器容积,则反应平衡正向移动
(3)在均为2 L的恒容密闭容器a和b中分别投入2 mol 和6 mol
和6 mol  ,在不同温度下进行
,在不同温度下进行 加氢制乙醇的反应,各容器中乙醇的物质的量与时间的关系如图所示:
加氢制乙醇的反应,各容器中乙醇的物质的量与时间的关系如图所示:

①容器a中0~10 min氢气的平均反应速率
___________ ;
②若容器a、b中的反应温度分别为 、
、 ,则判断
,则判断
___________ 0(填“>”或“<);
③若容器a中改变条件时,反应情况会由曲线a变为曲线c,则改变的单一条件可是___________ (填序号);
A.加入更高效的催化剂 B.升温 C.增大压强 D.分离出乙醇
④ 温度下反应达平衡时,容器a中气体总压强为4 MPa,则
温度下反应达平衡时,容器a中气体总压强为4 MPa,则 时该反应的平衡常数
时该反应的平衡常数
___________ (用平衡分压代替平衡浓度计算,气体的分压=气体总压强×气体的物质的量分数)。
(4)虽然由 催化加氢制乙醇目前还无法实现产业化,但该方法具有很多优点、具有广阔的综合利用前景,试说明原因(任写一个原因):
催化加氢制乙醇目前还无法实现产业化,但该方法具有很多优点、具有广阔的综合利用前景,试说明原因(任写一个原因):___________ 。
 转化为乙醇可实现碳循环。近年来,随着全球变暖及能源枯竭的加剧,由
转化为乙醇可实现碳循环。近年来,随着全球变暖及能源枯竭的加剧,由 制乙醇又再次成为各国的研究热点。
制乙醇又再次成为各国的研究热点。Ⅰ.
 转化为乙醇的一种途径如下:
转化为乙醇的一种途径如下: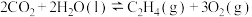
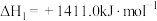
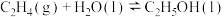
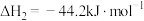
(1)则
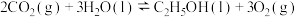

 。
。Ⅱ.已知
 催化加氢制乙醇原理为
催化加氢制乙醇原理为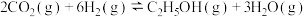 ,回答下列问题:
,回答下列问题:(2)在恒温恒容的密闭容器中,对
 催化加氢制乙醇反应体系说法错误的是
催化加氢制乙醇反应体系说法错误的是A.增大原料气中
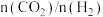 的比例,有利于提高
的比例,有利于提高 的转化率
的转化率B.若混合气体的密度保持不变,说明反应体系已达平衡
C.体系达平衡后,若压缩容器容积,则反应平衡正向移动
(3)在均为2 L的恒容密闭容器a和b中分别投入2 mol
 和6 mol
和6 mol  ,在不同温度下进行
,在不同温度下进行 加氢制乙醇的反应,各容器中乙醇的物质的量与时间的关系如图所示:
加氢制乙醇的反应,各容器中乙醇的物质的量与时间的关系如图所示:
①容器a中0~10 min氢气的平均反应速率

②若容器a、b中的反应温度分别为
 、
、 ,则判断
,则判断
③若容器a中改变条件时,反应情况会由曲线a变为曲线c,则改变的单一条件可是
A.加入更高效的催化剂 B.升温 C.增大压强 D.分离出乙醇
④
 温度下反应达平衡时,容器a中气体总压强为4 MPa,则
温度下反应达平衡时,容器a中气体总压强为4 MPa,则 时该反应的平衡常数
时该反应的平衡常数
(4)虽然由
 催化加氢制乙醇目前还无法实现产业化,但该方法具有很多优点、具有广阔的综合利用前景,试说明原因(任写一个原因):
催化加氢制乙醇目前还无法实现产业化,但该方法具有很多优点、具有广阔的综合利用前景,试说明原因(任写一个原因):
您最近一年使用:0次
2022-01-23更新
|
124次组卷
|
2卷引用:湖北省问津联合体2022-2023学年高二上学期10月质量检测化学试题
解题方法
7 . 当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。
反应①
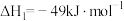
反应②
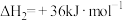
反应③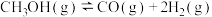

(1)
_______ ;反应③在_______ (填“高温”“低温”或“任意温度”)下能自发进行。
(2)反应① 在两种不同催化剂作用下建立平衡过程中,
在两种不同催化剂作用下建立平衡过程中, 的转化率[
的转化率[ ]随时间(t)的变化曲线如图1:
]随时间(t)的变化曲线如图1:
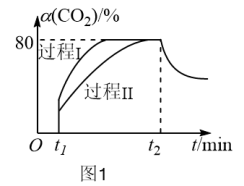
活化能大小关系过程Ⅱ_______ 过程Ⅰ(填“大于”“小于”或“等于”)
(3) 和
和 按物质的量1:3投料,总物质的量为a mol,在有催化剂的密闭容器中进行反应,测得
按物质的量1:3投料,总物质的量为a mol,在有催化剂的密闭容器中进行反应,测得 平衡转化率、
平衡转化率、 和CO选择性(转化的
和CO选择性(转化的 中生成
中生成 或CO的百分比)随温度、压强变化情况分别如图2、图3所示:
或CO的百分比)随温度、压强变化情况分别如图2、图3所示:
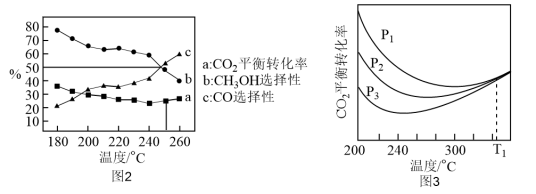
①下列说法正确的是_______ (填标号)。
A.升温,反应②的平衡正向移动
B.加压,反应①的平衡正向移动,平衡常数增大
C.及时分离出甲醇和水,循环使用 和
和 ,可提高原料利用率
,可提高原料利用率
D.升温,使反应①的 选择性降低;加压,对反应②的CO选择性无影响
选择性降低;加压,对反应②的CO选择性无影响
②250℃时,在体积为V L的容器中,反应①和②达到化学平衡, 转化率为25%,
转化率为25%, 和CO选择性均为50%,则该温度下反应②的平衡常数为
和CO选择性均为50%,则该温度下反应②的平衡常数为_______ 。
③如图2:240℃以上,随着温度升高,CO的平衡转化率升高,而 的选择性降低,分析其原因
的选择性降低,分析其原因_______ 。
Ⅱ.我国科学家研究出在S-In催化剂上实现高选择性、高活性电催化还原 制甲酸。
制甲酸。
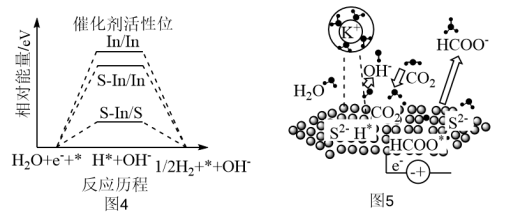
(4)图4表示不同催化剂及活性位上生成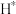 的能量变化,图5表示反应历程,其中吸附在催化剂表面的物质用*标注。下列说法正确的是_______(填标号)。
的能量变化,图5表示反应历程,其中吸附在催化剂表面的物质用*标注。下列说法正确的是_______(填标号)。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。
反应①

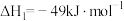
反应②

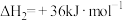
反应③
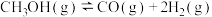

(1)

(2)反应①
 在两种不同催化剂作用下建立平衡过程中,
在两种不同催化剂作用下建立平衡过程中, 的转化率[
的转化率[ ]随时间(t)的变化曲线如图1:
]随时间(t)的变化曲线如图1:
活化能大小关系过程Ⅱ
(3)
 和
和 按物质的量1:3投料,总物质的量为a mol,在有催化剂的密闭容器中进行反应,测得
按物质的量1:3投料,总物质的量为a mol,在有催化剂的密闭容器中进行反应,测得 平衡转化率、
平衡转化率、 和CO选择性(转化的
和CO选择性(转化的 中生成
中生成 或CO的百分比)随温度、压强变化情况分别如图2、图3所示:
或CO的百分比)随温度、压强变化情况分别如图2、图3所示:
①下列说法正确的是
A.升温,反应②的平衡正向移动
B.加压,反应①的平衡正向移动,平衡常数增大
C.及时分离出甲醇和水,循环使用
 和
和 ,可提高原料利用率
,可提高原料利用率D.升温,使反应①的
 选择性降低;加压,对反应②的CO选择性无影响
选择性降低;加压,对反应②的CO选择性无影响②250℃时,在体积为V L的容器中,反应①和②达到化学平衡,
 转化率为25%,
转化率为25%, 和CO选择性均为50%,则该温度下反应②的平衡常数为
和CO选择性均为50%,则该温度下反应②的平衡常数为③如图2:240℃以上,随着温度升高,CO的平衡转化率升高,而
 的选择性降低,分析其原因
的选择性降低,分析其原因Ⅱ.我国科学家研究出在S-In催化剂上实现高选择性、高活性电催化还原
 制甲酸。
制甲酸。(4)图4表示不同催化剂及活性位上生成
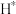 的能量变化,图5表示反应历程,其中吸附在催化剂表面的物质用*标注。下列说法正确的是_______(填标号)。
的能量变化,图5表示反应历程,其中吸附在催化剂表面的物质用*标注。下列说法正确的是_______(填标号)。
A. 经两步转化生成 经两步转化生成 |
B. 与 与 微粒间的静电作用促进了 微粒间的静电作用促进了 的活化 的活化 |
C.S-In/S表面更容易生成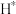 |
D.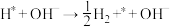 相对能量变化越大,越有利于抑制 相对能量变化越大,越有利于抑制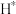 复合成 复合成 |
您最近一年使用:0次
8 . 丙烯是化工合成的重要原料,其制备工艺主要有如下两种:
工艺1:丙烷无氧脱氢工艺: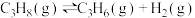
工艺2:丙烷氧化脱氢工艺:
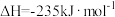
回答下列问题:
(1)根据下表数据,计算无氧脱氢工艺中的
______  ,与工艺1相比,工艺2的优点是
,与工艺1相比,工艺2的优点是___________ (从能源角度)。
(2)若提高工艺1丙烷的平衡转化率,下列措施不可行的是___________(填字母)。
(3)工艺1脱氢时以CeO2/VO3为催化剂,脱第1个氢原子的反应历程有两种情况(Ts表示过渡态):
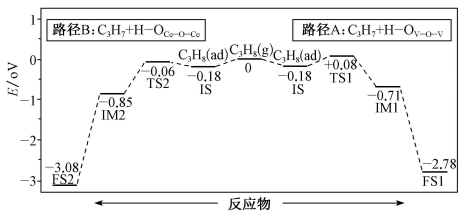
用图中数据可知,脱第1个氢原子时,最有可能按路径____ (填A或B),其原因是______ 。
(4)工艺1脱氢时,还会产生副产物C2H4,写出生成副产物的化学方程式:_______ ,若恒容反应容器中C3H8(g)的浓度为 ,丙烷的总平衡转化率为40%,丙烯的选择性为50%,则工艺1的平衡常数K=
,丙烷的总平衡转化率为40%,丙烯的选择性为50%,则工艺1的平衡常数K=_____ [结果保留两位有效数字,丙烯的选择性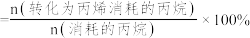 ]。
]。
工艺1:丙烷无氧脱氢工艺:
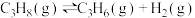
工艺2:丙烷氧化脱氢工艺:

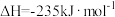
回答下列问题:
(1)根据下表数据,计算无氧脱氢工艺中的

 ,与工艺1相比,工艺2的优点是
,与工艺1相比,工艺2的优点是| 物质 | C3H8(g) | C3H6(g) | H2(g) |
燃烧热( ) ) | 2217.8 | 2058.0 | 285.8 |
(2)若提高工艺1丙烷的平衡转化率,下列措施不可行的是___________(填字母)。
| A.适当的升高温度 |
| B.增大压强 |
| C.提高恒容反应容器中丙烷的初始浓度 |
| D.向恒压反应容器中的丙烷掺入水蒸气(水蒸气不参与反应) |

用图中数据可知,脱第1个氢原子时,最有可能按路径
(4)工艺1脱氢时,还会产生副产物C2H4,写出生成副产物的化学方程式:
 ,丙烷的总平衡转化率为40%,丙烯的选择性为50%,则工艺1的平衡常数K=
,丙烷的总平衡转化率为40%,丙烯的选择性为50%,则工艺1的平衡常数K=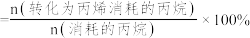 ]。
]。
您最近一年使用:0次
9 . 研究处理NOx对环境保护有着重要的意义。回答下列问题:
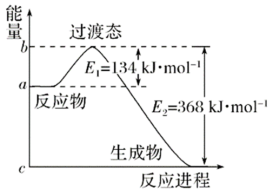
(1)如图是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,则E1__ (填“增大”“减小”或“不变”,下同),△H__ 。请写出NO2和CO反应的热化学方程式:___ 。
(2)一定条件下,用甲烷可以消除氮的氧化物(NOx)的污染。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160kJ•mol-1
下列选项正确的是__ (填标号)。
(3)利用反应C(s)+2NO(g)=N2(g)+CO2(g) △H=-34.0kJ•mol-1,一定条件下消除NO的污染。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率α(NO)随温度的变化如图所示:
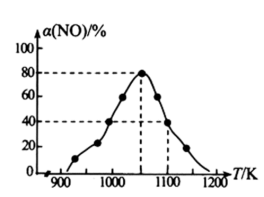
①由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是__ ;在1100K时,CO2的体积分数为__ 。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa时,该反应的化学平衡常数Kp=__ (已知:气体分压=气体总压×体积分数)。
(4)在汽车尾气的净化装置中CO和NO发生反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H2=-746.8kJ•mol-1。实验测得,v正=k正•c2(NO)•c2(CO),v逆=k逆•c(N2)•c2(CO2)(k正、k逆为速率常数,只与温度有关)。
N2(g)+2CO2(g) △H2=-746.8kJ•mol-1。实验测得,v正=k正•c2(NO)•c2(CO),v逆=k逆•c(N2)•c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数__ (填">”、“<”或“=”)k逆增大的倍数。
②若在1L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡时,CO的转化率为40%,则 =
=__ (保留2位有效数字)。
(1)如图是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,则E1

(2)一定条件下,用甲烷可以消除氮的氧化物(NOx)的污染。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160kJ•mol-1
下列选项正确的是
| A.CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ•mol-1 |
| B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) △H3>△H1 |
| C.若用0.2molCH4还原NO2至N2,则反应中放出的热量一定为173.4kJ |
| D.若用标准状况下2.24LCH4还原NO2至N2,整个过程中转移的电子为1.6mol |

①由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa时,该反应的化学平衡常数Kp=
(4)在汽车尾气的净化装置中CO和NO发生反应:2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H2=-746.8kJ•mol-1。实验测得,v正=k正•c2(NO)•c2(CO),v逆=k逆•c(N2)•c2(CO2)(k正、k逆为速率常数,只与温度有关)。
N2(g)+2CO2(g) △H2=-746.8kJ•mol-1。实验测得,v正=k正•c2(NO)•c2(CO),v逆=k逆•c(N2)•c2(CO2)(k正、k逆为速率常数,只与温度有关)。①达到平衡后,仅升高温度,k正增大的倍数
②若在1L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡时,CO的转化率为40%,则
 =
=
您最近一年使用:0次
10 . 二氧化碳加氢合成甲醇是化学固碳的一种有效途径,不仅可以有效减少空气中的CO2排放,而且还能制备出甲醇清洁能源。反应如下:
主反应I:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1
副反应II:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=+41kJ⋅mol-1
回答下列问题:
(1)已知CO(g)+2H2(g)⇌CH3OH(g) ΔH3=-99kJ⋅mol-1,则ΔH1=______ kJ⋅mol-1;有利于提高甲醇平衡产率的条件是_______ (填标号)
A.高温高压B.低温高压C.高温低压D.低温低压
(2)我国学者结合实验与计算机模拟结果,研究了CO2与H2在TiO2/Cu催化剂表面生成CH3OH和H2O的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。
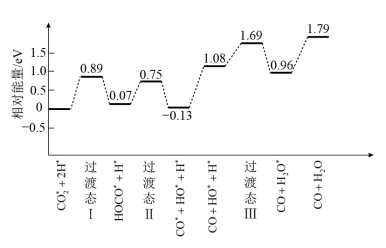
①该反应历程中最大的活化能Ea=___________ eV。
②后续的反应历程可简化为以下5个步骤(*表示催化剂活性位点),请完成历程中(iii)的反应方程式。
(i) ;
;
(ii) ;
;
(iii)___________ ;
(iv) ;
;
(v) 。
。
(3)当CO2和H2的投料比为1:3在不同的催化剂(Cat.1:Cu/TiO2;Cat.2:Cu/ZrO2)条件下反应相同的时间,CH3OH选择性和CO选择性(已知CH3OH的选择性 、CO的选择性
、CO的选择性 随着CO2转化率的变化如图所示:
随着CO2转化率的变化如图所示:
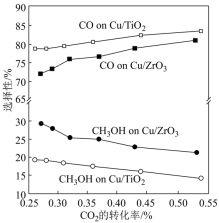
①由图可知,催化效果Cat.2___________ Cat.1(填“大于”或“小于”)。
②若温度升高,CO2的转化率增大,则CH3OH选择性降低的可能原因是___________ 。
(4)在一定条件下,向刚性容器中充入投料比为1:3的CO2和H2,达到平衡时CO2的转化率为20%,CH3OH的选择性为75%,则α(H2)=___________ (计算结果保留一位小数);反应II的压强平衡常数Kp=___________ 。
主反应I:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1
副反应II:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=+41kJ⋅mol-1
回答下列问题:
(1)已知CO(g)+2H2(g)⇌CH3OH(g) ΔH3=-99kJ⋅mol-1,则ΔH1=
A.高温高压B.低温高压C.高温低压D.低温低压
(2)我国学者结合实验与计算机模拟结果,研究了CO2与H2在TiO2/Cu催化剂表面生成CH3OH和H2O的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。

①该反应历程中最大的活化能Ea=
②后续的反应历程可简化为以下5个步骤(*表示催化剂活性位点),请完成历程中(iii)的反应方程式。
(i)
 ;
;(ii)
 ;
;(iii)
(iv)
 ;
;(v)
 。
。(3)当CO2和H2的投料比为1:3在不同的催化剂(Cat.1:Cu/TiO2;Cat.2:Cu/ZrO2)条件下反应相同的时间,CH3OH选择性和CO选择性(已知CH3OH的选择性
 、CO的选择性
、CO的选择性 随着CO2转化率的变化如图所示:
随着CO2转化率的变化如图所示:
①由图可知,催化效果Cat.2
②若温度升高,CO2的转化率增大,则CH3OH选择性降低的可能原因是
(4)在一定条件下,向刚性容器中充入投料比为1:3的CO2和H2,达到平衡时CO2的转化率为20%,CH3OH的选择性为75%,则α(H2)=
您最近一年使用:0次



