名校
解题方法
1 . 已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
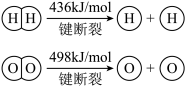
下列说法不正确 的是

下列说法
| A.利用该反应原理可设计氢氧燃料电池 |
| B.可推算H-O键的键能为926.8kJ/mol |
C.H2O(g)=H2(g)+ O2(g) ΔH=+241.8kJ/mol O2(g) ΔH=+241.8kJ/mol |
| D.H2分子和H2O分子中都只含共价键 |
您最近一年使用:0次
解题方法
2 . 天然气的主要成分为CH4,一般还含有C2H6等烃类,是重要的燃料和化工原料。
(1)乙烷在一定条件可发生如下反应:C2H6(g)=C2H4(g)+H2(g) ΔH=_______ kJ·mol−1。相关物质的燃烧热数据如下表所示:
(2)下表中的数据是破坏1 mol物质中的化学键所消耗的能量:
根据上述数据回答问题:按照反应 I2+H2=2HI生成2 mol HI_______ (填“吸收”或“放出”)的热量为_______ kJ。
(1)乙烷在一定条件可发生如下反应:C2H6(g)=C2H4(g)+H2(g) ΔH=
| 物质 | C2H6(g) | C2H4(g) | H2(g) |
| 燃烧热ΔH/( kJ·mol−1) | -1560 | -1411 | -286 |
(2)下表中的数据是破坏1 mol物质中的化学键所消耗的能量:
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量/kJ | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
根据上述数据回答问题:按照反应 I2+H2=2HI生成2 mol HI
您最近一年使用:0次
名校
3 . 用CO2和H2在一定条件下可转化生成甲醇蒸气和水蒸CO2(g)+3H2(g) CH3OH(g)+H2O(g);ΔH=-akJ/mol
CH3OH(g)+H2O(g);ΔH=-akJ/mol
(1)已知:①3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) ΔH=-247kJ/mol
CH3OCH3(g)+CO2(g) ΔH=-247kJ/mol
②2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH=-24kJ/mol
CH3OCH3(g)+H2O(g) ΔH=-24kJ/mol
③CO(g)+H2O(g) CO2(g)+H2(g) ΔH=-41kJ/mol
CO2(g)+H2(g) ΔH=-41kJ/mol
则a=___________ 。
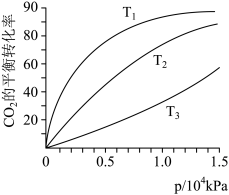
(2)CO2在不同温度下的平衡转化率与压强的关系如下图所示。请写出T1、T2、T3三者的大小关系___________ ,实际生产条件控制在T1、1.3×104kPa左右,选择此压强的理由是___________ 。
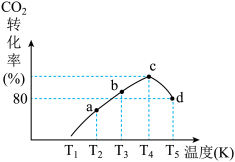
(3)一定条件下,在相同体积的恒容密闭容器中充入1.0molCO2和3.0molH2,相同时间段内测得CO2的转化率随温度变化如图所示:b点v正___________ v逆(填“>”“<”或“=”);温度高于T4,CO2的转化率降低的原因是___________ 。已知容器内的起始压强为200kPa,则图中d点对应温度下反应的平衡常数Kp=___________ (kPa)-2(结果保留两位有效数字)(KP为以分压表示的平衡常数,分压=总压×物质的量分数)
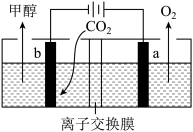
(4)用惰性电极电解强酸性的二氧化碳水溶液可得到甲醇,其原理如下图所示。
①b电极上的电极反应式为___________ ;
②该装置中使用的是___________ (填“阳”或“阴”)离子交换膜。
 CH3OH(g)+H2O(g);ΔH=-akJ/mol
CH3OH(g)+H2O(g);ΔH=-akJ/mol(1)已知:①3CO(g)+3H2(g)
 CH3OCH3(g)+CO2(g) ΔH=-247kJ/mol
CH3OCH3(g)+CO2(g) ΔH=-247kJ/mol②2CH3OH(g)
 CH3OCH3(g)+H2O(g) ΔH=-24kJ/mol
CH3OCH3(g)+H2O(g) ΔH=-24kJ/mol③CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH=-41kJ/mol
CO2(g)+H2(g) ΔH=-41kJ/mol则a=
(2)CO2在不同温度下的平衡转化率与压强的关系如下图所示。请写出T1、T2、T3三者的大小关系

(3)一定条件下,在相同体积的恒容密闭容器中充入1.0molCO2和3.0molH2,相同时间段内测得CO2的转化率随温度变化如图所示:b点v正

(4)用惰性电极电解强酸性的二氧化碳水溶液可得到甲醇,其原理如下图所示。
①b电极上的电极反应式为
②该装置中使用的是

您最近一年使用:0次
4 . (1)已知2molH2完全燃烧生成液态水时放出572kJ热量,则2molH2完全燃烧生成水蒸气时放出热量_______ (填大于、等于或小于)572kJ。
(2)现已知N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化如图所示(E1=1127kJ,E2=1173kJ):
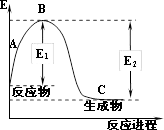
根据以上键能数据计算N—H键的键能为_______ kJ/mol。
(3)N4分子结构为正四面体,与白磷分子相似,如图所示。
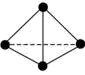
已知N-N键、N≡N键的键能分别为193kJ/mol、940kJ/mol,则1mol N4气体转化为N2时需___ (填“吸收”或“放出”)___ kJ能量。
(2)现已知N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化如图所示(E1=1127kJ,E2=1173kJ):

| 化学键 | H-H | N≡N |
| 键能(kJ/mol) | 436 | 946 |
根据以上键能数据计算N—H键的键能为
(3)N4分子结构为正四面体,与白磷分子相似,如图所示。

已知N-N键、N≡N键的键能分别为193kJ/mol、940kJ/mol,则1mol N4气体转化为N2时需
您最近一年使用:0次
名校
解题方法
5 . H2与N2在催化剂表面生成NH3,反应历程及能量变化示意如下:
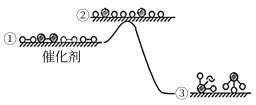
下列说法错误的是

下列说法错误的是
| A.①→②吸收能量 | B.②→③形成了N-H键 |
| C.选择不同的催化剂会改变反应热 | D.该反应为放热反应 |
您最近一年使用:0次
2021-07-28更新
|
314次组卷
|
4卷引用:广东省广州市番禺区洛溪新城中学2020-2021学年高一下学4月月考化学试题
6 . 多晶硅是制作光伏电池的关键材料。以下是粗硅制备多晶硅的简易过程。回答下列问题:
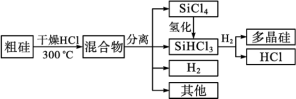
(1)硅粉与HCl在300 ℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,该反应的热化学方程式为_______ 。
(2)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
① SiCl4(g)+H2(g)⇌SiHCl3(g)+HCl(g) ΔH1>0
② 3SiCl4(g)+2H2(g)+Si(s)⇌4SiHCl3(g) ΔH2<0
③ 2SiCl4(g)+H2(g)+Si(s)+HCl(g)⇌3SiHCl3(g) ΔH3
反应③的ΔH3=_______ (用ΔH1、ΔH2表示)。
(3) 写出由二氧化硅制粗硅的化学方程式_______ 。

(1)硅粉与HCl在300 ℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,该反应的热化学方程式为
(2)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
① SiCl4(g)+H2(g)⇌SiHCl3(g)+HCl(g) ΔH1>0
② 3SiCl4(g)+2H2(g)+Si(s)⇌4SiHCl3(g) ΔH2<0
③ 2SiCl4(g)+H2(g)+Si(s)+HCl(g)⇌3SiHCl3(g) ΔH3
反应③的ΔH3=
(3) 写出由二氧化硅制粗硅的化学方程式
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题:
Ⅰ.已知:
 ,现用下图所示装置测定中和热。
,现用下图所示装置测定中和热。
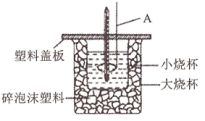
回答下列问题:
(1)碎泡沫塑料的作用是___________ ;若将A换为“铜丝搅拌棒”测得的 将
将___________ (填“偏大”、“偏小”或“不变”)。
(2)若用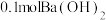 配制成稀溶液,与足量的稀硝酸反应,放出的热量为
配制成稀溶液,与足量的稀硝酸反应,放出的热量为___________ kJ。
Ⅱ.2021年5月29日天舟二号货运飞船成功发射,为中国空间站进一步开展在轨建造奠定了坚实基础,该飞船由长征七号遥三运载火箭搭载。长征七号遥三运载火箭使用煤油为燃料
(3)煤油的主要成分为 ,已知
,已知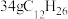 完全燃烧生成气态水时放出1386.2kJ热量;
完全燃烧生成气态水时放出1386.2kJ热量;
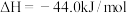 。则表示煤油燃烧热的热化学方程式为
。则表示煤油燃烧热的热化学方程式为___________ 。
(4)前期的火箭曾用液态肼(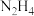 )与双氧水反应来提供能量。已知0.4mol液态肼与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量,则此反应的热化学方程式为
)与双氧水反应来提供能量。已知0.4mol液态肼与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量,则此反应的热化学方程式为___________ 。
Ⅲ.将氧化铁还原为铁的技术在人类文明进步中占据十分重要的地位。高炉炼铁中发生的部分反应为:
①
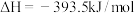
②

(5)已知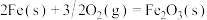
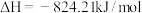 。则高炉内
。则高炉内 被CO还原为Fe的热化学方程式为
被CO还原为Fe的热化学方程式为___________ 。
(6)碳(s)在氧气不足的情况下燃烧,会生成CO,但同时也有部分生成 ,因此无法通过实验直接测得反应:
,因此无法通过实验直接测得反应: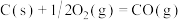 的
的 ,计算时需要测得的实验数据有
,计算时需要测得的实验数据有___________ 。若根据上述信息可计算出该反应的
___________ kJ/mol。
Ⅰ.已知:

 ,现用下图所示装置测定中和热。
,现用下图所示装置测定中和热。
回答下列问题:
(1)碎泡沫塑料的作用是
 将
将(2)若用
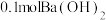 配制成稀溶液,与足量的稀硝酸反应,放出的热量为
配制成稀溶液,与足量的稀硝酸反应,放出的热量为Ⅱ.2021年5月29日天舟二号货运飞船成功发射,为中国空间站进一步开展在轨建造奠定了坚实基础,该飞船由长征七号遥三运载火箭搭载。长征七号遥三运载火箭使用煤油为燃料
(3)煤油的主要成分为
 ,已知
,已知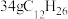 完全燃烧生成气态水时放出1386.2kJ热量;
完全燃烧生成气态水时放出1386.2kJ热量;
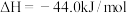 。则表示煤油燃烧热的热化学方程式为
。则表示煤油燃烧热的热化学方程式为(4)前期的火箭曾用液态肼(
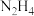 )与双氧水反应来提供能量。已知0.4mol液态肼与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量,则此反应的热化学方程式为
)与双氧水反应来提供能量。已知0.4mol液态肼与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量,则此反应的热化学方程式为Ⅲ.将氧化铁还原为铁的技术在人类文明进步中占据十分重要的地位。高炉炼铁中发生的部分反应为:
①

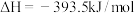
②


(5)已知
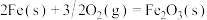
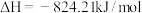 。则高炉内
。则高炉内 被CO还原为Fe的热化学方程式为
被CO还原为Fe的热化学方程式为(6)碳(s)在氧气不足的情况下燃烧,会生成CO,但同时也有部分生成
 ,因此无法通过实验直接测得反应:
,因此无法通过实验直接测得反应: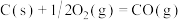 的
的 ,计算时需要测得的实验数据有
,计算时需要测得的实验数据有
您最近一年使用:0次
2021-07-22更新
|
256次组卷
|
2卷引用:四川省成都市龙泉驿区2020-2021学年高一下学期末学业质量监测联考化学试题
8 . 已知
①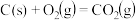
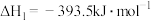
②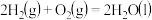
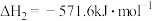
③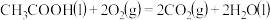
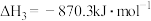
则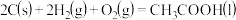 的
的 值为
值为
①
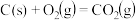
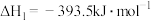
②
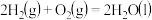
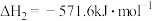
③
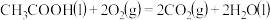
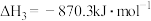
则
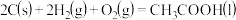 的
的 值为
值为A.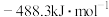 | B. |
C.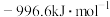 | D.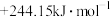 |
您最近一年使用:0次
2021-07-22更新
|
889次组卷
|
3卷引用:四川省成都市龙泉驿区2020-2021学年高一下学期末学业质量监测联考化学试题
9 . 随着低碳钢等洁净钢技术的发展,Al2O3-C耐火材料和钢水之间的相互作用已成为当前的一个研究重点。请回答下列问题:
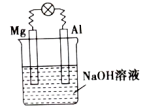
(1)将镁片、铝片平行插入一定浓度的NaOH溶液中,用导线连接成闭合回路,如图所示。写出铝电极的电极反应式:_____ 。
(2)在埋炭实验条件下,不同碳素材料的Al2O3-C耐火材料与铁液之间的可能反应如下:
①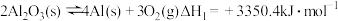
②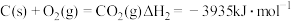
③
④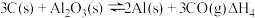 则
则

______  。
。
(3)直接碳热还原氧化铝法除需要高温外,系统中生成的碳化铝、碳氧化铝等会与生成的铝混合在一起,难以分离。实际生产中,至今仍未用直接碳热还原氧化铝法来炼铝。氧化铝碳热还原氯化法炼铝是生产铝的一种可行性新方法,其反应过程如下:
⑤
⑥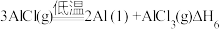
反应⑤、反应⑥中自由能( )与温度(T)的变化关系如图所示,由此判断反应⑤对应图中的曲线
)与温度(T)的变化关系如图所示,由此判断反应⑤对应图中的曲线____ (填“I”或“II”),试分析氧化铝碳热还原氯化法炼铝的可行性:______
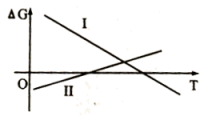
(4)在埋炭情况下,碳过剩时,碳的氧化反应主要考虑: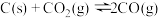 。在实验室研究该反应,一定温度下,向某体积可变的恒压密闭容器(总压强为p总)中加入足量的碳和2 molCO2(g),平衡时体系中气体体积分数与温度的关系如图所示。
。在实验室研究该反应,一定温度下,向某体积可变的恒压密闭容器(总压强为p总)中加入足量的碳和2 molCO2(g),平衡时体系中气体体积分数与温度的关系如图所示。
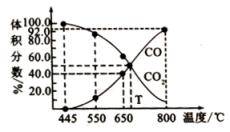
①650℃反应达到平衡时,容器体积为10L,则平衡时c(CO)=___________ 。
②T℃时,若向平衡体系中再充入一定量n(CO):n(CO2)=3:2的混合气体,则平衡___________ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
③800℃时,如图CO的体积分数为92%,用平衡分压代替平衡浓度表示的化学平衡常数Kp=___________ [用含p总的代数式表示,气体分压(p分)=气体总压(p总) 体积分数]。
体积分数]。
(1)将镁片、铝片平行插入一定浓度的NaOH溶液中,用导线连接成闭合回路,如图所示。写出铝电极的电极反应式:

(2)在埋炭实验条件下,不同碳素材料的Al2O3-C耐火材料与铁液之间的可能反应如下:
①
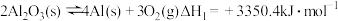
②
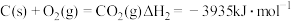
③

④
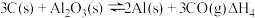 则
则
 。
。(3)直接碳热还原氧化铝法除需要高温外,系统中生成的碳化铝、碳氧化铝等会与生成的铝混合在一起,难以分离。实际生产中,至今仍未用直接碳热还原氧化铝法来炼铝。氧化铝碳热还原氯化法炼铝是生产铝的一种可行性新方法,其反应过程如下:
⑤

⑥
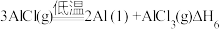
反应⑤、反应⑥中自由能(
 )与温度(T)的变化关系如图所示,由此判断反应⑤对应图中的曲线
)与温度(T)的变化关系如图所示,由此判断反应⑤对应图中的曲线
(4)在埋炭情况下,碳过剩时,碳的氧化反应主要考虑:
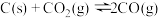 。在实验室研究该反应,一定温度下,向某体积可变的恒压密闭容器(总压强为p总)中加入足量的碳和2 molCO2(g),平衡时体系中气体体积分数与温度的关系如图所示。
。在实验室研究该反应,一定温度下,向某体积可变的恒压密闭容器(总压强为p总)中加入足量的碳和2 molCO2(g),平衡时体系中气体体积分数与温度的关系如图所示。
①650℃反应达到平衡时,容器体积为10L,则平衡时c(CO)=
②T℃时,若向平衡体系中再充入一定量n(CO):n(CO2)=3:2的混合气体,则平衡
③800℃时,如图CO的体积分数为92%,用平衡分压代替平衡浓度表示的化学平衡常数Kp=
 体积分数]。
体积分数]。
您最近一年使用:0次
10 . 某温度时,VIA元素单质与H2反应生成气态H2X的热化学方程式如下:
①H2(g)+ O2(g)=H2O(g) ΔH=-242kJ•mol-1
O2(g)=H2O(g) ΔH=-242kJ•mol-1
②H2(g)+S(g)=H2S(g) ΔH=-20kJ•mol-1
③H2(g)+Se(g)⇌H2Se(g) ΔH=+81kJ•mol-1
④H2O(g)=H2O(l) ∆H=-44kJ/mol
请回答:
(1)上述反应中属于放热反应的是_______ (填序号,下同),属于吸热反应的是_______ 。
(2)2gH2完全燃烧生成气态水,放出的热量为_______ 。
(3)请写出O2与H2S反应生成S的热化学方程式_______ 。
(4)根据下图写出热化学方程式_______ 。
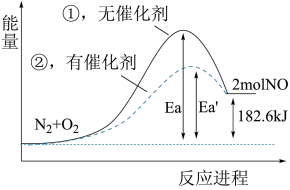
(5)加入催化剂该反应的反应热∆H是否发生了改变_______ (填“是”或“否”)。
(6)请写出H2燃烧热的热化学方程式_______ 。
①H2(g)+
 O2(g)=H2O(g) ΔH=-242kJ•mol-1
O2(g)=H2O(g) ΔH=-242kJ•mol-1②H2(g)+S(g)=H2S(g) ΔH=-20kJ•mol-1
③H2(g)+Se(g)⇌H2Se(g) ΔH=+81kJ•mol-1
④H2O(g)=H2O(l) ∆H=-44kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)2gH2完全燃烧生成气态水,放出的热量为
(3)请写出O2与H2S反应生成S的热化学方程式
(4)根据下图写出热化学方程式

(5)加入催化剂该反应的反应热∆H是否发生了改变
(6)请写出H2燃烧热的热化学方程式
您最近一年使用:0次



