1 . 氨气是一种重要的化学物质,可用于制取化肥和硝酸等。
(1)工业合成氨的热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol
表中a为___________ 。
(2)合成氨原料中的H2可用CO在高温下与水蒸气反应制得。已知在25℃、101 kPa 下:
I. 2C(石墨,s)+O2(g)=2CO(g) △H1=- 222 kJ/mol
II.2H2(g)+O2(g)=2H2O(g) △H2=- 242 kJ/mol
III. C(石墨,s)+ O2(g)=CO2(g) △H3=- 394kJ/mol
①25℃、101 kPa 下CO与水蒸气反应转化为H2的热化学方程式为___________ 。
②根据反应I、II、III,下列说法正确的是___________ (填选项字母)。
a.由反应II可以推知:2H2(g)+O2(g)=2H2O(l) △H4,则△H4小于△H2
b.反应III的反应热等于O2分子中化学键断裂时所吸收的总能量与CO2分子中化学键形成时所释放的总能量的差
c.下图可表示反应I的反应过程和能量的关系
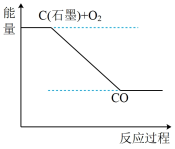 。
。
(1)工业合成氨的热化学方程式为:N2(g)+3H2(g)
 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol| N-H | H-H | N≡N | |
| 断开1 mol化学键需要吸收的能量/kJ | a | 436 | 946 |
(2)合成氨原料中的H2可用CO在高温下与水蒸气反应制得。已知在25℃、101 kPa 下:
I. 2C(石墨,s)+O2(g)=2CO(g) △H1=- 222 kJ/mol
II.2H2(g)+O2(g)=2H2O(g) △H2=- 242 kJ/mol
III. C(石墨,s)+ O2(g)=CO2(g) △H3=- 394kJ/mol
①25℃、101 kPa 下CO与水蒸气反应转化为H2的热化学方程式为
②根据反应I、II、III,下列说法正确的是
a.由反应II可以推知:2H2(g)+O2(g)=2H2O(l) △H4,则△H4小于△H2
b.反应III的反应热等于O2分子中化学键断裂时所吸收的总能量与CO2分子中化学键形成时所释放的总能量的差
c.下图可表示反应I的反应过程和能量的关系
 。
。
您最近一年使用:0次
2 . 下列与化学反应能量变化相关的叙述正确的是
| A.ΔH﹥0表示放热反应,ΔH﹤0表示吸热反应 |
| B.热化学方程式的化学计量数可以表示分子数或原子数,因此必须是整数 |
| C.根据盖斯定律,可计算某些难以直接测量的反应热 |
| D.同温同压下,H2( g)+Cl2(g)=2HCl (g),在光照和点燃条件的△H不同 |
您最近一年使用:0次
3 . Ⅰ.氨是工业生产硝酸的重要原料,请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:

(1)工业用甲烷制取氢气作为合成氨的原料,已知以下的热化学反应方程式:
①2CO(g)+O2(g)=2CO2(g)∆H=-566kJ/mol
②2H2(g)+O2(g)=2H2O(g)∆H=-484kJ/mol
③CH4(g)+2O2(g)=CO2(g)+2H2O(g)∆H=-890kJ/mol
则:CH4(g)+CO2(g)=2CO(g)+2H2(g)∆H=__ kJ/mol。
(2)一定温度下,将N2与H2以体积比1:2置于2L的密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g),下列能说明反应达到平衡状态的是
2NH3(g),下列能说明反应达到平衡状态的是___ 。
A.体系压强保持不变
B.混合气体颜色保持不变
C.N2与H2的物质的量之比保持不变
D.每消耗2molNH3的同时消耗1molN2
(3)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用氨转化法处理:已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为__ 。
Ⅱ.氮肥厂的废水直接排放会造成污染,目前氨氮废水处理方法主要有吹脱法、化学沉淀法、生物硝化反硝化法等。某氮肥厂的氨氮废水中氮元素多以NH 和NH3•H2O的形式存在。该厂技术团队设计该废水处理方案流程如图:
和NH3•H2O的形式存在。该厂技术团队设计该废水处理方案流程如图:
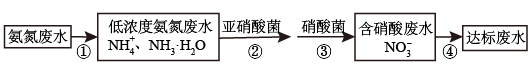
(4)检验某溶液中是否含有NH 的方法
的方法___ (写出所需试剂、操作及现象)。
(5)过程②、③:在微生物亚硝酸菌和硝酸菌作用下实现NH →NO
→NO →NO
→NO 的转化,称为硝化反应。1molNH
的转化,称为硝化反应。1molNH 可被
可被___ L(标准状况)O2最终氧化成NO 。
。
(6)过程④:在一定条件下向废水中加入甲醇(CH3OH)实现HNO2→N2转化,称为反硝化反应。此过程中甲醇(C元素-2价)转化为CO2,写出此过程的化学方程式___ 。

(1)工业用甲烷制取氢气作为合成氨的原料,已知以下的热化学反应方程式:
①2CO(g)+O2(g)=2CO2(g)∆H=-566kJ/mol
②2H2(g)+O2(g)=2H2O(g)∆H=-484kJ/mol
③CH4(g)+2O2(g)=CO2(g)+2H2O(g)∆H=-890kJ/mol
则:CH4(g)+CO2(g)=2CO(g)+2H2(g)∆H=
(2)一定温度下,将N2与H2以体积比1:2置于2L的密闭容器中发生反应:N2(g)+3H2(g)
 2NH3(g),下列能说明反应达到平衡状态的是
2NH3(g),下列能说明反应达到平衡状态的是A.体系压强保持不变
B.混合气体颜色保持不变
C.N2与H2的物质的量之比保持不变
D.每消耗2molNH3的同时消耗1molN2
(3)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用氨转化法处理:已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
Ⅱ.氮肥厂的废水直接排放会造成污染,目前氨氮废水处理方法主要有吹脱法、化学沉淀法、生物硝化反硝化法等。某氮肥厂的氨氮废水中氮元素多以NH
 和NH3•H2O的形式存在。该厂技术团队设计该废水处理方案流程如图:
和NH3•H2O的形式存在。该厂技术团队设计该废水处理方案流程如图:
(4)检验某溶液中是否含有NH
 的方法
的方法(5)过程②、③:在微生物亚硝酸菌和硝酸菌作用下实现NH
 →NO
→NO →NO
→NO 的转化,称为硝化反应。1molNH
的转化,称为硝化反应。1molNH 可被
可被 。
。(6)过程④:在一定条件下向废水中加入甲醇(CH3OH)实现HNO2→N2转化,称为反硝化反应。此过程中甲醇(C元素-2价)转化为CO2,写出此过程的化学方程式
您最近一年使用:0次
名校
解题方法
4 . I.已知下列热化学方程式:
①P4(s,白磷)+5O2(g)=P4O10(s);△H1=-2983.2kJ/mol
②P(s,红磷)+ O2(g)=
O2(g)= P4O10(s);△H1=-738.5kJ/mol
P4O10(s);△H1=-738.5kJ/mol
③CO(g)=C(s)+ O2(g);△H=+110.5kJ•mol-1
O2(g);△H=+110.5kJ•mol-1
④C(s)+O2(g)=CO2(g);△H=-393.5kJ•mol-1
回答下列问题:
(1)白磷的稳定性比红磷___________ (填“高”或“低”)
(2)表示CO燃烧热的热化学方程式为___________
II.一定条件下,在2L密闭容器中发生反应:3A(g)+B(s) 2C(g)。开始时加入4molA、6molB、2molC,在5min末测得C的物质的量是3mol。
2C(g)。开始时加入4molA、6molB、2molC,在5min末测得C的物质的量是3mol。
(1)用A的浓度变化表示反应的平均速率:___________ 。
(2)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①降低温度,化学反应速率___________ ;
②充入1molB,化学反应速率___________ ;
③将容器的体积变为1L,化学反应速率___________
①P4(s,白磷)+5O2(g)=P4O10(s);△H1=-2983.2kJ/mol
②P(s,红磷)+
 O2(g)=
O2(g)= P4O10(s);△H1=-738.5kJ/mol
P4O10(s);△H1=-738.5kJ/mol③CO(g)=C(s)+
 O2(g);△H=+110.5kJ•mol-1
O2(g);△H=+110.5kJ•mol-1④C(s)+O2(g)=CO2(g);△H=-393.5kJ•mol-1
回答下列问题:
(1)白磷的稳定性比红磷
(2)表示CO燃烧热的热化学方程式为
II.一定条件下,在2L密闭容器中发生反应:3A(g)+B(s)
 2C(g)。开始时加入4molA、6molB、2molC,在5min末测得C的物质的量是3mol。
2C(g)。开始时加入4molA、6molB、2molC,在5min末测得C的物质的量是3mol。(1)用A的浓度变化表示反应的平均速率:
(2)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①降低温度,化学反应速率
②充入1molB,化学反应速率
③将容器的体积变为1L,化学反应速率
您最近一年使用:0次
名校
5 . 能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。阅读下列有关能源的材料,回答有关问题:
(1)从能量的角度看,旧键断裂,新键形成必然有能量变化。已知拆开1molH-H键、1molI-I、1molH-I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1molHI需要___________ (填“放出”或“吸收”)___________ kJ的热量。
(2)在生产和生活中经常遇到化学能与电能的相互转化。在如图甲、乙两装置中,甲中负极电极反应式为___________ ,溶液中的阴离子向___________ 极移动(填“Zn”或“Pt”);乙中铜电极作负极,发生___________ 反应(填“氧化”或“还原”)。
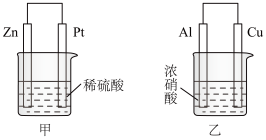
(1)从能量的角度看,旧键断裂,新键形成必然有能量变化。已知拆开1molH-H键、1molI-I、1molH-I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1molHI需要
(2)在生产和生活中经常遇到化学能与电能的相互转化。在如图甲、乙两装置中,甲中负极电极反应式为

您最近一年使用:0次
名校
解题方法
6 . 氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
(1)汽车尾气中常含有碳烟、CO、NO等有害物质,尾气中含有碳烟的主要原因为______ 。
(2)已知在298 K和101 kPa条件下,有如下反应:反应①:C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol
反应②:N2(g)+O2(g)=2NO(g) ΔH2=+180.5kJ·mol
若反应 CO2(g)+
CO2(g)+ N2(g)⇌
N2(g)⇌ C(s)+NO(g)的活化能为a kJ·mol
C(s)+NO(g)的活化能为a kJ·mol ,则反应C(s)+2NO(g)⇌CO2(g)+N2(g)的活化能为
,则反应C(s)+2NO(g)⇌CO2(g)+N2(g)的活化能为____ kJ·mol
(3)在常压下,已知反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g) ΔH(298 K)= -113.0 kJ·mol ,ΔS(298 K)= -145.3×10-3kJ/(mol·K) ,据此可判断该反应在常温下
,ΔS(298 K)= -145.3×10-3kJ/(mol·K) ,据此可判断该反应在常温下___ (填“能”或“不能”)自发进行。
(4)向容积为2L的真空密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)⇌ N2 (g)+CO2(g),NO和N2的物质的量变化如下表所示,在T1℃、T2℃分别到达平衡时容器的总压强分别为p1 kPa、p2 kPa。
①0~10min内,以NO表示的该反应速率v(NO)=_____ kPa·min-1。
②第15 min后,温度调整到T2,数据变化如上表所示,则p1____ p2(填“>”、“<”或“=”)。
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,再次达平衡时NO的体积百分含量为________ 。
(1)汽车尾气中常含有碳烟、CO、NO等有害物质,尾气中含有碳烟的主要原因为
(2)已知在298 K和101 kPa条件下,有如下反应:反应①:C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol

反应②:N2(g)+O2(g)=2NO(g) ΔH2=+180.5kJ·mol

若反应
 CO2(g)+
CO2(g)+ N2(g)⇌
N2(g)⇌ C(s)+NO(g)的活化能为a kJ·mol
C(s)+NO(g)的活化能为a kJ·mol ,则反应C(s)+2NO(g)⇌CO2(g)+N2(g)的活化能为
,则反应C(s)+2NO(g)⇌CO2(g)+N2(g)的活化能为
(3)在常压下,已知反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g) ΔH(298 K)= -113.0 kJ·mol
 ,ΔS(298 K)= -145.3×10-3kJ/(mol·K) ,据此可判断该反应在常温下
,ΔS(298 K)= -145.3×10-3kJ/(mol·K) ,据此可判断该反应在常温下(4)向容积为2L的真空密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)⇌ N2 (g)+CO2(g),NO和N2的物质的量变化如下表所示,在T1℃、T2℃分别到达平衡时容器的总压强分别为p1 kPa、p2 kPa。
| 物质的量/mol | T1℃ | T2℃ | |||||
| 0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min | |
| NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
| N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
①0~10min内,以NO表示的该反应速率v(NO)=
②第15 min后,温度调整到T2,数据变化如上表所示,则p1
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,再次达平衡时NO的体积百分含量为
您最近一年使用:0次
名校
7 . (1)在高温、高压、催化剂作用下,1mol石墨转化为金刚石,吸收1.9 kJ的热量。该反应的ΔH ___________ 0 (填“>”或“<”),对于石墨和金刚石,___________ 更稳定。
(2)用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应反应热的测定实验。回答下列问题:
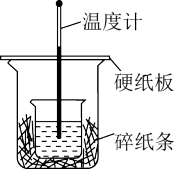
①从实验装置上看,图中尚缺少的一种玻璃用品是___________ 。
②大烧杯上如不盖硬纸板,测得的反应热数值___________ (填“偏大、偏小、无影响”)。
③用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的反应热的数值会___________ (填“偏大”、“偏小”、“无影响”)。
(3)在25℃、101 kPa下,1g CH3OH(l)完全燃烧生成CO2和液态水时放热22.68 kJ。写出表示CH3OH燃烧热的热化学方程式___________ 。
(4)已知几种化学键的键能如表所示:
则反应Cl2(g)+ 3F2(g) 2ClF3(g) 的ΔH =
2ClF3(g) 的ΔH =___________ kJ/mol
(5)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+ 4NO2 (g)=4NO(g)+ CO2 (g)+ 2H2O(1) △H1 = -662kJ·mol-1
②CH4 (g)+ 4NO(g) =2N2 (g)+ CO2 (g)+ 2H2O(1) △H2 = -1251 kJ·mol-1
据此,写出CH4将NO2还原为N2的热化学方程式:___________ 。
(2)用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应反应热的测定实验。回答下列问题:

①从实验装置上看,图中尚缺少的一种玻璃用品是
②大烧杯上如不盖硬纸板,测得的反应热数值
③用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的反应热的数值会
(3)在25℃、101 kPa下,1g CH3OH(l)完全燃烧生成CO2和液态水时放热22.68 kJ。写出表示CH3OH燃烧热的热化学方程式
(4)已知几种化学键的键能如表所示:
| 化学键 | Cl—Cl | F—F | Cl—F |
| 键能/ (kJ/mol) | 242 | 159 | 172 |
则反应Cl2(g)+ 3F2(g)
 2ClF3(g) 的ΔH =
2ClF3(g) 的ΔH =(5)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+ 4NO2 (g)=4NO(g)+ CO2 (g)+ 2H2O(1) △H1 = -662kJ·mol-1
②CH4 (g)+ 4NO(g) =2N2 (g)+ CO2 (g)+ 2H2O(1) △H2 = -1251 kJ·mol-1
据此,写出CH4将NO2还原为N2的热化学方程式:
您最近一年使用:0次
解题方法
8 . 联氨( )是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料。回答下列问题:
)是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料。回答下列问题:
(1)工业上利用 和
和 合成
合成 ,用
,用 进一步制备联氨
进一步制备联氨 。
。
①已知断开(或形成) 键、
键、 键分别需要吸收(或放出)
键分别需要吸收(或放出)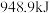 ,
, 的热量,合成
的热量,合成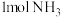 可放出
可放出 的热量,则形成
的热量,则形成 放出的热量为
放出的热量为___________  (保留一位小数)。
(保留一位小数)。
②工业上一种制备联氨的方法为 。该反应涉及物质中属于离子化合物的是
。该反应涉及物质中属于离子化合物的是___________ (填写化学式)。制备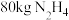 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为___________  。
。
(2)发射航天器时常以 为燃料,
为燃料, 为推进剂。
为推进剂。
已知
ⅰ. 的摩尔燃烧焓为
的摩尔燃烧焓为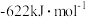 。
。
ⅱ. 与
与 反应的物质和能量变化示意图如下:
反应的物质和能量变化示意图如下:
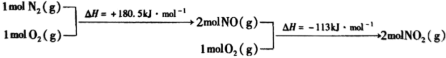
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
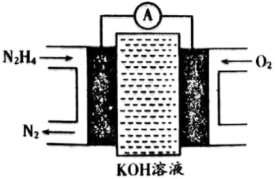
(3)一种联氨燃料电池的工作原理如图所示。放电一段时间,电解质溶液中 的物质的量浓度
的物质的量浓度___________ (填“增大”“减小”或“不变”),负极反应式为___________ 。
 )是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料。回答下列问题:
)是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料。回答下列问题:(1)工业上利用
 和
和 合成
合成 ,用
,用 进一步制备联氨
进一步制备联氨 。
。①已知断开(或形成)
 键、
键、 键分别需要吸收(或放出)
键分别需要吸收(或放出) ,
, 的热量,合成
的热量,合成 可放出
可放出 的热量,则形成
的热量,则形成 放出的热量为
放出的热量为 (保留一位小数)。
(保留一位小数)。②工业上一种制备联氨的方法为
 。该反应涉及物质中属于离子化合物的是
。该反应涉及物质中属于离子化合物的是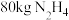 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为 。
。(2)发射航天器时常以
 为燃料,
为燃料, 为推进剂。
为推进剂。已知
ⅰ.
 的摩尔燃烧焓为
的摩尔燃烧焓为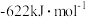 。
。ⅱ.
 与
与 反应的物质和能量变化示意图如下:
反应的物质和能量变化示意图如下: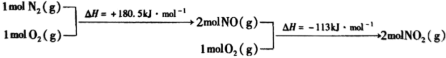
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(3)一种联氨燃料电池的工作原理如图所示。放电一段时间,电解质溶液中
 的物质的量浓度
的物质的量浓度
您最近一年使用:0次
9 . 目前,汽车尾气系统中均安装了催化转化器,大大减少了CO和NOx汽车尾气的排放。
(1)在催化剂作用下CO还原NO、NO2。
标准摩尔生成焓是指由稳态单质生成1mol该化合物的焓变,25℃下几种物质的标准生成焓如下:
ⅰ.CO(g)+NO2(g) CO2(g)+NO(g) ΔH1
CO2(g)+NO(g) ΔH1
ⅱ.2CO(g)+2NO(g) 2CO2(g)+N2(g) ΔH2=-623KJ• mol-1
2CO2(g)+N2(g) ΔH2=-623KJ• mol-1
ΔH1=___________ ;写出用 CO还原NO2生成两种无污染的气态物质总反应的热化学方程式:___________
人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(2)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,负极电极反应式为:___________ 。
(3)一种以 CO为燃料,以空气为氧化剂,以熔融态 K2CO3为电解质的燃料电池,工作原理如下图所示:
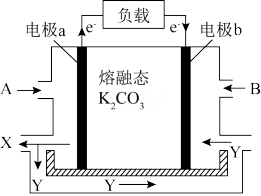
①电极a为___________ (填“ 正极”或“ 负极” ),Y物质为___________ ;
②正极上的电极反应式为___________ 。
(1)在催化剂作用下CO还原NO、NO2。
标准摩尔生成焓是指由稳态单质生成1mol该化合物的焓变,25℃下几种物质的标准生成焓如下:
| NO2 | CO | CO2 | NO | |
| 标准生成焓/kJ•mol-1 | 33.1 | -110.5 | -183.6 | 90.3 |
 CO2(g)+NO(g) ΔH1
CO2(g)+NO(g) ΔH1ⅱ.2CO(g)+2NO(g)
 2CO2(g)+N2(g) ΔH2=-623KJ• mol-1
2CO2(g)+N2(g) ΔH2=-623KJ• mol-1ΔH1=
人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(2)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,负极电极反应式为:
(3)一种以 CO为燃料,以空气为氧化剂,以熔融态 K2CO3为电解质的燃料电池,工作原理如下图所示:

①电极a为
②正极上的电极反应式为
您最近一年使用:0次
10 . 物质的摩尔燃烧焓是指在一定温度和压强条件下,1mol物质完全氧化为同温下的指定产物时的焓变,其中物质中所含的N元素氧化为N2(g)、H元素氧化为H2O(l)、C元素氧化为CO2(g)。
已知:①几种物质的摩尔燃烧焓:
②298k,101kPa时,部分化学键键能:
③H2O(l)=H2O(g) △H=+44.0kJ/mol
回答下列问题:
(1)计算反应2CO(g)+O2(g)=2CO2(g)的焓变△H1=___________ kJ·mol-1,由此可求CO的化学键C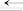 O键能a=
O键能a=___________ kJ·mol-1。
(2)已知相同条件下,石墨比金刚石稳定,则1mol金刚石的燃烧放热___________ 393.5kJ(填“>”、“<”、“=”)。
(3)写出常温下氢气燃烧的热化学方程式___________ ,则反应CO(g)+H2O(g)=CO2(g)+H2(g)的焓变△H2=___________ kJ·mol-1。
已知:①几种物质的摩尔燃烧焓:
| 物质 | 石墨(s) | H2(g) | CO(g) |
| △H/(kJ·mol—1) | -393.5 | -285.8 | -283.0 |
②298k,101kPa时,部分化学键键能:
| 化学键 | C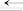 O O | O=O | C=O | C-O |
| E/(kJ·mol-1) | a | 498 | 745 | 351 |
③H2O(l)=H2O(g) △H=+44.0kJ/mol
回答下列问题:
(1)计算反应2CO(g)+O2(g)=2CO2(g)的焓变△H1=
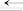 O键能a=
O键能a=(2)已知相同条件下,石墨比金刚石稳定,则1mol金刚石的燃烧放热
(3)写出常温下氢气燃烧的热化学方程式
您最近一年使用:0次



