名校
解题方法
1 . 工业合成氨的反应N2+3H2⇌2NH3的能量变化如图所示,请回答有关问题:
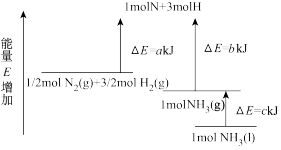
(1)合成1molNH3(l)____ (填“吸收”或“放出”)____ kJ的热量。
(2)推测反应2NH3(l)⇌2N2(g)+3H2(g)比反应2NH3(g)⇌2N2(g)+3H2(g)___ (填“吸收”或“放出”)的热量___ (填“多”或“少”)。
(3)已知:P(s,白磷)=P(s,黑磷),每1molP(s,白磷)发生反应,放出39.3kJ的热量,P(s,白磷)=P(s,红磷),每1molP(s,白磷)发生反应,放出17.6kJ的热量,由此推知,其中最稳定的磷单质是__ (填“黑磷”或“红磷”)。
(4)某实验小组同学对电化学原理进行了一系列探究活动。
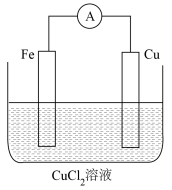
该电池基于总反应____ (用离子方程式表示)来设计的,一段时间后,铜极质量变化32g,则导线中通过____ mol电子。

(1)合成1molNH3(l)
(2)推测反应2NH3(l)⇌2N2(g)+3H2(g)比反应2NH3(g)⇌2N2(g)+3H2(g)
(3)已知:P(s,白磷)=P(s,黑磷),每1molP(s,白磷)发生反应,放出39.3kJ的热量,P(s,白磷)=P(s,红磷),每1molP(s,白磷)发生反应,放出17.6kJ的热量,由此推知,其中最稳定的磷单质是
(4)某实验小组同学对电化学原理进行了一系列探究活动。

该电池基于总反应
您最近一年使用:0次
名校
解题方法
2 .  催化加氢制备
催化加氢制备 是
是 资源化利用的重要途径。已知下图所示的反应的能量变化。
资源化利用的重要途径。已知下图所示的反应的能量变化。

下列说法不正确 的是
 催化加氢制备
催化加氢制备 是
是 资源化利用的重要途径。已知下图所示的反应的能量变化。
资源化利用的重要途径。已知下图所示的反应的能量变化。
下列说法
| A.由图1推知反应物断键吸收的能量小于生成物成键释放的能量 |
B.图2中,若生成的 为液态,则能量变化曲线为① 为液态,则能量变化曲线为① |
C. |
D.制备 的反应使用催化剂时,其 的反应使用催化剂时,其 不变 不变 |
您最近一年使用:0次
2021-05-10更新
|
807次组卷
|
8卷引用:北京一零一中学2020-2021学年高一下学期期末考试化学试题
北京一零一中学2020-2021学年高一下学期期末考试化学试题北京市海淀区2021届高三二模化学试题(已下线)2021年高考化学押题预测卷(北京卷)(02)湖南省五市十校教研教改共同体2021-2022学年高一下学期期末考试化学试题河南省中原名校2022-2023学年高二上学期第一次联考化学试题(已下线)题型14 从吸热与放热角度突破反应热图像北京交通大学附属中学2023-2024学年高三上学期12月月考化学试题 北京市第十二中学2023-2024学年高二上学期期中考试化学试题
3 . 按要求填空:
(1)相对分子质量为72的烷烃的分子式为___________ ,结构有___________ 种,分别写出它们的结构简式___________ 。
(2)下列物质熔沸点由高到低的顺序是:①CH4;②C3H8;③CH3CH(CH3)2 ;④CH3CH2CH2CH3;___________ (填序号)
(3)4 g甲烷在氧气中燃烧生成CO2和液态水,放出222.5 kJ热量,写出表示甲烷燃烧热的热化学方程式___________ 。
(4)已知:①Fe(s)+ O2(g)=FeO(s) ΔH1=—272.0 kJ·mol-1
O2(g)=FeO(s) ΔH1=—272.0 kJ·mol-1
②2Al(s)+ O2(g)=Al2O3(s) ΔH2=—1675.7 kJ·mol-1
O2(g)=Al2O3(s) ΔH2=—1675.7 kJ·mol-1
Al和FeO发生反应的热化学方程式是___________ 。
(1)相对分子质量为72的烷烃的分子式为
(2)下列物质熔沸点由高到低的顺序是:①CH4;②C3H8;③CH3CH(CH3)2 ;④CH3CH2CH2CH3;
(3)4 g甲烷在氧气中燃烧生成CO2和液态水,放出222.5 kJ热量,写出表示甲烷燃烧热的热化学方程式
(4)已知:①Fe(s)+
 O2(g)=FeO(s) ΔH1=—272.0 kJ·mol-1
O2(g)=FeO(s) ΔH1=—272.0 kJ·mol-1②2Al(s)+
 O2(g)=Al2O3(s) ΔH2=—1675.7 kJ·mol-1
O2(g)=Al2O3(s) ΔH2=—1675.7 kJ·mol-1Al和FeO发生反应的热化学方程式是
您最近一年使用:0次
4 . 化学反应往往伴随着能量的变化,请完成以下问题
Ⅰ.已知:2H2(g)+O2(g)=2H2O(g) ΔΗ=-483.6kJ·mol-1 ,N2(g)+2O2(g)=2NO2(g) ΔΗ=+67.7kJ·mol-1;则反应4H2(g)+2NO2(g)=N2(g)+4H2O(g)的反应热ΔΗ=_______ 。
II.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) =CH3OH(g),反应过程中的能量变化情况如图所示。
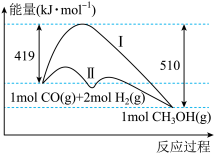
(1)曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。该反应是_______ (填“吸热”或“放热”)反应。计算当反应生成1.5molCH3OH(g)时,能量变化值是_______ kJ。
(2)选择适宜的催化剂_______ (填“能”或“不能”)改变该反应的反应热。
(3)推测反应CH3OH(g) =CO(g)+2H2(g)是_______ (填“吸热”或“放热”)反应。
III.断开1molH—H键、1molN—H键、1molN≡N键分别需要吸收能量为436kJ、391kJ、946kJ,则1molH2与足量N2反应生成NH3需_______ (填“吸收”或“放出”)能量_______ kJ。(小数点后保留两位数字),事实上,反应的热量总小于理论值,理由是_______ 。
Ⅰ.已知:2H2(g)+O2(g)=2H2O(g) ΔΗ=-483.6kJ·mol-1 ,N2(g)+2O2(g)=2NO2(g) ΔΗ=+67.7kJ·mol-1;则反应4H2(g)+2NO2(g)=N2(g)+4H2O(g)的反应热ΔΗ=
II.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) =CH3OH(g),反应过程中的能量变化情况如图所示。

(1)曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。该反应是
(2)选择适宜的催化剂
(3)推测反应CH3OH(g) =CO(g)+2H2(g)是
III.断开1molH—H键、1molN—H键、1molN≡N键分别需要吸收能量为436kJ、391kJ、946kJ,则1molH2与足量N2反应生成NH3需
您最近一年使用:0次
5 . NH3和联氨(N2H4)是两种重要的氮氢化合物,在科研和生产中应用广泛。
(1)①已知:
注:拆开气态物质中 1 mol 某种共价键需要吸收的能量,就是该共价键的键能。
N2(g)+3H2(g) 2NH3(g) ∆H=
2NH3(g) ∆H=__________ kJ/mol
②联氨(N2H4)和N2O4 可作为火箭推进剂。
已知:N2(g)+2O2(g)=N2O4(g) ∆H=10.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) ∆H=-543kJ/mol
N2H4(g)和N2O4(g)反应生成 N2(g)和H2O(g)的热化学方程式为_______ 。
(2)一定温度下,向恒容的密闭容器中充入N2 和H2 发生反应:N2+3H2 2NH3,测得各组分浓度随时间变化如图所示。
2NH3,测得各组分浓度随时间变化如图所示。
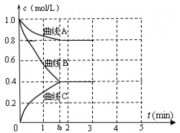
①表示c(N2)的曲线是_______ 。(填“曲线 A”、“曲线B”或“曲线C”)
②0~t0时,v(H2)=_______ mol·L-1·min-1。
③下列措施不能使该反应速率加快的是_______ 。
a.升高温度 b.降低压强 c.使用催化剂
④下列能说明该反应达到平衡的是_______ 。
a.混合气体的压强不再变化 b.2c(H2)= 3c(NH3) c.混合气体的质量不再变化
(1)①已知:
| 共价键 | 键能/ kJ·mol-1 |
| H-H | 436 |
| N≡N | 946 |
| N-H | 391 |
注:拆开气态物质中 1 mol 某种共价键需要吸收的能量,就是该共价键的键能。
N2(g)+3H2(g)
 2NH3(g) ∆H=
2NH3(g) ∆H=②联氨(N2H4)和N2O4 可作为火箭推进剂。
已知:N2(g)+2O2(g)=N2O4(g) ∆H=10.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) ∆H=-543kJ/mol
N2H4(g)和N2O4(g)反应生成 N2(g)和H2O(g)的热化学方程式为
(2)一定温度下,向恒容的密闭容器中充入N2 和H2 发生反应:N2+3H2
 2NH3,测得各组分浓度随时间变化如图所示。
2NH3,测得各组分浓度随时间变化如图所示。
①表示c(N2)的曲线是
②0~t0时,v(H2)=
③下列措施不能使该反应速率加快的是
a.升高温度 b.降低压强 c.使用催化剂
④下列能说明该反应达到平衡的是
a.混合气体的压强不再变化 b.2c(H2)= 3c(NH3) c.混合气体的质量不再变化
您最近一年使用:0次
名校
解题方法
6 . 在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为
反应I:CO2(g)+4H2(g)=CH4(g)+2H2O(g)ΔH=-164.7kJ·mol-1
反应II:CO2(g)+H2(g)=CO(g)+H2O(g)ΔH=41.2kJ·mol-1
反应III:2CO(g)+2H2(g)=CO2(g)+CH4(g)ΔH=-247.1kJ·mol-1
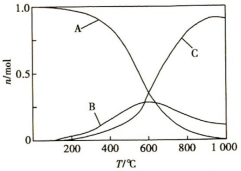
向恒压、密闭容器中通入lmolCO2和4molH2,平衡时CH4、CO、CO2的物质的量随温度的变化如图所示,下列说法不正确的是
反应I:CO2(g)+4H2(g)=CH4(g)+2H2O(g)ΔH=-164.7kJ·mol-1
反应II:CO2(g)+H2(g)=CO(g)+H2O(g)ΔH=41.2kJ·mol-1
反应III:2CO(g)+2H2(g)=CO2(g)+CH4(g)ΔH=-247.1kJ·mol-1
向恒压、密闭容器中通入lmolCO2和4molH2,平衡时CH4、CO、CO2的物质的量随温度的变化如图所示,下列说法不正确的是

| A.图中曲线A表示CO2的物质的量随温度的变化 |
| B.图中曲线B表示CH4的物质的量随温度的变化 |
| C.图中曲线C表示CO的物质的量随温度的变化 |
| D.CH4(g)+H2O(g)=CO(g)+3H2(g)的ΔH=-205.9kJ·mol-1 |
您最近一年使用:0次
名校
解题方法
7 . 生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在 下,
下, 氢气完全燃烧生成液态水放出
氢气完全燃烧生成液态水放出 的热量,
的热量,
①请写出表示氢气燃烧热的热化学方程式____ 。
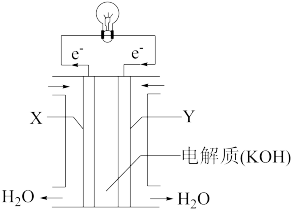
②将上述反应设计成下图所示的原电池,其中Y为___ 极(填“正”或“负”),该极电极反应式为___ 。
(2)最新一期国际学术期刊《自然·纳米技术》介绍了我国科学家曾杰团队的成果:在含铂高效催化剂作用下把二氧化碳高效转化清洁液态燃料——甲醇 。
。
①该法利用 制取甲醇的有关化学反应如下:
制取甲醇的有关化学反应如下:
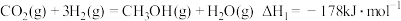
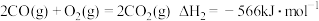
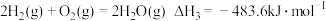
已知:i.断开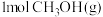 中的化学键共吸收
中的化学键共吸收 的能量
的能量
ii.反应①中部分化学键键能数据如下:
由此计算断开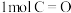 需要吸收
需要吸收____ kJ的能量,
____  。
。
②甲醇燃烧时发生如下反应(a、b、c、d均大于0):
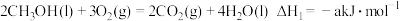
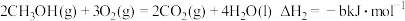
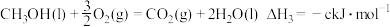
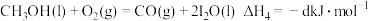
由此知,a、b、c、d由小到大排序为_______ 。
③将甲醇完全燃烧生成液态水的反应设计成原电池,以 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式__ 。
(1)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在
 下,
下, 氢气完全燃烧生成液态水放出
氢气完全燃烧生成液态水放出 的热量,
的热量,①请写出表示氢气燃烧热的热化学方程式
②将上述反应设计成下图所示的原电池,其中Y为

(2)最新一期国际学术期刊《自然·纳米技术》介绍了我国科学家曾杰团队的成果:在含铂高效催化剂作用下把二氧化碳高效转化清洁液态燃料——甲醇
 。
。①该法利用
 制取甲醇的有关化学反应如下:
制取甲醇的有关化学反应如下: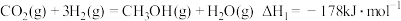
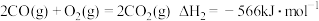
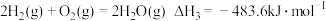
已知:i.断开
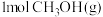 中的化学键共吸收
中的化学键共吸收 的能量
的能量ii.反应①中部分化学键键能数据如下:
| 化学键 | H-H | H-O |
键能/( ) ) | 436 | 463 |
由此计算断开
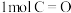 需要吸收
需要吸收
 。
。②甲醇燃烧时发生如下反应(a、b、c、d均大于0):
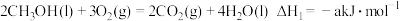
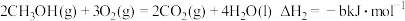
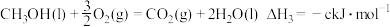
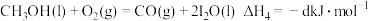
由此知,a、b、c、d由小到大排序为
③将甲醇完全燃烧生成液态水的反应设计成原电池,以
 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式
您最近一年使用:0次
名校
8 . 室温下,将 溶于水会使溶液温度降低,热效应为
溶于水会使溶液温度降低,热效应为 ,将
,将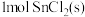 溶于水会使溶液温度升高,热效应为
溶于水会使溶液温度升高,热效应为 ;
; 受热分解的化学方程式为
受热分解的化学方程式为 ,热效应为
,热效应为 。则下列判断正确的是
。则下列判断正确的是
 溶于水会使溶液温度降低,热效应为
溶于水会使溶液温度降低,热效应为 ,将
,将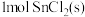 溶于水会使溶液温度升高,热效应为
溶于水会使溶液温度升高,热效应为 ;
; 受热分解的化学方程式为
受热分解的化学方程式为 ,热效应为
,热效应为 。则下列判断正确的是
。则下列判断正确的是A. | B.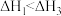 | C. | D. |
您最近一年使用:0次
9 . 化学反应往往伴随着能量的变化,请完成以下问题
Ⅰ.已知:2H2(g)+O2(g)=2H2O(g) ΔΗ=-483.6kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔΗ=+67.7kJ·mol-1
则反应4H2(g)+2NO2(g)=N2(g)+4H2O(g)的反应热ΔΗ=_____ 。
Ⅱ.断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子,所吸收的能量称为A—B键的键能。下表列出了一些化学键的键能E:
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应为__________ (填“吸热”或“放热”)反应。
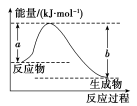
(2)若图示表示反应H2(g)+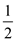 O2(g)=H2O(g) ΔH=-242 kJ·mol-1,x=
O2(g)=H2O(g) ΔH=-242 kJ·mol-1,x=___________ 。
(3)由非金属性,可用CuCl2作催化剂,在450 ℃利用空气中的氧气跟氯化氢反应制氯气,反应的化学方程式为_________________________ 。
若忽略温度和压强对反应热的影响,根据上题中的有关数据,计算当反应中有1 mol 电子转移时,反应的能量变化为______ 。
Ⅰ.已知:2H2(g)+O2(g)=2H2O(g) ΔΗ=-483.6kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔΗ=+67.7kJ·mol-1
则反应4H2(g)+2NO2(g)=N2(g)+4H2O(g)的反应热ΔΗ=
Ⅱ.断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子,所吸收的能量称为A—B键的键能。下表列出了一些化学键的键能E:
| 化学键 | H—H | Cl—Cl | O=O | C—Cl | C—H | O—H | H—Cl |
| E/(kJ·mol-1) | 436 | 247 | x | 330 | 413 | 463 | 431 |
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应为

(2)若图示表示反应H2(g)+
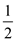 O2(g)=H2O(g) ΔH=-242 kJ·mol-1,x=
O2(g)=H2O(g) ΔH=-242 kJ·mol-1,x=(3)由非金属性,可用CuCl2作催化剂,在450 ℃利用空气中的氧气跟氯化氢反应制氯气,反应的化学方程式为
若忽略温度和压强对反应热的影响,根据上题中的有关数据,计算当反应中有1 mol 电子转移时,反应的能量变化为
您最近一年使用:0次
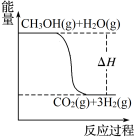
10 . 下列说法正确的是

| A.红热的C 与H2O 蒸气反应制取水煤气是放热反应 |
| B.反应物的总能量低于生成物的总能量时,一定不能发生反应 |
| C.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照或点燃的条件下的 ΔH 相同 |
| D.由图可知:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH>0 |
您最近一年使用:0次



