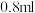名校
解题方法
1 . 实验小组探究 溶液与
溶液与 溶液的反应:
溶液的反应:
【资料】① 是强电解质,具有强氧化性。
是强电解质,具有强氧化性。 易被还原为
易被还原为 ;
;
② 可与
可与 发生反应:
发生反应:
③在溶液中 淀粉复合物必须有足够的浓度才能显示明显的蓝色
淀粉复合物必须有足够的浓度才能显示明显的蓝色
Ⅰ.实验小组设计了下列实验验证了 溶液与
溶液与 溶液的反应:
溶液的反应:
(1)实验1-1的目的是_______ 。
(2)请用离子方程式表示实验1-2中的化学反应_______ 。
Ⅱ.实验小组发现, 溶液中若含有
溶液中若含有 ,溶液并不会立刻变蓝,而会等待一段时间后再变蓝。为了解释这一现象,甲同学对此提出两种猜想:
,溶液并不会立刻变蓝,而会等待一段时间后再变蓝。为了解释这一现象,甲同学对此提出两种猜想:
猜想1:其他条件相同时, 与
与 反应速率_______
反应速率_______ 与
与 的反应速率,使溶液中
的反应速率,使溶液中 浓度降低,化学反应速率变慢。(填“
浓度降低,化学反应速率变慢。(填“ ”或“
”或“ ”)
”)
猜想2:其他条件相同时, 与
与 不反应。
不反应。 与
与 反应速率_______
反应速率_______ 与
与 的反应速率(填“
的反应速率(填“ ”或“
”或“ ”)。
”)。
(3)请补全猜想1:_______ 与猜想2:_______ 。
(4)根据资料2可知 的还原性
的还原性_______ (填“强于”或“弱于”) ,甲同学认为,该事实可以用来作为
,甲同学认为,该事实可以用来作为_______ (填“猜想1”或“猜想2”)的依据。
Ⅲ.为了进一步研究 的作用,小组同学分别向两支试管中依次加入下列试剂,并记录变他时间,如下表所示。
的作用,小组同学分别向两支试管中依次加入下列试剂,并记录变他时间,如下表所示。
(5)请补全表格中①_______ 与②_______
(6)乙同学根据现有数据证明Ⅱ中猜想1不成立,理由是_______ 。
Ⅳ.查阅文献表明Ⅱ中猜想2成立:
(7)下列说法正确的是_______(填字母)。
(8)结合实验2-2的数据,计算 内的
内的 消耗的速率
消耗的速率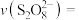
_______ 
 溶液与
溶液与 溶液的反应:
溶液的反应:【资料】①
 是强电解质,具有强氧化性。
是强电解质,具有强氧化性。 易被还原为
易被还原为 ;
;②
 可与
可与 发生反应:
发生反应:
③在溶液中
 淀粉复合物必须有足够的浓度才能显示明显的蓝色
淀粉复合物必须有足够的浓度才能显示明显的蓝色Ⅰ.实验小组设计了下列实验验证了
 溶液与
溶液与 溶液的反应:
溶液的反应:编号 | 1-1 | 1-2 |
实验操作 |
|
|
现象 | 无明显现象 | 溶液立即变蓝 |
(2)请用离子方程式表示实验1-2中的化学反应
Ⅱ.实验小组发现,
 溶液中若含有
溶液中若含有 ,溶液并不会立刻变蓝,而会等待一段时间后再变蓝。为了解释这一现象,甲同学对此提出两种猜想:
,溶液并不会立刻变蓝,而会等待一段时间后再变蓝。为了解释这一现象,甲同学对此提出两种猜想:猜想1:其他条件相同时,
 与
与 反应速率_______
反应速率_______ 与
与 的反应速率,使溶液中
的反应速率,使溶液中 浓度降低,化学反应速率变慢。(填“
浓度降低,化学反应速率变慢。(填“ ”或“
”或“ ”)
”)猜想2:其他条件相同时,
 与
与 不反应。
不反应。 与
与 反应速率_______
反应速率_______ 与
与 的反应速率(填“
的反应速率(填“ ”或“
”或“ ”)。
”)。(3)请补全猜想1:
(4)根据资料2可知
 的还原性
的还原性 ,甲同学认为,该事实可以用来作为
,甲同学认为,该事实可以用来作为Ⅲ.为了进一步研究
 的作用,小组同学分别向两支试管中依次加入下列试剂,并记录变他时间,如下表所示。
的作用,小组同学分别向两支试管中依次加入下列试剂,并记录变他时间,如下表所示。编号 |
|
| 淀粉 溶液 |
| ① | 变色时间 |
2-1 |
|
| 2滴 |
| ② | 立即 |
2-2 |
|
| 2滴 |
|
|
|
(6)乙同学根据现有数据证明Ⅱ中猜想1不成立,理由是
Ⅳ.查阅文献表明Ⅱ中猜想2成立:
(7)下列说法正确的是_______(填字母)。
A.增加溶液中 浓度, 浓度, 的初始反应速率会增加 的初始反应速率会增加 |
B.增加溶液中 浓度,溶液变蓝时间可能增加 浓度,溶液变蓝时间可能增加 |
C.增加溶液中 浓度,溶液可能无法变蓝 浓度,溶液可能无法变蓝 |
| D.升高溶液温度,溶液开始变蓝时间可能增加 |
 内的
内的 消耗的速率
消耗的速率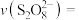

您最近半年使用:0次
名校
解题方法
2 . Ⅰ.某实验小组以 分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
(1)实验①和②的目的是探究___________ 对反应速率的影响。实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下 稳定,不易分解。
稳定,不易分解。
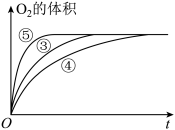
(2)实验③④⑤,测得生成氧气的体积随时间变化的关系如图。分析图能够得出的实验结论:_____ 性环境能够增大 分解的速率。
分解的速率。
(3)已知 溶液中主要含有
溶液中主要含有 、
、 和
和 三种微粒。为了证明
三种微粒。为了证明 对
对 分解无催化作用,实验小组在查阅资料得知
分解无催化作用,实验小组在查阅资料得知 不会影响
不会影响 的分解后,补充做了实验:往
的分解后,补充做了实验:往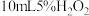 溶液中加入
溶液中加入___________ ,观察到___________ 。
(4)该小组预测同为第四周期Ⅷ族的 、
、 、
、 可能有相似的催化作用。查阅资料:
可能有相似的催化作用。查阅资料: (其中
(其中 、
、 均为+2价)也可用作
均为+2价)也可用作 分解的催化剂,具有较高的活性。如图表示催化剂
分解的催化剂,具有较高的活性。如图表示催化剂 在10℃时催化分解6%的
在10℃时催化分解6%的 溶液的相对初始速率随
溶液的相对初始速率随 变化曲线。则
变化曲线。则 、
、 两种离子中催化效果更好的是
两种离子中催化效果更好的是___________ 。

Ⅱ.为进一步研究浓度对反应速率的影响,该实验小组又设计了如下实验方案,记录溶液褪色所需的时间。(反应方程式为: )
)
(5)忽略混合前后溶液体积的变化,实验2中用草酸表示的反应速率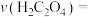
______ 。
(6)褪色时间: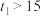 ,则该组实验得出的结论是
,则该组实验得出的结论是___________ 。
(7)实验过程中同学还发现,酸性高锰酸钾溶液与草酸溶液反应开始时,溶液褪色慢,但过了一段时间后溶液褪色明显加快。除了温度的影响,出现此现象还可能的原因是___________ 。
 分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。| 分组实验 | 催化剂 | |
| ① | 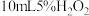 溶液 溶液 | 无 |
| ② |  溶液 溶液 | 无 |
| ③ | 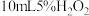 溶液 溶液 | 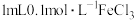 溶液 溶液 |
| ④ | 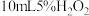 溶液+少量稀盐酸 溶液+少量稀盐酸 | 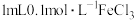 溶液 溶液 |
| ⑤ | 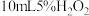 溶液+少量 溶液+少量 溶液 溶液 | 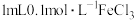 溶液 溶液 |
(1)实验①和②的目的是探究
 稳定,不易分解。
稳定,不易分解。(2)实验③④⑤,测得生成氧气的体积随时间变化的关系如图。分析图能够得出的实验结论:
 分解的速率。
分解的速率。
(3)已知
 溶液中主要含有
溶液中主要含有 、
、 和
和 三种微粒。为了证明
三种微粒。为了证明 对
对 分解无催化作用,实验小组在查阅资料得知
分解无催化作用,实验小组在查阅资料得知 不会影响
不会影响 的分解后,补充做了实验:往
的分解后,补充做了实验:往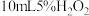 溶液中加入
溶液中加入(4)该小组预测同为第四周期Ⅷ族的
 、
、 、
、 可能有相似的催化作用。查阅资料:
可能有相似的催化作用。查阅资料: (其中
(其中 、
、 均为+2价)也可用作
均为+2价)也可用作 分解的催化剂,具有较高的活性。如图表示催化剂
分解的催化剂,具有较高的活性。如图表示催化剂 在10℃时催化分解6%的
在10℃时催化分解6%的 溶液的相对初始速率随
溶液的相对初始速率随 变化曲线。则
变化曲线。则 、
、 两种离子中催化效果更好的是
两种离子中催化效果更好的是
Ⅱ.为进一步研究浓度对反应速率的影响,该实验小组又设计了如下实验方案,记录溶液褪色所需的时间。(反应方程式为:
 )
)| 实验操作 | 褪色时间 | |
| 实验1 |  的草酸溶液与 的草酸溶液与 的高锰酸钾酸性溶液混合 的高锰酸钾酸性溶液混合 |  |
| 实验2 | 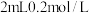 的草酸溶液与 的草酸溶液与 的高锰酸钾酸性溶液混合 的高锰酸钾酸性溶液混合 | 15 |
(5)忽略混合前后溶液体积的变化,实验2中用草酸表示的反应速率
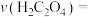
(6)褪色时间:
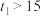 ,则该组实验得出的结论是
,则该组实验得出的结论是(7)实验过程中同学还发现,酸性高锰酸钾溶液与草酸溶液反应开始时,溶液褪色慢,但过了一段时间后溶液褪色明显加快。除了温度的影响,出现此现象还可能的原因是
您最近半年使用:0次
名校
解题方法
3 . 调控化学反应速率对化工生产有重要的意义 ,某校实验小组欲通过实验探究浓度、催化剂、温度等条件对反应速率的影响。
I.第一实验小组以H2O2分解为例,研究浓度、催化剂、溶液的酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
(1)H2O2分解的化学反应方程式为_______ 。
(2)选取①②在探究浓度对速率的影响时,时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是_______ 。
(3)选取_______ (填实验序号)实验,可完成催化剂对反应速率影响的探究
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图所示。分析图示能够得出的实验结论是_______ 。

II.第二实验小组欲用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素(离子方程式为2MnO +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O)。该实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图甲所示:
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O)。该实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图甲所示:
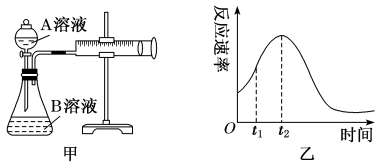
(5)该实验探究的是_______ 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是_______ (填实验序号)。
(6)若实验①在2min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO )=
)=_______ mol·L-1(假设混合溶液的体积为50 mL),2min内H2C2O4的消耗速率为v (H2C2O4) =_______ mol·L-1·min-1
(7)小组同学发现反应速率变化如图乙,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂,②_______ 。
I.第一实验小组以H2O2分解为例,研究浓度、催化剂、溶液的酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
| 编号 | 反应物 | 催化剂 |
| ① | 10 mL 2%H2O2溶液 | 无 |
| ② | 10 mL 5%H2O2溶液 | 无 |
| ③ | 10 mL 5%H2O2溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
| ④ | 10 mL 5%H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
| ⑤ | 10 mL 5%H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
| ⑥ | 10 mL 5%H2O2溶液+1 mL H2O | 无 |
(2)选取①②在探究浓度对速率的影响时,时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是
(3)选取
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图所示。分析图示能够得出的实验结论是

II.第二实验小组欲用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素(离子方程式为2MnO
 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O)。该实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图甲所示:
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O)。该实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化),实验装置如图甲所示:
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1 mol·L-1 H2C2O4溶液 | 30mL 0.01 mol·L-1 KMnO4溶液 |
| ② | 20mL 0.2 mol·L-1 H2C2O4溶液 | 30mL0.01 mol·L-1 KMnO4溶液 |
(6)若实验①在2min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO
 )=
)=(7)小组同学发现反应速率变化如图乙,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂,②
您最近半年使用:0次
4 . 海带中含有丰富的碘元素,某化学兴趣小组设计如下所示的流程图提取碘:
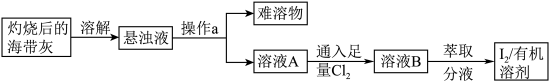
请回答下列问题:
(1)加水溶解海带灰,应采用的装置是_______ (填字母序号)
A.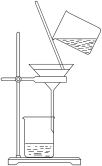 B.
B. C.
C.
(2)操作a的名称是_______ (填“过滤”或“蒸发”);
(3)溶液A中通入足量 发生的反应为:
发生的反应为: ,反应物
,反应物 表现
表现_______ (填“氧化性”或“还原性”);
(4)工业上合成氨的反应为: 。一定条件下,将2 mol
。一定条件下,将2 mol  和6 mol
和6 mol  置于1 L的密闭容器中,10 min后测得
置于1 L的密闭容器中,10 min后测得 为0.4 mol。
为0.4 mol。
①用 的浓度变化表示该反应0~10 min的平均速率为
的浓度变化表示该反应0~10 min的平均速率为_______ mol/(L·min);
②其他条件不变时,压缩容器体积,增大压强,该反应的速率将_______ (填“增大”或“减小”)。

请回答下列问题:
(1)加水溶解海带灰,应采用的装置是
A.
 B.
B. C.
C.
(2)操作a的名称是
(3)溶液A中通入足量
 发生的反应为:
发生的反应为: ,反应物
,反应物 表现
表现(4)工业上合成氨的反应为:
 。一定条件下,将2 mol
。一定条件下,将2 mol  和6 mol
和6 mol  置于1 L的密闭容器中,10 min后测得
置于1 L的密闭容器中,10 min后测得 为0.4 mol。
为0.4 mol。①用
 的浓度变化表示该反应0~10 min的平均速率为
的浓度变化表示该反应0~10 min的平均速率为②其他条件不变时,压缩容器体积,增大压强,该反应的速率将
您最近半年使用:0次
5 . 用 溶液氧化废水中的还原性污染物M。为研究降解效果,设计如下对比实验探究温度、
溶液氧化废水中的还原性污染物M。为研究降解效果,设计如下对比实验探究温度、 对降解速率和效果的影响,实验测得
对降解速率和效果的影响,实验测得 的浓度与时间关系如图所示。下列说法正确的是
的浓度与时间关系如图所示。下列说法正确的是

 溶液氧化废水中的还原性污染物M。为研究降解效果,设计如下对比实验探究温度、
溶液氧化废水中的还原性污染物M。为研究降解效果,设计如下对比实验探究温度、 对降解速率和效果的影响,实验测得
对降解速率和效果的影响,实验测得 的浓度与时间关系如图所示。下列说法正确的是
的浓度与时间关系如图所示。下列说法正确的是| 实验编号 | 温度/ | pH |
| ① | 25 | 1 |
| ② | 45 | 1 |
| ③ | 25 | 7 |

A. 中 中 元素的化合价为 元素的化合价为 价,因此有较强的氧化性 价,因此有较强的氧化性 |
B.实验①中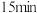 时 时 的降解速率为 的降解速率为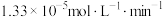 |
C.若其他条件相同,则实验①②说明升高温度, 的降解速率增大 的降解速率增大 |
D.若其他条件相同,则实验①③说明 值越大, 值越大, 的降解速率越大 的降解速率越大 |
您最近半年使用:0次
名校
6 . 图是铁元素在元素周期表中的有关信息。

(1)写出铁在周期表中的位置_______ 。“55.85”是_______ 。
(2)自然界中存在的54Fe和56Fe,它们互称为_______ 。
(3)久置的FeSO4溶液变黄,一般认为是二价铁被氧化为三价铁的缘故。某研究小组为研究溶液中Fe2+被O2氧化的过程,查阅资料发现:溶液中Fe2+的氧化过程分为先后两步,首先是Fe2+水解,接着水解产物被O2氧化。于是小组同学决定研究常温下不同pH对Fe2+被O2氧化的影响,并测定了Fe2+氧化率随时间变化的关系,结果如图。
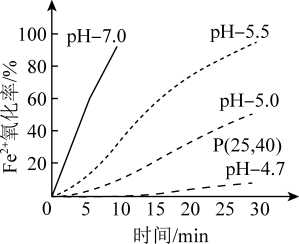
①写出Fe2+水解的离子方程式_______ ;要抑制FeSO4水解,可以采取的措施是_______ 。
②若配制的FeSO4溶液浓度为0.01 mol/L,反应过程中溶液体积不变,计算图中P点Fe2+的氧化速率_______ 。
③结合图示分析不同pH对Fe2+被O2氧化的反应产生了怎样的影响_______ 。
④研究小组在查阅资料时还得知:氧气的氧化性随溶液的酸性增强而增强。通过以上研究可知,配制FeSO4溶液的正确做法是_______ 。

(1)写出铁在周期表中的位置
(2)自然界中存在的54Fe和56Fe,它们互称为
(3)久置的FeSO4溶液变黄,一般认为是二价铁被氧化为三价铁的缘故。某研究小组为研究溶液中Fe2+被O2氧化的过程,查阅资料发现:溶液中Fe2+的氧化过程分为先后两步,首先是Fe2+水解,接着水解产物被O2氧化。于是小组同学决定研究常温下不同pH对Fe2+被O2氧化的影响,并测定了Fe2+氧化率随时间变化的关系,结果如图。

①写出Fe2+水解的离子方程式
②若配制的FeSO4溶液浓度为0.01 mol/L,反应过程中溶液体积不变,计算图中P点Fe2+的氧化速率
③结合图示分析不同pH对Fe2+被O2氧化的反应产生了怎样的影响
④研究小组在查阅资料时还得知:氧气的氧化性随溶液的酸性增强而增强。通过以上研究可知,配制FeSO4溶液的正确做法是
您最近半年使用:0次
名校
7 . 某实验小组为探究酸性条件下碘化钾与过氧化氧反应的化学反应速率,进行了以下实验探究。
(1)实验一:向硫酸酸化的过氧化氢溶液中加入碘化钾、淀粉和硫代硫酸钠( )的混合溶液,一段时间后溶液变蓝。该小组查阅资料知体系中存在下列两个主要反应:
)的混合溶液,一段时间后溶液变蓝。该小组查阅资料知体系中存在下列两个主要反应:
反应ⅰ: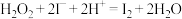 ;
;
反应ⅱ: 。
。
为了证实上述反应过程,进行下列实验(所用试剂浓度均为 )
)
实验二:向酸化的 溶液中加入淀粉KI溶液,溶液几秒后变为蓝色。再向已经变蓝的溶液中加入
溶液中加入淀粉KI溶液,溶液几秒后变为蓝色。再向已经变蓝的溶液中加入 溶液,溶液立即褪色。
溶液,溶液立即褪色。
根据此现象可知反应ⅰ的速率_______ 反应ⅱ的速率(填“大于”、“小于”或“等于”),解释实验一中溶液混合一段时间后才变蓝的原因是_______ 。
(2)为了探究 对反应速率的影响,设计两组对比实验,按下表中的试剂用量将其迅速混合观察现象。(各实验均在室温条件下进行)
对反应速率的影响,设计两组对比实验,按下表中的试剂用量将其迅速混合观察现象。(各实验均在室温条件下进行)
①V1=_______ ,V2=_______ 。
②对比实验I和实验II,
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)利用实验I的数据,计算反应ⅱ在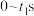 的化学反应速率
的化学反应速率
_______  ;反应ⅰ在
;反应ⅰ在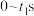 的化学反应速率
的化学反应速率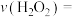
_______ 
(1)实验一:向硫酸酸化的过氧化氢溶液中加入碘化钾、淀粉和硫代硫酸钠(
 )的混合溶液,一段时间后溶液变蓝。该小组查阅资料知体系中存在下列两个主要反应:
)的混合溶液,一段时间后溶液变蓝。该小组查阅资料知体系中存在下列两个主要反应:反应ⅰ:
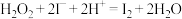 ;
;反应ⅱ:
 。
。为了证实上述反应过程,进行下列实验(所用试剂浓度均为
 )
)实验二:向酸化的
 溶液中加入淀粉KI溶液,溶液几秒后变为蓝色。再向已经变蓝的溶液中加入
溶液中加入淀粉KI溶液,溶液几秒后变为蓝色。再向已经变蓝的溶液中加入 溶液,溶液立即褪色。
溶液,溶液立即褪色。根据此现象可知反应ⅰ的速率
(2)为了探究
 对反应速率的影响,设计两组对比实验,按下表中的试剂用量将其迅速混合观察现象。(各实验均在室温条件下进行)
对反应速率的影响,设计两组对比实验,按下表中的试剂用量将其迅速混合观察现象。(各实验均在室温条件下进行)| 实验编号 | 试剂体积/mL | 溶液开始变蓝的时间/s | ||||
  |   |   |  KI(含淀粉) |  | ||
| I | 40 | 40 | 20 | 40 | 20 |  |
| II | V1 | 20 | 20 | 40 | V2 |  |
②对比实验I和实验II,

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)利用实验I的数据,计算反应ⅱ在
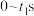 的化学反应速率
的化学反应速率
 ;反应ⅰ在
;反应ⅰ在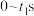 的化学反应速率
的化学反应速率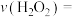

您最近半年使用:0次
2022-07-14更新
|
1227次组卷
|
5卷引用:山东省菏泽市2021-2022学年高一下学期期末教学质量检测化学试题
名校
8 . 雾霾严重危害人类健康和生态环境,开发稳定高效的脱硫脱硝工艺是当前国内外研究的热点。
(1)天然气中含有的微量H2S会腐蚀管道和设备,在1200℃下进行脱硫处理,H2S会被氧气氧化为SO2,并产生水蒸气。
请写出该条件下反应的热化学方程式:_______ 。
(2)已知物质的氧化性或还原性强弱与溶液的pH有关。利用 NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝,将NO、SO2氧化为硝酸和硫酸而除去。在温度一定时, 、溶液pH对脱硫脱硝的影响如图所示:
、溶液pH对脱硫脱硝的影响如图所示:
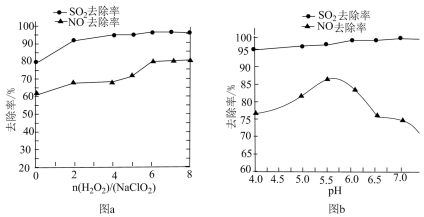
①从图a和图b中可知脱硫脱硝最佳 是
是_______ 、最佳pH是_______ 。
②图b中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因_______ 。
(3)臭氧也是理想的烟气脱硝剂,其脱硝的反应之一为 2NO2(g)+O3(g) N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
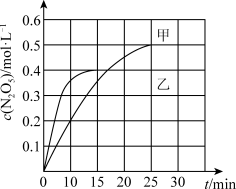
0~10 min内甲容器中反应的平均速率:v(NO2)=_______ mol·L-1·min-1
(1)天然气中含有的微量H2S会腐蚀管道和设备,在1200℃下进行脱硫处理,H2S会被氧气氧化为SO2,并产生水蒸气。
| 化学键 | H-S | O=O | H-O | SO2中共价键 |
| 键能/(kJ▪mol-1) | 339 | 498 | 464 | 1083 |
请写出该条件下反应的热化学方程式:
(2)已知物质的氧化性或还原性强弱与溶液的pH有关。利用 NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝,将NO、SO2氧化为硝酸和硫酸而除去。在温度一定时,
 、溶液pH对脱硫脱硝的影响如图所示:
、溶液pH对脱硫脱硝的影响如图所示:
①从图a和图b中可知脱硫脱硝最佳
 是
是②图b中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因
(3)臭氧也是理想的烟气脱硝剂,其脱硝的反应之一为 2NO2(g)+O3(g)
 N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
N2O5(g)+O2(g),不同温度下,在体积为1 L的甲、乙两个恒容密闭容器中均充入l mol O3和2 mol NO2,相关信息如下图所示,请回答下列问题:
0~10 min内甲容器中反应的平均速率:v(NO2)=
您最近半年使用:0次
名校
9 . 完成下列问题。
(1)为了证明Ag+能将Fe2+氧化为Fe3+,某同学设计了如下图所示装置:
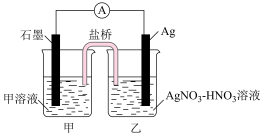
①其中甲溶液是_______ 。
②Ag电极为该电池的______ 极(填“阴或阳”或者“正或负”)
③该电池的总反应方程式为________ 。
(2)铵盐是一种重要的水体污染物。某课题组利用电解法,在含Cl-的水样中,探究将 转化为N2而脱氮的影响因素和反应机理。电解法脱氮的原理可能如下:
转化为N2而脱氮的影响因素和反应机理。电解法脱氮的原理可能如下:
①直接电氧化
在碱性条件下,阳极的电极反应式为______ 。
②间接电氧化
利用电解产生的Cl2,与H2O作用生成HClO进行脱氮。请写出HClO在酸性条件下氧化 的离子方程式
的离子方程式_____ 。25℃时,反应进行10min时,溶液的pH由6变为2时,其NH4+的平均反应速率为____ mol∙L−1∙min−1。
(1)为了证明Ag+能将Fe2+氧化为Fe3+,某同学设计了如下图所示装置:

①其中甲溶液是
②Ag电极为该电池的
③该电池的总反应方程式为
(2)铵盐是一种重要的水体污染物。某课题组利用电解法,在含Cl-的水样中,探究将
 转化为N2而脱氮的影响因素和反应机理。电解法脱氮的原理可能如下:
转化为N2而脱氮的影响因素和反应机理。电解法脱氮的原理可能如下:①直接电氧化
在碱性条件下,阳极的电极反应式为
②间接电氧化
利用电解产生的Cl2,与H2O作用生成HClO进行脱氮。请写出HClO在酸性条件下氧化
 的离子方程式
的离子方程式
您最近半年使用:0次
名校
解题方法
10 . Ⅰ.为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
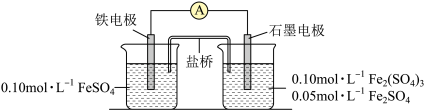
回答下列问题:
(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择_______ 作为电解质。
(2)电流表显示电子由铁电极流向石墨电极。电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L−1石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=_______ 。
(3)基于该装置的电极反应可得出以下结论因此:Fe2+氧化性小于_______ ,还原性小于_______ 。
(4)实验前需要对铁电极表面活化。在FeSO4溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是_______ 。
Ⅱ.某小组用酸性 溶液与
溶液与 溶液反应过程中溶液紫色消失快慢的方法,研究影响化学反应速率的因素。实验条件作如下表限定:每次实验中酸性
溶液反应过程中溶液紫色消失快慢的方法,研究影响化学反应速率的因素。实验条件作如下表限定:每次实验中酸性 溶液、
溶液、 溶液
溶液 的用量均为
的用量均为 。
。
(5)写出反应的离子方程式:_______ 。
(6)请完成以下实验设计表:完成iv的实验条件,并将实验目的补充完整 。
(7)某同学对实验 分别进行了3次实验,测得以下数据:
分别进行了3次实验,测得以下数据:
实验ii中用酸性 溶液的浓度变化量来表示的化学反应速率为
溶液的浓度变化量来表示的化学反应速率为_______ 。

回答下列问题:
(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择
| 阳离子 | u∞×108/(m2·s−1·V−1) | 阴离子 | u∞×108/(m2·s−1·V−1) |
| Li+ | 4.07 | HCO3- | 4.61 |
| Na+ | 5.19 | NO3- | 7.40 |
| Ca2+ | 6.59 | Cl− | 7.91 |
| K+ | 7.62 | SO42- | 8.27 |
(3)基于该装置的电极反应可得出以下结论因此:Fe2+氧化性小于
(4)实验前需要对铁电极表面活化。在FeSO4溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是
Ⅱ.某小组用酸性
 溶液与
溶液与 溶液反应过程中溶液紫色消失快慢的方法,研究影响化学反应速率的因素。实验条件作如下表限定:每次实验中酸性
溶液反应过程中溶液紫色消失快慢的方法,研究影响化学反应速率的因素。实验条件作如下表限定:每次实验中酸性 溶液、
溶液、 溶液
溶液 的用量均为
的用量均为 。
。(5)写出反应的离子方程式:
(6)请完成以下实验设计表:完成iv的实验条件,并将
| 实验编号 | 温度/K | 酸性 溶液的浓度 溶液的浓度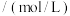 | 催化剂的用量 | 实验目的 |
| i | 298 | 0.01 | 0.5 | a.实验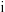 和 和 探究酸性 探究酸性 溶液的浓度对该反应速率的影响; 溶液的浓度对该反应速率的影响;b.实验 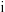 和 和 探究② 探究②c.实验 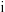 和 和 探究催化剂对该反应速率的影响 探究催化剂对该反应速率的影响 |
| ii | 298 | 0.001 | 0.5 | |
| iii | 323 | 0.01 | 0.5 | |
| iv | ① 填写实验条件 填写实验条件 | |||
 分别进行了3次实验,测得以下数据:
分别进行了3次实验,测得以下数据:| 实验编号 | 溶液褪色所需时间 | ||
| 第1次 | 第2次 | 第3次 | |
| ii | 4.9 | 5.1 | 5.0 |
 溶液的浓度变化量来表示的化学反应速率为
溶液的浓度变化量来表示的化学反应速率为
您最近半年使用:0次