1 . Ⅰ.某探究性学习小组利用 溶液和酸性
溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
(1)通过实验A、B可探究___________ (填外部因素)的改变对反应速率的影响,其中
___________ ;
___________ ;通过实验___________ 可探究温度变化对化学反应速率的影响。
(2)若 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是___________ ;利用实验B中数据计算,用 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为___________ mol/(L·min)。
Ⅱ.在2L密闭容器中进行反应:mX(g)+nY(g)=pZ(g)+qQ(g),式中 为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:
为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:
已知2min内v(Q)=0.3mol·L−1·min−1,v (Z):v (Y)=2:3。
(3)化学方程式中m=___________ ,n=___________ ,p=___________ ,q=___________ 。
 溶液和酸性
溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。| 实验序号 | 实验温度/K |  溶液(含硫酸) 溶液(含硫酸) |  溶液 溶液 |  | 溶液颜色褪至无色时所需时间/s | ||
 | 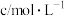 |  | 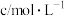 |  | |||
| A | 293 | 2 | 0.02 | 5 | 0.1 | 5 |  |
| B |  | 2 | 0.02 | 4 | 0.1 |  | 8 |
| C | 313 | 2 | 0.02 |  | 0.1 | 6 |  |


(2)若
 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为Ⅱ.在2L密闭容器中进行反应:mX(g)+nY(g)=pZ(g)+qQ(g),式中
 为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:
为化学计量数。在0~3min内,各物质物质的量的变化如下表所示:| X | Y | Z | Q | |
| 起始/mol | 1.2 | 0 | ||
| 2min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3min末/mol | 0.8 |
(3)化学方程式中m=
您最近一年使用:0次
2 . 某温度下,加入一定量的X和Y在溶液中发生反应: ,X、Z的消耗速率与其本身在体系中物质的量浓度关系如图,已知:v消耗(X)=k1c(X),v消耗(Z)=k2c2(Z),k1和k2是速率常数,下列说法正确的是
,X、Z的消耗速率与其本身在体系中物质的量浓度关系如图,已知:v消耗(X)=k1c(X),v消耗(Z)=k2c2(Z),k1和k2是速率常数,下列说法正确的是

 ,X、Z的消耗速率与其本身在体系中物质的量浓度关系如图,已知:v消耗(X)=k1c(X),v消耗(Z)=k2c2(Z),k1和k2是速率常数,下列说法正确的是
,X、Z的消耗速率与其本身在体系中物质的量浓度关系如图,已知:v消耗(X)=k1c(X),v消耗(Z)=k2c2(Z),k1和k2是速率常数,下列说法正确的是
| A.P点时,该反应达到平衡状态 |
B.该反应的平衡常数 |
C.若tmin时,体系中 ,则0~tmin内用X表示的平均反应速率 ,则0~tmin内用X表示的平均反应速率 |
D.X和Z均为c1 时,向溶液中加入少量Y(溶液体积不变),平衡时 时,向溶液中加入少量Y(溶液体积不变),平衡时 |
您最近一年使用:0次
3 . 在恒温恒容密闭容器中充入一定量W(g),发生如下反应:

反应②和③的速率方程分别为 和
和 ,其中
,其中 、
、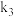 分别为反应②和③的速率常数、反应③的活化能大于反应②,测得W(g)的浓度随时间的变化如下表:
分别为反应②和③的速率常数、反应③的活化能大于反应②,测得W(g)的浓度随时间的变化如下表:
下列说法正确的是

反应②和③的速率方程分别为
 和
和 ,其中
,其中 、
、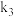 分别为反应②和③的速率常数、反应③的活化能大于反应②,测得W(g)的浓度随时间的变化如下表:
分别为反应②和③的速率常数、反应③的活化能大于反应②,测得W(g)的浓度随时间的变化如下表:| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0.160 | 0.113 | 0.080 | 0.056 | 0.040 | 0.028 |
A. 内,W的平均反应速率为 内,W的平均反应速率为 |
B.若升高温度,平衡时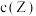 减小 减小 |
C.若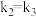 ,平衡时 ,平衡时 |
| D.若增大容器容积,平衡时Y的产率增大 |
您最近一年使用:0次
名校
4 . 臭氧是理想的烟气脱硝剂,其脱硝反应为: ,反应在恒容密闭容器中进行,下列由该反应相关图象作出的判断正确的是
,反应在恒容密闭容器中进行,下列由该反应相关图象作出的判断正确的是
 ,反应在恒容密闭容器中进行,下列由该反应相关图象作出的判断正确的是
,反应在恒容密闭容器中进行,下列由该反应相关图象作出的判断正确的是| A | B | C | D |
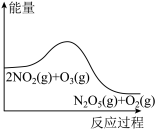 |  | 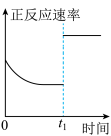 | 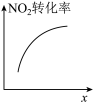 |
| 降低温度,平衡常数变大 |  内,反应速率为 内,反应速率为 |  时仅加入催化剂,平衡向正方向移动 时仅加入催化剂,平衡向正方向移动 | 达平衡时,仅改变x,则x为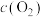 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 2023年7月1日我国开始实施汽车尾气排放“国六b”标准,研究汽车尾气中 等污染物的转化对环境保护具有重要意义。一种脱硝方法是利用
等污染物的转化对环境保护具有重要意义。一种脱硝方法是利用 将
将 氧化为高价态氮氧化物
氧化为高价态氮氧化物 反应机理如下:
反应机理如下:
ⅰ)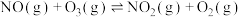
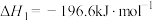
ⅱ)

(1)已知反应ⅱ的逆反应活化能为 ,则其正反应的活化能为
,则其正反应的活化能为___________  。
。
(2)在一恒温恒容的容器中发生上述反应ⅰ、ⅱ,若降低 的浓度,
的浓度, 的转化率
的转化率___________ (填“增大”、“减小”或“不变”);保持恒温恒容,下列描述不能说明反应已达到平衡的是___________ 。
A.
B.容器中气体的平均相对分子质量不随时间变化
C.某时刻容器中 与
与 的物质的量之比为
的物质的量之比为
D.容器中气体的总压强不随时间而变化
(3)将 、
、 充入恒容密闭容器中,起始时浓度均为
充入恒容密闭容器中,起始时浓度均为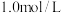 ,下图是温度为
,下图是温度为 、
、 时,
时,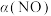 随时间变化图。
随时间变化图。 温度下,
温度下, ,反应的平均速率
,反应的平均速率
___________ 。若只发生反应ⅰ,反应速率 ,其中
,其中 、
、 只与温度及活化能有关,若加入正催化剂,
只与温度及活化能有关,若加入正催化剂, 和
和 均
均___________ (填“变大”、“变小”或“不变”)。M点与N点对应的 的大小关系:M
的大小关系:M___________ N(填“>”、“<”或“=”),N点时
___________ 。

(4)用惰性电极电解食盐水对烟气脱氮,将含NO的烟气通入电解池,其中NO被阳极产生的 氧化为
氧化为 ,则电解池中发生的总的离子反应方程式为
,则电解池中发生的总的离子反应方程式为___________ 。
 等污染物的转化对环境保护具有重要意义。一种脱硝方法是利用
等污染物的转化对环境保护具有重要意义。一种脱硝方法是利用 将
将 氧化为高价态氮氧化物
氧化为高价态氮氧化物 反应机理如下:
反应机理如下:ⅰ)
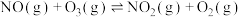
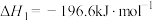
ⅱ)


(1)已知反应ⅱ的逆反应活化能为
 ,则其正反应的活化能为
,则其正反应的活化能为 。
。(2)在一恒温恒容的容器中发生上述反应ⅰ、ⅱ,若降低
 的浓度,
的浓度, 的转化率
的转化率A.

B.容器中气体的平均相对分子质量不随时间变化
C.某时刻容器中
 与
与 的物质的量之比为
的物质的量之比为
D.容器中气体的总压强不随时间而变化
(3)将
 、
、 充入恒容密闭容器中,起始时浓度均为
充入恒容密闭容器中,起始时浓度均为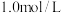 ,下图是温度为
,下图是温度为 、
、 时,
时,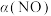 随时间变化图。
随时间变化图。 温度下,
温度下, ,反应的平均速率
,反应的平均速率
 ,其中
,其中 、
、 只与温度及活化能有关,若加入正催化剂,
只与温度及活化能有关,若加入正催化剂, 和
和 均
均 的大小关系:M
的大小关系:M

(4)用惰性电极电解食盐水对烟气脱氮,将含NO的烟气通入电解池,其中NO被阳极产生的
 氧化为
氧化为 ,则电解池中发生的总的离子反应方程式为
,则电解池中发生的总的离子反应方程式为
您最近一年使用:0次
解题方法
6 . 我国力争2030年前实现碳达峰, 的捕集、利用已成为科学家研究的热点。
的捕集、利用已成为科学家研究的热点。 在固体催化剂表面加氢合成甲烷过程中发生如下反应:
在固体催化剂表面加氢合成甲烷过程中发生如下反应:
主反应Ⅰ:
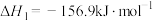
副反应Ⅱ:

(1) 的
的
___________  ,从化学平衡移动的角度分析,为了提高甲烷的产率,反应适宜在
,从化学平衡移动的角度分析,为了提高甲烷的产率,反应适宜在___________ 条件下进行。
A.低温、低压 B.低温、高压 C.高温、高压 D.高温、低压
(2)若在恒容绝热的容器中只发生副反应Ⅱ,下列能说明该反应一定达到平衡状态的是___________。
(3)在一定条件下,在某催化剂作用下,向恒容密闭容器中充入一定量的 和
和 ,若只发生主反应Ⅰ,测得在相同时间内,不同温度下
,若只发生主反应Ⅰ,测得在相同时间内,不同温度下 的转化率如图所示,已知
的转化率如图所示,已知 时已达平衡状态。
时已达平衡状态。
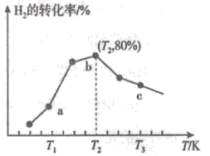
①a点
___________ 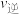 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
②c点的转化率比b点低的原因是___________ ;
③温度为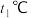 时,将等物质的量的
时,将等物质的量的 和
和 充入体积为1L的密闭容器中,若只发生主反应Ⅰ,该反应的平衡常数K=2.实验测得:
充入体积为1L的密闭容器中,若只发生主反应Ⅰ,该反应的平衡常数K=2.实验测得: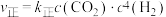 、
、 ,
, 、
、 为速率常数。温度为
为速率常数。温度为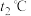 ,达平衡时:
,达平衡时: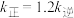 ,则
,则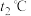
___________ (填“>”、“<”或“=”)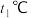 。
。
(4)500℃时,向IL恒容密闭容器中充入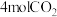 和
和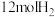 ,初始压强为p,20min时主、副反应都达到平衡状态,测得
,初始压强为p,20min时主、副反应都达到平衡状态,测得 ,体系压强为
,体系压强为 ,则0~20min内
,则0~20min内
___________  ;500℃,副反应Ⅱ的压强平衡常数Kp=
;500℃,副反应Ⅱ的压强平衡常数Kp=___________ (用平衡分压代替平衡浓度来计算,分压=总压×物质的量分数,计算结果保留2位有效数字)。
 的捕集、利用已成为科学家研究的热点。
的捕集、利用已成为科学家研究的热点。 在固体催化剂表面加氢合成甲烷过程中发生如下反应:
在固体催化剂表面加氢合成甲烷过程中发生如下反应:主反应Ⅰ:

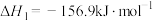
副反应Ⅱ:


(1)
 的
的
 ,从化学平衡移动的角度分析,为了提高甲烷的产率,反应适宜在
,从化学平衡移动的角度分析,为了提高甲烷的产率,反应适宜在A.低温、低压 B.低温、高压 C.高温、高压 D.高温、低压
(2)若在恒容绝热的容器中只发生副反应Ⅱ,下列能说明该反应一定达到平衡状态的是___________。
| A.容器内气体密度不再改变 |
| B.容器内的压强不再改变 |
C.容器内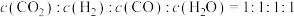 |
| D.单位时间内,断开H-H键的数目和断开H-O键的数目之比为1∶2 |
 和
和 ,若只发生主反应Ⅰ,测得在相同时间内,不同温度下
,若只发生主反应Ⅰ,测得在相同时间内,不同温度下 的转化率如图所示,已知
的转化率如图所示,已知 时已达平衡状态。
时已达平衡状态。
①a点

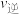 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);②c点的转化率比b点低的原因是
③温度为
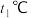 时,将等物质的量的
时,将等物质的量的 和
和 充入体积为1L的密闭容器中,若只发生主反应Ⅰ,该反应的平衡常数K=2.实验测得:
充入体积为1L的密闭容器中,若只发生主反应Ⅰ,该反应的平衡常数K=2.实验测得: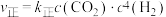 、
、 ,
, 、
、 为速率常数。温度为
为速率常数。温度为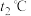 ,达平衡时:
,达平衡时: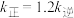 ,则
,则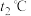
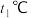 。
。(4)500℃时,向IL恒容密闭容器中充入
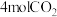 和
和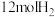 ,初始压强为p,20min时主、副反应都达到平衡状态,测得
,初始压强为p,20min时主、副反应都达到平衡状态,测得 ,体系压强为
,体系压强为 ,则0~20min内
,则0~20min内
 ;500℃,副反应Ⅱ的压强平衡常数Kp=
;500℃,副反应Ⅱ的压强平衡常数Kp=
您最近一年使用:0次
解题方法
7 . 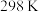 时,测得溶液中反应
时,测得溶液中反应 在不同浓度时的速率如下表所示:
在不同浓度时的速率如下表所示:
下列说法正确的是
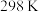 时,测得溶液中反应
时,测得溶液中反应 在不同浓度时的速率如下表所示:
在不同浓度时的速率如下表所示:| 实验编号 | 1 | 2 | 3 | 4 | 5 |
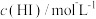 | 0.100 | 0.200 | 0.300 | 0.100 | 0.100 |
 | 0.100 | 0.100 | 0.100 | 0.200 | 0.300 |
 | 0.00760 | 0.0153 | 0.0227 | 0.0151 | 0.0228 |
A.该反应的速率方程可表示为 |
B.反应开始后的某一时刻存在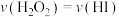 |
C.反应速率常数 与浓度有关 与浓度有关 |
D.温度越高,该反应的反应速率常数 越大 越大 |
您最近一年使用:0次
解题方法
8 . 氮及其化合物在工农业生产、生活中有着重要作用。合成氨工业中:化学平衡常数K与温度t的关系如表,已知:
(1)试比较 、
、 的大小,
的大小,
___________  (填写“>”、“=”或“<”)
(填写“>”、“=”或“<”)
(2) 时当测得
时当测得 和
和 、
、 的物质的量浓度分别为
的物质的量浓度分别为 和
和 、
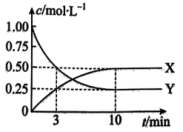
、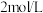 时,则该反应
时,则该反应
____________  (填写“>”、“=”或“<”)
(填写“>”、“=”或“<”)
(3)在恒温恒容的密闭容器中,下列能作为合成氨反应达到平衡的依据的是______________ 。
a.
b.容器内密度保持不变
c.混合气体的压强保持不变
d. 断裂时有
断裂时有 生成
生成
e. 、
、 、
、 的浓度之比为
的浓度之比为
(4)将 和
和 充入到
充入到 的恒容密闭容器中模拟合成氨反应。反应中某些物质浓度随时间变化的曲线如图所示。
的恒容密闭容器中模拟合成氨反应。反应中某些物质浓度随时间变化的曲线如图所示。
①曲线Y表示___________ (填写“ ”、“
”、“ ”或“
”或“ ”)的物质的量浓度随时间变化。
”)的物质的量浓度随时间变化。
② 内,氢气的反应速率为
内,氢气的反应速率为_____________ (保留2位有效数字)。
③平衡时氮气的转化率
_______________ 。
(5)如图是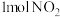 和
和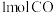 反应生成
反应生成 和
和 过程中能量变化示意图,请写出
过程中能量变化示意图,请写出 和
和 反应的热化学方程式
反应的热化学方程式________________________________ 。


| 600 | 500 | 400 |
K |
|
| 0.5 |
(1)试比较
 、
、 的大小,
的大小,
 (填写“>”、“=”或“<”)
(填写“>”、“=”或“<”)(2)
 时当测得
时当测得 和
和 、
、 的物质的量浓度分别为
的物质的量浓度分别为 和
和 、
、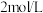 时,则该反应
时,则该反应
 (填写“>”、“=”或“<”)
(填写“>”、“=”或“<”)(3)在恒温恒容的密闭容器中,下列能作为合成氨反应达到平衡的依据的是
a.

b.容器内密度保持不变
c.混合气体的压强保持不变
d.
 断裂时有
断裂时有 生成
生成e.
 、
、 、
、 的浓度之比为
的浓度之比为
(4)将
 和
和 充入到
充入到 的恒容密闭容器中模拟合成氨反应。反应中某些物质浓度随时间变化的曲线如图所示。
的恒容密闭容器中模拟合成氨反应。反应中某些物质浓度随时间变化的曲线如图所示。
①曲线Y表示
 ”、“
”、“ ”或“
”或“ ”)的物质的量浓度随时间变化。
”)的物质的量浓度随时间变化。②
 内,氢气的反应速率为
内,氢气的反应速率为③平衡时氮气的转化率

(5)如图是
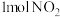 和
和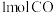 反应生成
反应生成 和
和 过程中能量变化示意图,请写出
过程中能量变化示意图,请写出 和
和 反应的热化学方程式
反应的热化学方程式
您最近一年使用:0次
解题方法
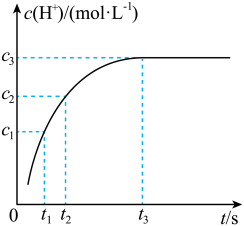
9 . 稀土被称为新材料的宝库。稀土中的镧系离于可用离子交换法分离,其反应可表示为: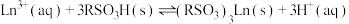 。某温度时,
。某温度时, 随时间变化关系如图所示。下列说法正确的是
随时间变化关系如图所示。下列说法正确的是
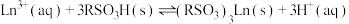 。某温度时,
。某温度时, 随时间变化关系如图所示。下列说法正确的是
随时间变化关系如图所示。下列说法正确的是
A. 时的正反应速率大于 时的正反应速率大于 时的逆反应速率 时的逆反应速率 |
B. 时间段的平均反应速率为: 时间段的平均反应速率为: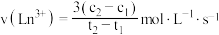 |
C. 时增大 时增大 ,该平衡左移,平衡常数减小 ,该平衡左移,平衡常数减小 |
D. 时离子交换反应停止 时离子交换反应停止 |
您最近一年使用:0次
2024-01-22更新
|
807次组卷
|
6卷引用:江西省宜春市丰城市第九中学2023-2024学年高三(复读班)上学期期末考试化学试题
江西省宜春市丰城市第九中学2023-2024学年高三(复读班)上学期期末考试化学试题2024年1月安徽普通高等学校招生考试适应性测试化学试题(已下线)选择题6-10(已下线)2024年1月“九省联考”安徽真题完全解读与考后提升(已下线)热点13 化学反应速率与化学平衡(已下线)专题06 化学反应速率与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
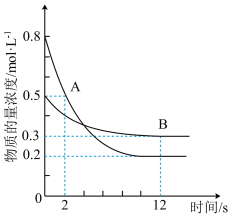
10 . 某温度下,在容积为2 L的密闭容器中投入一定量的A、B发生反应3A(g)+bB(g) cC(g) ΔH=-Q kJ·mol-1(Q>0),12 s时反应达到平衡,生成C的物质的量为0.8 mol,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是
cC(g) ΔH=-Q kJ·mol-1(Q>0),12 s时反应达到平衡,生成C的物质的量为0.8 mol,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是
 cC(g) ΔH=-Q kJ·mol-1(Q>0),12 s时反应达到平衡,生成C的物质的量为0.8 mol,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是
cC(g) ΔH=-Q kJ·mol-1(Q>0),12 s时反应达到平衡,生成C的物质的量为0.8 mol,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是
| A.前12 s内,A的平均反应速率为0.025 mol·L-1·s-1 |
| B.12 s后,A的消耗速率等于B的生成速率 |
| C.化学计量数之比b:c=1:4 |
| D.12 s内,A和B反应放出的热量为0.4Q kJ |
您最近一年使用:0次
2024-01-08更新
|
172次组卷
|
3卷引用:江西省宜春市丰城中学2023-2024学年高二上学期1月期末考试化学试题




