解题方法
1 . 采用可再生的生物质原料生产乙醇,再脱水制乙烯的技术是调整能源结构、减少环境污染、促进国民经济的重要途径之一、一定温度下,在某密闭容器中进行乙醇脱水制乙烯的反应: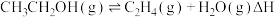 ,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是
,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是
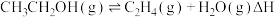 ,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是
,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是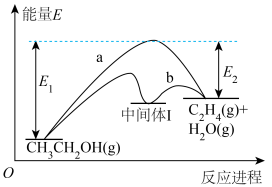
A.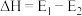 |
B.在 路径中,乙醇 路径中,乙醇 中间体Ⅰ为反应的决速步骤 中间体Ⅰ为反应的决速步骤 |
C.b路径的反应速率大于 路径的 路径的 |
D.反应达到平衡后, 路径中 路径中 的产率比 的产率比 路径的高 路径的高 |
您最近一年使用:0次
名校
解题方法
2 . 汽车尾气中含NO等有毒气体,活性炭处理尾气的方法: 。其他条件不变,只改变一个条件,不能使该反应中生成氮气的速率增大的是
。其他条件不变,只改变一个条件,不能使该反应中生成氮气的速率增大的是
 。其他条件不变,只改变一个条件,不能使该反应中生成氮气的速率增大的是
。其他条件不变,只改变一个条件,不能使该反应中生成氮气的速率增大的是| A.升高温度 | B.减小容器容积 |
| C.恒容时充入Ne | D.使用合适的催化剂 |
您最近一年使用:0次
名校
解题方法
3 . 汽车尾气处理的反应为2NO(g)+2CO(g) N2(g)+2CO2(g) △H=-746kJ•mol-1。下列说法正确的是
N2(g)+2CO2(g) △H=-746kJ•mol-1。下列说法正确的是
 N2(g)+2CO2(g) △H=-746kJ•mol-1。下列说法正确的是
N2(g)+2CO2(g) △H=-746kJ•mol-1。下列说法正确的是| A.升高温度可使v正增大、v逆减小 |
| B.使用高效催化剂可以提高活化分子的百分含量 |
| C.反应达到化学平衡状态时,2v正(NO)=v逆(N2) |
| D.CO和CO2的物质的量相等时,反应达到化学平衡状态 |
您最近一年使用:0次
2023-02-23更新
|
219次组卷
|
3卷引用:四川省雅安市2022-2023学年高二上学期期末考试化学试题
四川省雅安市2022-2023学年高二上学期期末考试化学试题(已下线)第04讲 化学平衡状态 化学平衡常数-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)江西省宜春市宜丰中学2023-2024学年高二上学期9月月考化学试题
解题方法
4 . 下列事实或做法的目的是加快化学反应速率的是
| A.谷物酿酒时加入酒曲酶 | B.铁制品表面刷油漆 |
| C.茶叶使用真空包装 | D.肉类食品在低温冷藏 |
您最近一年使用:0次
名校
解题方法
5 . 日常生活中的下列做法不是为了加快化学反应速率的是
| A.清洗水壶垢用较浓白醋 | B.将煤块粉碎后燃烧 |
| C.发馒头加酵母粉 | D.月饼盒内放置还原性铁粉 |
您最近一年使用:0次
2021-01-28更新
|
548次组卷
|
8卷引用:四川省雅安市2021-2022学年高二上学期期末检测化学试题
名校
解题方法
6 . 下列关于化学反应速率及化学平衡的说法,正确的是( )
| A.升高温度能增大单位体积内活化分子数目,加快反应速率 |
| B.增大反应物浓度,可增大活化分子的百分数,因而反应速率加快 |
| C.化学反应条件改变,已处于化学平衡的可逆反应一定发生平衡移动 |
| D.催化剂可以提高化学反应的选择性,进而提高反应物的平衡转化率 |
您最近一年使用:0次
2020-10-28更新
|
478次组卷
|
6卷引用:四川省荥经中学2023-2024学年高二上学期期中考试化学试题
四川省荥经中学2023-2024学年高二上学期期中考试化学试题四川省成都市第七中学2020-2021学年高二上学期十月阶段性考试化学试题四川省成都外国语学校2021-2022学年高二上学期10月月考化学试题广西百色中学2021-2022学年高二上学期第一次月考化学试题四川省遂宁中学校2020-2021学年高二上学期第二次月考化学试题(已下线)专题10 化学反应速率与平衡-2023年高考化学一轮复习小题多维练(全国通用)
名校
解题方法
7 . 下列条件一定能使反应速率加快的是( )
①增加反应物物质的量 ②升高温度 ③缩小反应容器的体积 ④加入生成物 ⑤加入MnO2
①增加反应物物质的量 ②升高温度 ③缩小反应容器的体积 ④加入生成物 ⑤加入MnO2
| A.①②③ | B.③ | C.② | D.②③ |
您最近一年使用:0次
名校
8 . 我国有较多的科研人员在研究甲醛的氧化,有人提出HCHO( )与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程示意图如图(图中只画出了HAP的部分结构)。
)与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程示意图如图(图中只画出了HAP的部分结构)。
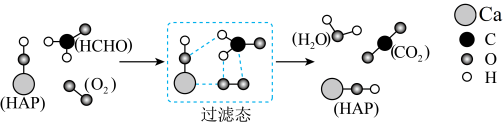
| A.该反应的氧化产物是CO2 |
| B.HCHO在反应过程中有C=O键发生断裂 |
| C.根据图示信息,CO2分子中的氧原子全部来自O2 |
| D.HAP能提高HCHO与O2应的活化能,但不改变反应路径 |
您最近一年使用:0次
2020-06-08更新
|
516次组卷
|
8卷引用:四川省雅安市天立学校2022-2023学年高二下学期6月月考化学试题
9 . 对某一可逆反应来说,使用催化剂的作用是( )
| A.提高反应物的平衡转化率 | B.以同样程度改变正、逆反应速率 |
| C.增大反应的活化能 | D.改变平衡混合物的组成 |
您最近一年使用:0次
13-14高一下·四川雅安·期中
名校
解题方法
10 . 影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1)设计实验方案来研究影响化学反应速率的因素。甲同学的实验报告如下表:
(1)甲同学表中实验步骤②为_________________________________________ 。
(2)甲同学的实验目的是_____________ ;要得出正确的实验结论,还需控制的实验条件是____________ 。乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验。
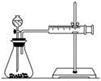
(3)乙同学在实验中应该测定的数据是___________________________________________________ 。
(4)乙同学完成该实验应选用的实验药品是________ ,该实验中不选用某浓度的硫酸,理由是___________ 。
实验二:已知 2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(5)针对上述实验现象,丙同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是______________ 的影响。
(6)若用实验证明你的猜想,除高锰酸钾酸性溶液、草酸溶液外,还需要选择的试剂最合理的是________ (填字母)。
A.硫酸钾 B.硫酸锰 C.二氯化锰 D.水
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1)设计实验方案来研究影响化学反应速率的因素。甲同学的实验报告如下表:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2 mol·L-1的硫酸于试管中 | 反应速率Mg>Fe,Cu不反应 | 金属的性质越活泼,反应速率越快 |
| ②____________ | 反应物浓度越大,反应速率越快 |
(1)甲同学表中实验步骤②为
(2)甲同学的实验目的是

(3)乙同学在实验中应该测定的数据是
(4)乙同学完成该实验应选用的实验药品是
实验二:已知 2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(5)针对上述实验现象,丙同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是
(6)若用实验证明你的猜想,除高锰酸钾酸性溶液、草酸溶液外,还需要选择的试剂最合理的是
A.硫酸钾 B.硫酸锰 C.二氯化锰 D.水
您最近一年使用:0次
2016-12-09更新
|
1625次组卷
|
8卷引用:2013-2014四川省雅安中学下学期期中考试高一化学试卷
(已下线)2013-2014四川省雅安中学下学期期中考试高一化学试卷(已下线)2013-2014重庆市重庆一中下学期期中考试高二化学试卷新疆阿勒泰地区2019-2020学年高一下学期期末考试化学(B)试题(已下线)第15讲 化学反应速率-2021年高考化学一轮复习名师精讲练(已下线)第二章 化学反应速率和化学平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)内蒙古包头市第一中学2020-2021学年高二上学期第一次月考化学试题江苏省海安市2020-2021学年高二上学期期中考试化学试题江西省丰城市第九中学2021-2022学年高二上学期期中考试(日新班)化学试题



