名校
解题方法
1 . 阅读题目,回答问题:
(1)FeCl3常用于腐蚀印刷电路铜板,若将此反应设计成原电池,请写出该原电池正极电极反应为___________ 。
(2)为探究 在
在 制取
制取 反应中的作用,某兴趣小组进行下列实验:向试管中加入
反应中的作用,某兴趣小组进行下列实验:向试管中加入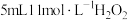 溶液,静置几分钟,无明显现象;滴加2滴
溶液,静置几分钟,无明显现象;滴加2滴 溶液,立即产生大量气泡,加
溶液,立即产生大量气泡,加 溶液反应
溶液反应 后,
后, 的浓度变为
的浓度变为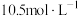 ,则20min内H2O2的平均反应速率为
,则20min内H2O2的平均反应速率为___________ 。
(3)H2O2是实验室常见的强氧化剂,在医疗上可用作消毒剂等。某兴趣小组为探究外界条件对H2O2分解反应速率的影响,设计如表所示实验。填写表中空白内容:
(4)如图装置可以把氢气中蕴含的化学能转化为电能,被称为氢氧燃料电池。
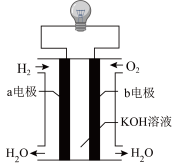
①该电池的正极是电极___________ (填“a”或“b”),负极发生反应的方程式为___________ 。
②电池工作时,当外电路中转移 电子时,消耗的
电子时,消耗的 在标准状况下体积为
在标准状况下体积为___________ 。
(1)FeCl3常用于腐蚀印刷电路铜板,若将此反应设计成原电池,请写出该原电池正极电极反应为
(2)为探究
 在
在 制取
制取 反应中的作用,某兴趣小组进行下列实验:向试管中加入
反应中的作用,某兴趣小组进行下列实验:向试管中加入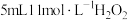 溶液,静置几分钟,无明显现象;滴加2滴
溶液,静置几分钟,无明显现象;滴加2滴 溶液,立即产生大量气泡,加
溶液,立即产生大量气泡,加 溶液反应
溶液反应 后,
后, 的浓度变为
的浓度变为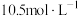 ,则20min内H2O2的平均反应速率为
,则20min内H2O2的平均反应速率为(3)H2O2是实验室常见的强氧化剂,在医疗上可用作消毒剂等。某兴趣小组为探究外界条件对H2O2分解反应速率的影响,设计如表所示实验。填写表中空白内容:
| 试管编号 | 实验目的 |  溶液 溶液 | 温度 | 水的体积/mL |  溶液体积/mL 溶液体积/mL | |
| 质量分数 | 体积/mL | |||||
| I | 为编号Ⅱ实验的参照 | 12% | 5.0 | 常温 | 0 | 0 |
| Ⅱ | 温度对反应速率的影响 | 12% | 5.0 | 60℃ | 0 | 0 |
| Ⅲ | 为编号Ⅳ实验的参照 | 4.0% | 5.0 | 常温 | ① | 0 |
| Ⅳ | ② | 4.0% | 5.0 | 常温 | 0 | 1.0 |

①该电池的正极是电极
②电池工作时,当外电路中转移
 电子时,消耗的
电子时,消耗的 在标准状况下体积为
在标准状况下体积为
您最近半年使用:0次
2023-05-16更新
|
227次组卷
|
2卷引用:广东省广州市第六十五中学2022-2023学年高一下学期期中考试化学试题
2 . 氨气广泛应用于化肥、制药、合成纤维等领域。
I.工业上可由氢气和氮气合成氨气。若用 、
、 、
、 、
、 分别表示
分别表示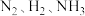 和固体催化剂,则在固体催化剂表面合成氨的过程如图所示:
和固体催化剂,则在固体催化剂表面合成氨的过程如图所示:

(1)吸附后,能量状态最高的是___________ (填序号)。
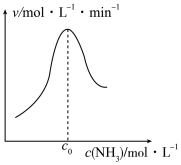
(2)结合上述过程,一定温度下在固体催化剂表面进行 的分解实验,发现
的分解实验,发现 的分解速率与其浓度的关系如图所示。从吸附和解吸过程分析,
的分解速率与其浓度的关系如图所示。从吸附和解吸过程分析,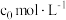 前反应速率增加的原因可能是
前反应速率增加的原因可能是___________ ;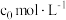 之后反应速率降低的原因可能是
之后反应速率降低的原因可能是___________ 。
II.利用 在催化剂(
在催化剂( )作用下将
)作用下将 还原为
还原为 是目前应用最为广泛的氮氧化物(
是目前应用最为广泛的氮氧化物( )净化方法,其原理是:
)净化方法,其原理是:
主板应: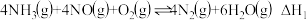
副反应: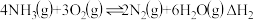
(3)根据盖斯定律可得: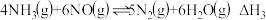
则 =
=___________ (用含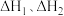 的式子表示)。
的式子表示)。
(4)催化剂 中的
中的 是活性组分。在反应器中以一定流速通过混合气
是活性组分。在反应器中以一定流速通过混合气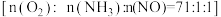 ,在不同温度下进行该催化反应,
,在不同温度下进行该催化反应, 的质量分数对单位时间内NO去除率的影响如图所示。
的质量分数对单位时间内NO去除率的影响如图所示。
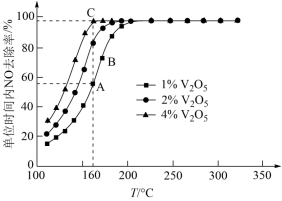
①从起始至对应A、B、C三点的平均反应速率由小到大的顺序为___________ 。
② 的质量分数对该催化剂活性的影响是
的质量分数对该催化剂活性的影响是___________ 。
(5)一定温度下,向1 L恒容密闭容器(含催化剂)中投入1 mol 和1.5 mol NO,发生反应
和1.5 mol NO,发生反应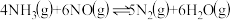 。达到平衡状态时,NO的转化率为60%,则平衡常数为
。达到平衡状态时,NO的转化率为60%,则平衡常数为___________  (列出计算式即可)。
(列出计算式即可)。
I.工业上可由氢气和氮气合成氨气。若用
 、
、 、
、 、
、 分别表示
分别表示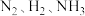 和固体催化剂,则在固体催化剂表面合成氨的过程如图所示:
和固体催化剂,则在固体催化剂表面合成氨的过程如图所示:
(1)吸附后,能量状态最高的是
(2)结合上述过程,一定温度下在固体催化剂表面进行
 的分解实验,发现
的分解实验,发现 的分解速率与其浓度的关系如图所示。从吸附和解吸过程分析,
的分解速率与其浓度的关系如图所示。从吸附和解吸过程分析,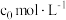 前反应速率增加的原因可能是
前反应速率增加的原因可能是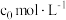 之后反应速率降低的原因可能是
之后反应速率降低的原因可能是
II.利用
 在催化剂(
在催化剂( )作用下将
)作用下将 还原为
还原为 是目前应用最为广泛的氮氧化物(
是目前应用最为广泛的氮氧化物( )净化方法,其原理是:
)净化方法,其原理是:主板应:
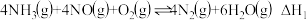
副反应:
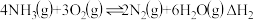
(3)根据盖斯定律可得:
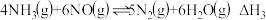
则
 =
=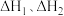 的式子表示)。
的式子表示)。(4)催化剂
 中的
中的 是活性组分。在反应器中以一定流速通过混合气
是活性组分。在反应器中以一定流速通过混合气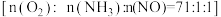 ,在不同温度下进行该催化反应,
,在不同温度下进行该催化反应, 的质量分数对单位时间内NO去除率的影响如图所示。
的质量分数对单位时间内NO去除率的影响如图所示。
①从起始至对应A、B、C三点的平均反应速率由小到大的顺序为
②
 的质量分数对该催化剂活性的影响是
的质量分数对该催化剂活性的影响是(5)一定温度下,向1 L恒容密闭容器(含催化剂)中投入1 mol
 和1.5 mol NO,发生反应
和1.5 mol NO,发生反应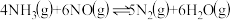 。达到平衡状态时,NO的转化率为60%,则平衡常数为
。达到平衡状态时,NO的转化率为60%,则平衡常数为 (列出计算式即可)。
(列出计算式即可)。
您最近半年使用:0次
名校
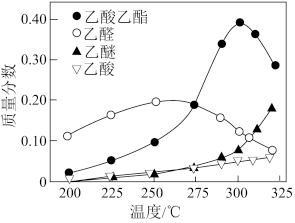
3 . 科学家研究了乙醇催化合成乙酸乙酯2C2H5OH(g) CH3COOC2H5(g)+2H2(g)的新方法。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。下列推测合理的是
CH3COOC2H5(g)+2H2(g)的新方法。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。下列推测合理的是
 CH3COOC2H5(g)+2H2(g)的新方法。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。下列推测合理的是
CH3COOC2H5(g)+2H2(g)的新方法。在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。下列推测合理的是
| A.乙醛是该反应的催化剂 |
| B.加压有利于提高乙酸乙酯的产率 |
| C.提高催化剂的活性和选择性,减少乙醚等副产物是工艺的关键 |
| D.随着温度的升高,乙酸乙酯的质量分数先增大后减小,说明该反应是吸热反应 |
您最近半年使用:0次
2023-02-22更新
|
173次组卷
|
2卷引用:广东省大湾区2022-2023学年高二上学期期末联考化学试题
4 .  的捕集和利用具有重要意义。
的捕集和利用具有重要意义。
 .
. 的催化氧化
的催化氧化
(1) 在
在 表面催化氧化的过程始于
表面催化氧化的过程始于 与
与 形成的酸性位点(如图所示),并生成金属硫酸盐(
形成的酸性位点(如图所示),并生成金属硫酸盐(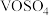 )中间体。
)中间体。___________ 。
②写出中间体受热分解产生 、
、 的化学方程式:
的化学方程式:___________ 。
(2)一定温度下,恒压密闭容器中发生反应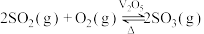
 ,
, 平衡转化率与反应温度和压强的关系如图所示。
平衡转化率与反应温度和压强的关系如图所示。
___________ (填“=0”或“>0”或“<0”)。
②实际生产中选择图中C点的反应条件,不选择A、B点的理由分别是___________ 。
 .
. 的催化还原
的催化还原
(3) 催化剂能催化CO还原
催化剂能催化CO还原 ,反应为
,反应为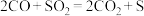 。将
。将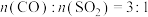 的混合气体(载气为
的混合气体(载气为 )匀速通过装有
)匀速通过装有 催化剂的反应器,测得催化剂活化(催化剂在活化过程中一般经历反应物的吸附、脱附和催化活化等阶段)前后的X-射线衍射图如下图所示(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同,峰越强,物质含量越多)。
催化剂的反应器,测得催化剂活化(催化剂在活化过程中一般经历反应物的吸附、脱附和催化活化等阶段)前后的X-射线衍射图如下图所示(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同,峰越强,物质含量越多)。___________ (填化学式)。
②谱峰4在活化前后也发生了一定变化,即部分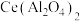 转变为
转变为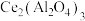 ,写出对应的化学反应方程式:
,写出对应的化学反应方程式:___________ 。
③实验中反应物的配比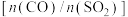 设定为3∶1而不是2∶1的可能原因是
设定为3∶1而不是2∶1的可能原因是___________ 。
 的捕集和利用具有重要意义。
的捕集和利用具有重要意义。 .
. 的催化氧化
的催化氧化(1)
 在
在 表面催化氧化的过程始于
表面催化氧化的过程始于 与
与 形成的酸性位点(如图所示),并生成金属硫酸盐(
形成的酸性位点(如图所示),并生成金属硫酸盐(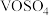 )中间体。
)中间体。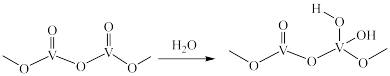
②写出中间体受热分解产生
 、
、 的化学方程式:
的化学方程式:(2)一定温度下,恒压密闭容器中发生反应
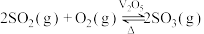
 ,
, 平衡转化率与反应温度和压强的关系如图所示。
平衡转化率与反应温度和压强的关系如图所示。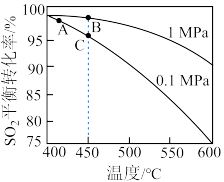

②实际生产中选择图中C点的反应条件,不选择A、B点的理由分别是
 .
. 的催化还原
的催化还原(3)
 催化剂能催化CO还原
催化剂能催化CO还原 ,反应为
,反应为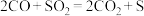 。将
。将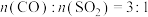 的混合气体(载气为
的混合气体(载气为 )匀速通过装有
)匀速通过装有 催化剂的反应器,测得催化剂活化(催化剂在活化过程中一般经历反应物的吸附、脱附和催化活化等阶段)前后的X-射线衍射图如下图所示(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同,峰越强,物质含量越多)。
催化剂的反应器,测得催化剂活化(催化剂在活化过程中一般经历反应物的吸附、脱附和催化活化等阶段)前后的X-射线衍射图如下图所示(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同,峰越强,物质含量越多)。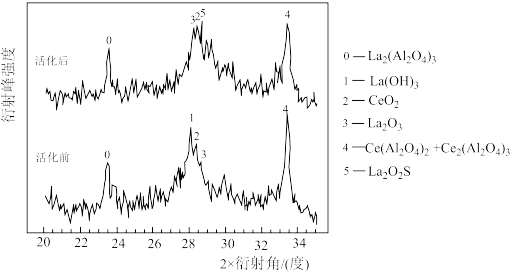
②谱峰4在活化前后也发生了一定变化,即部分
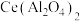 转变为
转变为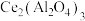 ,写出对应的化学反应方程式:
,写出对应的化学反应方程式:③实验中反应物的配比
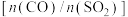 设定为3∶1而不是2∶1的可能原因是
设定为3∶1而不是2∶1的可能原因是
您最近半年使用:0次
名校
5 . 下列条件下进行反应2H2O2=2H2O+O2↑,其中反应速率最快的是
| 选项 | H2O2的质量分数 | 温度 | 催化剂 |
| A | 10% | 5℃ | MnO2 |
| B | 10% | 40℃ | |
| MnO2 | |||
| C | 20% | 5℃ | 无 |
| D | 20% | 40℃ | MnO2 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-01-10更新
|
212次组卷
|
2卷引用:2023年四川省2021级普通高中学业水平考试化学试题
名校
6 . 中国科学家以 和
和 为原料,经催化可转化为有机物,其微观反应原理如下图所示。下列说法正确的是
为原料,经催化可转化为有机物,其微观反应原理如下图所示。下列说法正确的是
 和
和 为原料,经催化可转化为有机物,其微观反应原理如下图所示。下列说法正确的是
为原料,经催化可转化为有机物,其微观反应原理如下图所示。下列说法正确的是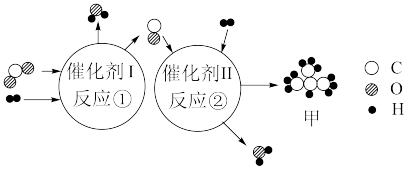
| A.反应①反应前后各元素化合价不变 |
B.反应①的化学方程式为 |
C.在反应②中,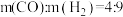 |
| D.在甲物质中,氢元素的质量分数约为17.24% |
您最近半年使用:0次
2022-09-01更新
|
224次组卷
|
3卷引用:四川省绵阳南山中学2022-2023学年高一上学期入学考试化学试题
解题方法
7 . 以某金属氧化物(用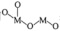 表示)为催化剂,同时消除
表示)为催化剂,同时消除 、NO污染的反应历程如图所示。下列说法错误的是
、NO污染的反应历程如图所示。下列说法错误的是
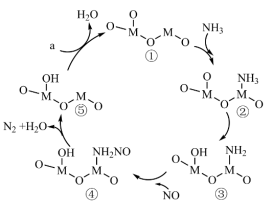
A.在相同条件下, 比NO更易与M形成配位键 比NO更易与M形成配位键 |
| B.反应历程中至少发生3个氧化还原反应 |
| C.通过定量测定发现,反应历程中物质④含量最少,其可能原因是③→④为快反应 |
D.若a为常见非金属单质,则⑤→①的反应可能为 |
您最近半年使用:0次
名校
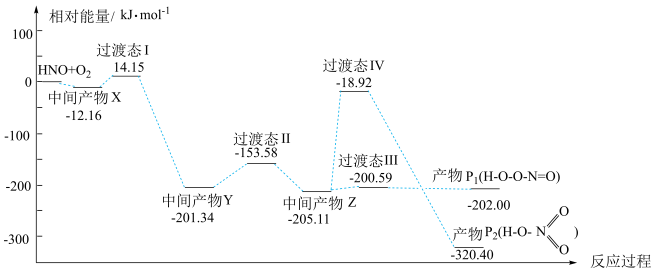
8 . 自由基是化学键断裂时产生的含未成对电子的中间体,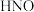 自由基与
自由基与 反应过程的能量变化如图所示。下列说法正确的是
反应过程的能量变化如图所示。下列说法正确的是
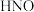 自由基与
自由基与 反应过程的能量变化如图所示。下列说法正确的是
反应过程的能量变化如图所示。下列说法正确的是
A.产物 的键能总和大于产物 的键能总和大于产物 的键能总和 的键能总和 |
B.产物 与 与 的分子式相同,但稳定性 的分子式相同,但稳定性 强于 强于 |
C.可以通过选择合适的催化剂,提高产物中 的含量 的含量 |
D.相同条件下,中间产物 转化为产物的速率: 转化为产物的速率: |
您最近半年使用:0次
9 . 某实验小组探究浓度、温度及催化剂对 分解速率的影响。回答下列问题:
分解速率的影响。回答下列问题:
(1)实验室可用过氧化钠固体与稀硫酸反应(温度不高于15℃)制取少量20% ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________ 。
(2)将上述制得的 进行实验:其中实验I与实验II是为了探究浓度对
进行实验:其中实验I与实验II是为了探究浓度对 分解反应速率的影响,实验I与实验II是为了探究温度对
分解反应速率的影响,实验I与实验II是为了探究温度对 分解反应速率的影响。
分解反应速率的影响。
填写表中缺少的内容:①___________ ,②___________ ,③___________ 。
(3)探究 ,
, 对
对 分解反应速率影响的实验设计如图所示。有同学对该实验设计提出疑问,认为不能比较
分解反应速率影响的实验设计如图所示。有同学对该实验设计提出疑问,认为不能比较 ,
, 对
对 分解反应速率的影响,提出的疑问是
分解反应速率的影响,提出的疑问是___________ ,改进办法是___________ ,改进后,判断 ,
, 对
对 分解反应速率影响的依据是
分解反应速率影响的依据是___________ (填实验现象)。

 分解速率的影响。回答下列问题:
分解速率的影响。回答下列问题:(1)实验室可用过氧化钠固体与稀硫酸反应(温度不高于15℃)制取少量20%
 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(2)将上述制得的
 进行实验:其中实验I与实验II是为了探究浓度对
进行实验:其中实验I与实验II是为了探究浓度对 分解反应速率的影响,实验I与实验II是为了探究温度对
分解反应速率的影响,实验I与实验II是为了探究温度对 分解反应速率的影响。
分解反应速率的影响。| 实验编号 |  溶液 溶液 | 温度/℃ | 水的体积/ mL | |
| 质量分数 | 体积/mL | |||
| I | 20% | 5.0 | 30 | 10.0 |
| II | 20% | ① | 30 | 5.0 |
| III | ② | ③ | 40 | 10.0 |
(3)探究
 ,
, 对
对 分解反应速率影响的实验设计如图所示。有同学对该实验设计提出疑问,认为不能比较
分解反应速率影响的实验设计如图所示。有同学对该实验设计提出疑问,认为不能比较 ,
, 对
对 分解反应速率的影响,提出的疑问是
分解反应速率的影响,提出的疑问是 ,
, 对
对 分解反应速率影响的依据是
分解反应速率影响的依据是
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
10 . 将模拟烟气(主要成分为NO、NH3、O2)匀速通过装有催化剂的反应管,NH3和NO反应机理可表示为(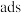 表示吸附态)。
表示吸附态)。
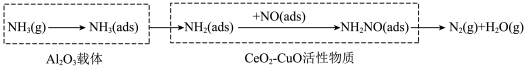
负载不同含量CeO2的催化剂对NO的脱除率随温度的变化如图所示。
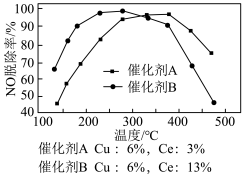
(1)130~200℃温度范围内,随着温度的升高,NO脱除率均迅速增大原因是_______ 。
(2)催化剂的催化效率与反应物在载体表面的吸附和活性物质表面的反应有关。温度高于400℃,使用催化剂B的NO脱除率明显低于催化剂A,其原因是_______ 。
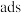 表示吸附态)。
表示吸附态)。
负载不同含量CeO2的催化剂对NO的脱除率随温度的变化如图所示。

(1)130~200℃温度范围内,随着温度的升高,NO脱除率均迅速增大原因是
(2)催化剂的催化效率与反应物在载体表面的吸附和活性物质表面的反应有关。温度高于400℃,使用催化剂B的NO脱除率明显低于催化剂A,其原因是
您最近半年使用:0次



