1 . 2022年4月16日,中国空间站的3名航天员乘神舟十三号载人飞船平安返回地球。空间站处理CO2的一种重要方法是对CO2进行收集和再生处理,重新生成可供人体呼吸的氧气。其技术路线可分为以下三步:
Ⅰ.固态胺吸收与浓缩CO2
在水蒸气存在下固态胺吸收CO2反应生成酸式碳酸盐(该反应是放热反应),再解吸出CO2的简单方法是加热。
Ⅱ.CO2的加氢甲烷化
H2还原CO2制CH4的部分反应如下:
i.CO2(g)+H2(g) CO(g)+H2O(g) △H1=+41kJ•mol-1
CO(g)+H2O(g) △H1=+41kJ•mol-1
ii.CO(g)+3H2(g) CH4(g)+H2O(g) △H2=-246kJ•mol-1
CH4(g)+H2O(g) △H2=-246kJ•mol-1
(1)反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的△H=
CH4(g)+2H2O(g)的△H=________ kJ•mol-1。
(2)向恒容绝热的密闭容器中充入amolCO与2amolH2(g),进行反应ii,下列能判断反应已达化学平衡状态的是________
a.容器中混合气体密度不变 b.混合气体中c(CH4)与c(H2O)之比不变
c.v正(H2)=3v逆(H2O) d.容器内温度不变
Ⅲ.CO2和H2合成甲烷也是CO2资源化利用的重要方法。对于上述(1)的反应CO2(g)+4H2(g) CH4(g)+2H2O(g) △H,催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如图所示:
CH4(g)+2H2O(g) △H,催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如图所示:_______ 。
(4)对比上述两种催化剂的催化性能,工业上应选择的催化剂是_______ ,使用的合适温度为_______ 。
(5)控制起始时 =4,p=1atm,恒容条件下,若只发生反应i、ii,平衡时各物质的量分数随温度的变化如图所示:
=4,p=1atm,恒容条件下,若只发生反应i、ii,平衡时各物质的量分数随温度的变化如图所示:________ (填“a”、“b”或“c”);温度低于500℃时,CO的物质的量分数约为0,说明此条件下,反应________ (填“i”或“ii”)化学平衡常数大,反应完全。
②M点(T<500℃)时,平衡分压p(CO2)=________ atm,反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的平衡常数Kp=
CH4(g)+2H2O(g)的平衡常数Kp=________ atm-2(用平衡分压代替平衡浓度计算,分压总压物质的量分数)。
Ⅰ.固态胺吸收与浓缩CO2
在水蒸气存在下固态胺吸收CO2反应生成酸式碳酸盐(该反应是放热反应),再解吸出CO2的简单方法是加热。
Ⅱ.CO2的加氢甲烷化
H2还原CO2制CH4的部分反应如下:
i.CO2(g)+H2(g)
 CO(g)+H2O(g) △H1=+41kJ•mol-1
CO(g)+H2O(g) △H1=+41kJ•mol-1ii.CO(g)+3H2(g)
 CH4(g)+H2O(g) △H2=-246kJ•mol-1
CH4(g)+H2O(g) △H2=-246kJ•mol-1(1)反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g)的△H=
CH4(g)+2H2O(g)的△H=(2)向恒容绝热的密闭容器中充入amolCO与2amolH2(g),进行反应ii,下列能判断反应已达化学平衡状态的是
a.容器中混合气体密度不变 b.混合气体中c(CH4)与c(H2O)之比不变
c.v正(H2)=3v逆(H2O) d.容器内温度不变
Ⅲ.CO2和H2合成甲烷也是CO2资源化利用的重要方法。对于上述(1)的反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H,催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如图所示:
CH4(g)+2H2O(g) △H,催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如图所示: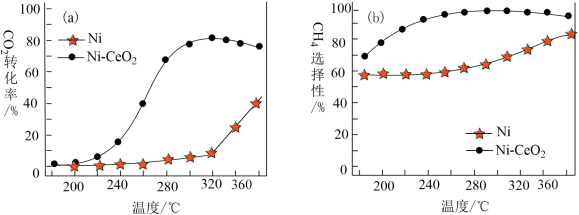
(4)对比上述两种催化剂的催化性能,工业上应选择的催化剂是
(5)控制起始时
 =4,p=1atm,恒容条件下,若只发生反应i、ii,平衡时各物质的量分数随温度的变化如图所示:
=4,p=1atm,恒容条件下,若只发生反应i、ii,平衡时各物质的量分数随温度的变化如图所示: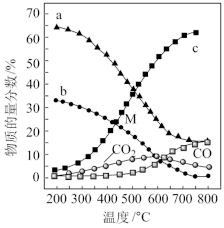
②M点(T<500℃)时,平衡分压p(CO2)=
 CH4(g)+2H2O(g)的平衡常数Kp=
CH4(g)+2H2O(g)的平衡常数Kp=
您最近一年使用:0次
2023-10-26更新
|
749次组卷
|
4卷引用:2024届江西省南昌市第十九中学高三下学期模拟预测化学试题
名校
2 . (1)2017年中科院某研究团队通过设计一种新型Na-Fe3O4/HZSM-5多功能复合催化剂,成功实现了CO2直接加氢制取辛烷值汽油,该研究成果被评价为“CO2催化转化领域的突破性进展”。
已知:H2(g)+1/2O2(g)=H2O(l) ΔH1 = -aKJ/mol
C8H18(1 )+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol
)+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol
试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方程式_________________________________ 。
(2)利用CO2及H2为原料,在合适的催化剂(如Cu/ZnO催化剂)作用下,也可合成CH3OH,涉及的反应有:
甲:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1
CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1
乙:CO2(g)+H2(g) CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2
CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2
①CO(g)+2H2(g) CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=______ (用含K1、K2的表达式表示),该反应△H_____ 0(填“大于”或“小于”)。
②提高CO2转化为CH3OH平衡转化率的措施有___________ (填写两项)。
③催化剂和反应体系的关系就像锁和钥匙的关系一样,具有高度的选择性。下列四组实验,控制CO2和H2初始投料比均为1:2.2,经过相同反应时间(t1min)。
由表格中的数据可知,相同温度下不同的催化剂对CO2的转化为CH3OH的选择性有显著影响,根据上表所给数据结合反应原理,所得最优选项为___________ (填字母符号)。
(3)以CO、H2为原料合成 甲醇的反应为:CO(g)+2H2(g)
甲醇的反应为:CO(g)+2H2(g) CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
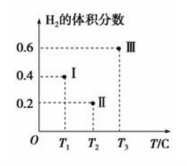
①0~5min时间内容器Ⅱ中用CH3OH表示的化学反应速率为_________________ 。
②三个容器中一定达到平衡状态的是容器________ (填写容器代号)。
已知:H2(g)+1/2O2(g)=H2O(l) ΔH1 = -aKJ/mol
C8H18(1
 )+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol
)+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方程式
(2)利用CO2及H2为原料,在合适的催化剂(如Cu/ZnO催化剂)作用下,也可合成CH3OH,涉及的反应有:
甲:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1
CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1乙:CO2(g)+H2(g)
 CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2
CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2①CO(g)+2H2(g)
 CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=②提高CO2转化为CH3OH平衡转化率的措施有
③催化剂和反应体系的关系就像锁和钥匙的关系一样,具有高度的选择性。下列四组实验,控制CO2和H2初始投料比均为1:2.2,经过相同反应时间(t1min)。
| 温度(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) | 综合选项 |
| 543 | Cu/ZnO纳米棒材料 | 12.3 | 42.3 | A |
| 543 | Cu/ZnO纳米片材料 | 11.9 | 72.7 | B |
| 553 | Cu/ZnO纳米棒材料 | 15.3 | 39.1 | C |
| 553 | Cu/ZnO纳米片材料 | 12.0 | 70.6 | D |
由表格中的数据可知,相同温度下不同的催化剂对CO2的转化为CH3OH的选择性有显著影响,根据上表所给数据结合反应原理,所得最优选项为
(3)以CO、H2为原料合成
 甲醇的反应为:CO(g)+2H2(g)
甲醇的反应为:CO(g)+2H2(g) CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
①0~5min时间内容器Ⅱ中用CH3OH表示的化学反应速率为
②三个容器中一定达到平衡状态的是容器
您最近一年使用:0次
2018-08-09更新
|
1197次组卷
|
8卷引用:江西省宜丰中学2019届高三上学期第四次月考理科综合化学试题
解题方法
3 .  减排能有效降低温室效应,同时,
减排能有效降低温室效应,同时, 也是一种重要的资源,因此研究
也是一种重要的资源,因此研究 捕集与转化对实现“碳中和”目标具有重要意义而备受关注。
捕集与转化对实现“碳中和”目标具有重要意义而备受关注。
(1)某研究机构成功合成了氮掺杂多孔有机聚合物DLU-1吸附剂,用于烟道气(主要是 和
和 )和天然气中
)和天然气中 的捕集。为考查样品对单组分气体的吸附性能,测定在1bar,273和298K下的单组分气体吸附等温线如图,请阐述DLU-1吸附剂能做捕获剂的理由:
的捕集。为考查样品对单组分气体的吸附性能,测定在1bar,273和298K下的单组分气体吸附等温线如图,请阐述DLU-1吸附剂能做捕获剂的理由:_____________ 。 和
和 反应合成二甲醚,
反应合成二甲醚,
 )
)
①恒温恒容下,充入等物质的量的 和
和 充分反应,以下叙述能说明该反应达到平衡状态的
充分反应,以下叙述能说明该反应达到平衡状态的_____________ (填序号)。
A. 的物质的量分数保持不变
的物质的量分数保持不变
B.容器中混合气体的密度保持不变
C.容器中混合气体的平均摩尔质量保持不变
D.断裂 键的同时断裂
键的同时断裂 键
键
②在某压强下,合成二甲醚的反应在不同温度、不同投料比时, 的平衡转化率如图所示,则
的平衡转化率如图所示,则
_____________  (填“>”或“<”)。
(填“>”或“<”)。 温度下,将
温度下,将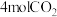 和
和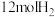 充入2L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率
充入2L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率
_____________ 。
(3)工业上可以利用二氧化碳合成甲醇,已知
①
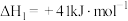
②

a.若③ 正反应的活化能为
正反应的活化能为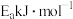 ,则逆反应的活化能为
,则逆反应的活化能为_____________  (用含Ea的式子表示)
(用含Ea的式子表示)
b.某一刚性容器中充入 和
和 ,起始压强为
,起始压强为 ,在催化剂存在条件下发生上述三个反应,测得温度与平衡转化率、产物选择性的关系如图所示。已知:选择性
,在催化剂存在条件下发生上述三个反应,测得温度与平衡转化率、产物选择性的关系如图所示。已知:选择性 。240℃平衡时,反应③的压强平衡常数
。240℃平衡时,反应③的压强平衡常数 为
为_____________ 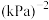 (用含p的式子列出计算式,不用化简)
(用含p的式子列出计算式,不用化简) 为原料,电解法制取乙烯、乙烷的装置如图,生成乙烯的电极反应式为:
为原料,电解法制取乙烯、乙烷的装置如图,生成乙烯的电极反应式为:_____________ .
 减排能有效降低温室效应,同时,
减排能有效降低温室效应,同时, 也是一种重要的资源,因此研究
也是一种重要的资源,因此研究 捕集与转化对实现“碳中和”目标具有重要意义而备受关注。
捕集与转化对实现“碳中和”目标具有重要意义而备受关注。(1)某研究机构成功合成了氮掺杂多孔有机聚合物DLU-1吸附剂,用于烟道气(主要是
 和
和 )和天然气中
)和天然气中 的捕集。为考查样品对单组分气体的吸附性能,测定在1bar,273和298K下的单组分气体吸附等温线如图,请阐述DLU-1吸附剂能做捕获剂的理由:
的捕集。为考查样品对单组分气体的吸附性能,测定在1bar,273和298K下的单组分气体吸附等温线如图,请阐述DLU-1吸附剂能做捕获剂的理由:
 和
和 反应合成二甲醚,
反应合成二甲醚,
 )
)①恒温恒容下,充入等物质的量的
 和
和 充分反应,以下叙述能说明该反应达到平衡状态的
充分反应,以下叙述能说明该反应达到平衡状态的A.
 的物质的量分数保持不变
的物质的量分数保持不变B.容器中混合气体的密度保持不变
C.容器中混合气体的平均摩尔质量保持不变
D.断裂
 键的同时断裂
键的同时断裂 键
键②在某压强下,合成二甲醚的反应在不同温度、不同投料比时,
 的平衡转化率如图所示,则
的平衡转化率如图所示,则
 (填“>”或“<”)。
(填“>”或“<”)。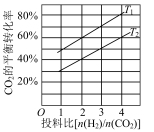
 温度下,将
温度下,将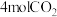 和
和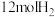 充入2L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率
充入2L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率
(3)工业上可以利用二氧化碳合成甲醇,已知
①

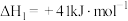
②


a.若③
 正反应的活化能为
正反应的活化能为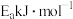 ,则逆反应的活化能为
,则逆反应的活化能为 (用含Ea的式子表示)
(用含Ea的式子表示)b.某一刚性容器中充入
 和
和 ,起始压强为
,起始压强为 ,在催化剂存在条件下发生上述三个反应,测得温度与平衡转化率、产物选择性的关系如图所示。已知:选择性
,在催化剂存在条件下发生上述三个反应,测得温度与平衡转化率、产物选择性的关系如图所示。已知:选择性 。240℃平衡时,反应③的压强平衡常数
。240℃平衡时,反应③的压强平衡常数 为
为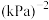 (用含p的式子列出计算式,不用化简)
(用含p的式子列出计算式,不用化简)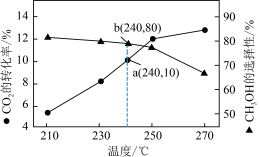
 为原料,电解法制取乙烯、乙烷的装置如图,生成乙烯的电极反应式为:
为原料,电解法制取乙烯、乙烷的装置如图,生成乙烯的电极反应式为: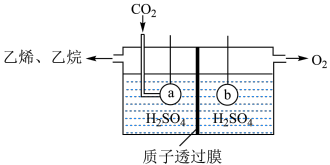
您最近一年使用:0次
名校
解题方法
4 . 在化学反应的研究和实际应用中,人们除了选择合适的化学反应以实现新期特的物质转化或能量转化,还要关注化学反应进行的快慢和程度,以提高生产效率。
(1)控制条件,让反应在恒容密闭容器中进行如下反应: 。用传感器测得不同时间NO和CO的浓度如表。
。用传感器测得不同时间NO和CO的浓度如表。
前2s内的平均反应速率
___________ ,从表格看,已达化学平衡的时间段为:___________ 。
(2)如图是在一定温度下,某固定容积的密闭容器中充入一定量的 气体后,发生反应
气体后,发生反应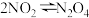 ,已知
,已知 是红棕色气体,
是红棕色气体, 是无色气体。反应速率(v)与时间(t)的关系曲线。
是无色气体。反应速率(v)与时间(t)的关系曲线。
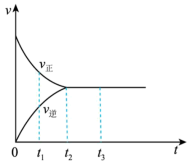
下列叙述正确的是___________ 。
a. 时,反应未达到平衡,
时,反应未达到平衡, 浓度在减小
浓度在减小
b. 时,反应达到平衡,反应不再进行
时,反应达到平衡,反应不再进行
c. 各物质浓度不再变化
各物质浓度不再变化
d. 各物质浓度相等
各物质浓度相等
e. ,
, 浓度增大
浓度增大
f.反应过程中气体的颜色不变
(3)在压强为 条件下,
条件下, 与
与 的混合气体在催化剂作用下能自发放热反应生成甲醇:
的混合气体在催化剂作用下能自发放热反应生成甲醇: 。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:
。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:
___________ ,
___________ 。
(4)比较相同浓度的 溶液和不同浓度的
溶液和不同浓度的 溶液反应的反应快慢可通过测定
溶液反应的反应快慢可通过测定___________ 来实现。
(5)在四个不同的容器中,在不同的条件下进行合成氨反应: 根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
(1)控制条件,让反应在恒容密闭容器中进行如下反应:
 。用传感器测得不同时间NO和CO的浓度如表。
。用传感器测得不同时间NO和CO的浓度如表。时间 | 0 | 1 | 2 | 3 | 4 | 5 |
 | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |

(2)如图是在一定温度下,某固定容积的密闭容器中充入一定量的
 气体后,发生反应
气体后,发生反应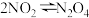 ,已知
,已知 是红棕色气体,
是红棕色气体, 是无色气体。反应速率(v)与时间(t)的关系曲线。
是无色气体。反应速率(v)与时间(t)的关系曲线。
下列叙述正确的是
a.
 时,反应未达到平衡,
时,反应未达到平衡, 浓度在减小
浓度在减小b.
 时,反应达到平衡,反应不再进行
时,反应达到平衡,反应不再进行c.
 各物质浓度不再变化
各物质浓度不再变化 d.
 各物质浓度相等
各物质浓度相等e.
 ,
, 浓度增大
浓度增大 f.反应过程中气体的颜色不变
(3)在压强为
 条件下,
条件下, 与
与 的混合气体在催化剂作用下能自发放热反应生成甲醇:
的混合气体在催化剂作用下能自发放热反应生成甲醇: 。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:
。为了寻得合成甲醇的适宜温度与压强,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。表中剩余的实验数据:

| 实验编号 |  (℃) (℃) |  |  |
| ① | 180 |  | 0.1 |
| ② |  |  | 5 |
| ③ | 350 |  | 5 |
 溶液和不同浓度的
溶液和不同浓度的 溶液反应的反应快慢可通过测定
溶液反应的反应快慢可通过测定(5)在四个不同的容器中,在不同的条件下进行合成氨反应:
 根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________A. | B. |
C. | D. |
您最近一年使用:0次
2023-05-16更新
|
480次组卷
|
2卷引用:江西省上犹中学2022-2023学年高一下学期6月期末考试化学试题
名校
解题方法
5 . 尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
(1)在尿素合成塔中发生的反应可表示为2NH3(g)+CO2(g) NH2COONH4(l)
NH2COONH4(l) [CO(NH2)2](s)+H2O(g);其中第一步反应为快速反应,ΔH1=-119.2kJ·mol-1,第二步反应为慢速反应,ΔH2=+15.5kJ·mol-1,已知在其他条件相同时,活化能越低化学反应速率越快。则下列图象能表示尿素合成塔中发生反应的能量变化历程的是___________(填标号)。
[CO(NH2)2](s)+H2O(g);其中第一步反应为快速反应,ΔH1=-119.2kJ·mol-1,第二步反应为慢速反应,ΔH2=+15.5kJ·mol-1,已知在其他条件相同时,活化能越低化学反应速率越快。则下列图象能表示尿素合成塔中发生反应的能量变化历程的是___________(填标号)。
(2)T℃,在2L的密闭容器中,通入2molNH3和1molCO2,保持体积不变,发生反应2NH3(g)+CO2(g) [CO(NH2)2](s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
[CO(NH2)2](s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
①NH3的平衡转化率为___________ 。
②能说明上述反应达到平衡状态的是___________ (填标号)。
A.n(CO2):n(NH3)=1:2
B.混合气体的密度不再发生变化
C. 单位时间内消耗2molNH3,同时生成1molH2O
D.CO2的体积分数在混合气体中保持不变
③若10min时保持温度和压强不变,再向容器中同时充入0.5molCO2和0.5molH2O(g),则此时平衡___________ (填“正向”,“逆向”或“不”)移动。
(3)一定温度下,某恒容密闭容器中发生反应2NH3(g)+CO2(g) [CO(NH2)2](s)+H2O(g),若原料气中
[CO(NH2)2](s)+H2O(g),若原料气中 =m,测得m与某反应物的平衡转化率(α)的关系如图所示。
=m,测得m与某反应物的平衡转化率(α)的关系如图所示。
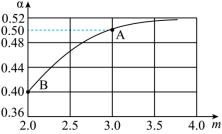
①上图中表示的是反应物___________ 的平衡转化率。
②若平衡时A点容器内总压强为0.5MPa,则上述反应的平衡常数Kp=___________ (MPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)在尿素合成塔中发生的反应可表示为2NH3(g)+CO2(g)
 NH2COONH4(l)
NH2COONH4(l) [CO(NH2)2](s)+H2O(g);其中第一步反应为快速反应,ΔH1=-119.2kJ·mol-1,第二步反应为慢速反应,ΔH2=+15.5kJ·mol-1,已知在其他条件相同时,活化能越低化学反应速率越快。则下列图象能表示尿素合成塔中发生反应的能量变化历程的是___________(填标号)。
[CO(NH2)2](s)+H2O(g);其中第一步反应为快速反应,ΔH1=-119.2kJ·mol-1,第二步反应为慢速反应,ΔH2=+15.5kJ·mol-1,已知在其他条件相同时,活化能越低化学反应速率越快。则下列图象能表示尿素合成塔中发生反应的能量变化历程的是___________(填标号)。A.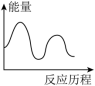 | B.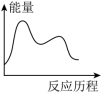 |
C.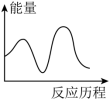 | D.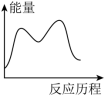 |
 [CO(NH2)2](s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
[CO(NH2)2](s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:①NH3的平衡转化率为
②能说明上述反应达到平衡状态的是
A.n(CO2):n(NH3)=1:2
B.混合气体的密度不再发生变化
C. 单位时间内消耗2molNH3,同时生成1molH2O
D.CO2的体积分数在混合气体中保持不变
③若10min时保持温度和压强不变,再向容器中同时充入0.5molCO2和0.5molH2O(g),则此时平衡
(3)一定温度下,某恒容密闭容器中发生反应2NH3(g)+CO2(g)
 [CO(NH2)2](s)+H2O(g),若原料气中
[CO(NH2)2](s)+H2O(g),若原料气中 =m,测得m与某反应物的平衡转化率(α)的关系如图所示。
=m,测得m与某反应物的平衡转化率(α)的关系如图所示。
①上图中表示的是反应物
②若平衡时A点容器内总压强为0.5MPa,则上述反应的平衡常数Kp=
您最近一年使用:0次
名校
6 . 丙烯是极为重要的有机合成原料,丙烷脱氢和丙烷氧化脱氢是制备丙烯的两种新方法。
回答下列问题:
(1)已知:①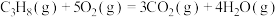

②

丙烷氧化脱氢原理为
 ,则
,则
_______ 。若一定温度下在某恒容密闭容器中进行氧化脱氢反应,下列事实不能表明反应达到平衡状态的是_______ (填选项字母)。
A.气体密度不再改变 B.混合气体平均摩尔质量不再改变
C.体系压强不再改变 D. 、
、 的生成速率相等
的生成速率相等
(2)已知丙烷脱氢反应为
 。丙烷脱氢与丙烷氧化脱氢制备丙烯相比。优缺点分别是
。丙烷脱氢与丙烷氧化脱氢制备丙烯相比。优缺点分别是_______ 。
(3)向某密闭容器中加入 丙烷,控制适当的条件使其发生反应:
丙烷,控制适当的条件使其发生反应: 。测得丙烷的平衡转化率与温度、压强的关系如图所示:
。测得丙烷的平衡转化率与温度、压强的关系如图所示:
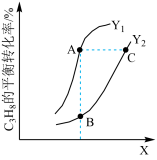
①X表示_______ (填“温度”或“压强”),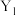
_______  (填“>”或“<”)。
(填“>”或“<”)。
②A、B、C三点对应反应平衡常数大小关系为_______ 。
(4) ℃时,向容积为
℃时,向容积为 的恒容密闭容器中加入
的恒容密闭容器中加入 丙烷,发生反应
丙烷,发生反应 ,
, 末达到平衡,测得丙烷的转化率为80%,
末达到平衡,测得丙烷的转化率为80%, 内,平均反应速率
内,平均反应速率
_______  ,该温度下反应的平衡常数
,该温度下反应的平衡常数
_______ 。
回答下列问题:
(1)已知:①
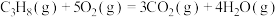

②


丙烷氧化脱氢原理为

 ,则
,则
A.气体密度不再改变 B.混合气体平均摩尔质量不再改变
C.体系压强不再改变 D.
 、
、 的生成速率相等
的生成速率相等(2)已知丙烷脱氢反应为

 。丙烷脱氢与丙烷氧化脱氢制备丙烯相比。优缺点分别是
。丙烷脱氢与丙烷氧化脱氢制备丙烯相比。优缺点分别是(3)向某密闭容器中加入
 丙烷,控制适当的条件使其发生反应:
丙烷,控制适当的条件使其发生反应: 。测得丙烷的平衡转化率与温度、压强的关系如图所示:
。测得丙烷的平衡转化率与温度、压强的关系如图所示:
①X表示
 (填“>”或“<”)。
(填“>”或“<”)。②A、B、C三点对应反应平衡常数大小关系为
(4)
 ℃时,向容积为
℃时,向容积为 的恒容密闭容器中加入
的恒容密闭容器中加入 丙烷,发生反应
丙烷,发生反应 ,
, 末达到平衡,测得丙烷的转化率为80%,
末达到平衡,测得丙烷的转化率为80%, 内,平均反应速率
内,平均反应速率
 ,该温度下反应的平衡常数
,该温度下反应的平衡常数
您最近一年使用:0次
解题方法
7 . 尿素是重要的化工原料,也是常用复肥。以氨为原料合成尿素的相关反应如下:
①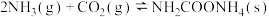
 ;
;
②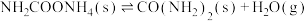
 ;
;
③
 ;
;
④
 。
。
下列叙述正确的是
①
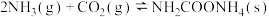
 ;
;②
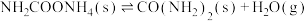
 ;
;③

 ;
;④

 。
。下列叙述正确的是
| A.反应①是放热反应,反应②和反应③都是吸热反应 |
| B.反应②中生成物总能量低于反应物总能量 |
| C.在恒容密闭容器中仅发生反应②,当气体摩尔质量不变时反应达到平衡状态 |
D.上述反应④中 |
您最近一年使用:0次
8 . 实现“双碳达标”有效途径之一是固定二氧化碳。工业上,可利用CO2和天然气反应制备合成气,再以合成气为原料制备高附加值产品。
主反应: ;
;
副反应: 。
。
回答下列问题:
(1)几种可燃物的燃烧热数据如下:
上述反应中, =
=___________  。
。
(2)在恒温恒容条件下,向密闭容器中充入1mlCO2和1mCH4 ,发生上述反应。下列情况不能说明反应已达到平衡状态的是___________(填字母)。
(3)在制备合成气的反应中,CO2的平转化率与温度,压强的关系如图1所示。
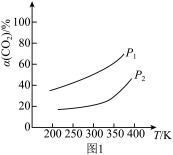
判断P1、P2大小关系:P1___________ P2(填“>”“<”或“=”),判断依据是___________ 。
(4)利用合或气合成CH3OH的原理是 。
。
向恒容密闭容器中充入1molCO和2molH2,不同条件下合成CH3OH(g),平衡时CH3OH(g)的体积分数与温度,压强的关系如图2所示。
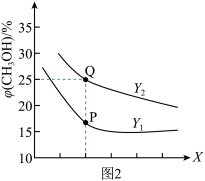
①图2中X代表___________ (填“湿度”或“压强”)。Q点对应的容器体积为2L,此时容器内压强为akPa,P点压强平面常数Kp=___________ (要求带单位)。
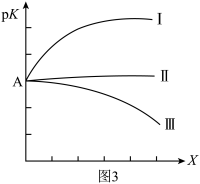
②图3能正确表示平衡数的负对数pK(pK=-lgk)与X的关系的是曲线___________ (填序号)。
主反应:
 ;
;副反应:
 。
。回答下列问题:
(1)几种可燃物的燃烧热数据如下:
| 物质 | CO | H2 | CH4 |
燃烧热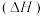 /KJ/mol /KJ/mol | -283 | -286 | -890 |
 =
= 。
。(2)在恒温恒容条件下,向密闭容器中充入1mlCO2和1mCH4 ,发生上述反应。下列情况不能说明反应已达到平衡状态的是___________(填字母)。
| A.混合气体总压强不随时间变化 |
| B.混合气体密度不随时间变化 |
| C.混合气体中CH4的体积分数不随时间变化 |
| D.混合气体的平均摩尔质量不随时间变化 |

判断P1、P2大小关系:P1
(4)利用合或气合成CH3OH的原理是
 。
。向恒容密闭容器中充入1molCO和2molH2,不同条件下合成CH3OH(g),平衡时CH3OH(g)的体积分数与温度,压强的关系如图2所示。

①图2中X代表
②图3能正确表示平衡数的负对数pK(pK=-lgk)与X的关系的是曲线

您最近一年使用:0次
解题方法
9 . 近年,甲醇的制取与应用在全球引发了关于“甲醇经济”的广泛探讨。以下是两种制取过程:
一、利用CO2制取甲醇
当原料组成为n(CO2): n(H2)=1: 3通入某密闭容器,合成CH3OH的反应体系中主要包含以下反应:
反应①: CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
反应②: CO2(g)+H2(g) CO(g)+H2O(g) ΔH=+41.2kJ/mol
CO(g)+H2O(g) ΔH=+41.2kJ/mol
(1)已知反应②的v 正=k正c(CO2)·c(H2), v逆=k逆c(H2O) ·c(CO)(k正、k逆为速率常数,与温度、催化剂有关)若平衡后升高温度,则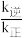
___________ (填“增大”、“不变”或“减小”);若反应体系在恒容容器中发生,下列情况下反应一定达到平衡状态的是___________ 。
A.容器内的压强不再改变
B.容器内气体密度不再改变
C.容器内c(CO2): c(H2): c(CO): c(H2O)=1: 1: 1: 1
D.单位时间内,断开C=O键的数目和断开H-O键的数目相同
(2)维持压强为6.4MPa,测得不同温度下,反应经过相同时间时CO2的转化率、甲醇的选择性如图所示[CH3OH的选择性= ]。
]。
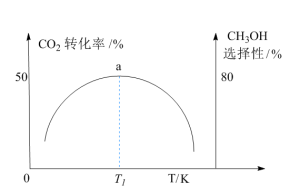
①ΔH1___________ 0(填“<”或“>”),判断的依据是___________ 。
②T1K时,若反应从开始到达到a点所用时间为5 min, 则v(CH3OH)=___________ MPa·min-1,反应②的Kp=___________ (Kp指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=p总×A的物质的量分数,计算结果保留2位有效数字)。
二、利用烯烃催化制取甲醇
制取过程中发生如下反应:
反应I: C3H6(g)+3H2O(g) 3CH3OH(g) ΔH2
3CH3OH(g) ΔH2
反应II: C2H4(g)+2H2O(g) 2CH3OH(g) ΔH3
2CH3OH(g) ΔH3
反应III: 3C2H4(g) 2C3H6(g) ΔH4
2C3H6(g) ΔH4
(3)反应I、III的vantHoff实验数据如图所示(vantHoff经验公式RInK=- +C,
+C,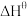 为标准焓变,K为平衡常数,R和C为常数)。根据图判断:
为标准焓变,K为平衡常数,R和C为常数)。根据图判断:

ΔH3=___________ (用含ΔH2和ΔH4的计算式表示),反应III的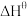 =
= ___________ kJ ·mol-1。
一、利用CO2制取甲醇
当原料组成为n(CO2): n(H2)=1: 3通入某密闭容器,合成CH3OH的反应体系中主要包含以下反应:
反应①: CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1反应②: CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=+41.2kJ/mol
CO(g)+H2O(g) ΔH=+41.2kJ/mol(1)已知反应②的v 正=k正c(CO2)·c(H2), v逆=k逆c(H2O) ·c(CO)(k正、k逆为速率常数,与温度、催化剂有关)若平衡后升高温度,则
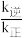
A.容器内的压强不再改变
B.容器内气体密度不再改变
C.容器内c(CO2): c(H2): c(CO): c(H2O)=1: 1: 1: 1
D.单位时间内,断开C=O键的数目和断开H-O键的数目相同
(2)维持压强为6.4MPa,测得不同温度下,反应经过相同时间时CO2的转化率、甲醇的选择性如图所示[CH3OH的选择性=
 ]。
]。
①ΔH1
②T1K时,若反应从开始到达到a点所用时间为5 min, 则v(CH3OH)=
二、利用烯烃催化制取甲醇
制取过程中发生如下反应:
反应I: C3H6(g)+3H2O(g)
 3CH3OH(g) ΔH2
3CH3OH(g) ΔH2反应II: C2H4(g)+2H2O(g)
 2CH3OH(g) ΔH3
2CH3OH(g) ΔH3反应III: 3C2H4(g)
 2C3H6(g) ΔH4
2C3H6(g) ΔH4(3)反应I、III的vantHoff实验数据如图所示(vantHoff经验公式RInK=-
 +C,
+C,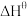 为标准焓变,K为平衡常数,R和C为常数)。根据图判断:
为标准焓变,K为平衡常数,R和C为常数)。根据图判断:
ΔH3=
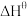 =
=
您最近一年使用:0次
名校
解题方法
10 . 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的炭即可产生水煤气。反应为C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,能使化学反应速率加快的措施有
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,能使化学反应速率加快的措施有_______ (填序号)。
①增加C的物质的量 ②升高反应温度
③随时吸收CO、H2转化为CH3OH ④密闭定容容器中充入CO(g)
(2)在2 L密闭绝热容器中,投入4 mol N2和6 mol H2,在一定条件下生成NH3,测得不同温度下,平衡时NH3的物质的量数据如下表:
①下列能说明该反应已达到平衡状态的是_______ 。
A.3v正(H2)=2v逆(NH3) B.容器内气体压强不变
C.混合气体的密度不变 D.混合气的温度保持不变
②在T3温度下,达到平衡时N2的体积分数_______ 。
(3)T℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g) 2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
2NH3(g),反应过程中各物质浓度的变化曲线如图所示:

①表示H2浓度变化的曲线是_______ (填“A”、“B”或“C”)。
②在0~25 min内N2的平均反应速率为_______ 。
(4)CO2与NH3反应可合成尿素:CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g);在T1℃时,将1 mol CO2和2 mol NH3置于1 L密闭容器中,发生上述反应,在t时刻,测得容器中CO2转化率约为73%。保持其他初始实验条件不变,分别在温度为T2℃、T3℃、T4℃、T5℃时,重复上述实验,经过相同时间测得CO2转化率并绘制变化曲线如图所示。
CO(NH2)2(s)+H2O(g);在T1℃时,将1 mol CO2和2 mol NH3置于1 L密闭容器中,发生上述反应,在t时刻,测得容器中CO2转化率约为73%。保持其他初始实验条件不变,分别在温度为T2℃、T3℃、T4℃、T5℃时,重复上述实验,经过相同时间测得CO2转化率并绘制变化曲线如图所示。
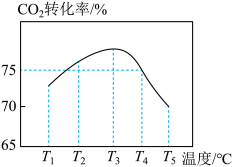
①该反应的ΔH_______ (填“>”或“<”)0。
②T4℃时反应的平衡常数K=_______ 。
③T1~T3℃之间,CO2转化率逐渐增大,其原因是_______
(1)将水蒸气通过红热的炭即可产生水煤气。反应为C(s)+H2O(g)
 CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,能使化学反应速率加快的措施有
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,能使化学反应速率加快的措施有①增加C的物质的量 ②升高反应温度
③随时吸收CO、H2转化为CH3OH ④密闭定容容器中充入CO(g)
(2)在2 L密闭绝热容器中,投入4 mol N2和6 mol H2,在一定条件下生成NH3,测得不同温度下,平衡时NH3的物质的量数据如下表:
| 温度/K | T1 | T2 | T3 | T4 |
| n(NH3)/mol | 3.6 | 3.2 | 2.8 | 2.0 |
A.3v正(H2)=2v逆(NH3) B.容器内气体压强不变
C.混合气体的密度不变 D.混合气的温度保持不变
②在T3温度下,达到平衡时N2的体积分数
(3)T℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g)
 2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
①表示H2浓度变化的曲线是
②在0~25 min内N2的平均反应速率为
(4)CO2与NH3反应可合成尿素:CO2(g)+2NH3(g)
 CO(NH2)2(s)+H2O(g);在T1℃时,将1 mol CO2和2 mol NH3置于1 L密闭容器中,发生上述反应,在t时刻,测得容器中CO2转化率约为73%。保持其他初始实验条件不变,分别在温度为T2℃、T3℃、T4℃、T5℃时,重复上述实验,经过相同时间测得CO2转化率并绘制变化曲线如图所示。
CO(NH2)2(s)+H2O(g);在T1℃时,将1 mol CO2和2 mol NH3置于1 L密闭容器中,发生上述反应,在t时刻,测得容器中CO2转化率约为73%。保持其他初始实验条件不变,分别在温度为T2℃、T3℃、T4℃、T5℃时,重复上述实验,经过相同时间测得CO2转化率并绘制变化曲线如图所示。
①该反应的ΔH
②T4℃时反应的平衡常数K=
③T1~T3℃之间,CO2转化率逐渐增大,其原因是
您最近一年使用:0次
2023-02-02更新
|
178次组卷
|
2卷引用:江西省吉水中学2023届高三下学期一模考试化学试题



