名校
1 . 我国科学工作者首次在实验室实现了二氧化碳到淀粉的人工合成,其合成路线中的第一步反应为CO2 g 3H2 g CH3OHg H2Og 。在不同温度T1、T2 T1<T2 条件下,在容积为2L的刚性容器中投入2 molCO2和6 molH2,发生上述反应,实验测得两容器中CO2或CH3OH 的物质的量随时间的变化关系如图所示。下列说法中错误的是
CH3OHg H2Og 。在不同温度T1、T2 T1<T2 条件下,在容积为2L的刚性容器中投入2 molCO2和6 molH2,发生上述反应,实验测得两容器中CO2或CH3OH 的物质的量随时间的变化关系如图所示。下列说法中错误的是
 CH3OHg H2Og 。在不同温度T1、T2 T1<T2 条件下,在容积为2L的刚性容器中投入2 molCO2和6 molH2,发生上述反应,实验测得两容器中CO2或CH3OH 的物质的量随时间的变化关系如图所示。下列说法中错误的是
CH3OHg H2Og 。在不同温度T1、T2 T1<T2 条件下,在容积为2L的刚性容器中投入2 molCO2和6 molH2,发生上述反应,实验测得两容器中CO2或CH3OH 的物质的量随时间的变化关系如图所示。下列说法中错误的是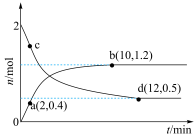
| A.ab 段用CH3OH 的表示平均反应速率为0.050mol L1 min1 |
| B.a 点时CO2的转化率为 20% |
| C.曲线 cd 对应T2 条件下的反应 |
| D.在同一温度条件下,当容器中混合气体的密度不随时间变化时,该反应达到平衡状态 |
您最近一年使用:0次
解题方法
2 . 我国科学工作者首次在实验室实现了二氧化碳到淀粉的人工合成,其合成路线中的第一步反应为 。在不同温度
。在不同温度 、
、 条件下,在容积为2L的刚性容器中投入2 mol
条件下,在容积为2L的刚性容器中投入2 mol  和6 mol
和6 mol  ,发生上述反应,实验测得两容器中
,发生上述反应,实验测得两容器中 或
或 的物质的量随时间的变化关系如图所示。下列说法错误的是
的物质的量随时间的变化关系如图所示。下列说法错误的是
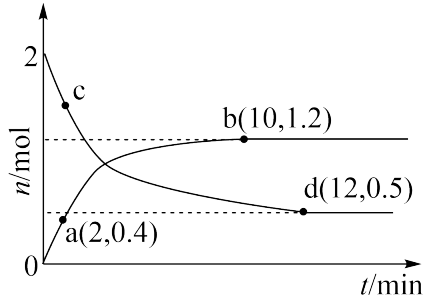
 。在不同温度
。在不同温度 、
、 条件下,在容积为2L的刚性容器中投入2 mol
条件下,在容积为2L的刚性容器中投入2 mol  和6 mol
和6 mol  ,发生上述反应,实验测得两容器中
,发生上述反应,实验测得两容器中 或
或 的物质的量随时间的变化关系如图所示。下列说法错误的是
的物质的量随时间的变化关系如图所示。下列说法错误的是
A.ab段用 的表示平均反应速率为 的表示平均反应速率为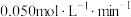 |
| B.当容器中混合气体的密度不随时间变化时,该反应达到平衡状态 |
C.曲线cd对应 条件下的反应 条件下的反应 |
D.a点时 的转化率为20% 的转化率为20% |
您最近一年使用:0次
名校
3 . (1)2017年中科院某研究团队通过设计一种新型Na-Fe3O4/HZSM-5多功能复合催化剂,成功实现了CO2直接加氢制取辛烷值汽油,该研究成果被评价为“CO2催化转化领域的突破性进展”。
已知:H2(g)+1/2O2(g)=H2O(l) ΔH1 = -aKJ/mol
C8H18(1 )+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol
)+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol
试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方程式_________________________________ 。
(2)利用CO2及H2为原料,在合适的催化剂(如Cu/ZnO催化剂)作用下,也可合成CH3OH,涉及的反应有:
甲:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1
CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1
乙:CO2(g)+H2(g) CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2
CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2
①CO(g)+2H2(g) CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=______ (用含K1、K2的表达式表示),该反应△H_____ 0(填“大于”或“小于”)。
②提高CO2转化为CH3OH平衡转化率的措施有___________ (填写两项)。
③催化剂和反应体系的关系就像锁和钥匙的关系一样,具有高度的选择性。下列四组实验,控制CO2和H2初始投料比均为1:2.2,经过相同反应时间(t1min)。
由表格中的数据可知,相同温度下不同的催化剂对CO2的转化为CH3OH的选择性有显著影响,根据上表所给数据结合反应原理,所得最优选项为___________ (填字母符号)。
(3)以CO、H2为原料合成 甲醇的反应为:CO(g)+2H2(g)
甲醇的反应为:CO(g)+2H2(g) CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
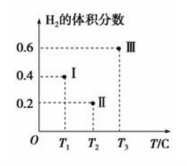
①0~5min时间内容器Ⅱ中用CH3OH表示的化学反应速率为_________________ 。
②三个容器中一定达到平衡状态的是容器________ (填写容器代号)。
已知:H2(g)+1/2O2(g)=H2O(l) ΔH1 = -aKJ/mol
C8H18(1
 )+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol
)+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方程式
(2)利用CO2及H2为原料,在合适的催化剂(如Cu/ZnO催化剂)作用下,也可合成CH3OH,涉及的反应有:
甲:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1
CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1乙:CO2(g)+H2(g)
 CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2
CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2①CO(g)+2H2(g)
 CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=②提高CO2转化为CH3OH平衡转化率的措施有
③催化剂和反应体系的关系就像锁和钥匙的关系一样,具有高度的选择性。下列四组实验,控制CO2和H2初始投料比均为1:2.2,经过相同反应时间(t1min)。
| 温度(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) | 综合选项 |
| 543 | Cu/ZnO纳米棒材料 | 12.3 | 42.3 | A |
| 543 | Cu/ZnO纳米片材料 | 11.9 | 72.7 | B |
| 553 | Cu/ZnO纳米棒材料 | 15.3 | 39.1 | C |
| 553 | Cu/ZnO纳米片材料 | 12.0 | 70.6 | D |
由表格中的数据可知,相同温度下不同的催化剂对CO2的转化为CH3OH的选择性有显著影响,根据上表所给数据结合反应原理,所得最优选项为
(3)以CO、H2为原料合成
 甲醇的反应为:CO(g)+2H2(g)
甲醇的反应为:CO(g)+2H2(g) CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
①0~5min时间内容器Ⅱ中用CH3OH表示的化学反应速率为
②三个容器中一定达到平衡状态的是容器
您最近一年使用:0次
2018-08-09更新
|
1197次组卷
|
8卷引用:【全国校级联考】山东省七校联合体2018届高三第二次联考理科综合化学试题
名校
解题方法
4 . 我国在第75届联合国大会上正式提出了2030年实现碳达峰、2060年实现碳中和的目标,所以研发利用二氧化碳技术,降低空气中二氧化碳含量成为重要的任务。
Ⅰ.化石燃料的燃烧产生大量的二氧化碳。已知25℃时,相关物质的摩尔燃烧焓数据如表:
(1)则25℃时H2(g)和C(石墨,s)生成C2H2(l)的热化学方程式为________ 。
Ⅱ.二氧化碳甲烷化反应合成替代天然气,是利用二氧化碳的技术之一。
甲烷化主反应:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H=-165kJ•mol-1
CH4(g)+2H2O(g) △H=-165kJ•mol-1
副反应:i.CO(g)+3H2(g) CH4(g)+H2O(g) ΔH1=_______。
CH4(g)+H2O(g) ΔH1=_______。
ii.CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.2kJ•mol-1;
CO(g)+H2O(g) △H2=+41.2kJ•mol-1;
iii.CO2(g)+2H2(g) C(s)+2H2O(g) △H3=-90kJ•mol-1;
C(s)+2H2O(g) △H3=-90kJ•mol-1;
iv.C(s)+H2O(g) CO(g)+H2(g) △H4=+131.3kJ•mol-1。
CO(g)+H2(g) △H4=+131.3kJ•mol-1。
(2)反应i的ΔH1=_______ ,该反应在_______ (填“高温”或“低温”)条件下能够自发进行反应。
(3)在恒温恒容的密闭容器中,关于反应iii叙述正确的是_______ 。
(4)某容器中加入一定量的CO2和H2,保持温度和压强不变的情况下,达平衡后再向该容器中注入Ar稀释,反应iii的化学平衡将_______ (填“正向移动”“逆向移动”或“不移动”),平衡时,CO2的分压p(CO2)_______ (填“增大”、“减小”或“不变”,下同)。
(5)以4molH2和1molCO2为初始原料,在催化剂(Ni/xMg)作用下保持总压为P0时,若只发生反应4H2(g)+CO2(g) CH4(g)+2H2O(g),不同温度下在相同时间测得CO2的转化率如图所示。
CH4(g)+2H2O(g),不同温度下在相同时间测得CO2的转化率如图所示。
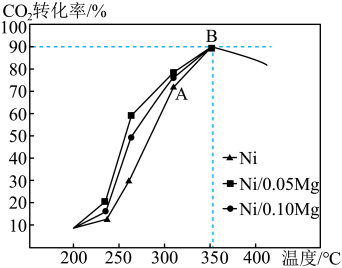
①B点的平衡常数KP=________ 。
②由图像可知,影响该催化剂活性的因素有________ 。
Ⅰ.化石燃料的燃烧产生大量的二氧化碳。已知25℃时,相关物质的摩尔燃烧焓数据如表:
| 物质 | H2(g) | C(石墨,s) | C2H2(l) |
| 摩尔燃烧焓ΔH(kJ•mol-1) | -285.8 | -393.5 | -1299.5 |
(1)则25℃时H2(g)和C(石墨,s)生成C2H2(l)的热化学方程式为
Ⅱ.二氧化碳甲烷化反应合成替代天然气,是利用二氧化碳的技术之一。
甲烷化主反应:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H=-165kJ•mol-1
CH4(g)+2H2O(g) △H=-165kJ•mol-1副反应:i.CO(g)+3H2(g)
 CH4(g)+H2O(g) ΔH1=_______。
CH4(g)+H2O(g) ΔH1=_______。ii.CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.2kJ•mol-1;
CO(g)+H2O(g) △H2=+41.2kJ•mol-1;iii.CO2(g)+2H2(g)
 C(s)+2H2O(g) △H3=-90kJ•mol-1;
C(s)+2H2O(g) △H3=-90kJ•mol-1;iv.C(s)+H2O(g)
 CO(g)+H2(g) △H4=+131.3kJ•mol-1。
CO(g)+H2(g) △H4=+131.3kJ•mol-1。(2)反应i的ΔH1=
(3)在恒温恒容的密闭容器中,关于反应iii叙述正确的是
| A.用CO2、H2、H2O表示的速率之比为1:2:2可以作为判断化学平衡的依据 |
| B.容器中气体的压强不变时,不能作为平衡的判断依据 |
| C.容器内的气体密度不变可以作为平衡的判断依据 |
| D.使用催化剂不能改变平衡转化率 |
(4)某容器中加入一定量的CO2和H2,保持温度和压强不变的情况下,达平衡后再向该容器中注入Ar稀释,反应iii的化学平衡将
(5)以4molH2和1molCO2为初始原料,在催化剂(Ni/xMg)作用下保持总压为P0时,若只发生反应4H2(g)+CO2(g)
 CH4(g)+2H2O(g),不同温度下在相同时间测得CO2的转化率如图所示。
CH4(g)+2H2O(g),不同温度下在相同时间测得CO2的转化率如图所示。
①B点的平衡常数KP=
②由图像可知,影响该催化剂活性的因素有
您最近一年使用:0次
解题方法
5 . 应对雾霾污染、改善空气质量需要从多方面入手。
Ⅰ.研究发现,NOx是雾霾的主要成分之一,NOx主要来源于汽车尾气。
已知:N2(g)+O2(g) 2NO(g) △H=+180.50 kJ·mol-1
2NO(g) △H=+180.50 kJ·mol-1
2CO(g)+O2(g) 2CO2(g) △H=-566.00 kJ·mol-1
2CO2(g) △H=-566.00 kJ·mol-1
(1)为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参与大气循环,写出该反应的热化学方程式_______ 。
Ⅱ.开发利用清洁能源可减少污染,解决雾霾问题。甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景,一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g) CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应。平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。
CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应。平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。
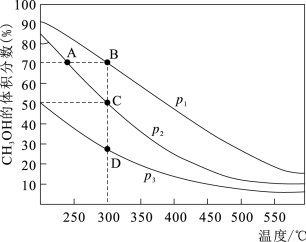
(2)该反应的反应热△H_______ 0(填“>”或“<”),压强的相对大小为p1_______ p2(填“>”或“<”)。
(3)该反应化学平衡常数表达式为_______ 。
(4)下列各项中,能说明该反应已经达到平衡的是_______。
(5)某温度下,在保证H2浓度不变的情况下,增大容器的体积,平衡_______ (填字母)。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(6)T1温度时,在容积为1 L的刚性密闭容器中充入1.0 molCH3OH(g)发生反应CH3OH(g) CO(g)+2H2(g),容器内的总压强p随时间t的变化如表所示:
CO(g)+2H2(g),容器内的总压强p随时间t的变化如表所示:
该温度下的平衡常数Kp = _______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(7)依据燃烧反应原理,合成的甲醇可以设计如图所示的燃料电池装置。
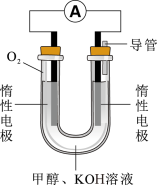
负极电极反应式为_______ 。
Ⅰ.研究发现,NOx是雾霾的主要成分之一,NOx主要来源于汽车尾气。
已知:N2(g)+O2(g)
 2NO(g) △H=+180.50 kJ·mol-1
2NO(g) △H=+180.50 kJ·mol-12CO(g)+O2(g)
 2CO2(g) △H=-566.00 kJ·mol-1
2CO2(g) △H=-566.00 kJ·mol-1(1)为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参与大气循环,写出该反应的热化学方程式
Ⅱ.开发利用清洁能源可减少污染,解决雾霾问题。甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景,一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)
 CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应。平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。
CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应。平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。
(2)该反应的反应热△H
(3)该反应化学平衡常数表达式为
(4)下列各项中,能说明该反应已经达到平衡的是_______。
| A.容器内气体压强不再变化 |
| B.v(CO) :v(H2) :v(CH3OH)=1:2:1 |
| C.容器内的密度不再变化 |
| D.容器内混合气体的平均相对分子质量不再变化 |
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(6)T1温度时,在容积为1 L的刚性密闭容器中充入1.0 molCH3OH(g)发生反应CH3OH(g)
 CO(g)+2H2(g),容器内的总压强p随时间t的变化如表所示:
CO(g)+2H2(g),容器内的总压强p随时间t的变化如表所示:| 反应时间 t/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
| 总压强p/kPa | 100.0 | 115.0 | 123.0 | 130.0 | 136.0 | 140.0 | 140.0 |
(7)依据燃烧反应原理,合成的甲醇可以设计如图所示的燃料电池装置。

负极电极反应式为
您最近一年使用:0次
2022-05-19更新
|
949次组卷
|
2卷引用:山东省潍坊高密市第三中学2022-2023学年高三上学期9月月考化学试题
名校
6 .  和
和 是重要的化工原料,可以用于合成甲醇等。
是重要的化工原料,可以用于合成甲醇等。
(1)已知:① 的燃烧热
的燃烧热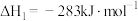 ;
;
②
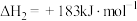 。
。
写出 和
和 反应生成无污染性气体的热化学反应方程式
反应生成无污染性气体的热化学反应方程式___________ 。
(2)以 和
和 为原料合成甲醇,该反应的热化学方程式为:
为原料合成甲醇,该反应的热化学方程式为:
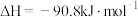
①若将等物质的量的 和
和 混合气体充入恒温恒容密闭容器中进行上述反应,下列事实能说明此反应已达到平衡状态的是
混合气体充入恒温恒容密闭容器中进行上述反应,下列事实能说明此反应已达到平衡状态的是___________ 。
a.容器内气体密度保持不变
b.混合气体的平均相对分子质量不变
c.生成 的速率与生成
的速率与生成 的速率相等
的速率相等
d. 的体积分数保持不变
的体积分数保持不变
②在容积为 的恒容密闭容器中,分别研究反应在300℃和400℃两种温度下合成甲醇的规律。下图是上述两种温度下不同的
的恒容密闭容器中,分别研究反应在300℃和400℃两种温度下合成甲醇的规律。下图是上述两种温度下不同的 和
和 的起始组成比(起始时
的起始组成比(起始时 的物质的量均为
的物质的量均为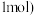 与
与 平衡转化率的关系。请回答下列问题:
平衡转化率的关系。请回答下列问题:
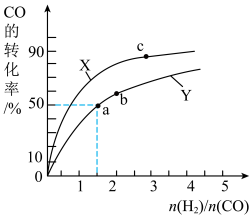
该反应在a、b和c三点对应化学平衡常数分别是 、
、 和
和 ,则其大小关系为
,则其大小关系为___________ (用“>”或“=”表示)。利用图中a点对应的数据,若反应 中达到平衡,则甲醇的反应速率为
中达到平衡,则甲醇的反应速率为___________  ,计算出曲线Y对应温度下
,计算出曲线Y对应温度下 的平衡常数
的平衡常数
___________ 。
③一定条件下,上述合成甲醇的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是___________ (填字母)。
a.甲醇物质的量增多
b.正反应速率先增大后减小
c.反应物的体积百分含量减小
d.容器中 的值变大
的值变大
 和
和 是重要的化工原料,可以用于合成甲醇等。
是重要的化工原料,可以用于合成甲醇等。(1)已知:①
 的燃烧热
的燃烧热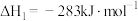 ;
;②

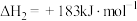 。
。写出
 和
和 反应生成无污染性气体的热化学反应方程式
反应生成无污染性气体的热化学反应方程式(2)以
 和
和 为原料合成甲醇,该反应的热化学方程式为:
为原料合成甲醇,该反应的热化学方程式为:
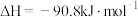
①若将等物质的量的
 和
和 混合气体充入恒温恒容密闭容器中进行上述反应,下列事实能说明此反应已达到平衡状态的是
混合气体充入恒温恒容密闭容器中进行上述反应,下列事实能说明此反应已达到平衡状态的是a.容器内气体密度保持不变
b.混合气体的平均相对分子质量不变
c.生成
 的速率与生成
的速率与生成 的速率相等
的速率相等d.
 的体积分数保持不变
的体积分数保持不变②在容积为
 的恒容密闭容器中,分别研究反应在300℃和400℃两种温度下合成甲醇的规律。下图是上述两种温度下不同的
的恒容密闭容器中,分别研究反应在300℃和400℃两种温度下合成甲醇的规律。下图是上述两种温度下不同的 和
和 的起始组成比(起始时
的起始组成比(起始时 的物质的量均为
的物质的量均为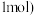 与
与 平衡转化率的关系。请回答下列问题:
平衡转化率的关系。请回答下列问题:
该反应在a、b和c三点对应化学平衡常数分别是
 、
、 和
和 ,则其大小关系为
,则其大小关系为 中达到平衡,则甲醇的反应速率为
中达到平衡,则甲醇的反应速率为 ,计算出曲线Y对应温度下
,计算出曲线Y对应温度下 的平衡常数
的平衡常数
③一定条件下,上述合成甲醇的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是
a.甲醇物质的量增多
b.正反应速率先增大后减小
c.反应物的体积百分含量减小
d.容器中
 的值变大
的值变大
您最近一年使用:0次
名校
7 . 氮及其化合物在工农业生产、生活中有着重要作用。合成氨工业中: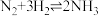
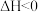 ,其化学平衡常数K与温度t的关系如表:
,其化学平衡常数K与温度t的关系如表:
完成下列填空:
(1)试比较 、
、 的大小,
的大小,
_______  (填写“>”、“=”或“<”)。
(填写“>”、“=”或“<”)。
(2)400℃时,反应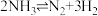 的化学平衡常数的值为
的化学平衡常数的值为_______ 。当测得 和
和 、
、 的物质的量浓度分别为3mol/L和2mol/L、1mol/L时,则该反应
的物质的量浓度分别为3mol/L和2mol/L、1mol/L时,则该反应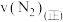
_______ 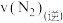 (填写“>”、“=”或“<”)。
(填写“>”、“=”或“<”)。
(3)在密闭恒容的容器中,下列能作为合成氨反应达到平衡的依据的是_______ 。
a.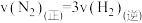 b.混合气体的密度保持不变
b.混合气体的密度保持不变
c.容器内压强保持不变 d. 、
、 、
、 的浓度之比为1:3:2
的浓度之比为1:3:2
(4)甲醇是一种可再生能源,具有广泛的开发和应用前景。以 、
、 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:
Ⅰ.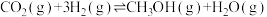
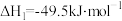
Ⅱ.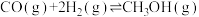
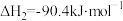
Ⅲ.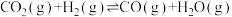
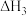
回答下列问题:④
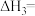
_______  。
。
②若体系中只发生反应Ⅰ,请写出反应Ⅰ的化学平衡常数表达式:K=_______ ;保持恒温恒容,将反应Ⅰ的平衡体系中各物质浓度均增大为原来的2倍,则化学平衡_______ (填“正向”“逆向”或“不”)移动,平衡常数K_______ (填“变大”“变小”或“不变”)。
③一定条件下,向体积为VL的恒容密闭容器中通入1mol 和3mol
和3mol 同时发生Ⅰ、Ⅱ、Ⅲ反应,达到平衡时,容器中
同时发生Ⅰ、Ⅱ、Ⅲ反应,达到平衡时,容器中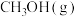 为amol,CO为bmol,此时
为amol,CO为bmol,此时 的浓度为
的浓度为_______ 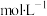 (用含a、b、V的代数式表示)
(用含a、b、V的代数式表示)
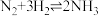
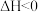 ,其化学平衡常数K与温度t的关系如表:
,其化学平衡常数K与温度t的关系如表:| t/℃ | 200 | 300 | 400 |
| K |  |  | 0.5 |
(1)试比较
 、
、 的大小,
的大小,
 (填写“>”、“=”或“<”)。
(填写“>”、“=”或“<”)。(2)400℃时,反应
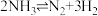 的化学平衡常数的值为
的化学平衡常数的值为 和
和 、
、 的物质的量浓度分别为3mol/L和2mol/L、1mol/L时,则该反应
的物质的量浓度分别为3mol/L和2mol/L、1mol/L时,则该反应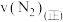
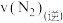 (填写“>”、“=”或“<”)。
(填写“>”、“=”或“<”)。(3)在密闭恒容的容器中,下列能作为合成氨反应达到平衡的依据的是
a.
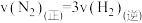 b.混合气体的密度保持不变
b.混合气体的密度保持不变c.容器内压强保持不变 d.
 、
、 、
、 的浓度之比为1:3:2
的浓度之比为1:3:2(4)甲醇是一种可再生能源,具有广泛的开发和应用前景。以
 、
、 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:Ⅰ.
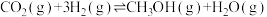
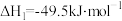
Ⅱ.
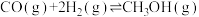
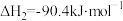
Ⅲ.
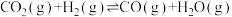
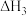
回答下列问题:④
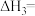
 。
。②若体系中只发生反应Ⅰ,请写出反应Ⅰ的化学平衡常数表达式:K=
③一定条件下,向体积为VL的恒容密闭容器中通入1mol
 和3mol
和3mol 同时发生Ⅰ、Ⅱ、Ⅲ反应,达到平衡时,容器中
同时发生Ⅰ、Ⅱ、Ⅲ反应,达到平衡时,容器中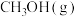 为amol,CO为bmol,此时
为amol,CO为bmol,此时 的浓度为
的浓度为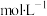 (用含a、b、V的代数式表示)
(用含a、b、V的代数式表示)
您最近一年使用:0次
解题方法
8 . 丙烯是重要的有机合成原料.由丙烷制备丙烯是近年来研究的热点,主要涉及如下反应:
反应甲2C3H8(g)+O2(g) 2C3H6(g)+2H2O(g) △H1=-225kJ•mol-1
2C3H6(g)+2H2O(g) △H1=-225kJ•mol-1
反应乙2C3H8(g)+7O2(g) 6CO(g)+8H2O(g) △H2=-2742kJ•mol-1
6CO(g)+8H2O(g) △H2=-2742kJ•mol-1
回答下列问题:
(1)反应C3H6(g)+3O2(g) 3CO(g)+3H2O(g) △H=
3CO(g)+3H2O(g) △H=_____ kJ•mol-1。
(2)在恒容绝热密闭容器中发生反应甲,下列能说明反应甲已达到平衡状态的有_____ (填标号)。
(3)在压强恒定为200kPa条件下,按起始投料n(C3H8):n(O2)=2:1充入装有催化剂的反应器中发生反应甲和反应乙,不同温度下,反应相同时间丙烷和氧气的转化率如图。
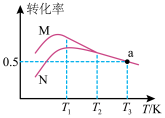
①曲线_____ (填“M”或“N”)表示O2的转化率。
②由图知,当温度高于T2时,可判断反应_____ (填“甲”或“乙”)不再发生,已知a点为平衡点,该点丙烷的分压p(C3H8)=_____ kPa(保留3位有效数字,下同),发生的反应在T3时的平衡常数Kp=_____ kPa(用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
反应甲2C3H8(g)+O2(g)
 2C3H6(g)+2H2O(g) △H1=-225kJ•mol-1
2C3H6(g)+2H2O(g) △H1=-225kJ•mol-1反应乙2C3H8(g)+7O2(g)
 6CO(g)+8H2O(g) △H2=-2742kJ•mol-1
6CO(g)+8H2O(g) △H2=-2742kJ•mol-1回答下列问题:
(1)反应C3H6(g)+3O2(g)
 3CO(g)+3H2O(g) △H=
3CO(g)+3H2O(g) △H=(2)在恒容绝热密闭容器中发生反应甲,下列能说明反应甲已达到平衡状态的有
| A.容器内温度不再变化 | B.v正(O2)=2v逆(C3H6) |
| C.混合气体的密度不再变化 | D.容器内压强不再变化 |
(3)在压强恒定为200kPa条件下,按起始投料n(C3H8):n(O2)=2:1充入装有催化剂的反应器中发生反应甲和反应乙,不同温度下,反应相同时间丙烷和氧气的转化率如图。

①曲线
②由图知,当温度高于T2时,可判断反应
您最近一年使用:0次
9 . 以二氧化碳为原料,不依赖植物光合作用,直接人工合成淀粉,看似科幻的一幕,真实地发生在实验室里。中国科学家首次实现了二氧化碳到淀粉的从头合成,相关成果北京时间9月24日由国际知名学术期刊《科学》在线发表,因此CO2的捕集、利用与封存成为科学家研究的重要课题。已知CO2经催化加氢可以生成多种低碳有机物。
I.CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=-49.5kJ·mol-1
II.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+40.9kJ·mol-1
III.CO(g)+2H2(g)=CH3OH(g) ΔH3
回答下列问题:
(1)反应III的ΔH3为_______ 。
(2)一定温度下,在一体积固定的密闭容器中进行反应I,测得CO2的物质的量浓度随反应时间的变化如图所示:
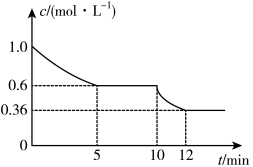
则反应进行的前5分钟内,H2的反应速率v(H2)=_______ ;10min时,改变的外界条件可能是_______ (任写两点)
(3)将CO2和H2按物质的量之比1:1投料发生反应II,下列不能说明反应已达平衡的是_______(填字母)。
(4)如图为一定比例的CO2+H2、CO+H2、CO/CO2+H2条件下甲醇生成速率与温度的关系。490K时,根据曲线a、c可判断合成甲醇的反应机理是_______ (填“A”或“B”)。
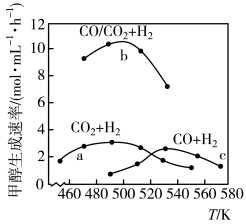
A.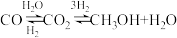
B.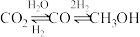
(5)C2H6(g)+2CO2(g) 4CO(g)+3H2(g) ΔH=+430KJ/mol,在四种不同的容器中发生上述反应,若初始温度、压强和反应物用量均相同,则CO2的转化率最高的是
4CO(g)+3H2(g) ΔH=+430KJ/mol,在四种不同的容器中发生上述反应,若初始温度、压强和反应物用量均相同,则CO2的转化率最高的是_______ (填字母)。
a.恒温恒容容器 b.恒容绝热容器 c.恒压绝热容器 d.恒温恒压容器
I.CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=-49.5kJ·mol-1
II.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+40.9kJ·mol-1
III.CO(g)+2H2(g)=CH3OH(g) ΔH3
回答下列问题:
(1)反应III的ΔH3为
(2)一定温度下,在一体积固定的密闭容器中进行反应I,测得CO2的物质的量浓度随反应时间的变化如图所示:

则反应进行的前5分钟内,H2的反应速率v(H2)=
(3)将CO2和H2按物质的量之比1:1投料发生反应II,下列不能说明反应已达平衡的是_______(填字母)。
| A.CO的浓度保持不变 |
| B.CO2和H2的转化率相等 |
| C.混合气体中CO2的百分含量不再发生变化 |
| D.单位时间内体系中减少1molH2的同时有1molH2O增加 |

A.
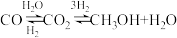
B.
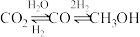
(5)C2H6(g)+2CO2(g)
 4CO(g)+3H2(g) ΔH=+430KJ/mol,在四种不同的容器中发生上述反应,若初始温度、压强和反应物用量均相同,则CO2的转化率最高的是
4CO(g)+3H2(g) ΔH=+430KJ/mol,在四种不同的容器中发生上述反应,若初始温度、压强和反应物用量均相同,则CO2的转化率最高的是a.恒温恒容容器 b.恒容绝热容器 c.恒压绝热容器 d.恒温恒压容器
您最近一年使用:0次
解题方法
10 . 1905年哈伯实现了以氮气和氢气为原料合成氨气,生产的氨制造氮肥服务于农业,养活了地球上三分之一的人口,哈伯也因此获得了1918年的诺贝尔化学奖。一百多年过去了,对合成氨的研究依然没有止步。
(1)工业合成氨的反应如下:N2+3H2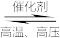 2NH3,已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molN—H键放出的能量为391kJ,则由N2和H2生成2molNH3
2NH3,已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molN—H键放出的能量为391kJ,则由N2和H2生成2molNH3___________ (填“放出”或“吸收”)的能量为___________ kJ。
(2)其他条件相同,在两个体积不变且相同的密闭容器中通入等量的NH3,在两种不同的温度下进行反应,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
根据上表数据回答:
①反应I从开始到10min,用NH3表示的反应速率为___________ ;
②反应Ⅱ一定达到了平衡状态的时间段为___________ (填字母)
a.10-20min b.20-30min c.30-40min
③反应Ⅱ达到最大限度时NH3的转化率为___________
④实验中T1___________ T2(填“>”“<”或“=”)
⑤下列能说明反应I达到化学平衡状态的是___________ (填字母)。
a.消耗2molNH3的同时生成3molH2
b.混合气体的密度不变
c.容器中的压强不随时间变化
d.N2、H2、NH3的物质的量之比为1∶3∶2
(1)工业合成氨的反应如下:N2+3H2
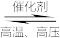 2NH3,已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molN—H键放出的能量为391kJ,则由N2和H2生成2molNH3
2NH3,已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molN—H键放出的能量为391kJ,则由N2和H2生成2molNH3(2)其他条件相同,在两个体积不变且相同的密闭容器中通入等量的NH3,在两种不同的温度下进行反应,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
I | T1 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
Ⅱ | T2 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上表数据回答:
①反应I从开始到10min,用NH3表示的反应速率为
②反应Ⅱ一定达到了平衡状态的时间段为
a.10-20min b.20-30min c.30-40min
③反应Ⅱ达到最大限度时NH3的转化率为
④实验中T1
⑤下列能说明反应I达到化学平衡状态的是
a.消耗2molNH3的同时生成3molH2
b.混合气体的密度不变
c.容器中的压强不随时间变化
d.N2、H2、NH3的物质的量之比为1∶3∶2
您最近一年使用:0次
2021-06-07更新
|
135次组卷
|
2卷引用:山东省济宁市邹城第一中学2021-2022学年高二上学期10月月考化学试卷



