1 . 在“碳达峰、碳中和”的大背景下, 的综合应用越来越受到重视。
的综合应用越来越受到重视。
(1)通过查阅资料,计算 的反应热。
的反应热。
ⅰ.查阅 、
、 和
和_______ 的燃烧热数据(填化学式)
ⅱ.查阅水的汽化热:

(2) 催化加氢制CH3OH,发生的主要反应有:
催化加氢制CH3OH,发生的主要反应有:
反应I:

反应Ⅱ: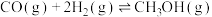

反应Ⅲ:

①反应Ⅱ自发进行的条件是_______ (填“高温”“低温”或“任意温度”)。
②反应Ⅲ在热力学上趋势大于反应I,其原因是_______ 。
(3)在5MPa下, 和
和 按物质的量之比1∶4进行投料,只发生上述(2)的反应I和反应Ⅲ,平衡时CO和
按物质的量之比1∶4进行投料,只发生上述(2)的反应I和反应Ⅲ,平衡时CO和 在含碳产物中的物质的量分数及
在含碳产物中的物质的量分数及 转化率随温度的变化如图所示。
转化率随温度的变化如图所示。_______ 。
②q曲线在250℃之后随温度升高而增大的原因是_______ 。
③250℃时,反应I的浓度平衡常数
_______ 。
(4)科学家利用电化学装置实现两种分子 和
和 的耦合转化,其原理如图所示,阳极的电极反应式为
的耦合转化,其原理如图所示,阳极的电极反应式为_______ ,理论上参加反应的 和
和 的物质的量之比为
的物质的量之比为_______ 。
 的综合应用越来越受到重视。
的综合应用越来越受到重视。(1)通过查阅资料,计算
 的反应热。
的反应热。ⅰ.查阅
 、
、 和
和ⅱ.查阅水的汽化热:


(2)
 催化加氢制CH3OH,发生的主要反应有:
催化加氢制CH3OH,发生的主要反应有:反应I:


反应Ⅱ:
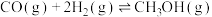

反应Ⅲ:


①反应Ⅱ自发进行的条件是
②反应Ⅲ在热力学上趋势大于反应I,其原因是
(3)在5MPa下,
 和
和 按物质的量之比1∶4进行投料,只发生上述(2)的反应I和反应Ⅲ,平衡时CO和
按物质的量之比1∶4进行投料,只发生上述(2)的反应I和反应Ⅲ,平衡时CO和 在含碳产物中的物质的量分数及
在含碳产物中的物质的量分数及 转化率随温度的变化如图所示。
转化率随温度的变化如图所示。
②q曲线在250℃之后随温度升高而增大的原因是
③250℃时,反应I的浓度平衡常数

(4)科学家利用电化学装置实现两种分子
 和
和 的耦合转化,其原理如图所示,阳极的电极反应式为
的耦合转化,其原理如图所示,阳极的电极反应式为 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
解题方法
2 . 某研究小组用新型催化剂对CO、NO催化转化进行研究,测得相同时间内NO的转化率、CO剩余的百分含量随温度变化情况如图所示。已知NO可发生下列反应:
反应Ⅰ: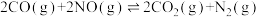

反应Ⅱ: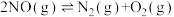

反应Ⅰ:
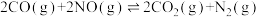

反应Ⅱ:
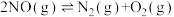

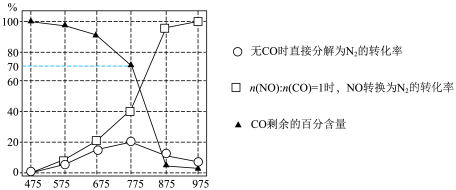
A. |
| B.温度大于775K时,催化剂活性降低 |
C.775K, 条件下,此时 条件下,此时 |
D.775K,无CO参加,只发生反应Ⅱ时的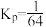 |
您最近一年使用:0次
名校
解题方法
3 . 石油工业生产中各个环节(如钻井、采油、油气输送和炼制)会产生硫化氢等废气,需要回收处理并加以利用。回答下列问题:
已知下列反应的热化学方程式:
①2H2S(g)⇌S2(g)+2H2(g) ΔH1=+180kJ⋅mol−1
②CS2(g)+2H2(g)⇌CH4(g)+S2(g) ΔH2=−81kJ⋅mol−1
(1)利用H2S与CH4反应制备H2
CH4(g)+2H2S(g)⇌CS2(g)+4H2(g)ΔH3则ΔH3=___________ ,在___________ 下该反应能自发进行(填“高温”或“低温”)。
(2)利用H2S热分解制备H2
向某密闭容器中通入2molH2S发生反应①,H2S分解的平衡转化率随温度和压强的变化情况如图所示:
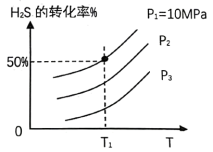
①P1、P2和P3由小到大的顺序为___________ ,理由是___________ 。
②T1温度下反应①的Kp=___________ Mpa.(Kp是以分压代替浓度计算的平衡常数,分压=总压×物质的量分数)。
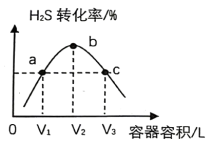
(3)一定温度下,向容积不等的恒容密闭容器中分别通入等量的H2S发生反应①,经过相同时间,测得各容器中H2S的转化率与容器容积的关系如图所示,有关说法正确的是___________。
(4)H2S的回收与利用先用足量NaOH溶液吸收H2S气体,再将吸收后的溶液用如下图所示的装置电解,碱性条件下,S2−被氧化生成S 。阳极区电解后溶液加入硫酸可得到单质硫。
。阳极区电解后溶液加入硫酸可得到单质硫。
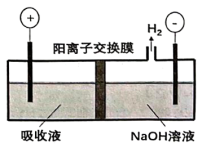
①Na+的移动方向是从___________ (填“左到右”或“右到左”)。
②阳极电极反应式为___________ 。
已知下列反应的热化学方程式:
①2H2S(g)⇌S2(g)+2H2(g) ΔH1=+180kJ⋅mol−1
②CS2(g)+2H2(g)⇌CH4(g)+S2(g) ΔH2=−81kJ⋅mol−1
(1)利用H2S与CH4反应制备H2
CH4(g)+2H2S(g)⇌CS2(g)+4H2(g)ΔH3则ΔH3=
(2)利用H2S热分解制备H2
向某密闭容器中通入2molH2S发生反应①,H2S分解的平衡转化率随温度和压强的变化情况如图所示:

①P1、P2和P3由小到大的顺序为
②T1温度下反应①的Kp=
(3)一定温度下,向容积不等的恒容密闭容器中分别通入等量的H2S发生反应①,经过相同时间,测得各容器中H2S的转化率与容器容积的关系如图所示,有关说法正确的是___________。

| A.b、c点的Q=K |
| B.正反应速率a>c |
| C.平衡常数Ka=Kb |
| D.在a点再通入H2S,平衡后H2S的转化率将增大 |
(4)H2S的回收与利用先用足量NaOH溶液吸收H2S气体,再将吸收后的溶液用如下图所示的装置电解,碱性条件下,S2−被氧化生成S
 。阳极区电解后溶液加入硫酸可得到单质硫。
。阳极区电解后溶液加入硫酸可得到单质硫。
①Na+的移动方向是从
②阳极电极反应式为
您最近一年使用:0次
名校
4 . 下列实验操作不能达到相应实验目的的是
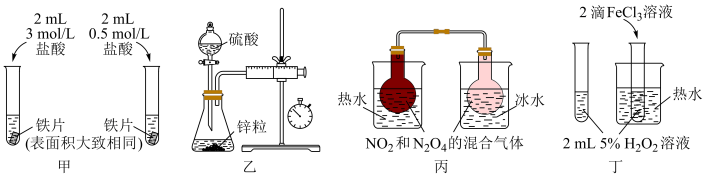

| A.利用甲装置探究浓度对化学反应速率的影响 |
| B.利用乙装置来测定化学反应速率 |
| C.利用丙装置来探究温度对化学平衡的影响 |
| D.利用丁装置来探究催化剂对化学反应速率的影响 |
您最近一年使用:0次
名校
5 . K、Ka、KW分别表示化学平衡常数、电离平衡常数和水的离子积常数,下列判断正确的是
| A.温度升高,三者都增大 |
| B.化学平衡常数的大小与温度、浓度、催化剂等有关 |
| C.室温下Ka(HCN)<Ka(HF),说明HF的电离度比HCN大 |
D.2SO2(g)+O2(g) 2SO3(g)平衡后,仅增大压强,平衡向右移动,K值不变 2SO3(g)平衡后,仅增大压强,平衡向右移动,K值不变 |
您最近一年使用:0次
名校
解题方法
6 . 党的二十大报告指出:“倡导绿色消费,推动形成绿色低碳的生产方式和生活方式”。将CO2应用于生产中实现其综合利用是目前的研究热点。回答下列问题:
(1)通过使用不同的新型催化剂,实现二氧化碳加氢合成转化为甲醇(CH3OH)也有广泛的应用。可能发生的反应如下:
反应I:

反应Ⅱ:

则反应Ⅲ: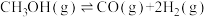

_______ 
(2)一定条件下, 的反应历程如图所示。该反应的反应速率由第
的反应历程如图所示。该反应的反应速率由第___________ (填“l”或“2”)步决定。

(3)为提高 的平衡产率,应选择的反应条件为___________(填标号)。
的平衡产率,应选择的反应条件为___________(填标号)。
(4)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测得CO2的平衡转化率随温度的变化关系如下图所示。

压强P1、P2、P3由小到大的顺序为___________ ; 图中To温度时,三条曲线几乎交于一点的原因是___________ 。
(5)一定条件下,向体积为2L 的恒容密闭容器中通入2mol CO2和6mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为xmol,CO为ymol,此时H2O(g)的浓度为___________ mol∙L−1(用含x、y的代数式表示,下同),反应Ⅱ的平衡常数为___________ 。
(1)通过使用不同的新型催化剂,实现二氧化碳加氢合成转化为甲醇(CH3OH)也有广泛的应用。可能发生的反应如下:
反应I:


反应Ⅱ:


则反应Ⅲ:
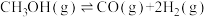


(2)一定条件下,
 的反应历程如图所示。该反应的反应速率由第
的反应历程如图所示。该反应的反应速率由第
(3)为提高
 的平衡产率,应选择的反应条件为___________(填标号)。
的平衡产率,应选择的反应条件为___________(填标号)。| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
(4)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测得CO2的平衡转化率随温度的变化关系如下图所示。

压强P1、P2、P3由小到大的顺序为
(5)一定条件下,向体积为2L 的恒容密闭容器中通入2mol CO2和6mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为xmol,CO为ymol,此时H2O(g)的浓度为
您最近一年使用:0次
7 . 以 为原料炼铁,主要发生如下反应:
为原料炼铁,主要发生如下反应:
反应I: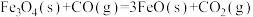
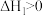
反应Ⅱ:

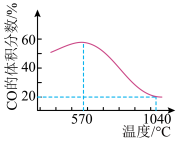
将一定体积CO 通入装有 粉末的反应器,其它条件不变,反应达平衡,测得 CO的体积分数随温度的变化关系如图所示。下列说法错误的是
粉末的反应器,其它条件不变,反应达平衡,测得 CO的体积分数随温度的变化关系如图所示。下列说法错误的是
 为原料炼铁,主要发生如下反应:
为原料炼铁,主要发生如下反应:反应I:
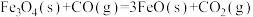
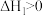
反应Ⅱ:


将一定体积CO 通入装有
 粉末的反应器,其它条件不变,反应达平衡,测得 CO的体积分数随温度的变化关系如图所示。下列说法错误的是
粉末的反应器,其它条件不变,反应达平衡,测得 CO的体积分数随温度的变化关系如图所示。下列说法错误的是
A. <0 <0 |
| B.在恒温、恒容条件下, 当容器压强保持不变,反应Ⅰ、 Ⅱ均达到平衡状态 |
| C.1040℃时, 反应Ⅰ的化学平衡常数K=4 |
D.反应温度较高时,  主要还原产物为 FeO 主要还原产物为 FeO |
您最近一年使用:0次
名校
8 . 下列实验过程能达到目的,且现象和结论正确的是
| 选项 | 实验目的 | 实验过程 | 现象和结论 |
| A. | 探究HA酸性强弱 | 等体积pH=3 的 HA 和HB 两种酸分别与足量的锌反应 | 相同时间内,HA 收集到的氢气多, 说明 HA是强酸 |
| B. | 探究压强对化学平衡的影响 | 在一定温度下的密闭容器中发生反应: , 平衡时 A 的浓度为0.5mol/L。保持温度不变,将容器扩大到原来的2倍,再次平衡时A的浓度为 0.3mol/L。 , 平衡时 A 的浓度为0.5mol/L。保持温度不变,将容器扩大到原来的2倍,再次平衡时A的浓度为 0.3mol/L。 | 说明该反应减压时,平衡向正反应方向移动 |
| C. | 探究温度对反应速率的影响 | 两支试管分别装5mL0.2mol·L⁻¹Na2S2O3溶液和5mL0.2mol·L⁻¹H2SO4溶液的混合溶液,分别放在热水和冷水中 | 热水中先出现浑浊,说明温度越高,反应速率越快 |
| D. | 探究可逆反应的热效应 | 已知CuCl2溶液中存在下列平衡: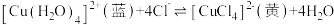 ,取一定浓度的CuCl2溶液,升高温度 ,取一定浓度的CuCl2溶液,升高温度 | 溶液由蓝色变为黄色,说明该反应ΔH<0 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 反应
 ,在某温度下达到平衡,下列各种情况不会使平衡发生移动的是
,在某温度下达到平衡,下列各种情况不会使平衡发生移动的是

 ,在某温度下达到平衡,下列各种情况不会使平衡发生移动的是
,在某温度下达到平衡,下列各种情况不会使平衡发生移动的是| A.温度、容积不变时,通入HCl气体 | B.移走一部分NH4HCO3固体 |
| C.其他条件不变,升高温度 | D.保持压强不变,充入氮气 |
您最近一年使用:0次
名校
解题方法
10 . 巴蜀中学化学兴趣小组对氨的化合物进行研究。回答下列问题:
(1)一定温度下,利用催化剂将NH3分解为N2和H2: △H=+90.8kJ/mol, 且该反应的
△H=+90.8kJ/mol, 且该反应的 ,则该反应自发进行的最低温度为
,则该反应自发进行的最低温度为___________ K。
(2)一定温度下,向刚性容器中充入一定量 NO2,发生反应: ,测得反应体系中气体体积分数与压强之间的关系如图所示:
,测得反应体系中气体体积分数与压强之间的关系如图所示:

①a、b、c三点逆反应速率由大到小的顺序为___________ ,平衡时若保持体积、温度不变,再向体系中加入 定量的Ne,则平衡___________ 移动(填“正向”“逆向”或“不”)。
②a点时 的转化率为
的转化率为___________ (保留三位有效数字)。
③在该条件下反应达平衡后,再充入一定量的 (g),则
(g),则
________ (填“变大”、“变小”或“不变”)。
(3)微生物燃料电池(MFC)是一种现代化氨氮去除技术。如图为MFC 碳氮联合同时去除的转化系统原理示意图。

① 电子的移动方向:沿导线___________ (填“从A到B”或“从B到A”)。
② A极的电极反应式为___________ 。
③ 标准状况下,B极上每生成2.24L气体时,理论上左室A 极区 H⁺的物质的量变化值为___________ mol。(忽略废水中  的影响)
的影响)
④ 好氧微生物反应器中化学反应方程式为___________ 。
(1)一定温度下,利用催化剂将NH3分解为N2和H2:
 △H=+90.8kJ/mol, 且该反应的
△H=+90.8kJ/mol, 且该反应的 ,则该反应自发进行的最低温度为
,则该反应自发进行的最低温度为(2)一定温度下,向刚性容器中充入一定量 NO2,发生反应:
 ,测得反应体系中气体体积分数与压强之间的关系如图所示:
,测得反应体系中气体体积分数与压强之间的关系如图所示:
①a、b、c三点逆反应速率由大到小的顺序为
②a点时
 的转化率为
的转化率为③在该条件下反应达平衡后,再充入一定量的
 (g),则
(g),则
(3)微生物燃料电池(MFC)是一种现代化氨氮去除技术。如图为MFC 碳氮联合同时去除的转化系统原理示意图。

① 电子的移动方向:沿导线
② A极的电极反应式为
③ 标准状况下,B极上每生成2.24L气体时,理论上左室A 极区 H⁺的物质的量变化值为
 的影响)
的影响)④ 好氧微生物反应器中化学反应方程式为
您最近一年使用:0次



