解题方法
1 . 已知 为可逆反应,某小组设计实验测定该反应平衡常数并探究影响化学平衡移动的因素。
为可逆反应,某小组设计实验测定该反应平衡常数并探究影响化学平衡移动的因素。
(1)配制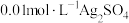 溶液和
溶液和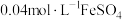 溶液。
溶液。
 基态核外电子排布式为
基态核外电子排布式为_______ ,实验中所需的玻璃仪器有容量瓶、量筒和_______ 。(从下图中选择,写出名称)
将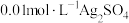 溶液与
溶液与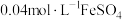 溶液等体积混合,产生灰黑色沉淀,溶液呈黄色,过滤得澄清滤液。(忽略反应引起的溶液体积变化)
溶液等体积混合,产生灰黑色沉淀,溶液呈黄色,过滤得澄清滤液。(忽略反应引起的溶液体积变化)
①甲同学通过测定滤液中 浓度测得K。取
浓度测得K。取 滤液,用
滤液,用 标准溶液滴定滤液中
标准溶液滴定滤液中 ,至滴定终点时消耗
,至滴定终点时消耗 标准溶液
标准溶液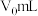 。滴定终点的现象为
。滴定终点的现象为_______ ,反应 的平衡常数
的平衡常数
_______ 。(用含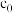 、
、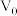 、V的计算式表示)
、V的计算式表示)
②乙同学通过测定滤液中 浓度测得K。取
浓度测得K。取 滤液,加入
滤液,加入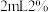 磺基水杨酸溶液,加入
磺基水杨酸溶液,加入 为9~11.5的缓冲溶液,测定吸光度。测得溶液中
为9~11.5的缓冲溶液,测定吸光度。测得溶液中 浓度为
浓度为 ,则
,则 的平衡常数
的平衡常数
_______ 。(用含c的计算式表示)
(3)该小组进一步研究常温下稀释对该平衡移动方向的影响。
用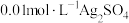 溶液和
溶液和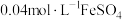 溶液,按下表配制总体积相同的系列溶液,测定平衡时
溶液,按下表配制总体积相同的系列溶液,测定平衡时 浓度,记录数据。
浓度,记录数据。

_______ ,
_______ 。 和
和 存在的关系是
存在的关系是_______ (用含 和
和 的不等式表示),该关系可以作为判断稀释对该平衡移动方向影响的证据。
的不等式表示),该关系可以作为判断稀释对该平衡移动方向影响的证据。
 为可逆反应,某小组设计实验测定该反应平衡常数并探究影响化学平衡移动的因素。
为可逆反应,某小组设计实验测定该反应平衡常数并探究影响化学平衡移动的因素。(1)配制
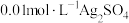 溶液和
溶液和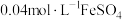 溶液。
溶液。 基态核外电子排布式为
基态核外电子排布式为
| 资料卡片 ⅰ. 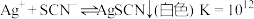 ; ;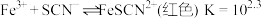 ⅱ.  为9~l1.5条件下 为9~l1.5条件下 和磺基水杨酸 和磺基水杨酸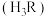 生成稳定的黄色络合物 生成稳定的黄色络合物 , , 可以通过测定吸光度得知其浓度。 可以通过测定吸光度得知其浓度。 |
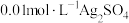 溶液与
溶液与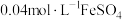 溶液等体积混合,产生灰黑色沉淀,溶液呈黄色,过滤得澄清滤液。(忽略反应引起的溶液体积变化)
溶液等体积混合,产生灰黑色沉淀,溶液呈黄色,过滤得澄清滤液。(忽略反应引起的溶液体积变化)①甲同学通过测定滤液中
 浓度测得K。取
浓度测得K。取 滤液,用
滤液,用 标准溶液滴定滤液中
标准溶液滴定滤液中 ,至滴定终点时消耗
,至滴定终点时消耗 标准溶液
标准溶液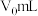 。滴定终点的现象为
。滴定终点的现象为 的平衡常数
的平衡常数
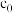 、
、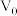 、V的计算式表示)
、V的计算式表示)②乙同学通过测定滤液中
 浓度测得K。取
浓度测得K。取 滤液,加入
滤液,加入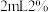 磺基水杨酸溶液,加入
磺基水杨酸溶液,加入 为9~11.5的缓冲溶液,测定吸光度。测得溶液中
为9~11.5的缓冲溶液,测定吸光度。测得溶液中 浓度为
浓度为 ,则
,则 的平衡常数
的平衡常数
(3)该小组进一步研究常温下稀释对该平衡移动方向的影响。
用
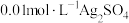 溶液和
溶液和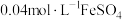 溶液,按下表配制总体积相同的系列溶液,测定平衡时
溶液,按下表配制总体积相同的系列溶液,测定平衡时 浓度,记录数据。
浓度,记录数据。| 序号 | 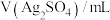 | 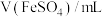 | 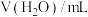 | 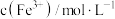 |
| Ⅰ | 10 | 10 |  | |
| Ⅱ | 2 | a | b |  |


 和
和 存在的关系是
存在的关系是 和
和 的不等式表示),该关系可以作为判断稀释对该平衡移动方向影响的证据。
的不等式表示),该关系可以作为判断稀释对该平衡移动方向影响的证据。
您最近半年使用:0次
2 . 铁的化合物在工业脱硫工艺中有着重要应用。
Ⅰ.电解脱硫
煤中的含硫物质主要是FeS2,电解脱硫原理如图。
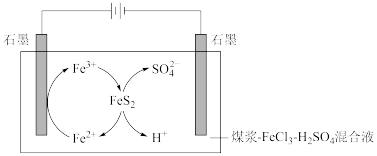
(1)阴极石墨棒上有无色气体产生,该气体是_______ (填化学式)。
(2)研究发现电解时若电压过高,阳极会有副反应发生,造成电解效率降低。某电压下电解100mL煤浆- FeCl3- H2SO4混合液,煤浆中除FeS2外无其它含硫物质, H2SO4浓度为0. 0lmol· L-1,当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c( )=0.02mol·L-1,若忽略电解前后溶液体积变化,电解效率η(
)=0.02mol·L-1,若忽略电解前后溶液体积变化,电解效率η( )=
)=_______ %[η(B)=  ]。
]。
(3)电解法脱硫的优点有_______ (写出一条即可)。
Ⅱ.生物脱硫
(4)Fe3+参与生物脱硫的过程分为吸收和再生两部分。
①吸收:Fe3+将工业废气中的H2S氧化为S
②再生:硫杆菌作用下O2氧化Fe2+再生Fe3+
硫杆菌生长的最佳pH范围是1. 4~3.0,但酸性条件不利于H2S的吸收,结合平衡移动原理解释原因_______ 。
Ⅲ.络合脱硫
(5)碱性条件有利于H2S的吸收,但Fe3+极易形成氢氧化物和硫化物沉淀,因此需将其制成可溶于水的配合物Fe(III)Ln(L表示配体,n表示配位数)。脱硫过程包含如下两步反应:
①碱性条件下,Fe(Ⅲ)Ln氧化H2S生成S8,离子方程式为_______ 。
②O2氧化再生Fe(Ⅲ)Ln,离子方程式为4Fe(Ⅱ)Ln+O2+2H2O=4Fe(Ⅲ)Ln +4OH-。脱硫过程总反应的化学方程式为_______ 。
(6)Na2H2Y (结构简式为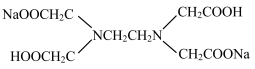 )溶液中,每个H2Y2-电离出2个H+生成酸根Y4-,然后与Fe3+配位。已知该配位反应受溶液pH的影响,若溶液pH太低或太高,分别存在的问题是
)溶液中,每个H2Y2-电离出2个H+生成酸根Y4-,然后与Fe3+配位。已知该配位反应受溶液pH的影响,若溶液pH太低或太高,分别存在的问题是_______ 。
Ⅰ.电解脱硫
煤中的含硫物质主要是FeS2,电解脱硫原理如图。

(1)阴极石墨棒上有无色气体产生,该气体是
(2)研究发现电解时若电压过高,阳极会有副反应发生,造成电解效率降低。某电压下电解100mL煤浆- FeCl3- H2SO4混合液,煤浆中除FeS2外无其它含硫物质, H2SO4浓度为0. 0lmol· L-1,当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c(
 )=0.02mol·L-1,若忽略电解前后溶液体积变化,电解效率η(
)=0.02mol·L-1,若忽略电解前后溶液体积变化,电解效率η( )=
)= ]。
]。(3)电解法脱硫的优点有
Ⅱ.生物脱硫
(4)Fe3+参与生物脱硫的过程分为吸收和再生两部分。
①吸收:Fe3+将工业废气中的H2S氧化为S
②再生:硫杆菌作用下O2氧化Fe2+再生Fe3+
硫杆菌生长的最佳pH范围是1. 4~3.0,但酸性条件不利于H2S的吸收,结合平衡移动原理解释原因
Ⅲ.络合脱硫
(5)碱性条件有利于H2S的吸收,但Fe3+极易形成氢氧化物和硫化物沉淀,因此需将其制成可溶于水的配合物Fe(III)Ln(L表示配体,n表示配位数)。脱硫过程包含如下两步反应:
①碱性条件下,Fe(Ⅲ)Ln氧化H2S生成S8,离子方程式为
②O2氧化再生Fe(Ⅲ)Ln,离子方程式为4Fe(Ⅱ)Ln+O2+2H2O=4Fe(Ⅲ)Ln +4OH-。脱硫过程总反应的化学方程式为
(6)Na2H2Y (结构简式为
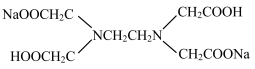 )溶液中,每个H2Y2-电离出2个H+生成酸根Y4-,然后与Fe3+配位。已知该配位反应受溶液pH的影响,若溶液pH太低或太高,分别存在的问题是
)溶液中,每个H2Y2-电离出2个H+生成酸根Y4-,然后与Fe3+配位。已知该配位反应受溶液pH的影响,若溶液pH太低或太高,分别存在的问题是
您最近半年使用:0次
解题方法
3 . 一种从含砷废水[砷主要以亚砷酸 形式存在]中回收砷的工艺流程如图所示。
形式存在]中回收砷的工艺流程如图所示。

已知:
Ⅰ. ;
;
Ⅱ.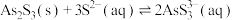 ;
;
Ⅲ.砷酸 在酸性条件下有氧化性,能将氢硝酸氧化为
在酸性条件下有氧化性,能将氢硝酸氧化为 。
。
下列说法错误的是
 形式存在]中回收砷的工艺流程如图所示。
形式存在]中回收砷的工艺流程如图所示。
已知:
Ⅰ.
 ;
;Ⅱ.
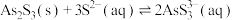 ;
;Ⅲ.砷酸
 在酸性条件下有氧化性,能将氢硝酸氧化为
在酸性条件下有氧化性,能将氢硝酸氧化为 。
。下列说法错误的是
A.“滤渣”为 |
B.“沉砷”过程中 可以用过量的 可以用过量的 代替 代替 |
C.用氧气进行氧化脱硫生成 单质时发生反应 单质时发生反应 |
| D.能用氢碘酸、淀粉溶液检验还原后的溶液中是否仍存在砷酸 |
您最近半年使用:0次
名校
解题方法
4 . 用下列装置不能达到实验目的的是
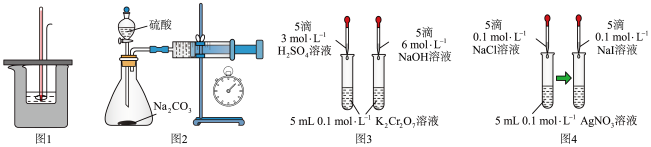

| A.图1:测量强酸强碱中和反应的反应热 |
B.图2:测定 和稀硫酸反应的速率 和稀硫酸反应的速率 |
| C.图3:验证浓度对化学平衡的影响 |
D.图4:证明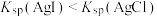 |
您最近半年使用:0次
2023-01-14更新
|
353次组卷
|
3卷引用:广东省佛山市2022~2023学年高二上学期期末考试化学试题
名校
解题方法
5 . 研究碘在不同溶剂中的溶解性。进行实验:
①向试管中放入一小粒碘晶体,再加入蒸馏水,充分溶解后,得到黄色溶液a和少量不溶的碘;
②取5mL溶液a,加入 四氯化碳,振荡,静置,液体分层,下层呈紫色,上层无色;
四氯化碳,振荡,静置,液体分层,下层呈紫色,上层无色;
③将②所得下层溶液全部取出,加入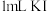 溶液,振荡,静置,下层溶液紫色变浅,上层溶液b呈黄色(颜色比溶液a深)。
溶液,振荡,静置,下层溶液紫色变浅,上层溶液b呈黄色(颜色比溶液a深)。
已知:ⅰ.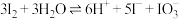 ;
;
ⅱ. 。
。
下列说法不正确 的是
①向试管中放入一小粒碘晶体,再加入蒸馏水,充分溶解后,得到黄色溶液a和少量不溶的碘;
②取5mL溶液a,加入
 四氯化碳,振荡,静置,液体分层,下层呈紫色,上层无色;
四氯化碳,振荡,静置,液体分层,下层呈紫色,上层无色;③将②所得下层溶液全部取出,加入
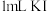 溶液,振荡,静置,下层溶液紫色变浅,上层溶液b呈黄色(颜色比溶液a深)。
溶液,振荡,静置,下层溶液紫色变浅,上层溶液b呈黄色(颜色比溶液a深)。已知:ⅰ.
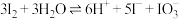 ;
;ⅱ.
 。
。下列说法
A. 是极性溶剂, 是极性溶剂, 是非极性溶剂,非极性的 是非极性溶剂,非极性的 更易溶于 更易溶于 |
| B.②中的下层溶液为碘的四氯化碳溶液 |
C.溶液b中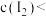 溶液a中 溶液a中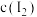 |
D.向①所得浊液中加入 ,使 ,使 增大,反应ⅰ平衡逆向移动,析出 增大,反应ⅰ平衡逆向移动,析出 |
您最近半年使用:0次
2023-01-06更新
|
743次组卷
|
4卷引用:北京市东城区2022-2023学年高三上学期1月期末统一检测化学试卷
解题方法
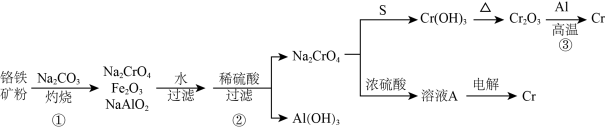
6 . 工业上以铭铁矿(主要成分为 ,含有少量
,含有少量 )为原料制备金属铬的流程如图。下列说法错误的是
)为原料制备金属铬的流程如图。下列说法错误的是
 ,含有少量
,含有少量 )为原料制备金属铬的流程如图。下列说法错误的是
)为原料制备金属铬的流程如图。下列说法错误的是
| A.反应①若在坩埚中进行,可以选择陶瓷坩埚 |
B.生成 的反应中氧化剂和还原剂的物质的量之比为2:1 的反应中氧化剂和还原剂的物质的量之比为2:1 |
C.加入浓硫酸发生反应的离子方程式: |
D.电解溶液 的阴极反应式: 的阴极反应式: |
您最近半年使用:0次
2022高二上·安徽阜阳·竞赛
解题方法
7 . 傲娇,来源日本ACGN的一个词语,指人物为了掩饰害羞腼腆而做出态度强硬高傲表里不一言行的代名词,常用来形容平常说话带刺,态度强硬高傲,但在一定的条件下害臊地黏腻在身边的人物。在化学中也有这样的原理,那就是勒夏特列原理。勒夏特列对于可逆反应平衡的移动总结出的规则在后人的二次总结下总结成了一条:平衡总是朝着能减小外界条件改变对其产生的影响的方向移动。已知相同条件下,每个产物浓度系数次幂的连乘积与每个反应物浓度系数次幂的连乘积之比是个常数。
初中的时候,我们学到的无机基本反应类型共4种:化合反应、分解反应、置换反应和复分解反应。其中,复分解反应发生的条件是:产物中必须存在沉淀、气体或H2O,那么,按照我们初中的知识,有两种物质在水溶液中混合后应该不反应,他们是我们平时吃的食盐A和波尔多液制备中属于盐的物质B。
可是,他们混合后真的不发生反应吗?
让我们来试验一下:
实验I:分别取25mL饱和A溶液与饱和B溶液,倒入小烧杯中,观察到溶液最终呈绿色;经过笔式酸度计测量可知,在此条件下测得酸度计在饱和A溶液溶液中的示数为7.01,在饱和B溶液中的示数为3.22,而在混合溶液中的示数为3.07。
实验II:将实验I中所得溶液均匀分成2份,分别标记成a、b两组,a组放入冰水中,而b组仍保存在小烧杯中。将小烧杯放在加热器上加热,一段时间后观察到a组溶液从绿色变成蓝色,b组溶液绿色加深。
实验III:向两个洁净的试管中分别加入等浓度的Cu(NO3)2溶液和CuCl2溶液,使用同一热源均匀加热,观察到加入CuCl2溶液的试管内溶液绿色逐渐加深。
下列说法正确的是
初中的时候,我们学到的无机基本反应类型共4种:化合反应、分解反应、置换反应和复分解反应。其中,复分解反应发生的条件是:产物中必须存在沉淀、气体或H2O,那么,按照我们初中的知识,有两种物质在水溶液中混合后应该不反应,他们是我们平时吃的食盐A和波尔多液制备中属于盐的物质B。
可是,他们混合后真的不发生反应吗?
让我们来试验一下:
实验I:分别取25mL饱和A溶液与饱和B溶液,倒入小烧杯中,观察到溶液最终呈绿色;经过笔式酸度计测量可知,在此条件下测得酸度计在饱和A溶液溶液中的示数为7.01,在饱和B溶液中的示数为3.22,而在混合溶液中的示数为3.07。
实验II:将实验I中所得溶液均匀分成2份,分别标记成a、b两组,a组放入冰水中,而b组仍保存在小烧杯中。将小烧杯放在加热器上加热,一段时间后观察到a组溶液从绿色变成蓝色,b组溶液绿色加深。
实验III:向两个洁净的试管中分别加入等浓度的Cu(NO3)2溶液和CuCl2溶液,使用同一热源均匀加热,观察到加入CuCl2溶液的试管内溶液绿色逐渐加深。
下列说法正确的是
| A.由实验I可知,A和B能够发生复分解反应。 |
| B.由实验II可知,从蓝色向绿色的转化可逆,且此反应是吸热反应。 |
| C.由实验III可知,反应中影响颜色的因素中有Cl-和Cu2+在溶液中的浓度。 |
| D.若已知铜盐水溶液中Cu元素以[Cu (H2O)4]2+存在,且反应后溶液中没有新离子产生,可推测产物为[CuCl4]2-和H2O。 |
您最近半年使用:0次
9-10高二下·北京·期末
名校
8 . 如图所示,三个烧瓶中分别充满NO2气体并分别装在盛有水的三个烧杯中,在①烧杯中加入CaO,在②烧杯中不加其他任何物质,在③烧杯中加入NH4Cl晶体,发现①中红棕色变深,③中红棕色变浅。已知:2NO2(红棕色) N2O4(无色),下列叙述正确的是
N2O4(无色),下列叙述正确的是
 N2O4(无色),下列叙述正确的是
N2O4(无色),下列叙述正确的是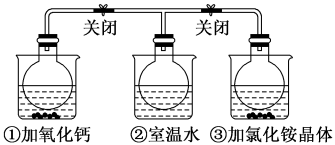
A.2NO2 N2O4是吸热反应 N2O4是吸热反应 |
| B.NH4Cl溶于水时吸收热量 |
| C.①烧瓶中平衡时混合气体的平均相对分子质量增大 |
| D.③烧瓶中气体的压强增大 |
您最近半年使用:0次
2022-08-28更新
|
1130次组卷
|
23卷引用:2010年北京市八一中学高二第二学期期末考试化学试卷
(已下线)2010年北京市八一中学高二第二学期期末考试化学试卷2018版化学(苏教版)高考总复习专题七课时跟踪训练--化学平衡的移动新疆生产建设兵团第二中学2017-2018学年高二上学期第四次月考(期末)化学试题【全国百强校】辽宁省鞍山市第一中学2018-2019学年高二下学期开学考试化学试题新疆自治区生产建设兵团第二中学2018-2019学年高二第一次月考化学试题陕西省延安市第一中学2019-2020学年高二上学期期中考试化学试题(已下线)专题7.2 化学平衡状态 化学平衡移动(练)-《2020年高考一轮复习讲练测》云南省普洱市江城县第一中学2019—2020学年高二上学期期末考试化学试题四川省泸州市泸县第二中学2019-2020学年高二下学期第一次在线月考化学试题黑龙江省大庆市第四中学2019-2020学年高二上学期第一次检测化学试题(已下线)2.3.2+影响化学平衡状态的因素-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)安徽省蚌埠田家炳中学2020-2021学年高二10月月考化学试题江西省上饶市2020-2021学年高二上学期期末教学质量测试化学试题江西省赣州市第一中学2020-2021学年高二下学期开学测试化学试题河南省信阳高级中学2020-2021学年高二下学期回顾测试化学试题福建省三明第一中学2021-2022学年高二上学期第一次月考化学试题福建省莆田市擢英中学2021-2022学年高二上学期第一次月考化学试卷(已下线)2.2.2 浓度商、温度对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)黑龙江省伊春市伊美区第二中学2021-2022学年高二上学期期中考试化学试题广东省深圳市宝安区宝安中学2022-2023学年高一上学期期中考试化学试题新疆奇台县第一中学2022-2023学年高二上学期期中考试化学试题山东省淄博市部分学校联考2022-2023学年高一下学期4月期中考试化学试题(已下线)选择题11-15
名校
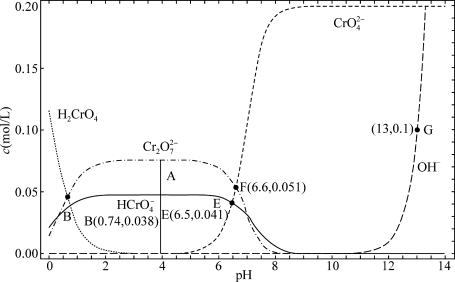
9 . 某温度下,改变0.1mol/L  溶液的pH时,各种含铬元素微粒及
溶液的pH时,各种含铬元素微粒及 浓度变化如图所示(已知
浓度变化如图所示(已知 是二元酸),下列有关说法中,正确的是
是二元酸),下列有关说法中,正确的是
 溶液的pH时,各种含铬元素微粒及
溶液的pH时,各种含铬元素微粒及 浓度变化如图所示(已知
浓度变化如图所示(已知 是二元酸),下列有关说法中,正确的是
是二元酸),下列有关说法中,正确的是
A.该温度下的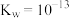 |
B.溶液中存在平衡 ,该温度下此反应的 ,该温度下此反应的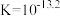 |
C.向0.1mol/L  溶液中加入一定量NaOH固体,溶液橙色变浅 溶液中加入一定量NaOH固体,溶液橙色变浅 |
D.E点溶液中存在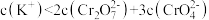 |
您最近半年使用:0次
名校
解题方法
10 . 实验小组同学为探究Fe2+性质,进行如下实验。
【实验Ⅰ】向2mL 溶液滴中几滴
溶液滴中几滴 KSCN溶液,无明显现象,再滴加几滴3%
KSCN溶液,无明显现象,再滴加几滴3% 溶液(用
溶液(用 酸化至
酸化至 ),溶液颜色变红。
),溶液颜色变红。
(1)甲同学通过上述实验分析 具有
具有_______ (填“氧化”或“还原”)性。
乙同学查阅资料发现 与
与 可发生反应,生成无色的配合物。为证实该性质,利用进行如下实验。
可发生反应,生成无色的配合物。为证实该性质,利用进行如下实验。
(2) 的制备:用过量
的制备:用过量 溶液与
溶液与 溶液反应得到
溶液反应得到 ,离子方程式为
,离子方程式为_______ 。
【实验Ⅱ】验证 与
与 发生反应
发生反应_______ 。
(4)从沉淀溶解平衡角度解释实验a和b最终溶液颜色不同的原因是_______ 。
丙同学设计实验进一步证明 可与
可与 反应。
反应。
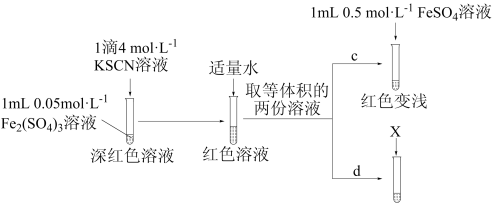
【实验Ⅲ】
①X为_______ 。
②实验能够证实 可与
可与 反应,则应观察到的现象是
反应,则应观察到的现象是_______ 。
(6)实验Ⅲ中若未加适量水稀释,则无法通过现象得出结论。推测加水稀释的目的可能有:使后续实验颜色变化易于观察;降低 ,
,_______ 。
【实验Ⅰ】向2mL
 溶液滴中几滴
溶液滴中几滴 KSCN溶液,无明显现象,再滴加几滴3%
KSCN溶液,无明显现象,再滴加几滴3% 溶液(用
溶液(用 酸化至
酸化至 ),溶液颜色变红。
),溶液颜色变红。(1)甲同学通过上述实验分析
 具有
具有乙同学查阅资料发现
 与
与 可发生反应,生成无色的配合物。为证实该性质,利用进行如下实验。
可发生反应,生成无色的配合物。为证实该性质,利用进行如下实验。(2)
 的制备:用过量
的制备:用过量 溶液与
溶液与 溶液反应得到
溶液反应得到 ,离子方程式为
,离子方程式为【实验Ⅱ】验证
 与
与 发生反应
发生反应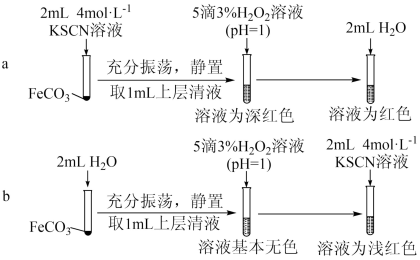
(4)从沉淀溶解平衡角度解释实验a和b最终溶液颜色不同的原因是
丙同学设计实验进一步证明
 可与
可与 反应。
反应。【实验Ⅲ】
①X为
②实验能够证实
 可与
可与 反应,则应观察到的现象是
反应,则应观察到的现象是(6)实验Ⅲ中若未加适量水稀释,则无法通过现象得出结论。推测加水稀释的目的可能有:使后续实验颜色变化易于观察;降低
 ,
,
您最近半年使用:0次
2022-05-30更新
|
1300次组卷
|
11卷引用:北京市东城区2022届高三综合练习(二模)化学试题
北京市东城区2022届高三综合练习(二模)化学试题北京市育才学校2022届高三下学期三模化学试题北京市一零一中学2022届高三三模化学试题(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)北京市北京一零一中学2022-2023学年高三上学期统练7化学试题北京市第八十中学2022-2023学年高三上学期期末测试化学试题(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)实验探究题北京师范大学附属中学预科部2023-2024学年高三上学期12月月考化学试题北京大学附属中学预科部2023-2024学年高三上学期12月阶段练习化学试题



