1 . 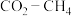 催化重整可获得合成气
催化重整可获得合成气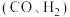 。重整过程中主要反应的热化学方程式为
。重整过程中主要反应的热化学方程式为
反应①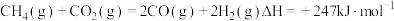
反应②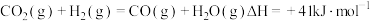
反应③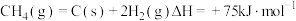
反应④
研究发现在密闭容器中 下,
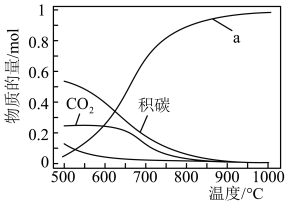
下,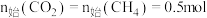 ,平衡时各含碳物种的物质的量随温度的变化如图所示。下列说法正确的是
,平衡时各含碳物种的物质的量随温度的变化如图所示。下列说法正确的是
 催化重整可获得合成气
催化重整可获得合成气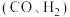 。重整过程中主要反应的热化学方程式为
。重整过程中主要反应的热化学方程式为反应①
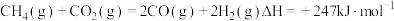
反应②
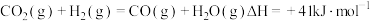
反应③
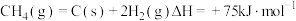
反应④

研究发现在密闭容器中
 下,
下,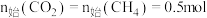 ,平衡时各含碳物种的物质的量随温度的变化如图所示。下列说法正确的是
,平衡时各含碳物种的物质的量随温度的变化如图所示。下列说法正确的是
A.图中a表示 |
B. 的 的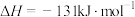 |
C.其他条件不变,在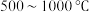 范围,随着温度的升高,平衡时 范围,随着温度的升高,平衡时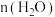 不断增大 不断增大 |
D.当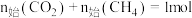 ,其他条件不变时,提高 ,其他条件不变时,提高 的值,能减少平衡时积碳量 的值,能减少平衡时积碳量 |
您最近一年使用:0次
2024-02-13更新
|
1186次组卷
|
4卷引用:江苏省南通市2024届高三上学期第一次调研测试(一模)化学试题
江苏省南通市2024届高三上学期第一次调研测试(一模)化学试题(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)山东省潍坊市2024届高高考模拟训练调研化学试题江苏省南京市2023-2024学年高二下学期期初学业质量调研化学试卷
名校
2 . 氰化氢(HCN,易挥发,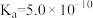 )主要应用于电镀、采矿、药物合成等工业生产。HCN、
)主要应用于电镀、采矿、药物合成等工业生产。HCN、 能抑制人体组织细胞内酶的活性,不能直接排放到环境中。
能抑制人体组织细胞内酶的活性,不能直接排放到环境中。
(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是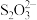 将
将 转化为
转化为 和
和 。验证该转化过程中生成
。验证该转化过程中生成 的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,_______ 。
(2)Cu2+可催化过氧化氢氧化废水中的 。
。
①反应不能在酸性条件下进行,原因是_______
②在含氰废水总量、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得 的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过
的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过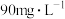 时,
时, 的氧化去除率有所下降,原因是
的氧化去除率有所下降,原因是_______ 。

(3)通过电激发产生 和
和 可处理废水中的
可处理废水中的 ,其可能的反应机理如图所示。
,其可能的反应机理如图所示。
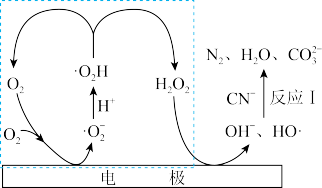
①反应I的离子方程式为_______ 。
②虚线方框内的过程可描述为_______ 。
(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应: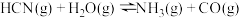

除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是_______ 。

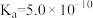 )主要应用于电镀、采矿、药物合成等工业生产。HCN、
)主要应用于电镀、采矿、药物合成等工业生产。HCN、 能抑制人体组织细胞内酶的活性,不能直接排放到环境中。
能抑制人体组织细胞内酶的活性,不能直接排放到环境中。(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是
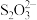 将
将 转化为
转化为 和
和 。验证该转化过程中生成
。验证该转化过程中生成 的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,(2)Cu2+可催化过氧化氢氧化废水中的
 。
。①反应不能在酸性条件下进行,原因是
②在含氰废水总量、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得
 的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过
的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过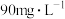 时,
时, 的氧化去除率有所下降,原因是
的氧化去除率有所下降,原因是
(3)通过电激发产生
 和
和 可处理废水中的
可处理废水中的 ,其可能的反应机理如图所示。
,其可能的反应机理如图所示。
①反应I的离子方程式为
②虚线方框内的过程可描述为
(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应:
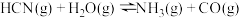

除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是

您最近一年使用:0次
2021-03-26更新
|
1190次组卷
|
6卷引用:江苏省七市(南通、泰州、扬州、徐州、淮安、连云港、宿迁)2021届高三第二次调研考试化学试题
名校
解题方法
3 . 根据下列图示所得结论正确的是
A.  图1表示1 LpH=2的某一元酸加水稀释至V L,pH随lgV的变化,说明该酸是弱酸 图1表示1 LpH=2的某一元酸加水稀释至V L,pH随lgV的变化,说明该酸是弱酸 |
B. 图2表示不同温度下水溶液中H+和OH-浓度的变化的曲线,说明图中温度T2>T1 图2表示不同温度下水溶液中H+和OH-浓度的变化的曲线,说明图中温度T2>T1 |
C. 图3表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,说明图中a点N2的转化率小于b点 图3表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,说明图中a点N2的转化率小于b点 |
D. 图4表示同 一温度下,在不同容积的容器中进行反应2BaO2(s) 图4表示同 一温度下,在不同容积的容器中进行反应2BaO2(s) 2BaO(s)+O2(g), O2的平衡浓度与容器容积的关系,说明改变压强平衡不发生移动 2BaO(s)+O2(g), O2的平衡浓度与容器容积的关系,说明改变压强平衡不发生移动 |
您最近一年使用:0次
2020-03-26更新
|
190次组卷
|
2卷引用:江苏省南通市如皋中学2019~2020学年高三下学期调研测试化学试题
名校
4 . 下列说法正确的是
| A.铜的金属活泼性比铁的弱,可在海轮外壳上镶入若干铜块以减缓其腐蚀 |
B.向0.1 mol·L-1 CH3COONa溶液中加入少量水,溶液中 减小 减小 |
C.一定温度下,增大反应2BaO2(s)  2BaO(s)+O2(g)容器的体积,平衡不移动 2BaO(s)+O2(g)容器的体积,平衡不移动 |
| D.反应TiO2(s) + 2Cl2(g)=TiCl4(g) + O2(g) ΔH>0能自发进行,其原因是ΔS>0 |
您最近一年使用:0次
2017-04-14更新
|
601次组卷
|
2卷引用:2017届江苏省南通市高三第一次模拟考试化学试卷
2011·江苏南通·一模
名校
5 . 向体积为2 L的密闭容器中充入2 mol SO2和1 mol O2,测得起始容器压强为p,一定条件下发生反应:2SO2(g)+O2(g) 2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
 2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是| A.充入2 mol SO3后,SO2的物质的量增大 |
| B.第一次反应达到平衡时共放出热量176.4 kJ |
| C.充入2 mol SO3达到新平衡时,容器内的压强为1.4p |
| D.降低容器的温度可使新平衡时各物质的体积分数与第一次平衡时相同 |
您最近一年使用:0次



