1 . 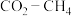 催化重整可获得合成气
催化重整可获得合成气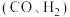 。重整过程中主要反应的热化学方程式为
。重整过程中主要反应的热化学方程式为
反应①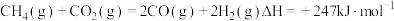
反应②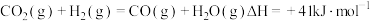
反应③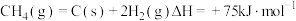
反应④
研究发现在密闭容器中 下,
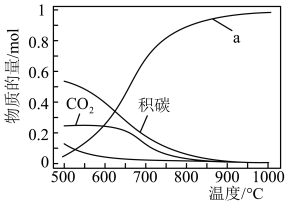
下,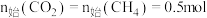 ,平衡时各含碳物种的物质的量随温度的变化如图所示。下列说法正确的是
,平衡时各含碳物种的物质的量随温度的变化如图所示。下列说法正确的是
 催化重整可获得合成气
催化重整可获得合成气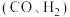 。重整过程中主要反应的热化学方程式为
。重整过程中主要反应的热化学方程式为反应①
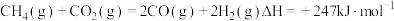
反应②
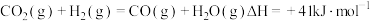
反应③
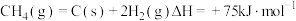
反应④

研究发现在密闭容器中
 下,
下,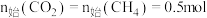 ,平衡时各含碳物种的物质的量随温度的变化如图所示。下列说法正确的是
,平衡时各含碳物种的物质的量随温度的变化如图所示。下列说法正确的是
A.图中a表示 |
B. 的 的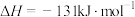 |
C.其他条件不变,在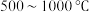 范围,随着温度的升高,平衡时 范围,随着温度的升高,平衡时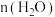 不断增大 不断增大 |
D.当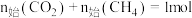 ,其他条件不变时,提高 ,其他条件不变时,提高 的值,能减少平衡时积碳量 的值,能减少平衡时积碳量 |
您最近一年使用:0次
2024-02-13更新
|
1127次组卷
|
4卷引用:江苏省南通市2024届高三上学期第一次调研测试(一模)化学试题
江苏省南通市2024届高三上学期第一次调研测试(一模)化学试题江苏省南京市2023-2024学年高二下学期期初学业质量调研化学试卷(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)山东省潍坊市2024届高高考模拟训练调研化学试题
2 . 一定条件下,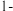 苯基丙炔(
苯基丙炔( )可与
)可与 发生催化加成,反应如下:
发生催化加成,反应如下:不正确 的是
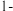 苯基丙炔(
苯基丙炔( )可与
)可与 发生催化加成,反应如下:
发生催化加成,反应如下: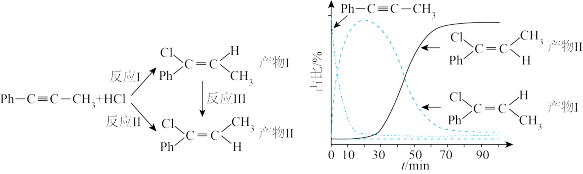
| A.反应焓变:反应I>反应Ⅱ |
| B.反应活化能:反应I<反应Ⅱ |
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例 浓度可增加平衡时产物Ⅱ和产物I的比例 |
| D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ |
您最近一年使用:0次
2023-06-21更新
|
7424次组卷
|
26卷引用:江苏省海安高级中学2023-2024学年高三上学期11月月考化学试题
江苏省海安高级中学2023-2024学年高三上学期11月月考化学试题2023年高考浙江卷化学真题(6月)(已下线)2023年高考浙江卷化学真题(6月)变式题(选择题11-16)(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第23讲化学反应与热能(已下线)第26讲化学反应速率及影响因素(已下线)实验03 探究外界条件对化学平衡移动的影响-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)辽宁省东北育才学校2023-2024学年高二上学期第一次月考化学试题(已下线)考点1 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点2 化学平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)江苏省扬州中学2023-2024学年高三上学期10月月考化学试题浙江省杭州第十四中学2023-2024学年高二上学期 期中考试化学试卷浙江省杭州第二中学2023-2024学年高二上学期期中考试化学试题山东省实验中学2023-2024学年高三上学期11月二诊化学试题(已下线)题型06 反应热的判断及计算-2024年高考化学答题技巧与模板构建陕西省西安中学2023-2024学年高三(实验版)上学期12月练考理科综合试题(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题03 化学平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)(已下线)题型12 化学平衡图表分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)10-2023新东方高二上期中考化学湖南省岳阳市第一中学2023-2024学年高三下学期开学化学试题湖北省沙市中学2023-2024学年高三下学期3月月考化学试题浙江省余姚中学2023-2024学年高二下学期3月质量检测化学试题2024届南昌市第十九中学高三下学期模拟预测化学试题
名校
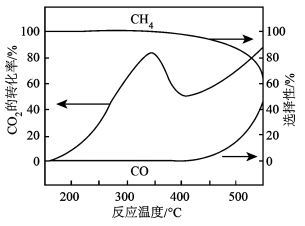
3 . CO2热还原制CH4和CO。在常压、Ru/TiO2催化下,CO2和H2混和气体(体积比1∶4)进行反应,测得CO2转化率、CH4和CO的选择性随温度变化如图所示。
反应I:
反应II: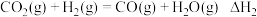
下列说法正确的是

反应I:

反应II:
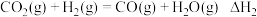
下列说法正确的是
| A.温度为320℃至370℃,CH4的产率降低 |
| B.一定温度下,加入CaO(s)能提高CO的平衡产率 |
| C.其他条件不变,升高温度,CH4的平衡转化率增大 |
D.其他条件不变,在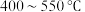 范围,CH4选择性减小是因为反应1平衡逆向移动 范围,CH4选择性减小是因为反应1平衡逆向移动 |
您最近一年使用:0次
4 . 苯乙烯是生产塑料和合成橡胶的重要有机原料,国内外目前生产苯乙烯的方法主要是乙苯用金属氧化物催化脱氢法。
I.直接脱氢法反应方程式为:

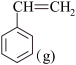 +H2(g)
+H2(g) 
(1)经研究表明,在固定空速(恒压)条件下,该反应存在乙苯的转化率较低、金属氧化物表面存在积碳等问题。若改通650℃水蒸气与乙苯混合气能够有效地解决这些问题,加入水蒸气的作用是___ 。
II.近年来,有研究者发现若将上述生产过程中通入水蒸气改为通入 ,在
,在 气氛中乙苯催化脱氢制苯乙烯更容易进行,
气氛中乙苯催化脱氢制苯乙烯更容易进行,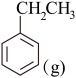 +CO2(g)
+CO2(g) 
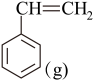
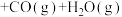
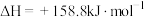
该反应由于催化剂金属氧化物的不同,可能存在三种反应机理
(2)①逆水煤气机理:即 与
与 反应,促进反应正向进行,该反应的热化学方程式为
反应,促进反应正向进行,该反应的热化学方程式为_______ 。
②晶格氧机理:Ar气氛下进行乙苯基本脱氢时消耗晶格氧,催化剂上金属钒(V)的化合价降低;将反应后的催化剂用 再生,可以重新得到高价态的钒(V),补充晶格氧。因此高价态的钒(V)是反应的催化活性中心,
再生,可以重新得到高价态的钒(V),补充晶格氧。因此高价态的钒(V)是反应的催化活性中心, 的作用是保持钒(V)物种处于高价态。催化循环可表示如下:
的作用是保持钒(V)物种处于高价态。催化循环可表示如下:

则上述机理图中物质X为_______ 。(填“ ”或“
”或“ ”)
”)
③550℃ 耦合乙苯
耦合乙苯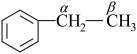 脱氢
脱氢
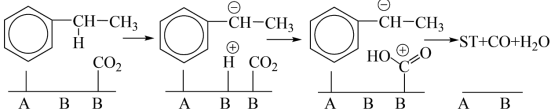
由图中过程可知,酸性位和碱性位都是反应的活性中心,乙苯脱氢是催化剂上的酸碱位协同作用的结果。酸性位上发生乙苯分子的吸附活化;弱碱性位参与脱去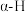 ,而强碱性位活化
,而强碱性位活化 ,被活化的
,被活化的 很容易和
很容易和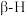 反应,生成苯乙烯。由于催化剂的碱性不同,在
反应,生成苯乙烯。由于催化剂的碱性不同,在 上发生的是直接脱氢,而在
上发生的是直接脱氢,而在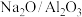 上发生的基本上是耦合脱氢的原因是
上发生的基本上是耦合脱氢的原因是_______ 。
(3)从资源综合利用角度分析,乙苯与 混合制苯乙烯的优点是:
混合制苯乙烯的优点是:_______ 。
(4)含苯乙烯的废水会对环境造成严重的污染,可采用电解法进行处理,其工作原理如图(电解液是含苯乙烯和硫酸的废水,pH=6.2),已知: (羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成
(羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成 和
和 。
。
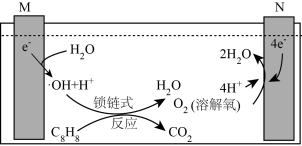
若电路中通过10mol电子,则有_______ g苯乙烯被羟基自由基完全氧化成 和
和 。
。
I.直接脱氢法反应方程式为:


 +H2(g)
+H2(g) 
(1)经研究表明,在固定空速(恒压)条件下,该反应存在乙苯的转化率较低、金属氧化物表面存在积碳等问题。若改通650℃水蒸气与乙苯混合气能够有效地解决这些问题,加入水蒸气的作用是
II.近年来,有研究者发现若将上述生产过程中通入水蒸气改为通入
 ,在
,在 气氛中乙苯催化脱氢制苯乙烯更容易进行,
气氛中乙苯催化脱氢制苯乙烯更容易进行, +CO2(g)
+CO2(g) 

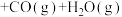
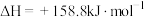
该反应由于催化剂金属氧化物的不同,可能存在三种反应机理
(2)①逆水煤气机理:即
 与
与 反应,促进反应正向进行,该反应的热化学方程式为
反应,促进反应正向进行,该反应的热化学方程式为②晶格氧机理:Ar气氛下进行乙苯基本脱氢时消耗晶格氧,催化剂上金属钒(V)的化合价降低;将反应后的催化剂用
 再生,可以重新得到高价态的钒(V),补充晶格氧。因此高价态的钒(V)是反应的催化活性中心,
再生,可以重新得到高价态的钒(V),补充晶格氧。因此高价态的钒(V)是反应的催化活性中心, 的作用是保持钒(V)物种处于高价态。催化循环可表示如下:
的作用是保持钒(V)物种处于高价态。催化循环可表示如下:
则上述机理图中物质X为
 ”或“
”或“ ”)
”)③550℃
 耦合乙苯
耦合乙苯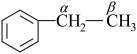 脱氢
脱氢
由图中过程可知,酸性位和碱性位都是反应的活性中心,乙苯脱氢是催化剂上的酸碱位协同作用的结果。酸性位上发生乙苯分子的吸附活化;弱碱性位参与脱去
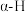 ,而强碱性位活化
,而强碱性位活化 ,被活化的
,被活化的 很容易和
很容易和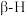 反应,生成苯乙烯。由于催化剂的碱性不同,在
反应,生成苯乙烯。由于催化剂的碱性不同,在 上发生的是直接脱氢,而在
上发生的是直接脱氢,而在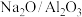 上发生的基本上是耦合脱氢的原因是
上发生的基本上是耦合脱氢的原因是(3)从资源综合利用角度分析,乙苯与
 混合制苯乙烯的优点是:
混合制苯乙烯的优点是:(4)含苯乙烯的废水会对环境造成严重的污染,可采用电解法进行处理,其工作原理如图(电解液是含苯乙烯和硫酸的废水,pH=6.2),已知:
 (羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成
(羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成 和
和 。
。
若电路中通过10mol电子,则有
 和
和 。
。
您最近一年使用:0次
5 . 化学常用图像直观地描述化学反应的进程或结果。下列与NH3有关的图像描述正确的是


A.图①表示 在t1时刻扩大容器体积,v逆随时间变化的曲线 在t1时刻扩大容器体积,v逆随时间变化的曲线 |
B.图②表示 平衡时NH3体积分数随起始 平衡时NH3体积分数随起始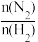 变化的曲线,则转化率:aA(H2)=aB(H2) 变化的曲线,则转化率:aA(H2)=aB(H2) |
| C.图③表示25℃时分别稀释pH=1的NaOH溶液和氨水时溶液pH的变化,曲线Ⅰ表示氨水 |
| D.图④可表示CH3COOH溶液中通入NH3至过量的过程中溶液导电性的变化 |
您最近一年使用:0次
6 . 硫及其化合物之间的转化在生产中有着重要作用。接触法制硫酸中, 制取
制取 的反应为
的反应为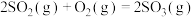
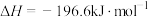 。反应在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
。反应在有、无催化剂条件下的能量变化如图所示。下列说法正确的是

 制取
制取 的反应为
的反应为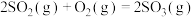
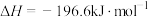 。反应在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
。反应在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
A. 催化时,该反应的速率取决于步骤① 催化时,该反应的速率取决于步骤① |
B.使用 作催化剂同时降低了正、逆反应的活化能 作催化剂同时降低了正、逆反应的活化能 |
C.其他条件相同,增大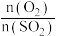 , , 的转化率下降 的转化率下降 |
D.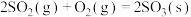 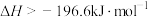 |
您最近一年使用:0次
解题方法
7 . 研究CO和 的应用对构建生态文明型社会具有重要意义。
的应用对构建生态文明型社会具有重要意义。
(1)用CO和 为原料可制取甲醇:
为原料可制取甲醇:
 。恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)充入一定量的CO和
。恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)充入一定量的CO和 。
。
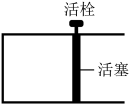
①能够说明反应已经处于平衡状态的是:_________ 。
A.容器内CO的物质的量浓度不变
B.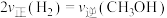
C.容器内气体压强不变
D.混合气体的密度不变
E.容器内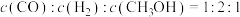
②若其他条件均保持不变,起始时拔去活栓,让活塞自由移动,则平衡时 的体积百分含量将
的体积百分含量将_________ (填“增大”、“减少”或“不变”)
(2)二氧化碳是潜在的碳资源,可以与 合成二甲醚(化学式为
合成二甲醚(化学式为 ),也可以与
),也可以与 直接转化为乙酸。
直接转化为乙酸。
①一种“二甲醚燃料电池”的结构如图所示,以熔融的碳酸钾为电解质,总反应为: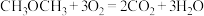 。该电池工作时,负极的电极反应为
。该电池工作时,负极的电极反应为_________ 。

②以二氧化钛表面覆盖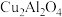 为催化剂,可以将
为催化剂,可以将 和
和 直接转化为乙酸。在不同温度下乙酸的生成速率如图所示。在250~300℃时,温度升高而乙酸的生成速率快速降低,原因可能是:
直接转化为乙酸。在不同温度下乙酸的生成速率如图所示。在250~300℃时,温度升高而乙酸的生成速率快速降低,原因可能是:_________ 。

 的应用对构建生态文明型社会具有重要意义。
的应用对构建生态文明型社会具有重要意义。(1)用CO和
 为原料可制取甲醇:
为原料可制取甲醇:
 。恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)充入一定量的CO和
。恒温时,向如图所示的密闭容器中(活栓已经固定住活塞)充入一定量的CO和 。
。
①能够说明反应已经处于平衡状态的是:
A.容器内CO的物质的量浓度不变
B.
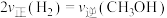
C.容器内气体压强不变
D.混合气体的密度不变
E.容器内
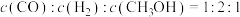
②若其他条件均保持不变,起始时拔去活栓,让活塞自由移动,则平衡时
 的体积百分含量将
的体积百分含量将(2)二氧化碳是潜在的碳资源,可以与
 合成二甲醚(化学式为
合成二甲醚(化学式为 ),也可以与
),也可以与 直接转化为乙酸。
直接转化为乙酸。①一种“二甲醚燃料电池”的结构如图所示,以熔融的碳酸钾为电解质,总反应为:
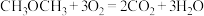 。该电池工作时,负极的电极反应为
。该电池工作时,负极的电极反应为
②以二氧化钛表面覆盖
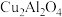 为催化剂,可以将
为催化剂,可以将 和
和 直接转化为乙酸。在不同温度下乙酸的生成速率如图所示。在250~300℃时,温度升高而乙酸的生成速率快速降低,原因可能是:
直接转化为乙酸。在不同温度下乙酸的生成速率如图所示。在250~300℃时,温度升高而乙酸的生成速率快速降低,原因可能是:
您最近一年使用:0次
8 . 某MOFs多孔材料孔径大小和形状恰好将N2O4“固定”,能高选择性吸附NO2。废气中的NO2被吸附后,经处理能全部转化为HNO3。原理示意图如下。

已知:2NO2(g)⇌N2O4(g)ΔH<0。下列说法不正确 的是

已知:2NO2(g)⇌N2O4(g)ΔH<0。下列说法
A.使用多孔材料不能改变2NO2(g) N2O4(g)的焓变 N2O4(g)的焓变 |
B.使用多孔材料能促进2NO2(g) N2O4(g)平衡正向移动 N2O4(g)平衡正向移动 |
| C.加入H2O和O2,发生化学反应方程式为:2N2O4+O2+2H2O=4HNO3 |
| D.温度升高会提高NO2的平衡转化率 |
您最近一年使用:0次
2022-11-27更新
|
531次组卷
|
5卷引用:江苏省南通市海安市2022-2023学年高三上学期11月期中化学试题
江苏省南通市海安市2022-2023学年高三上学期11月期中化学试题江苏省四所名校2022-2023学年高三上学期期中联考化学试题(已下线)专题卷11 化学反应速率与化学平衡归因分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)广东省湛江市普通高中2023届高三下学期4月模拟考试化学试题第二章 第二节 化学平衡 第3课时 影响化学平衡的因素
解题方法
9 . 硝化法是一种古老的生,产硫酸的方法,同时实现了氮氧化物的循环转化,主要反应为:NO2(g)+SO2(g)  SO3(g)+NO(g) ∆H= -41.8kJ·mol-1。SO2 和SO3都是呈酸性的物质,是大气污染,环境酸化的主要污染物。SO3 与水会生成重要的工业原料H2SO4。对于反应NO2(g)+ SO2(g)
SO3(g)+NO(g) ∆H= -41.8kJ·mol-1。SO2 和SO3都是呈酸性的物质,是大气污染,环境酸化的主要污染物。SO3 与水会生成重要的工业原料H2SO4。对于反应NO2(g)+ SO2(g)  SO3(g)+NO(g) ∆H= -41.8kJ·mol-1,下列说法正确的是
SO3(g)+NO(g) ∆H= -41.8kJ·mol-1,下列说法正确的是
 SO3(g)+NO(g) ∆H= -41.8kJ·mol-1。SO2 和SO3都是呈酸性的物质,是大气污染,环境酸化的主要污染物。SO3 与水会生成重要的工业原料H2SO4。对于反应NO2(g)+ SO2(g)
SO3(g)+NO(g) ∆H= -41.8kJ·mol-1。SO2 和SO3都是呈酸性的物质,是大气污染,环境酸化的主要污染物。SO3 与水会生成重要的工业原料H2SO4。对于反应NO2(g)+ SO2(g)  SO3(g)+NO(g) ∆H= -41.8kJ·mol-1,下列说法正确的是
SO3(g)+NO(g) ∆H= -41.8kJ·mol-1,下列说法正确的是A.其他条件相同,增大 ,NO2的转化率增大 ,NO2的转化率增大 |
| B.使用合适的催化剂能缩短该反应到达平衡的时间 |
| C.1mol NO2(g)与1mol SO2充分反应,放出41.8kJ的热量 |
| D.当容器中SO2、SO3的分子数之比等于1:1时,说明该反应到达化学平衡状态 |
您最近一年使用:0次
名校
解题方法
10 . 现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的正反应为____ 热反应,且m+n____ p(填“>”、“=”或“<”)。
(2)若容积不变加入B,则A的转化率____ ,B的转化率____ 。(填“增大”、“减小”或“不变”,下同)
(3)若升高温度,则平衡时B、C的浓度之比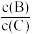 将
将____ 。
(4)若加入催化剂,平衡时气体混合物的总物质的量____ 。
(5)若B是有色物质,A、C均无色,体积不变、加入C时混合物颜色____ ;维持容器内压强不变,充入氖气时,混合物颜色____ 。(填“变深”、“变浅”或“不变”)
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)该反应的正反应为
(2)若容积不变加入B,则A的转化率
(3)若升高温度,则平衡时B、C的浓度之比
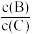 将
将(4)若加入催化剂,平衡时气体混合物的总物质的量
(5)若B是有色物质,A、C均无色,体积不变、加入C时混合物颜色
您最近一年使用:0次
2022-09-27更新
|
182次组卷
|
2卷引用:江苏省如皋中学2022-2023学年高二上学期8月综合测试化学试题



