17. 钴的氧化物常用于制取催化剂和颜科等。以钴矿[主要成分是CoO、Co
2O
3、Co(OH)
3,还含SiO
2及少量A1
2O
3、Fe
2O
3、CuO及MnO
2等]为原料可制取钴的氧化物。
(1)一种钴氧化物晶胞如图1所示,该氧化物中钴离子基态核外电子排布式为
_______。

(2)利用钴矿制取钴的氧化物的主要步骤如下:
①浸取:用盐酸和Na
2SO
3溶液浸取钴矿,浸取液中含有Al
3+、Fe
2+、Co
2+、Cu
2+、Mn
2+、Cl
-、

等离子。写出Co
2O
3发生反应的离子方程式
_______。
②除杂:向浸取液中先加入足量NaClO,氧化Fe
2+,再加入NaOH调节pH除去A1
3+、Fe
3+、Cu
2+。有关沉淀数据如表(“完全沉淀时金属离子浓度≤10×10
-5mol/L)。
| 沉淀 | Al(OH)3 | Fe (OH)3 | Co(OH)2 | Cu(OH)2 | Mn(OH)2 |
| 恰好完全沉淀时pH | 5.2 | 2.8 | 9.4 | 6.7 | 10.1 |
若浸取液中c(Co
2+)=0.1mol/L,则须调节溶液pH的范围是
_______(加入NaClO
3和NaOH时,溶液的体积变化忽略)。
③萃取、反萃取:向除杂后的溶液中,加入某有机酸萃取剂(HA)
2,发生反应:Co
2++n (HA)
2
CoA
2·(n-1) (HA)
2+2H
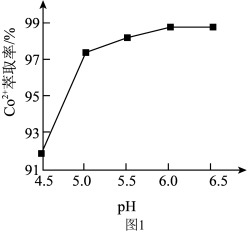
+。实验测得:当溶液pH处于4.5~6.5范围内,Co
2+萃取率随溶液pH的增大而增大(如图2所示),其原因是
_______。向萃取所得有机相中加入H
2SO
4,反萃取得到水相。该工艺中设计萃取、反萃取的目的是
_______。
④沉钴、热分解:向反萃取后得到的水相中加入(NH
4)
2C
2O
4溶液,过滤、洗涤、干燥,得到CoC
2O
4·2H
2O晶体。图为二水合草酸钴(CoC
2O
4·2H
2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物。
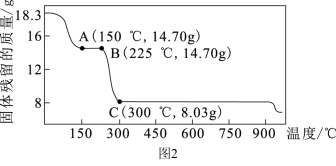
通过计算确定C点剩余固体的化学成分为
_______(填化学式)。试写出B点对应的物质与O
2在225~300℃发生反应的化学方程式:
_______。