解题方法
1 . 已知,25℃时K2Cr2O7溶液中存在以下平衡:
①Cr2O (aq)+H2O(l)
(aq)+H2O(l) 2CrO
2CrO (aq)+2H+(aq) K1=3.27×10-15
(aq)+2H+(aq) K1=3.27×10-15
②Cr2O (aq)+H2O(l)
(aq)+H2O(l) 2HCrO
2HCrO (aq) K2=3.0×10-2
(aq) K2=3.0×10-2
③HCrO (aq)
(aq) CrO
CrO (aq)+H+(aq) K3
(aq)+H+(aq) K3
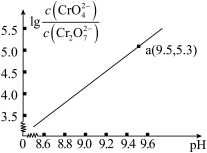
25℃时,0.1mol/LK2Cr2O7溶液中,lg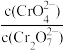 随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
①Cr2O
 (aq)+H2O(l)
(aq)+H2O(l) 2CrO
2CrO (aq)+2H+(aq) K1=3.27×10-15
(aq)+2H+(aq) K1=3.27×10-15②Cr2O
 (aq)+H2O(l)
(aq)+H2O(l) 2HCrO
2HCrO (aq) K2=3.0×10-2
(aq) K2=3.0×10-2③HCrO
 (aq)
(aq) CrO
CrO (aq)+H+(aq) K3
(aq)+H+(aq) K325℃时,0.1mol/LK2Cr2O7溶液中,lg
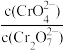 随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
随pH的变化关系如图所示(lg3.27=0.52,10-0.78=0.17)。下列说法错误的是
A.0.1mol/LK2Cr2O7溶液中,加入少量的HI气体,c(CrO )增大 )增大 |
| B.溶液颜色不再变化,可以判断该体系达到平衡 |
C.a点溶液中离子浓度关系:c(K+)>c(CrO )>c(Cr2O )>c(Cr2O )>c(H+) )>c(H+) |
D.反应③的化学平衡常数K3=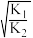 |
您最近半年使用:0次
2023-04-12更新
|
1220次组卷
|
6卷引用:湘豫名校联考2022-2023学年高三上学期一轮复习诊断考试(二)化学试题
湘豫名校联考2022-2023学年高三上学期一轮复习诊断考试(二)化学试题(已下线)专题十二化学反应速率与平衡(已下线)专题21 电解质溶液图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)仿真卷01-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点09 盘点溶液中的“四大”平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)2023年高考山东卷化学真题变式题(不定项选择题)
名校
2 . 一定条件下,某密闭容器内存在下列平衡:
 ;则下列有关说法正确的是
;则下列有关说法正确的是

 ;则下列有关说法正确的是
;则下列有关说法正确的是| A.缩小反应容器的体积,使压强增大,平衡不移动,混合气体颜色深浅不变 |
| B.保持容积不变,改变体系温度,体系颜色一定发生变化 |
| C.保持容积不变,继续充入HI气体,则HI的转化率将减小 |
D.保持温度不变,若使体系颜色变浅,则改变条件的瞬间 和 和 都将减小 都将减小 |
您最近半年使用:0次
22-23高二上·浙江杭州·期中
3 . 下列实验方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究反应物浓度对化学反应速率的影响 | 分别取10mL 0.lmol/LNa2S2O3溶液和5mL 0. lmol/L Na2S2O3溶液、5mL蒸馏水于两支试管中,然后同时加入10mL 0.1mol/LH2SO4溶液 | 前者出现浑浊的时间更短,说明增大Na2S2O3浓度,可以加快反应速率 |
| B | 探究压强对化学反应速率的影响 | 在容积不变的密闭容器中发生反应:N2(g) +3H2(g) 2NH3(g) 向其中通入氩气,反应速率不变 2NH3(g) 向其中通入氩气,反应速率不变 | 化学反应速率不受压强影响 |
| C | 探究温度对化学反应速率的影响 | 将装有NO2和N2O4混合气体的连同球分别浸泡在冰水和热水中2NO2(g)(红棕色) N2O4(g)(无色),△H< 0 N2O4(g)(无色),△H< 0 | 热水中气体颜色浅,冰水中颜色深 |
| D | 探究KI与FeCl3反应的限度 | 取1mL.0.1mol/LKI溶液于试管中,加入5mL0.1mol/L FeCl3溶液,充分反应后滴入5滴15%KSCN溶液 | 若溶液变血红色,则KI与FeCl3的反应有一定限度 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
21-22高二·浙江·期中
4 . 下列事实不能用勒夏特列原理解释的是
| A.工业生产硫酸的过程中使用适当过量的氧气,以提高二氧化硫的转化率 |
| B.红棕色的NO2加压后颜色先变深再变浅 |
| C.光照新制氯水时,溶液的pH逐渐减小 |
D.硫酸工业中的重要反应2SO2+O2 2SO3,工业上常加入V2O5做催化剂 2SO3,工业上常加入V2O5做催化剂 |
您最近半年使用:0次
名校
5 . 图1表示:以相同的滴速分别向同体积的蒸馏水和 溶液中滴入
溶液中滴入 溶液,氯离子浓度随氯化钠加入量的变化关系。图2表示:
溶液,氯离子浓度随氯化钠加入量的变化关系。图2表示: 溶液中氯离子浓度随温度变化关系。结合信息,下列推断合理的是
溶液中氯离子浓度随温度变化关系。结合信息,下列推断合理的是

已知: 溶液中存在平衡①:
溶液中存在平衡①: (蓝色)
(蓝色) 溶液呈绿色,溶液中存在平衡②:
溶液呈绿色,溶液中存在平衡②:
 溶液中滴入
溶液中滴入 溶液,氯离子浓度随氯化钠加入量的变化关系。图2表示:
溶液,氯离子浓度随氯化钠加入量的变化关系。图2表示: 溶液中氯离子浓度随温度变化关系。结合信息,下列推断合理的是
溶液中氯离子浓度随温度变化关系。结合信息,下列推断合理的是
已知:
 溶液中存在平衡①:
溶液中存在平衡①: (蓝色)
(蓝色) 溶液呈绿色,溶液中存在平衡②:
溶液呈绿色,溶液中存在平衡②:
| A.平衡①的存在是图1中两条曲线没有重合的主要原因 |
| B.由图2可知平衡②为放热反应 |
| C.平衡②是无水硫酸铜粉末和硫酸铜溶液颜色不同的原因 |
D. 溶液加水稀释,平衡②溶液逐渐变为蓝色 溶液加水稀释,平衡②溶液逐渐变为蓝色 |
您最近半年使用:0次
2023-03-25更新
|
314次组卷
|
2卷引用: 山东省青岛第二中学2022-2023学年高三上学期第二次月考化学试题
6 . 向恒温恒容密闭容器中通入2mol  和1mol
和1mol  ,反应
,反应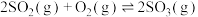 达到平衡后,再通入一定量
达到平衡后,再通入一定量 ,达到新平衡时,下列有关判断
,达到新平衡时,下列有关判断错误 的是
 和1mol
和1mol  ,反应
,反应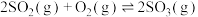 达到平衡后,再通入一定量
达到平衡后,再通入一定量 ,达到新平衡时,下列有关判断
,达到新平衡时,下列有关判断A. 的平衡浓度增大 的平衡浓度增大 | B.反应平衡常数增大 |
| C.正向反应速率增大 | D. 的转化总量增大 的转化总量增大 |
您最近半年使用:0次
2023-03-23更新
|
4803次组卷
|
14卷引用:2022年天津高考化学真题
2022年天津高考化学真题(已下线)题型24 单反应体系中的化学平衡(已下线)专题15 化学反应速率和化学平衡(已下线)专题15 化学反应速率和化学平衡(已下线)第13练 化学反应速率与化学平衡的综合考查 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)实验02 定性与定量研究影响化学反应速率的因素-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)(已下线)实验03 探究外界条件对化学平衡移动的影响-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)(已下线)第3讲 化学平衡计算 平衡常数课时3影响化学平衡的因素课堂例题云南省中央民族大学附属中学昆明五华实验学校2023-2024学年高二上学期期中考试化学试题天津市武清区城关中学2023-2024学年高三上学期第二次阶段性练习化学试题(已下线)题型13 化学平衡常数的计算及应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)湖南省岳阳市华容县2023-2024学年高二上学期期末考试化学试题
名校
解题方法
7 . 重铬酸铵[(NH4)2Cr2O7]可用作媒染剂和有机合成催化剂,具有强氧化性。实验室将NH3通入重铬酸(H2Cr2O7)溶液中制备[(NH4)2Cr2O7]的装置如图所示(夹持装置略)。回答下列问题:
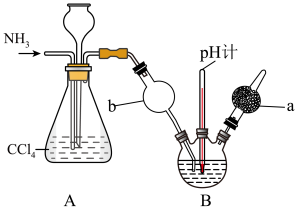
已知: (橙色)+H2O⇌2
(橙色)+H2O⇌2 (黄色)+2H+。
(黄色)+2H+。
(1)仪器a的名称是_______ ,A装置的作用为_______ 。
(2)在试管中加入少量(NH4)2Cr2O7固体,加水溶解,再滴加足量KOH浓溶液,振荡,微热,观察到的主要现象是_______ 。
(3)实验室常用甲醛法测定含(NH4)2Cr2O7的产品中(NH4)2Cr2O7的质量分数,其反应原理为2Ba2++ +H2O=2BaCrO4+2H+、4
+H2O=2BaCrO4+2H+、4 +6HCHO=(CH2)6N4H++6H2O+3H+,然后用NaOH标准溶液滴定反应生成的酸。
+6HCHO=(CH2)6N4H++6H2O+3H+,然后用NaOH标准溶液滴定反应生成的酸。
实验步骤:
I.称取样品12.00g,配成250mL溶液。
II.量取25.00mL样品溶液,用氯化钡溶液使Cr2O72-完全沉淀后,加入足量的20%中性甲醛溶液,摇匀,静置5min。
III.以酚酞作指示剂,用1.00mol·L-1的NaOH标准溶液滴定,记录数据。
IV.重复步骤II、III2~3次,处理数据。
①滴定终点的颜色变化为_______ 。
②用_______ (填“酸式”或“碱式”)滴定管量取25.00mL样品溶液于250mL锥形瓶中。
③与NaOH反应时,1mol(CH2)6N4H+与1molH+相当,步骤III中(CH2)6N4H+与NaOH发生反应的离子方程式是_______ 。
④若实验平均消耗NaOH溶液的体积为16.00mL,则所得产物中(NH4)2Cr2O7(摩尔质量为252g·mol-1)的质量分数为_______ %。
⑤若滴定终点时仰视读数,则测定的质量分数将_______ (填“偏大”、“偏小”或“不变”)。

已知:
 (橙色)+H2O⇌2
(橙色)+H2O⇌2 (黄色)+2H+。
(黄色)+2H+。(1)仪器a的名称是
(2)在试管中加入少量(NH4)2Cr2O7固体,加水溶解,再滴加足量KOH浓溶液,振荡,微热,观察到的主要现象是
(3)实验室常用甲醛法测定含(NH4)2Cr2O7的产品中(NH4)2Cr2O7的质量分数,其反应原理为2Ba2++
 +H2O=2BaCrO4+2H+、4
+H2O=2BaCrO4+2H+、4 +6HCHO=(CH2)6N4H++6H2O+3H+,然后用NaOH标准溶液滴定反应生成的酸。
+6HCHO=(CH2)6N4H++6H2O+3H+,然后用NaOH标准溶液滴定反应生成的酸。实验步骤:
I.称取样品12.00g,配成250mL溶液。
II.量取25.00mL样品溶液,用氯化钡溶液使Cr2O72-完全沉淀后,加入足量的20%中性甲醛溶液,摇匀,静置5min。
III.以酚酞作指示剂,用1.00mol·L-1的NaOH标准溶液滴定,记录数据。
IV.重复步骤II、III2~3次,处理数据。
①滴定终点的颜色变化为
②用
③与NaOH反应时,1mol(CH2)6N4H+与1molH+相当,步骤III中(CH2)6N4H+与NaOH发生反应的离子方程式是
④若实验平均消耗NaOH溶液的体积为16.00mL,则所得产物中(NH4)2Cr2O7(摩尔质量为252g·mol-1)的质量分数为
⑤若滴定终点时仰视读数,则测定的质量分数将
您最近半年使用:0次
名校
8 . 下列说法正确的是
A.恒温恒容下, ,当混合气体的密度不再发生变化时,能表明该反应达到平衡状态 ,当混合气体的密度不再发生变化时,能表明该反应达到平衡状态 |
B.恒温恒容下, 达到平衡,移走部分N,平衡向正反应方向移动 达到平衡,移走部分N,平衡向正反应方向移动 |
C.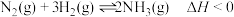 ,反应达至平衡后,升温,则反应速率 ,反应达至平衡后,升温,则反应速率 和 和 的平衡转化率均增大 的平衡转化率均增大 |
D.实验室制氢气,为了加快反应速率,可在稀硫酸中加少量 固体 固体 |
您最近半年使用:0次
2023-02-24更新
|
218次组卷
|
2卷引用:浙江省杭州第二中学2022-2023学年高二上学期期中考试化学(B卷)试题
9 . 在硫酸工业中,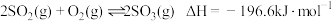 。在如下表所示温度、压强下,反应达平衡时
。在如下表所示温度、压强下,反应达平衡时 的转化率。
的转化率。
下列相关叙述正确的是
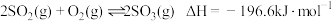 。在如下表所示温度、压强下,反应达平衡时
。在如下表所示温度、压强下,反应达平衡时 的转化率。
的转化率。温度/℃ | 平衡时 | ||
|
|
| |
450 | 97.5 | 99.2 | 99.7 |
550 | 85.6 | 94.9 | 98.3 |
A.实际生产中应采用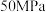 高压 高压 |
B.通入过量 可增大该反应的平衡常数 可增大该反应的平衡常数 |
C.回收并循环使用尾气中的 可提高其转化率 可提高其转化率 |
D.低温、高压条件下有利于提高 的反应速率 的反应速率 |
您最近半年使用:0次
名校
10 . 下列措施或事实不能用勒夏特列原理解释的是
| A.实验室常用排饱和食盐水的方法收集Cl2 |
| B.将一氧化碳中毒者放入高压氧舱,增大氧气浓度缓解病情 |
| C.啤酒瓶开启后,马上泛起大量泡沫 |
| D.工业合成氨在高温条件下进行 |
您最近半年使用:0次
2023-02-23更新
|
195次组卷
|
3卷引用:四川省雅安市2022-2023学年高二上学期期末考试化学试题
四川省雅安市2022-2023学年高二上学期期末考试化学试题广西博白县中学2022-2023学年高二下学期3月月考化学试题(已下线)第05讲 影响化学平衡的因素-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)