名校
1 . 氯化银的还原精炼技术是银回收精炼过程中的重要环节,有多种方法还原精炼。
(一)、甲小组选择强还原剂:肼(N2H4)。
在还原AgCl制取银的过程中有对环境无污染气体产生。
(1)①写出相关的化学反应方程式:___________ 。
【资料】工业上一般先向氯化银中加入氨水浆化,然后用N2H4还原,可有利于反应的进行。
②写出浆化过程中的离子反应式:___________ 。从N2H4发生的氧化反应(半反应)的角度分析加入氨水的作用___________ 。
(二)、乙小组换用铁粉还原AgCl制取银,探究其过程和影响因素。
【实验A】在试管中加入NaCl溶液,然后滴入AgNO3溶液,产生白色沉淀。滤出白色沉淀,继续实验如下:
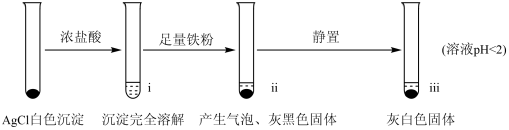
【资料】①AgCl+Cl- AgCl
AgCl
②Fe3++4Cl- FeCl
FeCl
(2)检验ⅱ中产物
①取ⅱ中上层清液,滴加K3[Fe(CN)6]溶液,___________ (填现象),说明溶液中含有Fe2+。
②取ⅱ中少量灰黑色固体,洗涤后将固体等分两份。取其中一份,加入___________ (填试剂)溶解,再加入NaCl溶液生成白色沉淀,证明灰黑色固体中含有Ag。向另一份加入KI溶液,无明显现象。
(3)检验ⅲ中产物。
①取ⅲ中灰白色固体,洗涤。进行如下实验,确认灰白色固体中含AgCl:
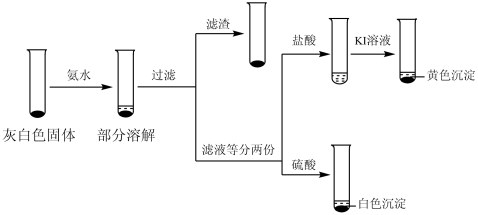
滤液加盐酸未产生沉淀,但加入硫酸后产生了白色沉淀,请结合离子方程式解释原因:___________ 。
②取iii中上层溶液,加几滴KSCN溶液。取样时间与溶液颜色如下表。
用离子方程式表示溶液变红的原因___________ ,Fe3++SCN- Fe(SCN)3。
Fe(SCN)3。
(4)小组同学认为不能排除O2直接氧化Ag继而生成AgCl,对此设计实验:___________ 。结果发现,该实验产生AgCl所需的时间更长。说明AgCl的产生主要与Fe3+有关。
(5)实验A中的i~iii中,i中AgCl溶解,iii中又生成AgCl的原因是:___________ 。
乙组实验反思:铁粉还原AgCl制取银时应控制铁粉、盐酸的浓度和浸泡时间等因素
(一)、甲小组选择强还原剂:肼(N2H4)。
在还原AgCl制取银的过程中有对环境无污染气体产生。
(1)①写出相关的化学反应方程式:
【资料】工业上一般先向氯化银中加入氨水浆化,然后用N2H4还原,可有利于反应的进行。
②写出浆化过程中的离子反应式:
(二)、乙小组换用铁粉还原AgCl制取银,探究其过程和影响因素。
【实验A】在试管中加入NaCl溶液,然后滴入AgNO3溶液,产生白色沉淀。滤出白色沉淀,继续实验如下:

【资料】①AgCl+Cl-
 AgCl
AgCl
②Fe3++4Cl-
 FeCl
FeCl
(2)检验ⅱ中产物
①取ⅱ中上层清液,滴加K3[Fe(CN)6]溶液,
②取ⅱ中少量灰黑色固体,洗涤后将固体等分两份。取其中一份,加入
(3)检验ⅲ中产物。
①取ⅲ中灰白色固体,洗涤。进行如下实验,确认灰白色固体中含AgCl:

滤液加盐酸未产生沉淀,但加入硫酸后产生了白色沉淀,请结合离子方程式解释原因:
②取iii中上层溶液,加几滴KSCN溶液。取样时间与溶液颜色如下表。
| 取样时间 | 10分钟 | 12小时 | 24小时 |
| 溶液颜色 | 浅红色 | 红色 | 深红色 |
 Fe(SCN)3。
Fe(SCN)3。(4)小组同学认为不能排除O2直接氧化Ag继而生成AgCl,对此设计实验:
(5)实验A中的i~iii中,i中AgCl溶解,iii中又生成AgCl的原因是:
乙组实验反思:铁粉还原AgCl制取银时应控制铁粉、盐酸的浓度和浸泡时间等因素
您最近半年使用:0次
名校
2 . 某实验小组同学依据资料深入探究Fe³+在水溶液中的行为。
资料:i.Fe³+在水溶液中以水合铁离子的形式存在,如[Fe(H2O)6]3+;[Fe(H2O)6] 3+发生如下水解反应:[Fe(H2O)6]3+(几乎无色)+nH2O [Fe(H2O)6-n(OH)n]3−n(黄色)+nH3O+(n=0~6)。
[Fe(H2O)6-n(OH)n]3−n(黄色)+nH3O+(n=0~6)。
ii.[FeCl4(H2O)2]-为黄色。
进行实验:【实验I】

【实验Ⅱ】分别用试管①、③中的试剂作为待测液,用色度计测定其透光率。透光率越小,溶液颜色越深;透光率越大,溶液颜色越浅。
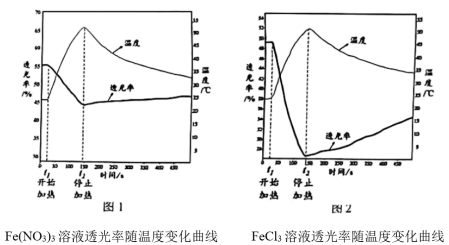
(1)实验1中,试管②溶液变为无色的原因是___________ 。
(2)实验I中,试管③溶液呈棕黄色与[FeCl4(H2O)2]-有关,支持此结论的实验现象是___________ 。
(3)由实验Ⅱ图1、2可知:加热时,溶液颜色___________ (填“变浅"、“变深”或“不变”)。
(4)由实验Ⅱ,可以得出如下结论:
[结论一]FeCl3溶液中存在可逆反应:[FeCl4(H2O)2]-+4H2O=[Fe(H2O)6]³++4Cl-得出此结论的理由是___________ 。
[结论二]结论一中反应的△H___________ (填“>0”或"<0")。
资料:i.Fe³+在水溶液中以水合铁离子的形式存在,如[Fe(H2O)6]3+;[Fe(H2O)6] 3+发生如下水解反应:[Fe(H2O)6]3+(几乎无色)+nH2O
 [Fe(H2O)6-n(OH)n]3−n(黄色)+nH3O+(n=0~6)。
[Fe(H2O)6-n(OH)n]3−n(黄色)+nH3O+(n=0~6)。ii.[FeCl4(H2O)2]-为黄色。
进行实验:【实验I】

【实验Ⅱ】分别用试管①、③中的试剂作为待测液,用色度计测定其透光率。透光率越小,溶液颜色越深;透光率越大,溶液颜色越浅。

(1)实验1中,试管②溶液变为无色的原因是
(2)实验I中,试管③溶液呈棕黄色与[FeCl4(H2O)2]-有关,支持此结论的实验现象是
(3)由实验Ⅱ图1、2可知:加热时,溶液颜色
(4)由实验Ⅱ,可以得出如下结论:
[结论一]FeCl3溶液中存在可逆反应:[FeCl4(H2O)2]-+4H2O=[Fe(H2O)6]³++4Cl-得出此结论的理由是
[结论二]结论一中反应的△H
您最近半年使用:0次
名校
3 . I.某小组对Cu与浓HNO3的反应进行研究。记录如下:
(1)Cu与浓HNO3反应的化学方程式是___________ 。
II.探究实验1中溶液A呈绿色而不是蓝色的原因。
(2)甲认为溶液呈绿色是由Cu2+离子浓度较大引起的。乙根据实验记录,认为此观点不正确,乙的依据是___________ 。
(3)乙认为溶液呈绿色是由溶解的NO2引起的。
进行实验2:先将NO2通入B中,再鼓入N2,结果证实假设成立。
则以上两步操作对应的现象分别是___________ 、___________ 。
(4)为深入研究,丙查阅资料,有如下信息:
i.溶有NO2的浓HNO3呈黄色;水或稀HNO3中通少量NO2溶液呈无色。
ii.NO2溶于水,会发生反应2NO2+H2O= HNO3+HNO2;
HNO2是弱酸,只能稳定存在于冷、稀的溶液中,否则易分解。
iii. 能与Cu2+反应:Cu2+(蓝色)+4
能与Cu2+反应:Cu2+(蓝色)+4

 (绿色)
(绿色)
据此,丙进一步假设:
①可能是A中剩余的浓HNO3溶解了NO2得到的黄色溶液与Cu(NO3)2的蓝色溶液混合而形成的绿色;
②可能是A中生成了 使溶液呈绿色。
使溶液呈绿色。
丙进行如下实验:
①亚硝酸分解的化学方程式是___________ 。
②请用平衡原理解释加入H2SO4后绿色溶液变蓝的原因:___________ 。
(5)根据实验得出结论:实验1中溶液A呈绿色的主要原因是___________ 。请依据实验现象阐述理由:___________ 。
| 装置 | 药品 | 现象 | |
| 实验1 | 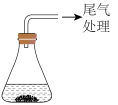 | 0.64gCu片(0.01mol) Cu片和20.0 mL浓HNO3 | Cu片消失,得到绿色溶液A,放置较长时间后得到蓝色溶 液B,…… |
(1)Cu与浓HNO3反应的化学方程式是
II.探究实验1中溶液A呈绿色而不是蓝色的原因。
(2)甲认为溶液呈绿色是由Cu2+离子浓度较大引起的。乙根据实验记录,认为此观点不正确,乙的依据是
(3)乙认为溶液呈绿色是由溶解的NO2引起的。
进行实验2:先将NO2通入B中,再鼓入N2,结果证实假设成立。
则以上两步操作对应的现象分别是
(4)为深入研究,丙查阅资料,有如下信息:
i.溶有NO2的浓HNO3呈黄色;水或稀HNO3中通少量NO2溶液呈无色。
ii.NO2溶于水,会发生反应2NO2+H2O= HNO3+HNO2;
HNO2是弱酸,只能稳定存在于冷、稀的溶液中,否则易分解。
iii.
 能与Cu2+反应:Cu2+(蓝色)+4
能与Cu2+反应:Cu2+(蓝色)+4

 (绿色)
(绿色)据此,丙进一步假设:
①可能是A中剩余的浓HNO3溶解了NO2得到的黄色溶液与Cu(NO3)2的蓝色溶液混合而形成的绿色;
②可能是A中生成了
 使溶液呈绿色。
使溶液呈绿色。丙进行如下实验:
| 操作 | 现象 | |
| 实验3 | i.配制与溶液A的c(H+)相同的HNO3溶液,取20.0mL,通入NO2气体 | 溶液呈黄色 |
| ii.再加0.01molCu(NO3)2固体搅拌至完全溶解 | 溶液变为绿色 | |
| iii.加水稀释 | 溶液立即变蓝 | |
| 实验4 | i.向20.0mL0.5mol/L Cu(NO3)2蓝色溶液中通入少量NO2 | 溶液呈绿色 |
| ii.加入稀H2SO4 | 有无色气体放出,遇空气变红棕色,溶液很快变为蓝色 |
②请用平衡原理解释加入H2SO4后绿色溶液变蓝的原因:
(5)根据实验得出结论:实验1中溶液A呈绿色的主要原因是
您最近半年使用:0次
名校
4 . 小组同学探究盐溶液对反应 (血红色)的影响。将
(血红色)的影响。将
 的
的 溶液与
溶液与 的
的 溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
ii. (黄色)
(黄色)
iii.已知 对实验无影响
对实验无影响
下列说法不正确的是
 (血红色)的影响。将
(血红色)的影响。将
 的
的 溶液与
溶液与 的
的 溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。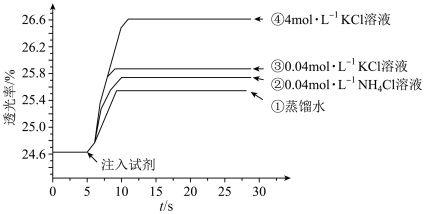
ii.
 (黄色)
(黄色)iii.已知
 对实验无影响
对实验无影响下列说法不正确的是
A.注入试剂①后溶液透光率增大,证明 逆向移动 逆向移动 |
B.透光率③比②高,可能是阳离子种类或溶液 不同导致的 不同导致的 |
C.透光率④比③高,可能发生了反应 |
D.若要证明试剂③中 对平衡体系有影响,还应使用 对平衡体系有影响,还应使用 的 的 溶液进行对照实验 溶液进行对照实验 |
您最近半年使用:0次
2023-11-21更新
|
340次组卷
|
7卷引用:北京市对外经济贸易大学附属中学2022-2023学年高二上学期期中考试化学试题
5 . 工业上用黄铜矿(主要成分是CuFeS2,还含有少量SiO2等)制备CuCl的工艺流程如图:
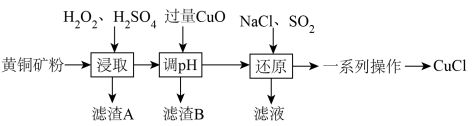
已知:①CuCl是一种难溶于水和乙醇的白色固体,在潮湿的空气中易水解氧化为碱式氯化铜Cu2(OH)3Cl。
(2)25℃时,Ksp[Cu(OH)2]=2.2×10-20、Ksp[Fe(OH)3]=1.0×10-38。
回答下列问题:
(1)“滤渣A”的主要成分是_______ (填化学式)。
(2)“浸取”时,H2O2的实际用量远远超过理论用量,可能原因是______ 。
(3)当溶液中离子浓度≤1.0×10-5mol•L-1时,可认为该离子已沉淀完全。加入CuO调pH,使溶液中Fe3+沉淀完全,此时,溶液中c(Cu2+)=0.22mol•L-1,则“调pH”的合理范围为_______ 。
(4)“还原”过程生成CuCl的离子方程式是_______ 。
(5)“一系列操作”是指:加入去氧水、过滤、用无水乙醇洗涤、真空干燥。加入去氧水的目的是______ 。
(6)①已知:CuCl的熔点为326℃,能升华,熔化呈液态时不导电。则CuCl晶体属于_______ (填晶体类型)。写出基态Cu+的核外电子排布式_______ 。
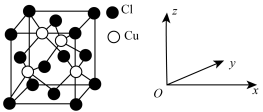
②原子坐标参数表示晶胞内部各原子的相对位置,图中 位置原子的坐标参数为(
位置原子的坐标参数为( ,
, ,
, ),则图中
),则图中 位置原子的坐标参数为
位置原子的坐标参数为_______ 。

已知:①CuCl是一种难溶于水和乙醇的白色固体,在潮湿的空气中易水解氧化为碱式氯化铜Cu2(OH)3Cl。
(2)25℃时,Ksp[Cu(OH)2]=2.2×10-20、Ksp[Fe(OH)3]=1.0×10-38。
回答下列问题:
(1)“滤渣A”的主要成分是
(2)“浸取”时,H2O2的实际用量远远超过理论用量,可能原因是
(3)当溶液中离子浓度≤1.0×10-5mol•L-1时,可认为该离子已沉淀完全。加入CuO调pH,使溶液中Fe3+沉淀完全,此时,溶液中c(Cu2+)=0.22mol•L-1,则“调pH”的合理范围为
(4)“还原”过程生成CuCl的离子方程式是
(5)“一系列操作”是指:加入去氧水、过滤、用无水乙醇洗涤、真空干燥。加入去氧水的目的是
(6)①已知:CuCl的熔点为326℃,能升华,熔化呈液态时不导电。则CuCl晶体属于
②原子坐标参数表示晶胞内部各原子的相对位置,图中
 位置原子的坐标参数为(
位置原子的坐标参数为( ,
, ,
, ),则图中
),则图中 位置原子的坐标参数为
位置原子的坐标参数为
您最近半年使用:0次
22-23高三下·重庆渝中·阶段练习
名校
6 . 25℃时,向恒容容器中加入A发生反应:① ;②
;② 。反应体系中
。反应体系中 、
、 、
、 的分压随时间t的变化曲线如图所示。下列说法正确的是
的分压随时间t的变化曲线如图所示。下列说法正确的是
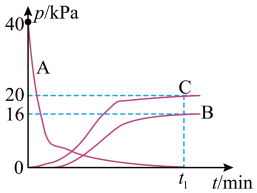
 ;②
;② 。反应体系中
。反应体系中 、
、 、
、 的分压随时间t的变化曲线如图所示。下列说法正确的是
的分压随时间t的变化曲线如图所示。下列说法正确的是
A.曲线C表示 的分压随时间的变化曲线 的分压随时间的变化曲线 |
B.25℃时,反应②的分压平衡常数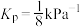 |
C.当 、 、 的分压相等时,反应②中的 的分压相等时,反应②中的 转化率为12.5% 转化率为12.5% |
D.时间 后,保持温度和体积不变,再充入 后,保持温度和体积不变,再充入 (g),则 (g),则 (g)的分压增大 (g)的分压增大 |
您最近半年使用:0次
2023-02-18更新
|
491次组卷
|
4卷引用:2022年重庆高考真题化学试题变式题(选择题11-14)
(已下线)2022年重庆高考真题化学试题变式题(选择题11-14)重庆市巴蜀中学校2023届高三下学期高考适应性月考卷(六)化学试题(已下线)素养卷04 化学反应速率与平衡图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)重庆市育才中学校2023-2024学年高二上学期三校联考模拟考化学试题(平行班)
2021高三·浙江·专题练习
解题方法
7 . 向平衡体系 中加入适量
中加入适量 固体,平衡逆向移动,溶液的颜色变浅。( )
固体,平衡逆向移动,溶液的颜色变浅。( )
 中加入适量
中加入适量 固体,平衡逆向移动,溶液的颜色变浅。( )
固体,平衡逆向移动,溶液的颜色变浅。( )
您最近半年使用:0次
2023-02-11更新
|
317次组卷
|
5卷引用:考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)
(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第七章 化学反应速率与化学平衡 第43讲 化学平衡移动原理及应用(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)考点22 化学平衡状态与化学平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
22-23高三下·重庆沙坪坝·阶段练习
名校
解题方法
8 . 尽管计算机模拟实验已经有相当广泛的应用,但化学仍然是一门以实际操作并进行相应探究的学科。下列实验操作、现象与相应结论或解释相对应的一组是
| 选项 | 实验操作 | 实验现象 | 结论或解释 |
| A | 在葡萄糖溶液中滴入少量酸性 溶液 溶液 |  溶液褪色 溶液褪色 | 醛基具有还原性 |
| B | 在 平衡体系中保持恒温恒容条件继续充入一定量 平衡体系中保持恒温恒容条件继续充入一定量 | 体系颜色变浅 | 反应物浓度增大,平衡向正向移动 |
| C | 在 气体氛围中点燃金属钠 气体氛围中点燃金属钠 | 产生浓烟并有黑色颗粒生成 | 单质还原性: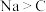 |
| D | 取适量 溶液于试管中,测定pH值,然后加热一段时间,冷却至原温度,再次测定该溶液pH值 溶液于试管中,测定pH值,然后加热一段时间,冷却至原温度,再次测定该溶液pH值 | 加热后pH值变小 |  的水解为吸热过程 的水解为吸热过程 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
9 . 下列叙述与图对应的是
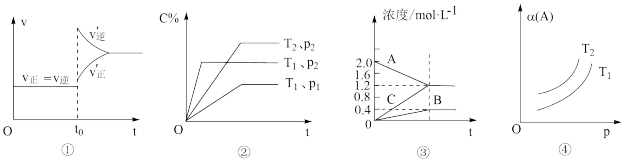

A.已达平衡状态的反应:N2(g)+3H2(g)  2NH3(g),图①表示在t0时刻充入了一定量的NH3,平衡逆向移动 2NH3(g),图①表示在t0时刻充入了一定量的NH3,平衡逆向移动 |
B.由图②可知,P2>P1、T1>T2满足反应:2A(g)+B(g)  2C(g) ΔH<0 2C(g) ΔH<0 |
| C.图③表示的反应方程式为:2A(g)=B(g)+3C(g) |
D.由图④可知,对于反应aA(g) bB(g)+cC(g),该反应用于工业生产时,采用的压强越大越好 bB(g)+cC(g),该反应用于工业生产时,采用的压强越大越好 |
您最近半年使用:0次
2023-02-02更新
|
396次组卷
|
2卷引用:四川省成都石室中学2022—2023学年高二上学期期中考试化学试题
名校
解题方法
10 . 下列实验中,对现象的解释不正确 的是
| 选项 | A | B | C | D |
| 装置及操作 |  向右轻轻推动活塞压缩体积 | 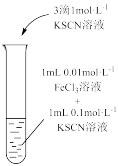 | 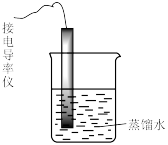 分别测定20℃和80℃蒸馏水的电导率 | 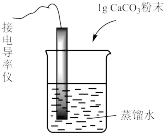 |
| 现象 | 气体红棕色先变深再变浅 | 溶液血红色加深 | 80℃蒸馏水的电导率大于20℃的 | 加入 粉末后电导率增大 粉末后电导率增大 |
| 解释 | 压强增大, 平衡先逆向移动,再正向移动 平衡先逆向移动,再正向移动 | 增大反应物浓度,  平衡正向移动 平衡正向移动 | 温度升高,水的电离平衡正向移动 |  在水中存在 在水中存在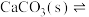  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-01-06更新
|
926次组卷
|
13卷引用:北京海淀区2022-2023学年高二上学期期末考试化学试题
北京海淀区2022-2023学年高二上学期期末考试化学试题北京一零一中学2022-2023高二上学期期末考试化学试题北京市首都师范大学附属中学2022-2023学年高二上学期期末考试化学试题北京市顺义牛栏山第一中学2022-2023学年高二下学期3月月考化学试题河南省濮阳市第一高级中学2022-2023学年高二下学期期中质量检测化学试题北京市顺义牛栏山第一中学2023-2024学年高二上学期期中考试化学试题北京市第三十五中学2023-2024学年高二上学期期中考试化学试题 北京市第十三中学2023-2024学年高二上学期期中考试化学试题北京师范大学附属中学2023-2024学年高二上学期期中考试化学试卷四川省德阳市什邡中学2023-2024学年高二上学期11月期中考试化学试题北京市第五十中学2023-2024学年高二上学期12月月考化学试题天津市部分区2023-2024学年高二上学期期末练习化学试题北京交通大学附属中学第二分校2023-2024学年高二上学期12月月考化学试题



