20-21高三上·云南德宏·期末
解题方法
1 . CoCO3可用作选矿剂、催化剂及伪装涂料的颜料。以含钴废渣(主要成分为CoO、Co2O3,还含有Al2O3、ZnO 等杂质) 为原料制备CoCO3的一种工艺流程如下:
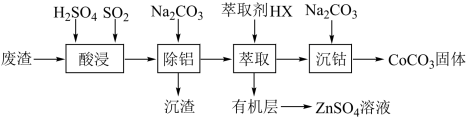
已知:①常温下,Ksp(CoCO3)=1.6×10-7
②相关金属离子[c(Mn+)=1.0mol·L-1]形成氢氧化物沉淀的pH范围如下:
(1)“酸浸”时加快溶解的方法有_______ (写出一种)。
(2)写出“酸浸”时发生氧化还原反应的化学方程式_______ 。
(3)“除铝”过程中需要调节溶液pH 的范围为_______ ,形成沉渣时发生反应的离子方程式为_______ 。
(4)“萃取”过程可表示为ZnSO4(水层)+2HX(有机层) ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是
ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是_______ 。
(5)“沉钴”后经过滤、洗涤、干燥可得CoCO3固体,其中洗涤沉淀的方法是_______ 。
(6)当Co2+沉淀完全时[c(Co2+)≤1×10-5mol·L-1],溶液中c(CO )至少应大于
)至少应大于_______ 。
(7)在空气中煅烧CoCO3生成钴的氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672 L(标准状况),则该钴的氧化物的化学式为_______ 。

已知:①常温下,Ksp(CoCO3)=1.6×10-7
②相关金属离子[c(Mn+)=1.0mol·L-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Co2+ | 7.6 | 9.4 |
| Al3+ | 3.0 | 5.0 |
| Zn2+ | 5.4 | 8.0 |
(2)写出“酸浸”时发生氧化还原反应的化学方程式
(3)“除铝”过程中需要调节溶液pH 的范围为
(4)“萃取”过程可表示为ZnSO4(水层)+2HX(有机层)
 ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是
ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是(5)“沉钴”后经过滤、洗涤、干燥可得CoCO3固体,其中洗涤沉淀的方法是
(6)当Co2+沉淀完全时[c(Co2+)≤1×10-5mol·L-1],溶液中c(CO
 )至少应大于
)至少应大于(7)在空气中煅烧CoCO3生成钴的氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672 L(标准状况),则该钴的氧化物的化学式为
您最近一年使用:0次
2 . CO2是一种温室气体,对人类的生存环境产生巨大的影响,将CO2作为原料转化为有用化学品,对实现碳中和及生态环境保护有着重要意义。
Ⅰ.工业上以CO2和NH3为原料合成尿素,在合成塔中存在如下转化:

(1)液相中,合成尿素的热化学方程式为:2NH3(l)+CO2(l)=H2O(l)+NH2CONH2(l) △H=___________ kJ/mol。
(2)在恒容密闭容器中发生反应:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) △H<0。下列说法正确的是
Ⅱ.可利用CO2和CH4催化制备合成气(CO、H2),在一定温度下容积为1 L密闭容器中,充入等物质的量CH4和CO2,加入Ni/Al2O3使其发生反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)
2CO(g)+2H2(g)
(3)反应达平衡后,平衡常数K=81,此时测得c(CO)为3 mol/L,则CH4的转化率为___________ (保留2位有效数字)。
(4)制备“合成气”反应历程分两步:
上述反应中C(ads)为吸附性活性炭,反应历程的能量图变化如下图所示:

①反应速率快慢比较:反应①___________ 反应②(填“>”“<”或“=”),请依据有效碰撞理论微观探析其原因___________ 。
②一定温度下,反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的平衡常数K=
2CO(g)+2H2(g)的平衡常数K=___________ (用k1、k2、k3、k4表示)。
(5)制备合成气(CO、H2)过程中发生副反应:CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.0 kJ/mol,在刚性密闭容器中,进料比
CO(g)+H2O(g) △H2=+41.0 kJ/mol,在刚性密闭容器中,进料比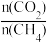 分别等于1.0、1.5、2.0,且反应达到平衡状态。反应体系中,
分别等于1.0、1.5、2.0,且反应达到平衡状态。反应体系中, 随温度变化的关系如图所示:
随温度变化的关系如图所示:

随着进料比 的增加,
的增加, 的值
的值___________ (填“增大”、“不变”或“减小”),其原因是___________ 。
Ⅰ.工业上以CO2和NH3为原料合成尿素,在合成塔中存在如下转化:

(1)液相中,合成尿素的热化学方程式为:2NH3(l)+CO2(l)=H2O(l)+NH2CONH2(l) △H=
(2)在恒容密闭容器中发生反应:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) △H<0。下列说法正确的是
| A.增大CO2的浓度,有利于NH3的转化率增大 |
| B.反应在任何温度下都能自发进行 |
| C.当混合气体的密度不再发生改变时反应达平衡状态 |
| D.充入He,压强增大,平衡向正反应移动 |
Ⅱ.可利用CO2和CH4催化制备合成气(CO、H2),在一定温度下容积为1 L密闭容器中,充入等物质的量CH4和CO2,加入Ni/Al2O3使其发生反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g)
2CO(g)+2H2(g)(3)反应达平衡后,平衡常数K=81,此时测得c(CO)为3 mol/L,则CH4的转化率为
(4)制备“合成气”反应历程分两步:
| 步骤 | 反应 | 正反应速率方程 | 逆反应速率方程 |
| 反应① | CH4(g) C(ads)+2H2(g) C(ads)+2H2(g) | v正=k1·c(CH4) | v逆=k2·c2(H2) |
| 反应② | C(ads)+CO2(g) 2CO(g) 2CO(g) | v正=k3·c(CO2) | v逆=k4·c2(CO) |

①反应速率快慢比较:反应①
②一定温度下,反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)的平衡常数K=
2CO(g)+2H2(g)的平衡常数K=(5)制备合成气(CO、H2)过程中发生副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.0 kJ/mol,在刚性密闭容器中,进料比
CO(g)+H2O(g) △H2=+41.0 kJ/mol,在刚性密闭容器中,进料比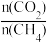 分别等于1.0、1.5、2.0,且反应达到平衡状态。反应体系中,
分别等于1.0、1.5、2.0,且反应达到平衡状态。反应体系中, 随温度变化的关系如图所示:
随温度变化的关系如图所示:
随着进料比
 的增加,
的增加, 的值
的值
您最近一年使用:0次
3 . 国家规定,排放的废水中氟的含量不得超过10.0mg·L-1,砷的含量不得超过0.5mg·L-1。硫酸工厂废水中除含有稀硫酸外,还含有H3AsO3、H2SiF6等物质。工业上常通过化学沉淀和氧化、吸附沉降处理废水,实现水体达标排放。
(1)化学沉淀:向废水中加入石灰乳[以Ca(OH)2为主]、过滤。滤渣中主要含有CaSO4、CaF2、SiO2和少量Ca3(AsO3)2。
①CaSO4中阴离子的空间构型为____ 。
②写出该过程中H2SiF6和石灰乳反应生成CaF2、SiO2的化学方程式:____ 。
③充分沉淀后测得废水中F-的含量为19.0mg·L-1,此时SO 的浓度为
的浓度为____ mol·L-1。[已知:Ksp(CaSO4)=5.0×10-5、Ksp(CaF2)=5.0×10-9]
(2)氧化、吸附沉降:利用NaClO和FeSO4进一步处理废水中残余的As(III)。已知:
ⅰ.NaClO能将As(III)氧化为As(V)、Fe(II)氧化为Fe(III)。形成的Fe(OH)3胶体吸附废水中的As(V)物种而沉降。
ⅱ.As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。
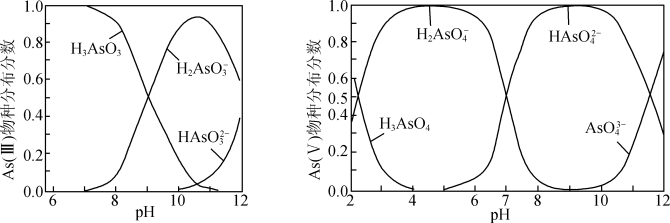
①向化学沉淀后的废水(pH≈8)中加入NaClO溶液,写出As(III)发生主要反应的离子方程式:____ 。
②其他条件相同的情况下,用以下两种方式向废水样中添加NaClO和FeSO4溶液。方式I:先加NaClO溶液,再加FeSO4溶液;方式II:先加FeSO4溶液,再加NaClO溶液。反应相同时间,测得As(III)的氧化效果方式II不如方式I,原因是____
(1)化学沉淀:向废水中加入石灰乳[以Ca(OH)2为主]、过滤。滤渣中主要含有CaSO4、CaF2、SiO2和少量Ca3(AsO3)2。
①CaSO4中阴离子的空间构型为
②写出该过程中H2SiF6和石灰乳反应生成CaF2、SiO2的化学方程式:
③充分沉淀后测得废水中F-的含量为19.0mg·L-1,此时SO
 的浓度为
的浓度为(2)氧化、吸附沉降:利用NaClO和FeSO4进一步处理废水中残余的As(III)。已知:
ⅰ.NaClO能将As(III)氧化为As(V)、Fe(II)氧化为Fe(III)。形成的Fe(OH)3胶体吸附废水中的As(V)物种而沉降。
ⅱ.As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。

①向化学沉淀后的废水(pH≈8)中加入NaClO溶液,写出As(III)发生主要反应的离子方程式:
②其他条件相同的情况下,用以下两种方式向废水样中添加NaClO和FeSO4溶液。方式I:先加NaClO溶液,再加FeSO4溶液;方式II:先加FeSO4溶液,再加NaClO溶液。反应相同时间,测得As(III)的氧化效果方式II不如方式I,原因是
您最近一年使用:0次
名校
解题方法
4 . 某温度下,改变0.1mol/LK2Cr2O7溶液的pH时,各种含铬元素微粒及OH-浓度变化如图所示(已知H2CrO4是二元酸),下列有关说法中正确的是


| A.该温度下的Kw=10-13 |
B.溶液中存在平衡 +H2O⇌2 +H2O⇌2 +2H+,该温度下此反应的K=10-13.2 +2H+,该温度下此反应的K=10-13.2 |
| C.向0.1mol/LK2Cr2O7溶液中加入一定量NaOH固体,溶液橙色加深 |
D.E点溶液中存在:c(K+)<2c( )+3c( )+3c( ) ) |
您最近一年使用:0次
2022-04-29更新
|
788次组卷
|
4卷引用:东北三省四城市联考暨沈阳市2021-2022学年高三质量监测(二)化学试题
东北三省四城市联考暨沈阳市2021-2022学年高三质量监测(二)化学试题(已下线)专项13 水溶液中的离子平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)辽宁省沈阳市同泽中学2022-2023学年高二12月月考化学试题湖北省武汉外国语学校2022-2023学年高二上学期期末考试化学试题
名校
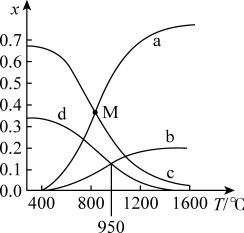
5 . 甲烷与硫化氢可通过重整反应制取氢气。现将原料按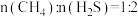 通入反应釜中,保持体系压强为0.1Mpa,研究不同温度对该反应体系的影响。当反应达到平衡时,体系中各组分的物质的量分数x随温度T的变化如图所示:
通入反应釜中,保持体系压强为0.1Mpa,研究不同温度对该反应体系的影响。当反应达到平衡时,体系中各组分的物质的量分数x随温度T的变化如图所示:
(1)已知该重整反应的另一个产物在常温下为液态,具有恶臭味,写出该物质的结构式:_______ ,此物质在该实验条件下为气态,写出该重整反应的热化学反应方程式:(反应热效应用Q表示)_______ 。
(2)图中表示 、
、 物质的量分数变化的曲线分别是:
物质的量分数变化的曲线分别是:_______ 、_______ 。
(3)反应达平衡的标志是_______(填标号)。
(4)由图可知该反应的Q_______ 0(填“>”、“<”或“=”),判断的理由是_______ 。
(5)M点对应温度下, 的转化率为
的转化率为_______ 。
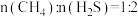 通入反应釜中,保持体系压强为0.1Mpa,研究不同温度对该反应体系的影响。当反应达到平衡时,体系中各组分的物质的量分数x随温度T的变化如图所示:
通入反应釜中,保持体系压强为0.1Mpa,研究不同温度对该反应体系的影响。当反应达到平衡时,体系中各组分的物质的量分数x随温度T的变化如图所示:
(1)已知该重整反应的另一个产物在常温下为液态,具有恶臭味,写出该物质的结构式:
(2)图中表示
 、
、 物质的量分数变化的曲线分别是:
物质的量分数变化的曲线分别是:(3)反应达平衡的标志是_______(填标号)。
A. |
B. 的体积分数不再变化 的体积分数不再变化 |
C. 不再变化 不再变化 |
| D.混合气体的密度不再改变 |
(5)M点对应温度下,
 的转化率为
的转化率为
您最近一年使用:0次
名校
6 . 已知:[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:[Co(H2O)6]2++4Cl- [CoCl4]2-+6H2O,用该溶液做实验,溶液的颜色变化如下:
[CoCl4]2-+6H2O,用该溶液做实验,溶液的颜色变化如下:
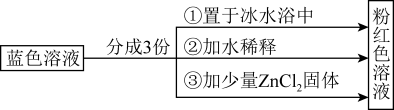
以下结论和解释正确的是
 [CoCl4]2-+6H2O,用该溶液做实验,溶液的颜色变化如下:
[CoCl4]2-+6H2O,用该溶液做实验,溶液的颜色变化如下:
以下结论和解释正确的是
| A.由实验①可推知正反应为放热反应 |
| B.等物质的量的[Co(H2O)6]2+和[CoCl4]2-中σ键数之比为9:4 |
| C.实验②是由于c(H2O)增大,导致平衡逆向移动 |
| D.由实验③可知配离子的稳定性:[ZnCl4]2-> [CoCl4]2- |
您最近一年使用:0次
2022-04-27更新
|
719次组卷
|
3卷引用:重庆市渝东六校共同体2021-2022学年高二下学期联合诊断性测试化学试题
7 . 为充分利用金属资源,某研究团队利用生产钴电极材料生的铜锰渣(含 、
、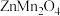 、
、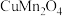 等物质)回收金属
等物质)回收金属 的一种流程如图所示:
的一种流程如图所示:
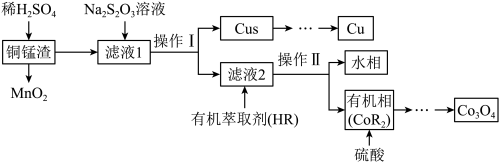
回答下列问题:
(1)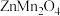 、
、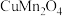 中Mn元素的化合价为
中Mn元素的化合价为___________ .
(2)写出铜锰渣中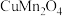 与稀硫酸反应的化学方程式
与稀硫酸反应的化学方程式_____________ .
(3)研究团队认为该工艺可能利用了如下反应原理沉淀滤液1中的Cu2+: ,
,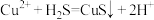 .析出的Cu沉淀中还混有少量的S单质,原因是
.析出的Cu沉淀中还混有少量的S单质,原因是__________ (用离子方程式解释).
(4)依据反应 萃取滤液2中的
萃取滤液2中的 并进行操作Ⅱ,操作Ⅱ的名称是
并进行操作Ⅱ,操作Ⅱ的名称是________ ;所得有机相中加入硫酸能进行反萃取的原因是________________________ (结合平衡移动原理解释).
(5)控制反应温度为 ,向滤液1中加入
,向滤液1中加入 溶液,不同金属沉淀率与
溶液,不同金属沉淀率与 用量倍数的关系如下图所示.
用量倍数的关系如下图所示.
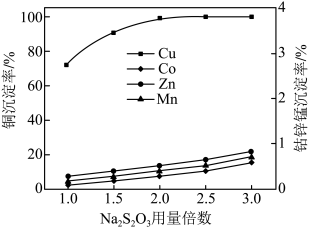
当 用量倍数为2.0时,水相中的金属阳离子主要含
用量倍数为2.0时,水相中的金属阳离子主要含 、
、_________ (填离子符号).
(6) 用作电池材料,使用KOH溶液作电解液,充电时
用作电池材料,使用KOH溶液作电解液,充电时 转化为
转化为 的电极反应式为
的电极反应式为____________________ .
 、
、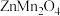 、
、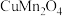 等物质)回收金属
等物质)回收金属 的一种流程如图所示:
的一种流程如图所示:
回答下列问题:
(1)
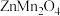 、
、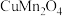 中Mn元素的化合价为
中Mn元素的化合价为(2)写出铜锰渣中
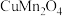 与稀硫酸反应的化学方程式
与稀硫酸反应的化学方程式(3)研究团队认为该工艺可能利用了如下反应原理沉淀滤液1中的Cu2+:
 ,
,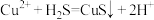 .析出的Cu沉淀中还混有少量的S单质,原因是
.析出的Cu沉淀中还混有少量的S单质,原因是(4)依据反应
 萃取滤液2中的
萃取滤液2中的 并进行操作Ⅱ,操作Ⅱ的名称是
并进行操作Ⅱ,操作Ⅱ的名称是(5)控制反应温度为
 ,向滤液1中加入
,向滤液1中加入 溶液,不同金属沉淀率与
溶液,不同金属沉淀率与 用量倍数的关系如下图所示.
用量倍数的关系如下图所示.
当
 用量倍数为2.0时,水相中的金属阳离子主要含
用量倍数为2.0时,水相中的金属阳离子主要含 、
、(6)
 用作电池材料,使用KOH溶液作电解液,充电时
用作电池材料,使用KOH溶液作电解液,充电时 转化为
转化为 的电极反应式为
的电极反应式为
您最近一年使用:0次
8 . 二氧化铈(CeO2)可用作玻璃工业添加剂和有机反应催化剂。以氟碳铈矿(主要含有CeFCO3)为原料制备二氧化铈的一种工艺流程如图:
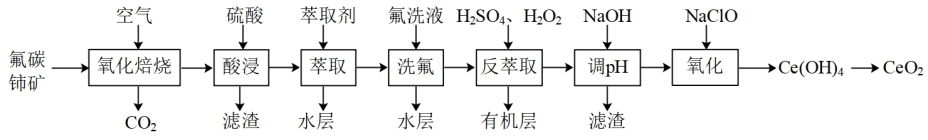
已知:①Ce4+能与F-结合成CeF3+,Al3+也能与F-结合成AlF ;②Ce4+能被萃取剂TBP萃取,而Ce3+不能。回答下列问题:
;②Ce4+能被萃取剂TBP萃取,而Ce3+不能。回答下列问题:
(1)“氧化焙烧”时,为了加快反应速率、提高原料利用率的措施有_______ 。(写一种,合理即可)
(2)“氧化焙烧”后的固体产物中含有CeO2和CeF4,二者物质的量之比为3:1,“酸浸”时发生反应的离子方程式为_______ 。
(3)TBP是一种有机萃取剂,“萃取”时发生反应:CeF3++TBP→CeTBP4++F-,氟洗液中添加Al3+的作用是_______ 。
(4)“反萃取”时加入H2SO4和H2O2的混合液,H2O2的作用为_______ 。
(5)“反萃取”后的水层溶液中c(Ce3+)=1mol·L-1,c(Al3+)=0.01mol·L-1。室温下,“调pH”时,先除去Al3+,若忽略过程中溶液的体积变化,则需加入NaOH调节溶液pH的范围为_______ ,过滤后,再向滤液加入NaOH使Ce3+沉淀完全(已知:室温下,当溶液中的离子浓度c≤1.0×10-5mol·L-1时,可认为该离子沉淀完全。K[Al(OH)3]=1.0×10-32,K[Ce(OH)3]=1.0×10-21)。
(6)“氧化”时发生反应的化学方程式为_______
(7)用10吨含70%CeFCO3的矿石,按上述工艺生产,制得CeO24.48吨,则CeO2的产率为_______ (保留三位有效数字)。

已知:①Ce4+能与F-结合成CeF3+,Al3+也能与F-结合成AlF
 ;②Ce4+能被萃取剂TBP萃取,而Ce3+不能。回答下列问题:
;②Ce4+能被萃取剂TBP萃取,而Ce3+不能。回答下列问题:(1)“氧化焙烧”时,为了加快反应速率、提高原料利用率的措施有
(2)“氧化焙烧”后的固体产物中含有CeO2和CeF4,二者物质的量之比为3:1,“酸浸”时发生反应的离子方程式为
(3)TBP是一种有机萃取剂,“萃取”时发生反应:CeF3++TBP→CeTBP4++F-,氟洗液中添加Al3+的作用是
(4)“反萃取”时加入H2SO4和H2O2的混合液,H2O2的作用为
(5)“反萃取”后的水层溶液中c(Ce3+)=1mol·L-1,c(Al3+)=0.01mol·L-1。室温下,“调pH”时,先除去Al3+,若忽略过程中溶液的体积变化,则需加入NaOH调节溶液pH的范围为
(6)“氧化”时发生反应的化学方程式为
(7)用10吨含70%CeFCO3的矿石,按上述工艺生产,制得CeO24.48吨,则CeO2的产率为
您最近一年使用:0次
解题方法
9 . 金属铬坚硬,耐腐蚀,可做镀层金属,并且在制皮革,羊毛,火柴,颜料等方面均有其应用。但是Cr(Ⅵ)致癌,因此国家对废水中Cr含量有严格的排放标准。已知: Ksp[Cr(OH)3]= 1 ×10-32。
(1)基态Cr原子外围电子排布式为_______ 。
(2)还原法
①可以选择焦亚硫酸钠或硫代硫酸钠(Na2S2O3在酸性条件下分解为HSO 、SO
、SO )处理含铬(VI)废水,处理费用低。其工艺流程如图:
)处理含铬(VI)废水,处理费用低。其工艺流程如图:

反应池中发生反应的离子方程式_______ 。
②Cr2O 在酸性条件下氧化性强,其他条件相同,pH<2.5时pH过低,充分反应后除铬率反而下降,可能的原因是
在酸性条件下氧化性强,其他条件相同,pH<2.5时pH过低,充分反应后除铬率反而下降,可能的原因是 _______ 。
③室温下,加入石灰乳调节pH,当Cr3+完全沉淀时[c(Cr3+)≤1 ×10-6mol/L],溶液pH范围是_______ 。
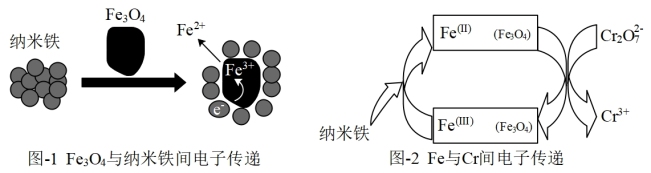
(3)Fe3O4/纳米Fe去除法
(i)某研究小组经查阅资料,发现磁铁矿Fe3O4辅助纳米Fe可以降解废水中的Cr2O 。为验证其准确性,进行了如下实验,相同时间内得到如下实验结果。
。为验证其准确性,进行了如下实验,相同时间内得到如下实验结果。
(ii)依据如下两个图示信息,上述实验3降解Cr2O 效率增大的原因是
效率增大的原因是 _______ 。
(1)基态Cr原子外围电子排布式为
(2)还原法
①可以选择焦亚硫酸钠或硫代硫酸钠(Na2S2O3在酸性条件下分解为HSO
 、SO
、SO )处理含铬(VI)废水,处理费用低。其工艺流程如图:
)处理含铬(VI)废水,处理费用低。其工艺流程如图:
反应池中发生反应的离子方程式
②Cr2O
 在酸性条件下氧化性强,其他条件相同,pH<2.5时pH过低,充分反应后除铬率反而下降,可能的原因是
在酸性条件下氧化性强,其他条件相同,pH<2.5时pH过低,充分反应后除铬率反而下降,可能的原因是 ③室温下,加入石灰乳调节pH,当Cr3+完全沉淀时[c(Cr3+)≤1 ×10-6mol/L],溶液pH范围是
(3)Fe3O4/纳米Fe去除法
(i)某研究小组经查阅资料,发现磁铁矿Fe3O4辅助纳米Fe可以降解废水中的Cr2O
 。为验证其准确性,进行了如下实验,相同时间内得到如下实验结果。
。为验证其准确性,进行了如下实验,相同时间内得到如下实验结果。| 实验编号 | 纳米 Fe(g/L) | Fe3O4(g/L) | Cr2O 实际降解率 实际降解率 |
| 1 | 0.05 | 0 | 51.4% |
| 2 | 0 | 2 | 7.12% |
| 3 | 0.05 | 2 | 86.67% |
 效率增大的原因是
效率增大的原因是 
您最近一年使用:0次
解题方法
10 . 镁条投入盐酸时,快速溶解并产生大量气泡;投入热水时,其表面会附着微量气泡。受此启发,某兴趣小组对Mg与NaHCO3溶液的反应进行了如下探究:
I.探究反应产生的气体成分。
(1)经检验反应产生的气体有H2,实验室检验H2的方法为_______ 。
(2)小组成员认为反应产生的气体中可能有CO2,并对此进行了如下实验(图1、图2中曲线②均为对应加入镁条的数据):
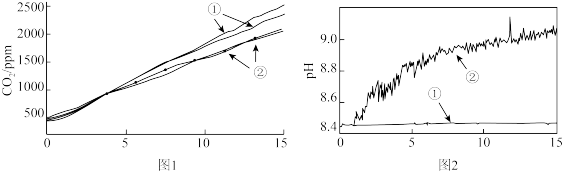
图1中曲线②对应的CO2含量逐渐增大的原因为_______ (用化学方程式表示);结合实验3解释,随着时间推移,图1中曲线②的数值低于曲线①的原因为_______ 。
II.探究Mg与NaHCO3溶液反应比与热水反应快的原因。
小组成员推测可能是溶液中的Na+或HCO 加快了该反应的发生,对比实验1设计实验如下:
加快了该反应的发生,对比实验1设计实验如下:
(3)结合实验1和4,可知溶液中的HCO 加快了反应的发生。
加快了反应的发生。
①实验4中横线处内容为_______ 。
②查阅文献可知,Mg(OH)2质地致密,MgCO3质地疏松,请结合必要的文字和化学用语解释HCO 能加快该反应的原因为
能加快该反应的原因为_______ 。
III.探究固体浑浊物的组成。
文献显示,固体浑浊物为Mg(OH)2和MgCO3的混合物。甲、乙两位同学设计不同方案,测定混合物组成。
(4)甲同学借助下图装置(可重复选用),通过测定固体热分解产物水及二氧化碳的质量,测定其组成。按照该方案,装置的连接顺序为_______ (填字母编号)。

(5)乙同学只测定了固体浑浊物在热分解前后的质量分别为3.42 g和2.00g,据此计算出固体浑浊物中n[Mg(OH)2]:n[MgCO3]=_______ 。
| 实验序号 | 实验操作 | 实验现象 |
| 1 | 向7.5 mL1mol·L-1NaHCO3溶液中加入长3cm的镁条 | 持续快速产生大量气泡,溶液略显浑浊 |
(1)经检验反应产生的气体有H2,实验室检验H2的方法为
(2)小组成员认为反应产生的气体中可能有CO2,并对此进行了如下实验(图1、图2中曲线②均为对应加入镁条的数据):
| 实验序号 | 实验操作 |
| 2 | 分别称取两份6.0 mL 1 mol·L-1NaHCO3溶液于两个相同塑料瓶中(其中一个加入0.1g镁条),塞紧CO2气体传感器,采集数据,各重复实验1次,得到图1所示曲线 |
| 3 | 分别称取两份30.0 mL 1 mol·L-1NaHCO3溶液于两个相同烧杯中(其中一个加入1.1g镁条),插入pH传感器,搅拌并采集数据,得到图2所示曲线 |

图1中曲线②对应的CO2含量逐渐增大的原因为
II.探究Mg与NaHCO3溶液反应比与热水反应快的原因。
小组成员推测可能是溶液中的Na+或HCO
 加快了该反应的发生,对比实验1设计实验如下:
加快了该反应的发生,对比实验1设计实验如下:| 实验序号 | 实验操作 | 实验现象 |
| 4 | 向_______溶液中加入长3 cm的镁条 | 持续快速产生大量气泡,溶液略显浑浊 |
 加快了反应的发生。
加快了反应的发生。①实验4中横线处内容为
②查阅文献可知,Mg(OH)2质地致密,MgCO3质地疏松,请结合必要的文字和化学用语解释HCO
 能加快该反应的原因为
能加快该反应的原因为III.探究固体浑浊物的组成。
文献显示,固体浑浊物为Mg(OH)2和MgCO3的混合物。甲、乙两位同学设计不同方案,测定混合物组成。
(4)甲同学借助下图装置(可重复选用),通过测定固体热分解产物水及二氧化碳的质量,测定其组成。按照该方案,装置的连接顺序为

(5)乙同学只测定了固体浑浊物在热分解前后的质量分别为3.42 g和2.00g,据此计算出固体浑浊物中n[Mg(OH)2]:n[MgCO3]=
您最近一年使用:0次
2022-04-09更新
|
1138次组卷
|
7卷引用:河北省石家庄市2022届高三毕业班教学质量检测二(一模)化学试题
河北省石家庄市2022届高三毕业班教学质量检测二(一模)化学试题(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)秘籍21 性质探究实验-备战2022年高考化学抢分秘籍(全国通用)(已下线)化学-2022年高考押题预测卷01(福建卷)(已下线)化学-2022年高考押题预测卷03(山东卷)(已下线)押江苏卷第17题 化学实验综合题 -备战2022年高考化学临考题号押题(江苏卷)(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(实验探究题)



