名校
1 . NH3是重要的化工原料,可以制备丙烯腈、尿素、硝酸等产品。回答下列问题:
(1)合成氨反应的能量变化如图甲所示(吸附在催化剂表面的物质用“*”表示)。
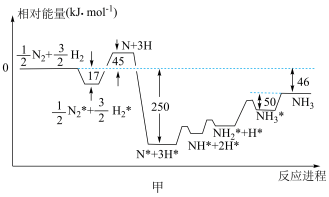
①该条件下,N2(g)+3H2(g) 2NH3(g) △H=
2NH3(g) △H=______ kJ•mol-1。
②实际生产中的工艺条件为:铁触媒作催化剂,控温773K,压强3.0×105Pa,原料气中n(N2):n(H2)=1:2.8。原料气中N2过量的理由是N2相对易得,______ 且N2的吸附分解是反应的决速步。(从平衡移动角度分析)
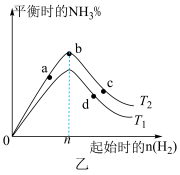
(2)其他条件不变,改变起始氢气的物质的量对工业合成氨反应的影响,实验结果如图乙所示(图中T表示温度)。则T2______ T1(填“>”“<”或“=”);a、b、c三点所处的平衡状态中,反应物N2的转化率最低的是______ (填字母)。
(3)以氨、丙烯、氧气为原料,可在催化剂存在下生成丙烯腈(C3H3N),同时得到副产物丙烯醛(C3H4O),热化学方程式如下:
主反应:C3H6(g)+NH3(g)+ O2(g)
O2(g) C3H3N(g)+3H2O(g) △H=-515kJ•mol-1;
C3H3N(g)+3H2O(g) △H=-515kJ•mol-1;
副反应:C3H6(g)+O2(g) C3H4O(g)+H2O(g) △H=-353kJ•mol-1
C3H4O(g)+H2O(g) △H=-353kJ•mol-1
已知:丙烯腈的选择性= ×100%,某气体分压=总压强×该气体物质的量分数。
×100%,某气体分压=总压强×该气体物质的量分数。
①一定条件下,平衡时丙烯腈的选择性与温度、压强的关系如图所示,则p1、p2、p3由大到小的顺序为________ 。
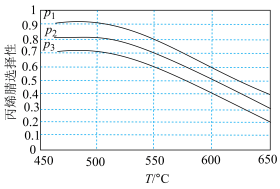
②某温度下,向100kPa的恒压密闭容器中通入1molC3H6、1molNH3和1.5molO2,发生上述反应。平衡时测得C3H6转化率为90%,H2O(g)的物质的量为2.5mol,则平衡时C3H3N的分压为______ kPa(保留3位有效数字),此温度下副反应的Kp=______ (计算结果保留三位有效数字)。
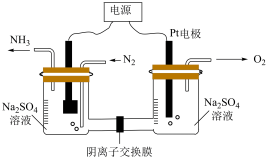
(4)常温常压下,以N2和H2O为原料的电化学合成氨是极具应用前途的绿色合成氨方法。实验室模拟氨的电化学合成过程如图所示,阴极的电极反应式为________ 。
(1)合成氨反应的能量变化如图甲所示(吸附在催化剂表面的物质用“*”表示)。

①该条件下,N2(g)+3H2(g)
 2NH3(g) △H=
2NH3(g) △H=②实际生产中的工艺条件为:铁触媒作催化剂,控温773K,压强3.0×105Pa,原料气中n(N2):n(H2)=1:2.8。原料气中N2过量的理由是N2相对易得,
(2)其他条件不变,改变起始氢气的物质的量对工业合成氨反应的影响,实验结果如图乙所示(图中T表示温度)。则T2

(3)以氨、丙烯、氧气为原料,可在催化剂存在下生成丙烯腈(C3H3N),同时得到副产物丙烯醛(C3H4O),热化学方程式如下:
主反应:C3H6(g)+NH3(g)+
 O2(g)
O2(g) C3H3N(g)+3H2O(g) △H=-515kJ•mol-1;
C3H3N(g)+3H2O(g) △H=-515kJ•mol-1;副反应:C3H6(g)+O2(g)
 C3H4O(g)+H2O(g) △H=-353kJ•mol-1
C3H4O(g)+H2O(g) △H=-353kJ•mol-1已知:丙烯腈的选择性=
 ×100%,某气体分压=总压强×该气体物质的量分数。
×100%,某气体分压=总压强×该气体物质的量分数。①一定条件下,平衡时丙烯腈的选择性与温度、压强的关系如图所示,则p1、p2、p3由大到小的顺序为

②某温度下,向100kPa的恒压密闭容器中通入1molC3H6、1molNH3和1.5molO2,发生上述反应。平衡时测得C3H6转化率为90%,H2O(g)的物质的量为2.5mol,则平衡时C3H3N的分压为
(4)常温常压下,以N2和H2O为原料的电化学合成氨是极具应用前途的绿色合成氨方法。实验室模拟氨的电化学合成过程如图所示,阴极的电极反应式为

您最近一年使用:0次
名校
解题方法
2 . 金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是将金红石TiO2 转化为TiCl4,再进一步还原得到钛。回答下列问题:
(1)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
(i)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) △H1=172kJ∙mol-1,Kp1=1.0×10-2
(ii)碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) △H2=-51kJ∙mol-1,Kp2=1.2×1012Pa
①反应2C(s)+O2(g)=2CO(g)的H 为___________ kJ mol-1, Kp =___________ Pa。
②碳氯化的反应趋势远大于直接氯化,其原因是___________ 。
③对于碳氯化反应:增大压强,平衡___________ 移动(填“向左”“向右”或“不”);温度升高,平衡转化率___________ (填“变大”“变小”或“不变”)。
(2)在1.0 105 Pa ,将TiO2、C、Cl2以物质的量比 1∶2.2∶2 进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
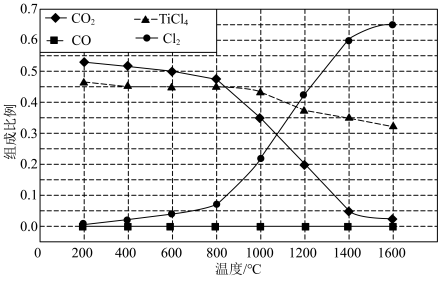
图中显示,在200℃平衡时TiO2 几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是___________ 。
(3)TiO2碳氯化是一个“气—固—固”反应,有利于TiO2 C “固—固”接触的措施是________ 。
(1)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
(i)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) △H1=172kJ∙mol-1,Kp1=1.0×10-2
(ii)碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) △H2=-51kJ∙mol-1,Kp2=1.2×1012Pa
①反应2C(s)+O2(g)=2CO(g)的H 为
②碳氯化的反应趋势远大于直接氯化,其原因是
③对于碳氯化反应:增大压强,平衡
(2)在1.0 105 Pa ,将TiO2、C、Cl2以物质的量比 1∶2.2∶2 进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。

图中显示,在200℃平衡时TiO2 几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是
(3)TiO2碳氯化是一个“气—固—固”反应,有利于TiO2 C “固—固”接触的措施是
您最近一年使用:0次
名校
解题方法
3 . 将 转化为
转化为 是工业上生产硫酸的关键步骤,发生的反应为
是工业上生产硫酸的关键步骤,发生的反应为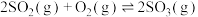

 ,某小组计划研究在相同温度下该反应的物质变化和能量变化,他们分别在恒温下的密闭容器中加入一定量的物质,获得如下数据:
,某小组计划研究在相同温度下该反应的物质变化和能量变化,他们分别在恒温下的密闭容器中加入一定量的物质,获得如下数据:
回答下列问题
(1)下列说法,能说明容器①内的反应达到平衡状态的是 。
(2)用含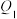 、
、 的代数式表示0-
的代数式表示0- 时间段内
时间段内 的反应速率
的反应速率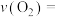
______________________ 。
(3) (g)与
(g)与 (g)在
(g)在 作催化剂的条件下的反应历程如下:
作催化剂的条件下的反应历程如下:
①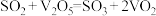 ;
;
②_______________________ (写出第2步反应的化学方程式);
 能加快反应速率的根本原因是
能加快反应速率的根本原因是________________________ 。
(4)其它条件不变,若将容器①改为绝热容器,则 的平衡转化率
的平衡转化率___________ (填“增大”“减小”或“不变”)。
(5)容器①②中均达到平衡时放出热量2
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(6)在450℃、100kPa的恒温恒压条件下, 的平衡体积分数随起始时投料
的平衡体积分数随起始时投料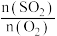 的变化如图所示,用平衡压强(平衡压强=该物质的体积分数×总压强)代替平衡浓度,则450℃时,该反应的
的变化如图所示,用平衡压强(平衡压强=该物质的体积分数×总压强)代替平衡浓度,则450℃时,该反应的
___________ (计算出具体数值)。
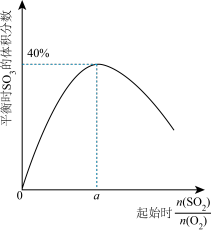
 转化为
转化为 是工业上生产硫酸的关键步骤,发生的反应为
是工业上生产硫酸的关键步骤,发生的反应为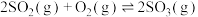

 ,某小组计划研究在相同温度下该反应的物质变化和能量变化,他们分别在恒温下的密闭容器中加入一定量的物质,获得如下数据:
,某小组计划研究在相同温度下该反应的物质变化和能量变化,他们分别在恒温下的密闭容器中加入一定量的物质,获得如下数据:容器编号 | 容器体积/L | 起始时各物质的物质的量/mol | 达到平衡的时间/min | 平衡时反应热量变化/kJ | ||
|
|
| ||||
① | 1 | 0.050 | 0.030 | 0 |
| 放出热量: |
② | 1 | 0.100 | 0.060 | 0 |
| 放出热量: |
(1)下列说法,能说明容器①内的反应达到平衡状态的是 。
| A.容器内气体总压强不再变化。 |
| B.混合气体密度不再变化。 |
| C.混合气体平均分子量不再变化。 |
D. 和 和 的物质的量之和为0.05mol且保持不变。 的物质的量之和为0.05mol且保持不变。 |
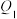 、
、 的代数式表示0-
的代数式表示0- 时间段内
时间段内 的反应速率
的反应速率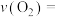
(3)
 (g)与
(g)与 (g)在
(g)在 作催化剂的条件下的反应历程如下:
作催化剂的条件下的反应历程如下:①
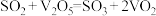 ;
;②
 能加快反应速率的根本原因是
能加快反应速率的根本原因是(4)其它条件不变,若将容器①改为绝热容器,则
 的平衡转化率
的平衡转化率(5)容器①②中均达到平衡时放出热量2

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(6)在450℃、100kPa的恒温恒压条件下,
 的平衡体积分数随起始时投料
的平衡体积分数随起始时投料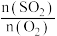 的变化如图所示,用平衡压强(平衡压强=该物质的体积分数×总压强)代替平衡浓度,则450℃时,该反应的
的变化如图所示,用平衡压强(平衡压强=该物质的体积分数×总压强)代替平衡浓度,则450℃时,该反应的

您最近一年使用:0次
名校
解题方法
4 . 二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。回答下列问题:
(1)CO2催化加氢生成乙烯和水的反应中,反应物的物质的量之比n(CO2)∶n(H2)=___________ 。当反应达到平衡时,若增大压强,则n(C2H4)___________ (填“变大”“变小”或“不变”)。
(2)理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1 MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
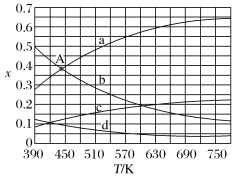
图中,表示H2、H2O变化的曲线分别是___________ 、___________ 。CO2催化加氢合成C2H4反应的ΔH___________ 0(填“大于”或“小于”)。
(3)根据图中点A(440 K,0.39),计算该温度时平衡分压p(H2O) =___________ ,p(C2H4)=___________ (分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C3H6、C3H8、C4H8等低碳烃。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当___________ 。
(1)CO2催化加氢生成乙烯和水的反应中,反应物的物质的量之比n(CO2)∶n(H2)=
(2)理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1 MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。

图中,表示H2、H2O变化的曲线分别是
(3)根据图中点A(440 K,0.39),计算该温度时平衡分压p(H2O) =
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C3H6、C3H8、C4H8等低碳烃。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当
您最近一年使用:0次
5 . 2021年,中国科学院天津工业生物技术研究所马延和研究员带领团队,采用一种类似“搭积木”的方式,从头设计、构建了11步反应的非自然固碳与淀粉合成途径,在实验室中首次实现从二氧化碳到淀粉分子的全合成。其原理首先是利用化学催化剂将高浓度二氧化碳在高密度氢能作用下合成CH3OH。已知:
i.CO2(g)+H2(g) CO(g)+H2O(g) △H1=+41.19kJ•mol-1
CO(g)+H2O(g) △H1=+41.19kJ•mol-1
ii.CO(g)+2H2(g) CH3OH(g) △H2
CH3OH(g) △H2
iii.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3=-49.58kJ•mol-1
CH3OH(g)+H2O(g) △H3=-49.58kJ•mol-1
请回答下列问题:
(1)写出反应i化学平衡常数的表达式:K=______ 。
(2)反应ii的△H2=______ ,在______ (填“较高”或“较低”)温度下有利于该反应自发进行。
(3)在容积为2L的密闭容器中充入1molCO2(g)和3molH2(g)发生上述反应iii,在两种不同的实验条件下进行反应,测得CH3OH(g)的物质的量随时间变化情况如图所示:
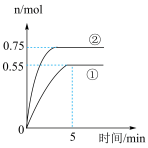
①前5min内实验①用CH3OH浓度变化表示的平均反应速率为______ ,实验②中CO2的平衡转化率为______ ,与①相比,②仅改变一种反应条件,所改变的条件是______ 。
②能说明上述反应达到平衡状态的是______ (填编号)。
a.容器内压强不再变化
b.单位时间内每消耗3molH2,同时生成1molH2O
c.CO2的浓度保持不变
d.v逆(CO2)=3v正(H2)
i.CO2(g)+H2(g)
 CO(g)+H2O(g) △H1=+41.19kJ•mol-1
CO(g)+H2O(g) △H1=+41.19kJ•mol-1ii.CO(g)+2H2(g)
 CH3OH(g) △H2
CH3OH(g) △H2iii.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3=-49.58kJ•mol-1
CH3OH(g)+H2O(g) △H3=-49.58kJ•mol-1请回答下列问题:
(1)写出反应i化学平衡常数的表达式:K=
(2)反应ii的△H2=
(3)在容积为2L的密闭容器中充入1molCO2(g)和3molH2(g)发生上述反应iii,在两种不同的实验条件下进行反应,测得CH3OH(g)的物质的量随时间变化情况如图所示:

①前5min内实验①用CH3OH浓度变化表示的平均反应速率为
②能说明上述反应达到平衡状态的是
a.容器内压强不再变化
b.单位时间内每消耗3molH2,同时生成1molH2O
c.CO2的浓度保持不变
d.v逆(CO2)=3v正(H2)
您最近一年使用:0次
名校
6 . 在密闭容器中进行如下反应:
 ,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
(1)增加 ,则平衡
,则平衡___________ (填“逆向移动”“正向移动”或“不移动”,下同),
___________ (填“增大”“减小”或“不变”,下同)。
(2)保持温度不变,增大反应容器的容积,则平衡___________ ,
___________ 。
(3)保持反应容器的容积和温度不变,通入 ,则平衡
,则平衡___________ ,
___________ 。
(4)保持反应容器的容积不变,升高温度,则平衡___________ ,
___________ 。

 ,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。(1)增加
 ,则平衡
,则平衡
(2)保持温度不变,增大反应容器的容积,则平衡

(3)保持反应容器的容积和温度不变,通入
 ,则平衡
,则平衡
(4)保持反应容器的容积不变,升高温度,则平衡

您最近一年使用:0次
2021-10-23更新
|
101次组卷
|
6卷引用:云南省保山第一中学2022-2023学年高二下学期期末考试化学试题
云南省保山第一中学2022-2023学年高二下学期期末考试化学试题云南省昌宁县第一中学2022-2023学年高二下学期期末考试化学试题山西省大同市平城中学校2021-2022学年高二上学期10月月考化学试卷(已下线)2.3.2 温度变化对化学平衡的影响(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)安徽省六安市晓天中学2021-2022学年高二上学期期中测试化学试题





