1 . 碳粉高温下还原 制取纳米级
制取纳米级 :
: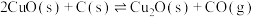
 ,反应达平衡后,下列说法正确的是
,反应达平衡后,下列说法正确的是
 制取纳米级
制取纳米级 :
: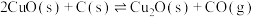
 ,反应达平衡后,下列说法正确的是
,反应达平衡后,下列说法正确的是A.升高温度, 增大、 增大、 减小 减小 |
B.保持温度不变,通入少量CO,达新平衡后 变大 变大 |
C.加入少量碳粉,可提高 的平衡转化率 的平衡转化率 |
D.分离出CO,有利于 的生成 的生成 |
您最近一年使用:0次
2 . 已知: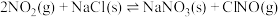
 ,下列说法正确的是
,下列说法正确的是
A.该反应的平衡常数可表达为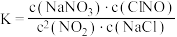 |
| B.该反应一定能自发进行 |
C.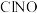 分子的VSEPR模型名称为平面三角形 分子的VSEPR模型名称为平面三角形 |
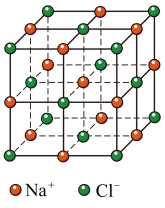
D. 晶胞(如图所示)中每个 晶胞(如图所示)中每个 周围与其距离最近的 周围与其距离最近的 有12个 有12个 |
您最近一年使用:0次
名校
3 .  消除
消除 的反应为:
的反应为: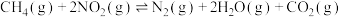
 。下列说法正确的是
。下列说法正确的是
 消除
消除 的反应为:
的反应为: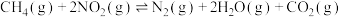
 。下列说法正确的是
。下列说法正确的是| A.正反应的活化能大于逆反应的活化能 |
| B.平衡时升高温度,v正增大,v逆减小 |
C.平衡常数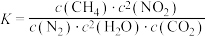 |
| D.该反应在任何温度下都可自发进行 |
您最近一年使用:0次
2023-05-19更新
|
759次组卷
|
9卷引用:海南省海口市2023年高三高考模拟化学试题
海南省海口市2023年高三高考模拟化学试题(已下线)第13练 化学反应速率与化学平衡的综合考查 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)考点巩固卷08 化学反应速率与化学平衡(3大考点45题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)河北省石家庄市第一中学2022-2023学年高一下学期7月期末化学试题(已下线)期中考试模拟试题(一)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)四川省自贡市第二十二中学校2023-2024学年高二上学期期中考试化学试题广东省惠州市龙门县高级中学2023-2024学年高二上学期期中考试化学试题甘肃省白银市会宁县第三中学2023-2024学年高二上学期期中考试化学试题
名校
4 . 将烟气和空气中的 通过催化方式直接还原为甲烷等燃料的过程具有非常重要的意义。
通过催化方式直接还原为甲烷等燃料的过程具有非常重要的意义。
I.光催化还原
(1)华中科技大学某团队构建了一种光催化剂使 和
和 反应生成
反应生成 和
和 ,其中
,其中 的转化率约为
的转化率约为 ,写出该化学方程式:
,写出该化学方程式:________________ 。
II.热催化还原——萨巴蒂尔反应: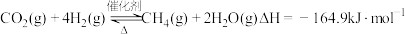
 时,在一恒容密闭容器中通入
时,在一恒容密闭容器中通入 、
、 ,至其分压分别为
,至其分压分别为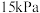 、
、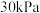 ,再加入催化剂并加热使其发生萨巴蒂尔反应。
,再加入催化剂并加热使其发生萨巴蒂尔反应。
(2)为使固体催化剂与反应物充分接触,应采取的措施是________________ 。
(3)写出该反应的平衡常数表达式:
________________ 。(用浓度表示)。
(4)研究表明 的反应速率
的反应速率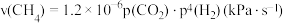 ,某时刻测得
,某时刻测得 的分压为
的分压为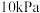 ,则该时刻
,则该时刻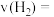
________  。
。
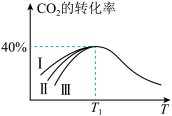
(5)相同时间内,不同催化剂(I、II、III)下,测得 的转化率如图所示。在
的转化率如图所示。在 时,不同催化剂下,
时,不同催化剂下, 的转化率相同的原因是
的转化率相同的原因是________________ 。
(6) 光催化还原和热催化还原法中更好的是
光催化还原和热催化还原法中更好的是________ ,简述理由:________ (答一条即可)。
 通过催化方式直接还原为甲烷等燃料的过程具有非常重要的意义。
通过催化方式直接还原为甲烷等燃料的过程具有非常重要的意义。I.光催化还原
(1)华中科技大学某团队构建了一种光催化剂使
 和
和 反应生成
反应生成 和
和 ,其中
,其中 的转化率约为
的转化率约为 ,写出该化学方程式:
,写出该化学方程式:II.热催化还原——萨巴蒂尔反应:
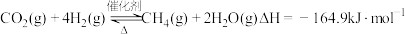
 时,在一恒容密闭容器中通入
时,在一恒容密闭容器中通入 、
、 ,至其分压分别为
,至其分压分别为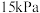 、
、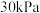 ,再加入催化剂并加热使其发生萨巴蒂尔反应。
,再加入催化剂并加热使其发生萨巴蒂尔反应。(2)为使固体催化剂与反应物充分接触,应采取的措施是
(3)写出该反应的平衡常数表达式:

(4)研究表明
 的反应速率
的反应速率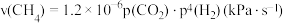 ,某时刻测得
,某时刻测得 的分压为
的分压为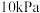 ,则该时刻
,则该时刻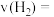
 。
。(5)相同时间内,不同催化剂(I、II、III)下,测得
 的转化率如图所示。在
的转化率如图所示。在 时,不同催化剂下,
时,不同催化剂下, 的转化率相同的原因是
的转化率相同的原因是
(6)
 光催化还原和热催化还原法中更好的是
光催化还原和热催化还原法中更好的是
您最近一年使用:0次
5 . 根据所学知识回答下列问题:
I.用纯净的锌粒与稀盐酸反应制取氢气,请回答:

(1)实验过程如图所示,化学反应速率最快的是_______
A.OE段 B.EF段 C.FG段
(2)请解释图中曲线变化的原因:_______ 。
(3)为了减缓上述反应的速率,欲向溶液中加入下列物质少许,可行的是_______。
II.在温度为373K时,将0.100mol N2O4气体通入1L的恒容密闭容器中,发生反应N2O4(g) 2NO2(g)。下图是测定到的N2O4的浓度变化曲线图。
2NO2(g)。下图是测定到的N2O4的浓度变化曲线图。

(4)计算在20至40秒时间内,NO2的平均生成速率为_______ 。
(5)该反应的化学平衡常数表达式为_______ 。
(6)下表是不同温度下测定得到的该反应的化学平衡常数。
据此可推测该反应(生成NO2)是_______ 反应(选填“吸热”或“放热”)。
(7)反应达平衡后再加入0.100mol的N2O4气体,推测反应重新达到平衡后N2O4的转化率_______ (选填“增大”、“不变”或“减小”)
I.用纯净的锌粒与稀盐酸反应制取氢气,请回答:

(1)实验过程如图所示,化学反应速率最快的是
A.OE段 B.EF段 C.FG段
(2)请解释图中曲线变化的原因:
(3)为了减缓上述反应的速率,欲向溶液中加入下列物质少许,可行的是_______。
| A.NaCl溶液 | B.硫酸铜溶液 | C.浓盐酸 | D.CH3COONa固体 |
II.在温度为373K时,将0.100mol N2O4气体通入1L的恒容密闭容器中,发生反应N2O4(g)
 2NO2(g)。下图是测定到的N2O4的浓度变化曲线图。
2NO2(g)。下图是测定到的N2O4的浓度变化曲线图。
(4)计算在20至40秒时间内,NO2的平均生成速率为
(5)该反应的化学平衡常数表达式为
(6)下表是不同温度下测定得到的该反应的化学平衡常数。
| T/K | 323 | 373 |
| K值 | 0.022 | 0.36 |
(7)反应达平衡后再加入0.100mol的N2O4气体,推测反应重新达到平衡后N2O4的转化率
您最近一年使用:0次
2022-11-04更新
|
171次组卷
|
2卷引用:海南省海口市秀英区某校2023-2024学年高二上学期期中检测化学试题
名校
6 . 一定温度下,某气态平衡体系的平衡常数表达式为 ,下列有关该平衡体系的说法正确的是
,下列有关该平衡体系的说法正确的是
 ,下列有关该平衡体系的说法正确的是
,下列有关该平衡体系的说法正确的是| A.升高温度,平衡常数K一定增大 |
| B.增大A的浓度,平衡向正反应方向移动 |
| C.增大压强,C的体积分数增大 |
| D.升高温度,若B的百分含量减少,则正反应是放热反应 |
您最近一年使用:0次
2021-11-06更新
|
468次组卷
|
27卷引用:海南省海口市秀英区某校2023-2024学年高二上学期期中检测化学试题
海南省海口市秀英区某校2023-2024学年高二上学期期中检测化学试题广西南宁市第三中学2017-2018学年高二上学期期末考试化学试题甘肃省民勤县第一中学2020-2021学年高二上学期第二次月考化学(理) 试题内蒙古自治区包头市第六中学2020-2021学年高二上学期期中考试化学试题辽宁省锦州市义县高中2020-2021学年高一下学期4月考试化学试题天津市实验中学滨海学校黄南民族班2020-2021学年高二下学期期中化学试题湖北省宜昌市夷陵中学2020-2021学年高二下学期五月份阶段性检测化学试题四川省广安市武胜烈面中学校2021-2022学年高二10月月考化学试题广西百色中学2021-2022学年高二上学期第一次月考化学试题重庆市2021-2022学年高二上学期期中考试化学试题福建省龙岩市六县一中2021-2022学年高二上学期期中联考化学试题贵州省黔西南州2021~2022学年高二上学期期中考试化学试题河南省部分名校2021-2022学年高二上学期阶段性检测(三)化学试题安徽省淮北师范大学附属实验中学2021-2022学年高二上学期期中考试化学试题福建省武平县第一中学2021-2022学年高二上学期期中考试化学试题(已下线)卷11 化学反应速率和平衡选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)安徽省六安市晓天中学2021-2022学年高二上学期期中测试化学试题浙江省金华市江南中学2021-2022学年高二上学期期中考试化学试题陕西省西安市雁塔区第二中学2021-2022学年高二上学期第一次月考化学试题福建省长汀县第一中学2022-2023学年高二上学期第一次月考化学试题河北省石家庄新乐市第一中学2022-2023学年高二上学期第一次月考化学试题海南省文昌中学2022-2023学年高二上学期第一次月考化学试题天津市第九十五中学益中学校2022-2023学年高二上学期期中考试化学试题福建省厦门市湖滨中学2022-2023学年高二上学期期中考试化学试题黑龙江省饶河县高级中学2022-2023学年高二上学期期中考试化学试题陕西省渭南市尚德中学2021-2022学年高二上学期第二次质量检测化学试题四川省眉山市仁寿县校际2023-2024学年高二上学期10月联考化学试题
7 . 已知:3H2(g)+N2(g) 2NH3(g);ΔH<0,
2NH3(g);ΔH<0,
请回答:(1)该反应的化学平衡常数表达式为_______ 。
(2)当温度T1>T2时,化学平衡常数K1_______ K2(填“>”、“<”或“=”)。
(3)在恒温、恒容的密闭容器中,下列描述能说明上述反应已达化学平衡状态的是______ (填字母序号)。
a.生成2mol NH3的同时,消耗1 mol N2 b.容器中各组分的物质的量浓度不随时间而变化
c.容器中混合气体的压强不随时间而变化 d.容器中气体的分子总数不随时间而变化
(4)在工业生产中,可使H2的转化率提高的措施_______ ;化学反应速率增大的措施_______ (各写一条合理措施即可)。
 2NH3(g);ΔH<0,
2NH3(g);ΔH<0,请回答:(1)该反应的化学平衡常数表达式为
(2)当温度T1>T2时,化学平衡常数K1
(3)在恒温、恒容的密闭容器中,下列描述能说明上述反应已达化学平衡状态的是
a.生成2mol NH3的同时,消耗1 mol N2 b.容器中各组分的物质的量浓度不随时间而变化
c.容器中混合气体的压强不随时间而变化 d.容器中气体的分子总数不随时间而变化
(4)在工业生产中,可使H2的转化率提高的措施
您最近一年使用:0次
8 . 在一定条件下,向容积为2 L的恒容密闭容器中充入1 mol CH3OH(g)和3 mol H2O(g),CH3OH(g)+H2O(g) CO2(g)+3H2(g) △H=+49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
CO2(g)+3H2(g) △H=+49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
(1)该条件下反应的化学平衡常数表达式为K=___________ 。
(2)平衡时升高温度,化学平衡常数的变化为___________ (填“变大”、“变小”或“不变”)。
(3)该条件下反应到达平衡时,CH3OH的转化率为___________ ,混合气体的压强是反应前的___________ 倍。
(4)该条件下判断该反应达平衡状态的依据是(填序号)___________ 。
a.v正(CH3OH)=v逆(CO2) b.混合气体的密度不变
c.c(CH3OH)=c(H2O) d.混合气体的总物质的量不变
(5)将体积压缩为原来的一半,下列描述正确的是( )
a.正反应速率减小,逆反应速率增大 b.正反应速率增大,逆反应速率增大
c.正反应速率小于逆反应速率 d.c(CO2)减小
 CO2(g)+3H2(g) △H=+49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
CO2(g)+3H2(g) △H=+49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则(1)该条件下反应的化学平衡常数表达式为K=
(2)平衡时升高温度,化学平衡常数的变化为
(3)该条件下反应到达平衡时,CH3OH的转化率为
(4)该条件下判断该反应达平衡状态的依据是(填序号)
a.v正(CH3OH)=v逆(CO2) b.混合气体的密度不变
c.c(CH3OH)=c(H2O) d.混合气体的总物质的量不变
(5)将体积压缩为原来的一半,下列描述正确的是
a.正反应速率减小,逆反应速率增大 b.正反应速率增大,逆反应速率增大
c.正反应速率小于逆反应速率 d.c(CO2)减小
您最近一年使用:0次
2021-01-13更新
|
308次组卷
|
2卷引用:海南省海口市琼山中学2019-2020学年度高二上学期第二次月考化学试题
名校
解题方法
9 . 实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求,依靠理论知识做基础。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为:K=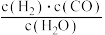 它所对应的化学反应为:
它所对应的化学反应为:___________ 。
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) CH3OH(g) △H =-90.8 kJ/mol
CH3OH(g) △H =-90.8 kJ/mol
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H =-23.5 kJ/mol
CH3OCH3(g)+H2O(g) △H =-23.5 kJ/mol
③CO(g)+H2O(g) CO2(g)+H2(g) △H =-41.3 kJ/mol
CO2(g)+H2(g) △H =-41.3 kJ/mol
总反应:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g) 的△H =
CH3OCH3(g)+CO2(g) 的△H =___________ ;
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g),该反应平衡常数随温度的变化如下表所示:
CO2(g)+H2(g),该反应平衡常数随温度的变化如下表所示:
该反应的正反应方向是___________ 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为 0.020 mol/L,在该条件下,CO的平衡转化率为:___________ 。
(4)从氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如 NO、NO2、N2O4等,对反应N2O4(g) 2NO2(g) △H>0,在温度为 T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如图甲所示。下列说法正确的是
2NO2(g) △H>0,在温度为 T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如图甲所示。下列说法正确的是___________ 。

A A、C 两点的反应速率:A>C
B A、C 两点气体的颜色:A 深,C浅
C A、C 两点的化学平衡常数:A>C
D 由状态 B 到状态 A,可以用加热的方法
(5)NO2可用氨水吸收生成NH4NO3,25℃时,将m mol NH4NO3溶于水,溶液显酸性,向该溶液滴加 n L 氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将___________ (填“正向”“不”或“逆向”)移动。
(6)某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图乙所示,电极为多孔的材料能吸附气体,同时也能使气体与电解质溶液充分接触。

①A电极为原电池的___________ 极(填“正”或“负”);
②溶液中的H+移向极(用 A、B 表示)___________ ;
③B电极的电极反应式为___________ ;
④电池的总反应式为___________ 。
(1)已知某反应的平衡表达式为:K=
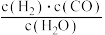 它所对应的化学反应为:
它所对应的化学反应为:(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)
 CH3OH(g) △H =-90.8 kJ/mol
CH3OH(g) △H =-90.8 kJ/mol②2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H =-23.5 kJ/mol
CH3OCH3(g)+H2O(g) △H =-23.5 kJ/mol ③CO(g)+H2O(g)
 CO2(g)+H2(g) △H =-41.3 kJ/mol
CO2(g)+H2(g) △H =-41.3 kJ/mol 总反应:3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g) 的△H =
CH3OCH3(g)+CO2(g) 的△H =(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)
 CO2(g)+H2(g),该反应平衡常数随温度的变化如下表所示:
CO2(g)+H2(g),该反应平衡常数随温度的变化如下表所示:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(4)从氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如 NO、NO2、N2O4等,对反应N2O4(g)
 2NO2(g) △H>0,在温度为 T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如图甲所示。下列说法正确的是
2NO2(g) △H>0,在温度为 T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如图甲所示。下列说法正确的是
A A、C 两点的反应速率:A>C
B A、C 两点气体的颜色:A 深,C浅
C A、C 两点的化学平衡常数:A>C
D 由状态 B 到状态 A,可以用加热的方法
(5)NO2可用氨水吸收生成NH4NO3,25℃时,将m mol NH4NO3溶于水,溶液显酸性,向该溶液滴加 n L 氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将
(6)某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图乙所示,电极为多孔的材料能吸附气体,同时也能使气体与电解质溶液充分接触。

①A电极为原电池的
②溶液中的H+移向极(用 A、B 表示)
③B电极的电极反应式为
④电池的总反应式为
您最近一年使用:0次
名校
解题方法
10 . 已知在容积为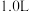 的恒容密闭容器中存在可逆反应:
的恒容密闭容器中存在可逆反应:
 。该可逆反应的平衡常数与温度的关系如表:
。该可逆反应的平衡常数与温度的关系如表:
请回答下列问题:
 该可逆反应的平衡常数表达式为
该可逆反应的平衡常数表达式为
________ 。
 如图是温度分别为
如图是温度分别为 和
和 时物质B的浓度与时间的变化关系:
时物质B的浓度与时间的变化关系:

①开始投料时,在容器中加入的物质一定有A、B、C中的________ 。
②图象中
________  填“大于”“小于”或“等于”
填“大于”“小于”或“等于” ,你做出该判断的理由是
,你做出该判断的理由是___________ 。
(3)判断上述可逆反应达到平衡状态的依据有________  填字母
填字母 。
。
 单位时间消耗A和B的物质的量之比为
单位时间消耗A和B的物质的量之比为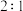
 体系压强不再随时间改变
体系压强不再随时间改变
 容器内气体的密度不再随时间改变
容器内气体的密度不再随时间改变
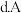 的浓度不再随时间改变
的浓度不再随时间改变
(4)该反应为____________ 热反应。
(5)温度为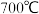 时,在容器中加入
时,在容器中加入 和
和 ,
,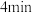 时反应达到平衡。
时反应达到平衡。
①平衡时容器内气体的总物质的量为________ 。
②A参加反应的物质的量为________ 。
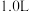 的恒容密闭容器中存在可逆反应:
的恒容密闭容器中存在可逆反应:
 。该可逆反应的平衡常数与温度的关系如表:
。该可逆反应的平衡常数与温度的关系如表:温度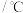 | 300 | 500 | 700 | 900 |
| 平衡常数 |  | 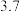 | 2 | 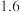 |
请回答下列问题:
 该可逆反应的平衡常数表达式为
该可逆反应的平衡常数表达式为
 如图是温度分别为
如图是温度分别为 和
和 时物质B的浓度与时间的变化关系:
时物质B的浓度与时间的变化关系:
①开始投料时,在容器中加入的物质一定有A、B、C中的
②图象中

 填“大于”“小于”或“等于”
填“大于”“小于”或“等于” ,你做出该判断的理由是
,你做出该判断的理由是(3)判断上述可逆反应达到平衡状态的依据有
 填字母
填字母 。
。 单位时间消耗A和B的物质的量之比为
单位时间消耗A和B的物质的量之比为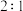
 体系压强不再随时间改变
体系压强不再随时间改变 容器内气体的密度不再随时间改变
容器内气体的密度不再随时间改变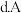 的浓度不再随时间改变
的浓度不再随时间改变(4)该反应为
(5)温度为
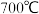 时,在容器中加入
时,在容器中加入 和
和 ,
,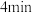 时反应达到平衡。
时反应达到平衡。①平衡时容器内气体的总物质的量为
②A参加反应的物质的量为
您最近一年使用:0次



