解题方法
1 . 下列不属于自发过程的是
| A | B | C | D |
 |  |  |  |
| 水从高处往低处流 | 冰在常温下融化 | 石墨转化为金刚石 | 铁在潮湿空气中生锈 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 关于反应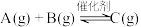
 ,下列说法正确的是
,下列说法正确的是
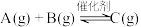
 ,下列说法正确的是
,下列说法正确的是| A.一定是自发反应 |
| B.温度升高,逆反应速率减慢 |
| C.反应物浓度增大,平衡向正反应方向进行 |
| D.催化剂不参与化学反应 |
您最近一年使用:0次
名校
3 . 2023年9月23日,杭州亚运会主火炬塔使用了燃烧高效、排放清洁、可再生、运输便捷的甲醇燃料,这是人类历史上第一次废碳再生利用,有利于推进“碳达峰”和“碳中和”。工业上用 来生产燃料甲醇的反应为
来生产燃料甲醇的反应为
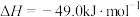 ,现将
,现将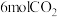 和
和 充入
充入 的恒温刚性密闭容器中,测得的氢气物质的量随时间变化如图中实线所示:
的恒温刚性密闭容器中,测得的氢气物质的量随时间变化如图中实线所示:
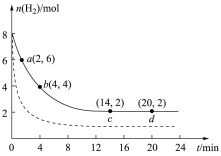
回答下列问题:
(1)该反应在
(2)下列说法不能表明该反应已经达到平衡状态的是_______(填选项字母)。
| A.压强保持不变 |
| B.混合气体的平均相对分子质量不变 |
C.混合气体中 的百分含量保持不变 的百分含量保持不变 |
D. |
(3)
 点正反应速率
点正反应速率 点逆反应速率,前
点逆反应速率,前 内,用
内,用 表示的平均反应速率为
表示的平均反应速率为(4)平衡时
 的转化率为
的转化率为
 。
。(5)仅改变某一实验条件再进行实验,测得
 的物质的量随时间变化如图中虚线所示,对应的实验条件改变的是
的物质的量随时间变化如图中虚线所示,对应的实验条件改变的是(6)如果要加快反应速率并且提高
 平衡转化率,可以采取的措施有
平衡转化率,可以采取的措施有(7)一定条件下,单位时间内不同温度下测定的
 转化率如图所示。温度高于
转化率如图所示。温度高于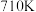 时,随温度的升高
时,随温度的升高 转化率降低的原因可能是
转化率降低的原因可能是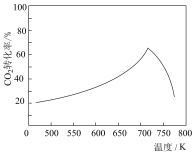
您最近一年使用:0次
4 . 究二氧化碳的回收对我国2060年实现碳中和具有现实意义:
(1)已知:①CO(g)+H2O(g) CO2(g)+H2(g) △H=-41kJ•mol-1
CO2(g)+H2(g) △H=-41kJ•mol-1
②C(s)+2H2(g) CH4(g) △H=-73kJ•mol-1
CH4(g) △H=-73kJ•mol-1
③2CO(g) CO2(g)+C(s) △H=-171kJ•mol-1
CO2(g)+C(s) △H=-171kJ•mol-1
写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:______ 。
(2)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) △H。
C2H5OH(g)+3H2O(g) △H。
①通过表格中的数值可以推断:其正反应在_____ (填“高温”、“低温”或“任何温度”)下能自发进行。
②CO2的平衡转化率与压强、温度及氢碳比m[m= ]的关系分别如图a和图b所示。
]的关系分别如图a和图b所示。
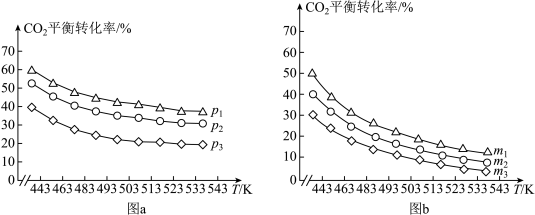
图a中压强从大到小的顺序为_____ ,图b中氢碳比m从大到小的顺序为_____ 。
(3)工业上也可以利用CO2和H2合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)某1L恒温恒容密闭容器中充入1molCO2和3molH2发生反应,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示:
CH3OH(g)+H2O(g)某1L恒温恒容密闭容器中充入1molCO2和3molH2发生反应,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示:
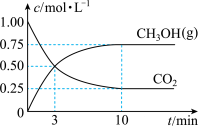
①0~3min内,H2的平均反应速率为_____ mol•L-1•min-1,该温度下的平衡常数为K=_____ (单位可忽略)。若达平衡时,保持温度不变,向容器中再充入CO2、H2、CH3OH和H2O各0.25mol,则此时v正_____ v逆(填“>”、“<”、或“=”)。
②下列说法能说明反应达到化学平衡状态的是_____ 。
A.H2的消耗速率与CH3OH的消耗速率之比为3∶1 B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.c(CO2)和c(H2O)的浓度相等时
(4)盖斯定律认为:不管化学过程是一步完成或分几步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
①已知:H2O(g)=H2O(l) △H1=-Q1kJ/mol
C2H5OH(g)=C2H5OH(l) △H2=-Q2kJ/mol
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H3=-Q3kJ/mol
若使46g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为______ kJ。
②碳(s)在氧气供应不充足时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应:C(s)+ O2(g)=CO(g)的△H。但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有
O2(g)=CO(g)的△H。但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有______ 。
(1)已知:①CO(g)+H2O(g)
 CO2(g)+H2(g) △H=-41kJ•mol-1
CO2(g)+H2(g) △H=-41kJ•mol-1②C(s)+2H2(g)
 CH4(g) △H=-73kJ•mol-1
CH4(g) △H=-73kJ•mol-1③2CO(g)
 CO2(g)+C(s) △H=-171kJ•mol-1
CO2(g)+C(s) △H=-171kJ•mol-1写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:
(2)工业上用二氧化碳催化加氢可合成乙醇,其反应原理为:2CO2(g)+6H2(g)
 C2H5OH(g)+3H2O(g) △H。
C2H5OH(g)+3H2O(g) △H。| 温度/ | 400 | 500 |
| 平衡常数K | 9 | 5.3 |
②CO2的平衡转化率与压强、温度及氢碳比m[m=
 ]的关系分别如图a和图b所示。
]的关系分别如图a和图b所示。
图a中压强从大到小的顺序为
(3)工业上也可以利用CO2和H2合成甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)某1L恒温恒容密闭容器中充入1molCO2和3molH2发生反应,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示:
CH3OH(g)+H2O(g)某1L恒温恒容密闭容器中充入1molCO2和3molH2发生反应,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示:
①0~3min内,H2的平均反应速率为
②下列说法能说明反应达到化学平衡状态的是
A.H2的消耗速率与CH3OH的消耗速率之比为3∶1 B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.c(CO2)和c(H2O)的浓度相等时
(4)盖斯定律认为:不管化学过程是一步完成或分几步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
①已知:H2O(g)=H2O(l) △H1=-Q1kJ/mol
C2H5OH(g)=C2H5OH(l) △H2=-Q2kJ/mol
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H3=-Q3kJ/mol
若使46g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为
②碳(s)在氧气供应不充足时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应:C(s)+
 O2(g)=CO(g)的△H。但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有
O2(g)=CO(g)的△H。但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有
您最近一年使用:0次
5 . 已知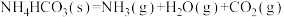
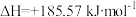 ,下列说法中正确的是
,下列说法中正确的是
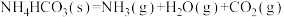
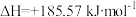 ,下列说法中正确的是
,下列说法中正确的是| A.该反应任何温度下都不能自发进行 |
| B.该反应能自发进行,由于该反应是一个熵增加的反应 |
| C.其他条件不变,使用催化剂可以改变化学反应进行的方向 |
| D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
您最近一年使用:0次
6 . 1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才,现将1molN2和3molH2投入1L的密闭容器,在一定条件下,利用反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H<0. 回答下列问题:
H<0. 回答下列问题:
(1)合成氨反应平衡常数的表达式为_______ 。温度升高,K值_______ (填“增大”“减小”或“不变"):使用催化剂,K值_______ (填“增大“减小”或“不变”)。
(2)反应的 S
S_______ 0(填“>”“<"或“=”)
(3)有利于提高平衡混合物中氨含量的条件有_______ (填序号)。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(4)当反应达到平衡后,向体系中充入N2的,平衡_______ 移动(填“正向”“逆向”或“不”);给体系升温,
_______ (填“增大”“减小”或不变”),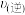
_______ (填“增大”“减小”或“不变”),平衡_______ 移动(填“正向”“逆向”或“不”)。
 2NH3(g)
2NH3(g)  H<0. 回答下列问题:
H<0. 回答下列问题:(1)合成氨反应平衡常数的表达式为
(2)反应的
 S
S(3)有利于提高平衡混合物中氨含量的条件有
A.低温 B.高温 C.低压 D.高压 E.催化剂
(4)当反应达到平衡后,向体系中充入N2的,平衡

您最近一年使用:0次
解题方法
7 . 下列对熵的理解错误的是
| A.等质量的同种物质气态时熵值最大,固态时熵值最小 |
| B.体系越有序,熵值越小;越混乱,熵值越大 |
| C.从焓判据来看,△H<0有利于反应的自发进行 |
| D.25℃、 1.01×105Pa时,2N2O5(g)=4NO2(g)+O2(g)是熵减反应 |
您最近一年使用:0次
解题方法
8 . 燃煤电厂锅炉尾气中的NO可通过主反应①: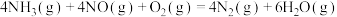
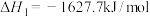 除去。温度高于300℃时,会发生副反应②:
除去。温度高于300℃时,会发生副反应②:
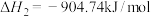 。在恒压、反应物起始比例一定的条件下,在不同催化剂作用下反应相同时间,NO转化率随温度变化的曲线如图所示。
。在恒压、反应物起始比例一定的条件下,在不同催化剂作用下反应相同时间,NO转化率随温度变化的曲线如图所示。
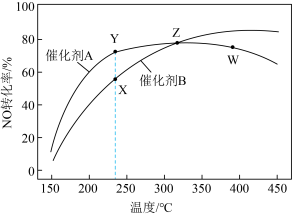
下列有关说法一定正确的是
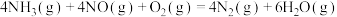
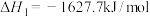 除去。温度高于300℃时,会发生副反应②:
除去。温度高于300℃时,会发生副反应②:
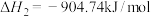 。在恒压、反应物起始比例一定的条件下,在不同催化剂作用下反应相同时间,NO转化率随温度变化的曲线如图所示。
。在恒压、反应物起始比例一定的条件下,在不同催化剂作用下反应相同时间,NO转化率随温度变化的曲线如图所示。
下列有关说法一定正确的是
A.反应  |
| B.低于300℃时,NO的平衡转化率:催化剂A>催化剂B |
| C.图中X点所示条件下,反应时间足够长,NO的转化率能达到Y点的值 |
| D.图中Z点到W点NO的转化率降低的原因是主反应的平衡逆向移动 |
您最近一年使用:0次
9 . 已知焦炭在炼铁高炉中发生的主要反应有
①

②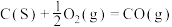
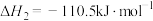
③
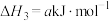
下列说法正确的是
①


②
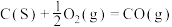
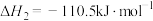
③

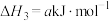
下列说法正确的是
A.1mol 和1mol 和1mol 的能量之和小于1mol 的能量之和小于1mol 的能量 的能量 |
B. |
| C.反应②的焓变和熵变均有利于该反应的自发进行 |
| D.反应③在较低温度下能自发进行 |
您最近一年使用:0次
10 . 下列对熵的理解错误的是
A.同一物质的熵值: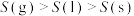 | B.熵增的反应不一定能自发进行 |
| C.反应体系的熵增较大,反应速率也可能较慢 | D.工业合成氨为熵减的反应,不能自发进行 |
您最近一年使用:0次



