解题方法
1 . 已知该产业链中,有炭参与的某反应平衡常数表达式为:K=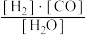 ,写出它所对应反应的化学方程式:
,写出它所对应反应的化学方程式:________ ,若该反应只有在持续高温下才能自发进行,则该反应为________ (“吸热”或“放热”)反应。
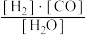 ,写出它所对应反应的化学方程式:
,写出它所对应反应的化学方程式:
您最近一年使用:0次
2 . 正确判断反应自发进行的方向对于生产实践具有重要的意义。回答下列问题:
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解 ,发生反应:
,发生反应: 。该反应的
。该反应的
___________ (填“>”、“<”或“=”,下同)0,
___________ 0,在低温下,该反应___________ (填“能”或“不能”)自发进行。
(2)超音速飞机在平流层飞行时,尾气中的 会破坏臭氧层。科学家正在研究利用催化技术将尾气中的
会破坏臭氧层。科学家正在研究利用催化技术将尾气中的 和
和 转变成
转变成 和
和 ,反应的方程式为
,反应的方程式为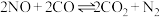 。反应在常温下能够自发进行,则反应的
。反应在常温下能够自发进行,则反应的
___________ (填“>”、“<”或“=”)0。
(3)某吸热反应能自发进行,则该反应的
___________ (填“>”或“<”)0。
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解
 ,发生反应:
,发生反应: 。该反应的
。该反应的

(2)超音速飞机在平流层飞行时,尾气中的
 会破坏臭氧层。科学家正在研究利用催化技术将尾气中的
会破坏臭氧层。科学家正在研究利用催化技术将尾气中的 和
和 转变成
转变成 和
和 ,反应的方程式为
,反应的方程式为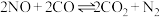 。反应在常温下能够自发进行,则反应的
。反应在常温下能够自发进行,则反应的
(3)某吸热反应能自发进行,则该反应的

您最近一年使用:0次
3 . 根据自发反应的条件回答下列问题:
(1)汽车燃油不完全燃烧时产生 ,有人设想按下列反应除去
,有人设想按下列反应除去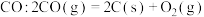 。已知该反应的
。已知该反应的 ,简述该设想能否实现的依据:
,简述该设想能否实现的依据:_______ 。
(2)运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
生产氢气:将水蒸气通过红热的炭即产生水煤气。
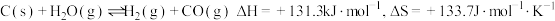
该反应在低温下_______ (填“能”或“不能”)自发进行。
(1)汽车燃油不完全燃烧时产生
 ,有人设想按下列反应除去
,有人设想按下列反应除去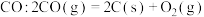 。已知该反应的
。已知该反应的 ,简述该设想能否实现的依据:
,简述该设想能否实现的依据:(2)运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
生产氢气:将水蒸气通过红热的炭即产生水煤气。
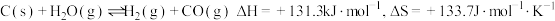
该反应在低温下
您最近一年使用:0次
4 . 铁触媒催化合成氨经历下图所示①⑧步基元反应(从状态I至状态VⅡ):
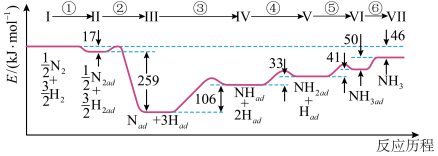
上图中“ad”表示吸附在催化剂表面的物质。
完成下列问题:
(1)催化反应往往经过物质在催化剂表面的“吸附”过程和脱离催化剂表面的“脱附”过程。其中,“吸附”过程是上图中的第___________ 步基元反应,“脱附”过程是___________ (填“吸热”或“放热”)过程。
(2)根据上图计算合成氨反应的焓变: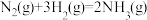 △H=
△H=_______ 。
(3)上述反应的△S_______ 0(填“>”、“<”或“=”)。已知:反应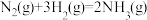 的
的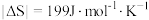 ,则合成氨反应能自发进行的温度是
,则合成氨反应能自发进行的温度是_______ 。
A.25℃ B.125℃ C.225℃ D.325℃

上图中“ad”表示吸附在催化剂表面的物质。
完成下列问题:
(1)催化反应往往经过物质在催化剂表面的“吸附”过程和脱离催化剂表面的“脱附”过程。其中,“吸附”过程是上图中的第
(2)根据上图计算合成氨反应的焓变:
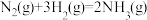 △H=
△H=(3)上述反应的△S
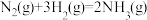 的
的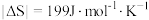 ,则合成氨反应能自发进行的温度是
,则合成氨反应能自发进行的温度是A.25℃ B.125℃ C.225℃ D.325℃
您最近一年使用:0次
解题方法
5 . 已知C2H5OH(l)=C2H4(g)+H2O(l)的ΔH=+45.78kJ·mol-1,ΔS=+126.19J·mol-1·K-1.
(1)请通过计算判断此反应在298K时能否自发进行:_____ 。
(2)该反应发生的条件是_____ 。
(1)请通过计算判断此反应在298K时能否自发进行:
(2)该反应发生的条件是
您最近一年使用:0次
6 . 回答下列问题。
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解CO2,发生反应:2CO2(g)=2CO(g)+O2(g),该反应的ΔH___________ (填“>”“<”或“=”)0,ΔS___________ (填“>”“<”或“=”)0,在低温下,该反应___________ (填“能”或“不能”)自发进行。
(2)已知在100kPa、298K时石灰石分解反应CaCO3(s)=CaO(s)+CO2(g)的ΔH>0,ΔS>0,则:
①该反应常温下___________ (填“能”或“不能”)自发进行。
②据本题反应数据分析,温度___________ (填“能”或“不能”)成为反应方向的决定因素。
(3)已知下列数据:CaO(s)+SO3(g)=CaSO4(s) ΔH=-401.9 kJ·mol-1
用CaO(s)吸收高炉废气中的SO3气体___________ (填“能”或“不能”)防止SO3污染环境。
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解CO2,发生反应:2CO2(g)=2CO(g)+O2(g),该反应的ΔH
(2)已知在100kPa、298K时石灰石分解反应CaCO3(s)=CaO(s)+CO2(g)的ΔH>0,ΔS>0,则:
①该反应常温下
②据本题反应数据分析,温度
(3)已知下列数据:CaO(s)+SO3(g)=CaSO4(s) ΔH=-401.9 kJ·mol-1
| CaSO4(s) | CaO(s) | SO3(g) | |
| S/J·mol-1·K-1 | 107.0 | 39.75 | 256.65 |
您最近一年使用:0次
7 . 碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。已知: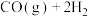
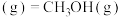
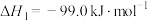 。
。
(1)该反应的熵变
_______ 0(填“>”“<”“=”),该反应自发进行的条件是_______ (填“低温”“高温”或“任意温度”)。
(2)反应
 ,则
,则
_______  (填“>”“<”“=”)。
(填“>”“<”“=”)。
(3)已知1g液态甲醇完全燃烧放出的热量为22.7kJ(298K、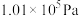 时测定)。写出该条件下表示甲醇燃烧热的热化学方程式
时测定)。写出该条件下表示甲醇燃烧热的热化学方程式_______ 。
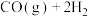
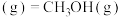
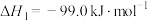 。
。(1)该反应的熵变

(2)反应

 ,则
,则
 (填“>”“<”“=”)。
(填“>”“<”“=”)。(3)已知1g液态甲醇完全燃烧放出的热量为22.7kJ(298K、
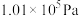 时测定)。写出该条件下表示甲醇燃烧热的热化学方程式
时测定)。写出该条件下表示甲醇燃烧热的热化学方程式
您最近一年使用:0次
解题方法
8 . 完成下列问题。
(1)一定温度下,体积为 的密闭容器中,
的密闭容器中, 、
、 间发生反应。各物质的物质的量随时间变化的关系如图所示。请回答下列问题:
间发生反应。各物质的物质的量随时间变化的关系如图所示。请回答下列问题:

①该反应的化学方程式可表示为___________ 。在0到 中内用
中内用 表示该反应的速率是
表示该反应的速率是___________ ,该反应达最大限度时 的转化率
的转化率___________ 。
②若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中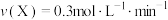 ,乙中
,乙中 ,则
,则___________ 中反应更快。
(2)已知在 、
、 下,
下,
 ,
,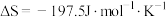 ,已知
,已知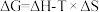 ,若
,若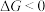 ,反应能够自发进行。请你判断该反应在室温下能否自发进行?简要写出推断的依据
,反应能够自发进行。请你判断该反应在室温下能否自发进行?简要写出推断的依据___________ 。
(1)一定温度下,体积为
 的密闭容器中,
的密闭容器中, 、
、 间发生反应。各物质的物质的量随时间变化的关系如图所示。请回答下列问题:
间发生反应。各物质的物质的量随时间变化的关系如图所示。请回答下列问题:
①该反应的化学方程式可表示为
 中内用
中内用 表示该反应的速率是
表示该反应的速率是 的转化率
的转化率②若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中
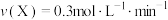 ,乙中
,乙中 ,则
,则(2)已知在
 、
、 下,
下,
 ,
,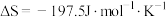 ,已知
,已知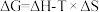 ,若
,若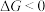 ,反应能够自发进行。请你判断该反应在室温下能否自发进行?简要写出推断的依据
,反应能够自发进行。请你判断该反应在室温下能否自发进行?简要写出推断的依据
您最近一年使用:0次
9 . 化学反应进行方向的判据
(1)焓变与反应的方向
放热反应过程中体系能量___________ ,因此具有___________ 进行的倾向,科学家提出用___________ 来判断反应进行的方向,这就是___________ 。
①多数放热反应是自发进行的。例如燃烧反应、中和反应等。②有些吸热反应也可以自发进行,如:2N2O5(g)⇌4NO2(g)+O2(g) ΔH=+109.8kJ·mol-1。
(2)熵变与反应的方向
①体系的熵值:体系的___________ 越大,体系的熵值就___________ 。
②同一物质的熵值:S(g)>S(l)>S(s),同一条件下,不同物质的___________ 不同。
(3)熵判据:体系有自发地向混乱度___________ (即熵增)的方向转变的倾向,因此可用___________ 来判断反应进行的方向。
(1)焓变与反应的方向
放热反应过程中体系能量
①多数放热反应是自发进行的。例如燃烧反应、中和反应等。②有些吸热反应也可以自发进行,如:2N2O5(g)⇌4NO2(g)+O2(g) ΔH=+109.8kJ·mol-1。
(2)熵变与反应的方向
①体系的熵值:体系的
②同一物质的熵值:S(g)>S(l)>S(s),同一条件下,不同物质的
(3)熵判据:体系有自发地向混乱度
您最近一年使用:0次
2023高二上·全国·专题练习
10 . 自由能与化学反应的方向
(1)自由能:符号为___________ ,单位为kJ·mol-1。
(2)自由能变化与焓变、熵变的关系:ΔG=ΔH-TΔS。ΔG不仅与___________ 有关,还与___________ 。
(3)反应方向与自由能的关系
①当ΔG<0时,反应___________ ;
②当ΔG=0时,反应___________ ;
③当ΔG>0时,反应___________ 。
(1)自由能:符号为
(2)自由能变化与焓变、熵变的关系:ΔG=ΔH-TΔS。ΔG不仅与
(3)反应方向与自由能的关系
①当ΔG<0时,反应
②当ΔG=0时,反应
③当ΔG>0时,反应
您最近一年使用:0次



