名校
1 . 下列说法中正确的是
| A.对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的速率与平衡常数均增大 |
| B.通过增高反应炉的高度,延长铁矿石和CO接触的时间,能减少尾气中CO的含量 |
| C.反应3C(s)+CaO(s)=CaC2(s)+CO(g)常温下不能自发进行,说明该反应的△H<0 |
| D.要想实现Cu+H2SO4(稀)=CuSO4+H2↑,可在电解池中进行,Cu作阳极 |
您最近一年使用:0次
名校
解题方法
2 . 中华传统文化蕴含着很多化学科学知识,下列说法错误的是
| A.“烈火焚烧若等闲”涉及的反应在高温下自发进行 |
| B.“水声冰下咽,沙路雪中平”未涉及化学变化 |
| C.“丹砂(HgS)烧之成水银,积变又还成丹砂”描述的是可逆反应 |
| D.“洪炉照破夜沉沉”中涉及的反应是放热反应 |
您最近一年使用:0次
2022-04-20更新
|
328次组卷
|
3卷引用:福建省泉州市第七中学 2020-2021学年高二上学期期中考试化学试题
福建省泉州市第七中学 2020-2021学年高二上学期期中考试化学试题陕西省咸阳市礼泉县2022-2023学年高二上学期中期学科素养评价化学试题(已下线)1.1.3 物质性质与变化(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)
3 . 尿素(NH2CONH2)又称碳酰胺,是含氮量最高的氮肥。工业上利用二氧化碳和氨气在一定条件下合成尿素,涉及的反应如下:
反应I:2NH3(g)+ CO2(g) H2NCOONH4(s)(氨基甲酸铵) ΔH1 = -272kJ·mol-1
H2NCOONH4(s)(氨基甲酸铵) ΔH1 = -272kJ·mol-1
反应II:H2NCOONH4(s) NH2CONH2(s)+ H2O(g) ΔH2 = +138kJ·mol-1
NH2CONH2(s)+ H2O(g) ΔH2 = +138kJ·mol-1
请回答:
(1)写出二氧化碳和氨气合成尿素的总热化学方程式_______ ,该反应自发进行的条件是_______ (填“低温”、“高温”或“任意条件”)。
(2)尿素(NH2CONH2)是一种重要的化工产品,有很多用途。化工生产中利用尿素溶液可吸收尾气中的氯气,生成两种无污染气体,其中一种气体是空气的主要成分,且溶液pH明显降低,该反应的化学方程式_______ 。
(3)合成氨工业先驱哈伯(P·Haber)利用N2和H2在Fe催化作用下最早人工合成氨气,该反应为: N2(g)+ 3H2(g) 2NH3(g) ΔH = -92.4 kJ·mol-1
2NH3(g) ΔH = -92.4 kJ·mol-1
①写出该反应的平衡常数表达式K =_______ 。
②关于合成氨工艺的下列理解,正确的是_______ 。
A.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
B.降低温度能使平衡向正反应方向进行且平衡常数不变
C.合成氨反应在不同温度下的ΔH和ΔS都小于零
D.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生
反应I:2NH3(g)+ CO2(g)
 H2NCOONH4(s)(氨基甲酸铵) ΔH1 = -272kJ·mol-1
H2NCOONH4(s)(氨基甲酸铵) ΔH1 = -272kJ·mol-1反应II:H2NCOONH4(s)
 NH2CONH2(s)+ H2O(g) ΔH2 = +138kJ·mol-1
NH2CONH2(s)+ H2O(g) ΔH2 = +138kJ·mol-1请回答:
(1)写出二氧化碳和氨气合成尿素的总热化学方程式
(2)尿素(NH2CONH2)是一种重要的化工产品,有很多用途。化工生产中利用尿素溶液可吸收尾气中的氯气,生成两种无污染气体,其中一种气体是空气的主要成分,且溶液pH明显降低,该反应的化学方程式
(3)合成氨工业先驱哈伯(P·Haber)利用N2和H2在Fe催化作用下最早人工合成氨气,该反应为: N2(g)+ 3H2(g)
 2NH3(g) ΔH = -92.4 kJ·mol-1
2NH3(g) ΔH = -92.4 kJ·mol-1①写出该反应的平衡常数表达式K =
②关于合成氨工艺的下列理解,正确的是
A.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
B.降低温度能使平衡向正反应方向进行且平衡常数不变
C.合成氨反应在不同温度下的ΔH和ΔS都小于零
D.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生
您最近一年使用:0次
4 . “冰,水为之,而寒于水”关于水凝结成冰的过程的描述正确的是
| A.△H>0,△S>0 | B.△H>0,△S<0 |
| C.△H<0,△S>0 | D.△H<0,△S<0 |
您最近一年使用:0次
2022-04-05更新
|
833次组卷
|
9卷引用:海南省儋州一中2018-2019学年高二上学期第二次月考化学试题
海南省儋州一中2018-2019学年高二上学期第二次月考化学试题贵州省毕节市第一中学2021-2022学年高二上学期第二次阶段性考试化学试题(已下线)2.3 化学反应的方向-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)湖南省长沙市长郡中学2022-2023学年高二上学期期中考试化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二下学期期末考试化学试题浙江省宁波市三锋联盟2022-2023学年高二上学期11月期中考试化学试题浙江省浙东北联盟(ZDB)2023-2024学年高二上学期期中考试化学试题广东省 江门市棠下中学2023-2024学年高二上学期期中考试化学试题2023-2024学年广东省江门市棠下中学、广东实验江门学校高二(上)期中化学试卷
5 . 下列关于反应热和热化学反应的描述中正确的是
| A.中和热为57.3 kJ∙mol−1,则浓H2SO4和NaOH反应的反应热为ΔH=−114.6 kJ∙mol−1 |
| B.2H2(g)+O2(g)=2H2O(g) △H1;2H2(g)+O2(g)=2H2O(l) △H2,则△H1>△H2 |
| C.2CO(g)+O2(g)=2CO2(g) ΔH=−283.0 kJ∙mol−1,则CO(g)的燃烧热是283.0 kJ∙mol−1 |
D.CH3Cl(g)+Cl2(g)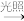 CH2Cl2(l)+HCl(g)常温下能自发进行,则该反应的ΔH>0 CH2Cl2(l)+HCl(g)常温下能自发进行,则该反应的ΔH>0 |
您最近一年使用:0次
名校
解题方法
6 . 下列说法错误的是
A.一定温度下,反应MgCl2(l) Mg(l)+ Cl2(g)的△H>0,△S>0 Mg(l)+ Cl2(g)的△H>0,△S>0 |
| B.△H<0,△S>0的反应在温度低时不能自发进行 |
| C.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| D.NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) △H=+185.57kJ/mol能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
您最近一年使用:0次
2022-03-22更新
|
538次组卷
|
14卷引用:山东省日照市莒县2019-2020学年高二上学期期中考试化学试题
山东省日照市莒县2019-2020学年高二上学期期中考试化学试题(已下线)第02章 化学反应速率和化学平衡(B卷提升篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)(已下线)2.4化学反应进行的方向(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)河北省邯郸市大名县第一中学2020-2021学年高二上学期10月月考化学(实验班)试题辽宁省沈阳市法库县高级中学2020-2021学年高二9月月考化学试题广东实验中学附属天河学校2020--2021学年高二上学期期中考试化学试题(已下线)【浙江新东方】绍兴qw105黑龙江省大庆市大庆实验中学2020-2021学年高二下学期开学考试化学试题(已下线)2.3 化学反应的方向-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)期中测试卷02-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版)陕西省宝鸡市长岭中学2021-2022学年高二上学期期中考试化学试题(已下线)2.3 化学反应的方向-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)内蒙古北京宽高四子王实验学校2021-2022学年高二上学期12月月考化学试题天津市第二南开学校2022-2023学年度高二上学期期中质量调查化学试题
7 . 下列过程属于熵增加的是。
| A.一定条件下水由气态变为液态 |
| B.高温高压条件下使石墨转化为金刚石 |
| C.散落的火柴的无序排列 |
| D.CO点燃时生成CO2 |
您最近一年使用:0次
名校
解题方法
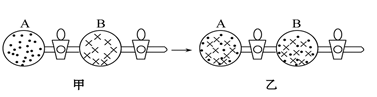
8 . 在图甲中的A、B两容器里,分别收集着两种互不作用的理想气体。若将中间活塞打开(如图乙所示),两种气体分子立即都分布在两个容器中。这是一个不伴随能量变化的自发过程。关于此过程的下列说法不正确的是。

| A.此过程为混乱程度小向混乱程度大的方向的变化过程,即熵增大的过程 |
| B.此过程为自发过程,而且没有热量的吸收或放出 |
| C.此过程从有序到无序,混乱度增大 |
| D.此过程是自发可逆的 |
您最近一年使用:0次
2022-01-17更新
|
315次组卷
|
24卷引用:2014-2015学年湖北省枣阳市高级中学高二下学期期末化学试卷
2014-2015学年湖北省枣阳市高级中学高二下学期期末化学试卷(已下线)同步君 选修4 第2章 第4节 化学反应进行的方向(已下线)2018年9月26日《每日一题》人教选修4-化学反应方向的判断人教版高二化学选修4 第二章 第四节 化学反应进行的方向练习题(已下线)2.2.1 化学反应的方向(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)鲁科版(2019)选择性必修1第2章 化学反应的方向、限度与速率 第1节 化学反应的方向高中必刷题高二选择性必修1第二章 化学反应速率与化学平衡 第三节 化学反应的方向辽宁省联合校2020-2021学年高二上学期第一次月考化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第1节 化学反应的方向新疆生产建设兵团第四师第一中学2020-2021学年高二上学期期中考试化学试题人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第三节 化学反应的方向辽宁省大连市普兰店区第三十八中学2020-2021学年高二上学期期末考试化学试题山东省德州市2020-2021学年高二上学期反应原理月考(A)化学试题高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第四节 化学反应进行的方向 化学反应进行的方向(已下线)作业05 化学反应的方向-2021年高二化学暑假作业(人教版2019)选择性必修1(SJ)专题2第二单元课时1 化学反应的方向选择性必修1 专题2 第二单元 课时1 化学反应的方向湖北省部分高中联考协作体2021-2022学年高二上学期期中考试化学试题(已下线)2.3 化学反应的方向(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第05练 化学反应的方向-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)(已下线)2.2.1 化学反应的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)2.1 化学反应的方向-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)云南省文山州第一中学2021-2022学年高二下学期3月份考试化学试题2.2.1化学反应的方向 课中
名校
解题方法
9 . 下列热化学方程式正确的是
| A.已知2C(s)+2O2(g)=2CO2(g) ΔH=akJ·mol-1,2C(s)+O2(g)=2CO(g) ΔH=bkJ·mol-1,则a<b |
| B.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH<0 |
| C.HCl和NaOH反应的中和热ΔH=-57.3kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1 |
| D.甲烷的燃烧热ΔH=-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3kJ·mol-1 |
您最近一年使用:0次
2022-01-03更新
|
298次组卷
|
13卷引用:【校级联考】江西省赣州市南康中学、于都中学2018-2019学年高二上学期第三次月考化学试题
【校级联考】江西省赣州市南康中学、于都中学2018-2019学年高二上学期第三次月考化学试题江西省赣州市南康区南康中学2020-2021学年高二上学期第三次大考化学试题河北省张家口市宣化第一中学2020-2021学年高二上学期1月月考化学试题广西钦州市第四中学2020-2021学年下学期高二3月月考化学(体艺班)试题辽宁省辽河油田第二高级中学2021-2022学年高二上学期开学考试化学试题(已下线)选择性必修1 综合检测(能力提升卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)山西省山西师范大学实验学校2021-2022学年高二上学期第二次月考化学试题山西省运城市芮城中学2021-2022学年高二上学期12月月考化学试题天津市武清区杨村第一中学2021-2022学年高二上学期第三次月考化学试题云南省楚雄天人中学2021-2022学年高二上学期12月月考化学试题(B卷)河南省焦作市第十一中学2023-2024学年高二上学期期中考试 化学试题江西省吉安市第三中学2023届高三一模考试化学试题(已下线)选择题6-10
名校
解题方法
10 . 研究化学反应进行的方向对于反应设计等具有重要意义,下列说法正确的是
A. 、 、 的反应在温度低时不能自发进行 的反应在温度低时不能自发进行 |
| B.在其他外界条件不变的情况下,汽车排气管中使用催化剂,可以改变产生尾气的反应的方向 |
C.反应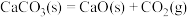 在室温下不能自发进行,说明该反应的 在室温下不能自发进行,说明该反应的 |
D.高温下, 反应能自发进行,则其 反应能自发进行,则其 、 、 |
您最近一年使用:0次
2021-12-21更新
|
352次组卷
|
14卷引用:甘肃省庆阳市第六中学2020-2021学年高二上学期期中考试化学(理)试题
甘肃省庆阳市第六中学2020-2021学年高二上学期期中考试化学(理)试题河北省石家庄市第二中学2019-2020学年高一下学期期末考试化学试题吉林省长春市农安县五校联考2020-2021学年高二上学期期末考试化学试题选择性必修1(SJ)专题2第二单元课时1 化学反应的方向吉林省长春外国语学校2021-2022学年高二上学期第一次月考化学试题甘肃省民乐县第一中学2021--2022学年高二上学期期中考试化学试题(已下线)专题2 综合评价(2)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)天津市实验中学滨海学校2021-2022学年高二上学期期中质量监测化学试题湖南省常德市西洞庭管理区第一中学2022-2023学年高二上学期第二次月考化学试题2.2.1化学反应的方向 课后章末检测卷(二)化学反应的方向、限度与速率山西大学附属中学校2022-2023学年高二上学期11月期中考试化学试题海南省三亚第一中学2023-2024学年高二上学期第一次月考化学试题 福建省福清西山学校2023-2024学年高二上学期12月月考化学试题



