13-14高二·全国·单元测试
名校
1 . 在任意温度下,下列反应一定能自发进行的是
A.2NaCl+2H2O 2NaOH+Cl2↑+H2↑ 2NaOH+Cl2↑+H2↑ |
| B.NH3(g)+HCl(g)=NH4Cl(s) ΔH<0 |
| C.CaCO3(s)=CaO(s)+CO2(g) ΔH>0 |
| D.X2Y2(s)=X2(g)+Y2(g) ΔH<0 |
您最近一年使用:0次
2021-03-12更新
|
120次组卷
|
10卷引用:2014年高中化学鲁科版选修四第2章 反应的方向限度与速率练习卷
(已下线)2014年高中化学鲁科版选修四第2章 反应的方向限度与速率练习卷(已下线)2014-2015学年湖北咸宁鄂南高级中学高二起点考试化学(A类)试卷贵州省安顺市平坝第一高级中学2019-2020学年高二上学期期中考试化学试题(已下线)【浙江新东方】高中化学20210304-002(已下线)第05练 化学反应的方向-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)安徽省舒城中学2021-2022学年高二下学期第一次月考化学试题作业(十) 化学反应的方向北京市广渠门中学2023-2024学年高二上学期期中考试化学试题 宁夏银川市育才中学2023-2024学年高二上学期期中考试化学试题(已下线)第28练 化学反应的方向-2023年高考化学一轮复习小题多维练(全国通用)
名校
2 . 将E(s)和F(g)加入密闭容器中,在一定条件下发生反应E(s)+4F(g) G(g),已知该反应的平衡常数如表所示。下列说法正确的是
G(g),已知该反应的平衡常数如表所示。下列说法正确的是
 G(g),已知该反应的平衡常数如表所示。下列说法正确的是
G(g),已知该反应的平衡常数如表所示。下列说法正确的是| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A.上述反应是熵增反应 |
B.25℃时,反应G(g) E(s)+4F(g)的平衡常数是0.5 E(s)+4F(g)的平衡常数是0.5 |
| C.在80℃时,测得某时刻F、G的浓度均为0.5mol·L-1,则此时v正>v逆 |
| D.恒温恒容下,向容器中再充入少量G(g),达到新平衡时,G的体积百分含量将增大 |
您最近一年使用:0次
2021-03-06更新
|
646次组卷
|
8卷引用:辽宁省大连市部分重点高中2019-2020学年高二上学期期中考试化学试题
名校
3 . 人体内的血红蛋白(Hb)可与O2结合形成HbO2,Hb(aq)也可以与CO结合,人体发生CO中毒的原理为:HbO2(aq)+CO(g) HbCO(aq)+O2(g) ΔH<0.下列说法
HbCO(aq)+O2(g) ΔH<0.下列说法不正确 的是
 HbCO(aq)+O2(g) ΔH<0.下列说法
HbCO(aq)+O2(g) ΔH<0.下列说法| A.海拔较高的地区由于气压较低,所以血红蛋白较难与O2结合,容易产生缺氧现象 |
| B.已知CO中毒为熵减过程,则理论上冬天比夏天可能更容易发生CO中毒现象 |
| C.把CO中毒的人转到高压氧仓中有助于缓解症状 |
D.此反应的平衡常数K=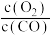 |
您最近一年使用:0次
2021-03-05更新
|
572次组卷
|
8卷引用:浙江省金华十校2021届高三11月选考化学模拟试卷
浙江省金华十校2021届高三11月选考化学模拟试卷重庆市第七中学校2021-2022学年高二上学期第一次月考化学试题重庆市石柱中学校2021-2022学年高二上学期第一次月考化学试题(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)专题10 化学反应速率与平衡-2023年高考化学一轮复习小题多维练(全国通用)甘肃省礼县第一中学2020-2021学年高一上学期期中测试化学试题
解题方法
4 . SO2是大气污染物之一,也是重要的化工原料。
(1)某温度下,反应
 的能量变化如图A.根据反应自发性判断,反应在
的能量变化如图A.根据反应自发性判断,反应在___________ (填“高温”“低温”或“任何温度”)条件下可能有自发性,逆反应的活化能为___________ 。
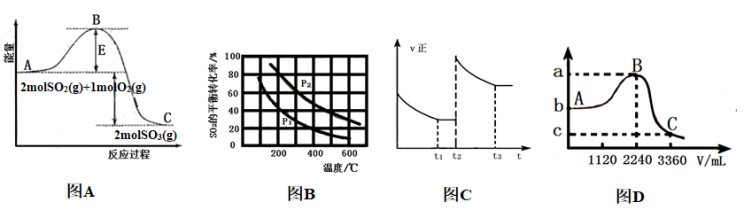
(2)将0.1 mol O2和0.2 mol SO2通入一容积可变的容器中进行反应: 。测得SO2的平衡转化率随温度、压强的变化如图B。
。测得SO2的平衡转化率随温度、压强的变化如图B。
①p1___________ (填“>”“<”或“=”)p2。
②若在300℃、压强为p2时,反应达到平衡,容器容积恰好为10 L,则此状态下反应的平衡常数K=___________ 。
③反应 在t1时刻达到平衡后,在t2时刻速率发生如图C所示变化,此刻改变的反应条件可能是
在t1时刻达到平衡后,在t2时刻速率发生如图C所示变化,此刻改变的反应条件可能是___________ (填标号)。
A.加压 B.向体系中再通入一定量SO2
C.升高温度 D.加催化剂
(3)常温下,向1 L H2S的水溶液中缓慢通入SO2气体(忽略溶液体积的变化),该溶液的pH与通入SO2气体的体积(标准状况)的关系如图D,则a=___________ 。
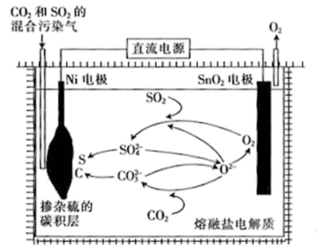
(4)用电解法处理CO2和SO2的混合污染气的原理如图所示,电解质为熔融碳酸盐和硫酸盐,通电一段时间后,Ni电极表面形成掺杂硫的碳积层,则与Ni电极相连的是电源的___________ (填“正极”或“负极”);阳极的电极反应式为___________ 。
(1)某温度下,反应

 的能量变化如图A.根据反应自发性判断,反应在
的能量变化如图A.根据反应自发性判断,反应在
(2)将0.1 mol O2和0.2 mol SO2通入一容积可变的容器中进行反应:
 。测得SO2的平衡转化率随温度、压强的变化如图B。
。测得SO2的平衡转化率随温度、压强的变化如图B。①p1
②若在300℃、压强为p2时,反应达到平衡,容器容积恰好为10 L,则此状态下反应的平衡常数K=
③反应
 在t1时刻达到平衡后,在t2时刻速率发生如图C所示变化,此刻改变的反应条件可能是
在t1时刻达到平衡后,在t2时刻速率发生如图C所示变化,此刻改变的反应条件可能是A.加压 B.向体系中再通入一定量SO2
C.升高温度 D.加催化剂
(3)常温下,向1 L H2S的水溶液中缓慢通入SO2气体(忽略溶液体积的变化),该溶液的pH与通入SO2气体的体积(标准状况)的关系如图D,则a=
(4)用电解法处理CO2和SO2的混合污染气的原理如图所示,电解质为熔融碳酸盐和硫酸盐,通电一段时间后,Ni电极表面形成掺杂硫的碳积层,则与Ni电极相连的是电源的

您最近一年使用:0次
名校
5 . 运用相关化学知识进行判断,下列结论错误的是
| A.某吸热反应能自发进行,因此该反应是熵增反应 |
| B.NH4F溶液不能存放于玻璃试剂瓶中 |
| C.可燃冰主要甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 |
| D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率 |
您最近一年使用:0次
2021-03-02更新
|
48次组卷
|
2卷引用:江西省抚州市金溪县第一中学2020-2021学年高二上学期第二次月考化学试题
6 . CO、CH4 和 N2H4都可以作为燃料。回答下列问题:
(1)工业制氢气原理如下:CH4(g)+H2O(g)⇌CO(g)+3H2(g) △H= +206.4 kJ·mol-1。该反应能自发进行的条件为:______ 。(选填“任何条件”、“低温”、“高温”、“任何条件均不能自发”)
(2)对于上述反应一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是______ 。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
(3)恒温恒容条件下,以下能说明该反应达到平衡状态的是______ 。
a.v消耗(CO)=v生成(H2O) b.c(H2O)=c(CO)
c.混合气体的总物质的量不再改变 d.混合气体的密度不再改变
e.混合气体平均相对分子质量不再改变 f.氢气的质量分数不再改变
(4)肼(N2H4)和NO2是一种双组分火箭推进剂。两种物质混合发生反应生成N2和H2O(g),已知8 g气体肼在上述反应中放出142 kJ热量,其热化学方程式为______ 。
(5)草酸与KMnO4在酸性条件下能够发生如下反应:MnO +H2C2O4+H+→Mn2++CO2↑+H2O(未配平)。用4 mL0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
+H2C2O4+H+→Mn2++CO2↑+H2O(未配平)。用4 mL0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
如果研究催化剂对化学反应速率的影响,应选用实验______ 和______ (用Ⅰ~Ⅳ表示)。
(1)工业制氢气原理如下:CH4(g)+H2O(g)⇌CO(g)+3H2(g) △H= +206.4 kJ·mol-1。该反应能自发进行的条件为:
(2)对于上述反应一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
(3)恒温恒容条件下,以下能说明该反应达到平衡状态的是
a.v消耗(CO)=v生成(H2O) b.c(H2O)=c(CO)
c.混合气体的总物质的量不再改变 d.混合气体的密度不再改变
e.混合气体平均相对分子质量不再改变 f.氢气的质量分数不再改变
(4)肼(N2H4)和NO2是一种双组分火箭推进剂。两种物质混合发生反应生成N2和H2O(g),已知8 g气体肼在上述反应中放出142 kJ热量,其热化学方程式为
(5)草酸与KMnO4在酸性条件下能够发生如下反应:MnO
 +H2C2O4+H+→Mn2++CO2↑+H2O(未配平)。用4 mL0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
+H2C2O4+H+→Mn2++CO2↑+H2O(未配平)。用4 mL0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2 | 20 | / |
| Ⅱ | 2 | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2 | 30 | / |
| Ⅳ | 1 | 20 | 1 mL蒸馏水 |
如果研究催化剂对化学反应速率的影响,应选用实验
您最近一年使用:0次
7 . 用 和
和 的混合溶液可提取废旧印刷电路板中的铜,其热化学方程式为
的混合溶液可提取废旧印刷电路板中的铜,其热化学方程式为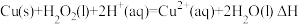
已知:①
②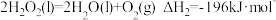 1
1
③
下列说法不正确的是
 和
和 的混合溶液可提取废旧印刷电路板中的铜,其热化学方程式为
的混合溶液可提取废旧印刷电路板中的铜,其热化学方程式为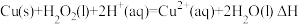
已知:①

②
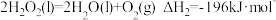 1
1③

下列说法不正确的是
A. |
| B.反应②在任何条件下都能自发进行 |
| C.反应③在溶液中进行,为吸热反应 |
D.已知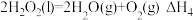 ,则 ,则 |
您最近一年使用:0次
名校
8 . 水在273 K、1.01×105Pa时可转化为固态,在373 K时则又可转化为气态。若分别用S(g)、S(1)、S(s)表示水的气、液、固三种状态的熵值,则下列表达式中,正确的是
| A.S(g)>S(1)>S(s) | B.S(g)<S(1)<S(s) | C.S(g)>S(1)= S(s) | D.S(g)>S(s)>S(1) |
您最近一年使用:0次
2021-02-23更新
|
83次组卷
|
2卷引用:湖北省石首市第一中学2020-2021学年高二上学期10月月考化学试题
名校
解题方法
9 . 下列说法中不正确的是
| A.一个反应能否自发进行,与焓变和熵变的共同影响有关 |
| B.若△H>0,△S<0,任何温度下都不能自发进行 |
| C.2Na2O2+2H2O = 4NaOH+O2↑在常温下能自发进行,既能用焓判据解释又能又熵判据解释 |
| D.2NO(g) +2CO(g) = N2(g) + 2CO2(g) 在常温下能自发进行,则该反应的△H>0 |
您最近一年使用:0次
2021-02-20更新
|
171次组卷
|
3卷引用:重庆市清华中学2020-2021学年高二11月月考化学试题
重庆市清华中学2020-2021学年高二11月月考化学试题(已下线)2.4 化学反应进行的方向-2021-2022学年高二化学课后培优练(人教版选修4)湖南省株洲市天元区名校2022-2023学年高二上学期12月月考化学试题
名校
10 . 已知:①N2O(g)+3H2(g)=N2H4(l)+H2O(l) ΔH1
②N2(g)+3H2(g)=2NH3(g) ΔH2
③2NH3(g)+3N2O(g)=4N2(g)+3H2O(l) ΔH3
④3N2H4(l)=4NH3(g)+N2(g) ΔH
下列有关说法正确的是
②N2(g)+3H2(g)=2NH3(g) ΔH2
③2NH3(g)+3N2O(g)=4N2(g)+3H2O(l) ΔH3
④3N2H4(l)=4NH3(g)+N2(g) ΔH
下列有关说法正确的是
| A.使用催化剂可使ΔH1变小 |
| B.反应②在一定条件下能自发进行,则ΔH2>0 |
| C.反应③若生成 28 g N2,转移的电子数为 1mol |
| D.ΔH=3(ΔH2-ΔH1)+ΔH3 |
您最近一年使用:0次



