解题方法
1 . 某学习小组为了探究 CH3COOH 的电离情况,进行了如下实验。
【实验一】配制并测定醋酸中 CH3COOH 的浓度。
将 0.2mol/L 醋酸稀释,并用 0.1000mol/L NaOH 溶液滴定 20.00mL 稀释后的溶液。4 次滴定消耗 NaOH 溶液的体积如下:
(1)该滴定涉及的离子反应方程式为__________________ 。
(2)滴定时量取 20.00ml 的待测液,选择的仪器为_______________ 。
A.酸式滴定管 B.碱式滴定管 C.量筒
(3)滴定时加入的指示剂为_______________ ,到达滴定终点的判断:_______________ 。
(4)该醋酸中 CH3COOH 的物质的量浓度为_______________ 。
(5)下列操作会导致测定 CH3COOH 的浓度偏低的是_______________。
【实验二】探究浓度对 CH3COOH 电离的影响。
用 PH 计测定 25℃时不同浓度的醋酸的 PH,结果如下:
(6)根据表中数据可以得出 CH3COOH 是弱电解质的结论,你认为得出此结论的依据是 _______________ 。
(7)根据表中数据还可以得出另一个结论:随着溶液中 CH3COOH 浓度的减小,CH3COOH 的电离程度将_______________ (填“增大”“减小”或“不变”)。
【实验一】配制并测定醋酸中 CH3COOH 的浓度。
将 0.2mol/L 醋酸稀释,并用 0.1000mol/L NaOH 溶液滴定 20.00mL 稀释后的溶液。4 次滴定消耗 NaOH 溶液的体积如下:
| 试验次数 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积/mL | 20.05 | 20.00 | 18.40 | 19.95 |
(2)滴定时量取 20.00ml 的待测液,选择的仪器为
A.酸式滴定管 B.碱式滴定管 C.量筒
(3)滴定时加入的指示剂为
(4)该醋酸中 CH3COOH 的物质的量浓度为
(5)下列操作会导致测定 CH3COOH 的浓度偏低的是_______________。
| A.酸式滴定管洗净后未用待装液润洗 |
| B.滴定前碱式滴定管尖端处有气泡,滴定后气泡消失 |
| C.摇动锥形瓶用力过猛,使少量溶液溅出 |
| D.滴定前仰视读数,滴定完毕俯视读数 |
【实验二】探究浓度对 CH3COOH 电离的影响。
用 PH 计测定 25℃时不同浓度的醋酸的 PH,结果如下:
| 浓度/(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.100 | 0.200 |
| PH | 3.88 | 3.38 | 3.23 | 2.88 | 2.83 |
(7)根据表中数据还可以得出另一个结论:随着溶液中 CH3COOH 浓度的减小,CH3COOH 的电离程度将
您最近一年使用:0次
2 . 室温时,向 20 mL 0.1 mol·L-1的 HA、HB 溶液中分别滴加 0.1 mol·L-1NaOH溶液,其 pH 变化分别对应如图中的Ⅰ、Ⅱ。下列说法不正确的是

| A.向 NaA 溶液中滴加 HB 溶液可产生 HA |
| B.加入 10mlNaOH 溶液时,HA 的导电性弱于 HB |
| C.滴加 NaOH 溶液至 pH=7 时,两种溶液中 c(A-)=c(B-) |
| D.滴加 20 mL NaOH 溶液时,Ⅰ中 H2O 的电离程度大于Ⅱ中 |
您最近一年使用:0次
3 . 下列说法正确的是
A.用铁片和稀硫酸反应制取 时,改用铁片和浓硫酸可以加快产生 时,改用铁片和浓硫酸可以加快产生 的速率 的速率 |
B.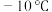 的液态水就会自动结冰成为固态,因为这是熵增的过程 的液态水就会自动结冰成为固态,因为这是熵增的过程 |
C.已知酸性: ,则等浓度等体积的 ,则等浓度等体积的 和 和 溶液中离子总数,前者大于后者 溶液中离子总数,前者大于后者 |
D.向 氨水中加入少量水,溶液中 氨水中加入少量水,溶液中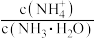 减小 减小 |
您最近一年使用:0次
名校
4 . 碳族元素的物质是化学世界中最庞大的家族,“天问一号”轨道飞行器近距离拍摄了火星北极,看到大量白色冰冻区域, 主要是二氧化碳低温凝结形成的干冰,虽然看起来和地球两极很像,但实际温度却比地球两极冷多了!
(1)已知 25℃时,H2CO3的Ka1=4.2×10-7、Ka2=4.8×10- 11,HCN的Ka=4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为___________ 。
(2)下列关于二氧化碳的说法正确的是___________。
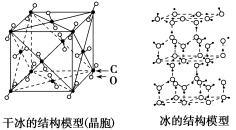
(3)干冰和冰的晶体模型如下图存在差别的本质原因___________ 。___________ 。
(5)金刚石晶体中,每个C被___________ 个六元环共用。
(6)晶体硅和碳化硅熔点较高的是___________ (填化学式)。
(7)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为___________ 。
(1)已知 25℃时,H2CO3的Ka1=4.2×10-7、Ka2=4.8×10- 11,HCN的Ka=4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为
(2)下列关于二氧化碳的说法正确的是___________。
A.电子式为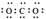 | B.空间填充模型为  |
| C.CO2 是极性分子, 能溶于水 | D.CO2 的水溶液能够导电,但 CO2是非电解质 |
(5)金刚石晶体中,每个C被
(6)晶体硅和碳化硅熔点较高的是
(7)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
您最近一年使用:0次
5 . 25℃时,草酸的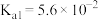 ,
, 。下列说法正确的是
。下列说法正确的是
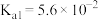 ,
, 。下列说法正确的是
。下列说法正确的是A.  溶液中: 溶液中: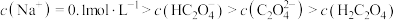 |
B.向 的 的 溶液中通入 溶液中通入 气体(忽略溶液体积的变化)至 气体(忽略溶液体积的变化)至 ,溶液 ,溶液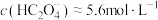 |
C.向 溶液中加入 溶液中加入 溶液至 溶液至 ,则 ,则 |
D.取 的 的 溶液10mL,加蒸馏水稀释至100mL,则该溶液 溶液10mL,加蒸馏水稀释至100mL,则该溶液 |
您最近一年使用:0次
6 . 神舟十三号航天员在中国空间站进行“天宫课堂”授课活动,其中太空“冰雪实验”演示的是过饱和醋酸钠溶液结晶现象。常温下,下列有关说法正确的是
A. 的醋酸溶液中加入醋酸钠固体,溶液pH增大醋酸电离常数减小 的醋酸溶液中加入醋酸钠固体,溶液pH增大醋酸电离常数减小 |
B.相同浓度的醋酸钠溶液和氢氧化钠溶液等体积混合后,溶液中存在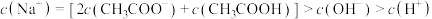 |
C.相同浓度的醋酸溶液和醋酸钠溶液等体积混合后pH约为4.7,溶液中存在: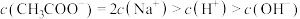 |
D.相同浓度的醋酸钠溶液和硫酸氢钠溶液等体积混合后,溶液中存在: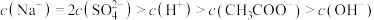 |
您最近一年使用:0次
7 . 常温下,下列有关氨水的说法正确的是
| A.等物质的量浓度的氨水与NaOH溶液,导电能力相同 |
B.往氨水中加水稀释, 逐渐减小 逐渐减小 |
C.pH均为10的氨水与 溶液中, 溶液中, 相等 相等 |
| D.pH=11的氨水与pH=3的盐酸等体积混合后溶液显酸性 |
您最近一年使用:0次
8 . 下列叙述正确的是
A.将 溶液从 溶液从 升温至 升温至 ,溶液中 ,溶液中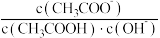 增大 增大 |
B.向盐酸中加入氨水至中性,溶液中 |
C. 时, 时, 的 的 溶液比等浓度的 溶液比等浓度的 溶液的导电能力弱 溶液的导电能力弱 |
D. 时, 时, 一元酸 一元酸 与 与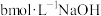 溶液等体积混合后所得溶液的 溶液等体积混合后所得溶液的 为 为 ,则 ,则 |
您最近一年使用:0次
9 . 现有常温下 的醋酸溶液,下列有关叙述正确的是
的醋酸溶液,下列有关叙述正确的是
 的醋酸溶液,下列有关叙述正确的是
的醋酸溶液,下列有关叙述正确的是A.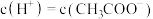 |
B.加入醋酸钠固体可抑制醋酸的电离,但电离常数 不变 不变 |
C.与 的 的 溶液等体积混合后,溶液呈碱性 溶液等体积混合后,溶液呈碱性 |
D.醋酸的物质的量浓度为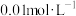 |
您最近一年使用:0次
10 . 25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示。则下列说法不正确的是
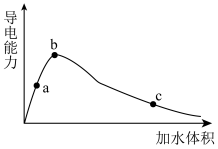
A.醋酸的电离程度: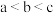 |
B.溶液中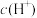 : : |
C.溶液中 : : |
D.从b点到c点,溶液中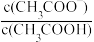 的比值增大 的比值增大 |
您最近一年使用:0次



