1 . 用平衡移动原理,分析一定温度下 在不同pH的
在不同pH的 体系中的可能产物。
体系中的可能产物。
已知:
ⅰ.图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。
ⅱ.2中曲线Ⅰ的离子浓度关系符合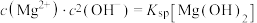 ;
;
曲线Ⅱ的离子浓度关系符合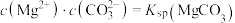 [注:起始
[注:起始 mol⋅L
mol⋅L ,不同pH下
,不同pH下 由图1得到]。
由图1得到]。
 在不同pH的
在不同pH的 体系中的可能产物。
体系中的可能产物。已知:
ⅰ.图1中曲线表示
 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。ⅱ.2中曲线Ⅰ的离子浓度关系符合
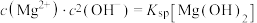 ;
;曲线Ⅱ的离子浓度关系符合
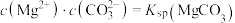 [注:起始
[注:起始 mol⋅L
mol⋅L ,不同pH下
,不同pH下 由图1得到]。
由图1得到]。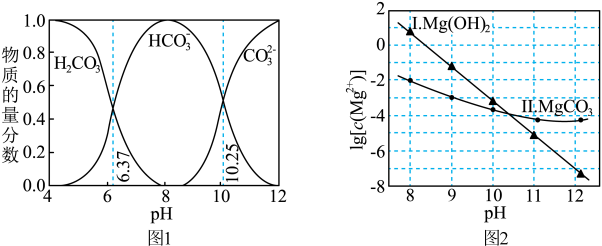
A.由图1可知,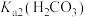 的数量级是 的数量级是 |
B.由图2,若初始状态 , , ,无沉淀生成 ,无沉淀生成 |
C.由图2,若初始状态 , ,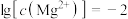 ,平衡后溶液中存在 ,平衡后溶液中存在 mol/L mol/L |
D.由图1和图2,若初始状态 , ,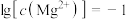 ,发生反应: ,发生反应: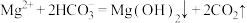 |
您最近一年使用:0次
2024-06-17更新
|
56次组卷
|
2卷引用:安徽省江南十校2023-2024学年高二下学期5月阶段联考化学B试题
2 . 常温下, 、HCOOH(甲酸)、二元弱酸
、HCOOH(甲酸)、二元弱酸 的电离常数见下表,下列说法正确的是
的电离常数见下表,下列说法正确的是
 、HCOOH(甲酸)、二元弱酸
、HCOOH(甲酸)、二元弱酸 的电离常数见下表,下列说法正确的是
的电离常数见下表,下列说法正确的是| 分子式 |  | HCOOH |  |
| 电离常数 |  |  |  、 、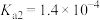 |
A.等物质的量浓度的几种溶液pH大小关系: |
B.HCOONa溶液中滴入少量 ,发生反应 ,发生反应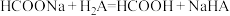 |
C.NaHA溶液中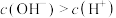 |
D. 的电离常数小于 的电离常数小于 |
您最近一年使用:0次
名校
解题方法
3 . 常温下,用 溶液滴定
溶液滴定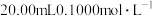 的三种一元酸溶液HX、HY、HZ,滴定曲线如图所示,下列说法正确的是
的三种一元酸溶液HX、HY、HZ,滴定曲线如图所示,下列说法正确的是
 溶液滴定
溶液滴定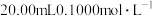 的三种一元酸溶液HX、HY、HZ,滴定曲线如图所示,下列说法正确的是
的三种一元酸溶液HX、HY、HZ,滴定曲线如图所示,下列说法正确的是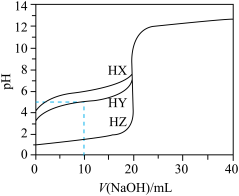
| A.用NaOH溶液滴定HX溶液时,可用甲基橙或酚酞作为指示剂 |
B.常温下 的三种盐溶液NaX、NaY、NaZ中, 的三种盐溶液NaX、NaY、NaZ中,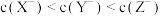 |
C.常温下一元酸HY的电离常数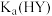 约为 约为 |
| D.滴定结束后读数时俯视凹液面,其它操作均正确,会使测得的结果偏大 |
您最近一年使用:0次
名校
4 . 已知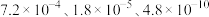 分别是下列有关三种酸常温下的电离平衡常数。若下列三个反应可以发生:①
分别是下列有关三种酸常温下的电离平衡常数。若下列三个反应可以发生:① ,②
,② ,③
,③ ,则下列说法错误的是
,则下列说法错误的是
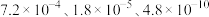 分别是下列有关三种酸常温下的电离平衡常数。若下列三个反应可以发生:①
分别是下列有关三种酸常温下的电离平衡常数。若下列三个反应可以发生:① ,②
,② ,③
,③ ,则下列说法错误的是
,则下列说法错误的是| A.只需要反应①②就可以判断三种酸的酸性强弱 |
B.反应③的平衡常数 |
C.向 稀溶液中加入少量 稀溶液中加入少量 固体,溶液中 固体,溶液中 减小 减小 |
D.在NaCN溶液中有 |
您最近一年使用:0次
名校
5 . 镍及其化合物在工业生产中有重要的用途, (二氯六氨合镍)是一种重要的配合物,实验室以
(二氯六氨合镍)是一种重要的配合物,实验室以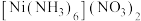 为原料制备
为原料制备 的装置如下:
的装置如下: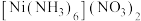 于装置c中,加入
于装置c中,加入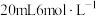 的
的 溶液至固体完全溶解,慢慢加入
溶液至固体完全溶解,慢慢加入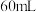 浓氨水和氯化铵的混合溶液,静置至沉淀完全。
浓氨水和氯化铵的混合溶液,静置至沉淀完全。
已知:①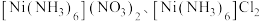 均为可溶于水、不溶于浓氨水和乙醇的蓝紫色水溶液均显碱性。
均为可溶于水、不溶于浓氨水和乙醇的蓝紫色水溶液均显碱性。
② 在热水中分解。
在热水中分解。
请回答:
(1)仪器a的名称为___________ ,装置c需置于冰水浴中的原因是___________ 。
(2) 可降低浓氨水的
可降低浓氨水的 ,利用平衡理论解释原因
,利用平衡理论解释原因___________ 。
(3)将装置c中的沉淀过滤,依次用___________ ,___________ 洗涤,室温真空干燥,即可获得纯净的蓝色晶体。
(4)实验室常用镍试剂检验 ,可观察到鲜红色沉淀。该沉淀的结构如图所示:
,可观察到鲜红色沉淀。该沉淀的结构如图所示:___________ ;
②该沉淀中不存在的作用力类型为___________ (填选项字母);
A.配位键 B.氢键 C.金属键 D. 键 E.
键 E. 键
键
③该沉淀中 的配位数为
的配位数为___________ 。
(5)为测定样品中氯的含量,称量 产品于锥形瓶中,用
产品于锥形瓶中,用 水溶解,加入稀硝酸至溶液呈弱酸性,滴入
水溶解,加入稀硝酸至溶液呈弱酸性,滴入 滴
滴 溶液作指示剂,用
溶液作指示剂,用 的
的 标准溶液滴定至终点,记录读数,重复操作
标准溶液滴定至终点,记录读数,重复操作 次,平均消耗
次,平均消耗 的体积为
的体积为 。计算该样品中氯的百分含量为
。计算该样品中氯的百分含量为___________ (保留三位有效数字)。
 (二氯六氨合镍)是一种重要的配合物,实验室以
(二氯六氨合镍)是一种重要的配合物,实验室以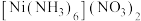 为原料制备
为原料制备 的装置如下:
的装置如下:
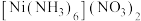 于装置c中,加入
于装置c中,加入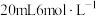 的
的 溶液至固体完全溶解,慢慢加入
溶液至固体完全溶解,慢慢加入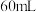 浓氨水和氯化铵的混合溶液,静置至沉淀完全。
浓氨水和氯化铵的混合溶液,静置至沉淀完全。已知:①
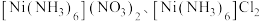 均为可溶于水、不溶于浓氨水和乙醇的蓝紫色水溶液均显碱性。
均为可溶于水、不溶于浓氨水和乙醇的蓝紫色水溶液均显碱性。②
 在热水中分解。
在热水中分解。请回答:
(1)仪器a的名称为
(2)
 可降低浓氨水的
可降低浓氨水的 ,利用平衡理论解释原因
,利用平衡理论解释原因(3)将装置c中的沉淀过滤,依次用
(4)实验室常用镍试剂检验
 ,可观察到鲜红色沉淀。该沉淀的结构如图所示:
,可观察到鲜红色沉淀。该沉淀的结构如图所示:
②该沉淀中不存在的作用力类型为
A.配位键 B.氢键 C.金属键 D.
 键 E.
键 E. 键
键③该沉淀中
 的配位数为
的配位数为(5)为测定样品中氯的含量,称量
 产品于锥形瓶中,用
产品于锥形瓶中,用 水溶解,加入稀硝酸至溶液呈弱酸性,滴入
水溶解,加入稀硝酸至溶液呈弱酸性,滴入 滴
滴 溶液作指示剂,用
溶液作指示剂,用 的
的 标准溶液滴定至终点,记录读数,重复操作
标准溶液滴定至终点,记录读数,重复操作 次,平均消耗
次,平均消耗 的体积为
的体积为 。计算该样品中氯的百分含量为
。计算该样品中氯的百分含量为
您最近一年使用:0次
名校
6 . 25℃时实验室模拟侯氏制碱碳酸化制 的过程,将
的过程,将 通入饱和氨盐水(溶质为
通入饱和氨盐水(溶质为 、NaCl)中,实验现象及数据如图1,含碳粒子在水溶液中的物质的量分数(δ)与pH的关系如图2。
、NaCl)中,实验现象及数据如图1,含碳粒子在水溶液中的物质的量分数(δ)与pH的关系如图2。
 的过程,将
的过程,将 通入饱和氨盐水(溶质为
通入饱和氨盐水(溶质为 、NaCl)中,实验现象及数据如图1,含碳粒子在水溶液中的物质的量分数(δ)与pH的关系如图2。
、NaCl)中,实验现象及数据如图1,含碳粒子在水溶液中的物质的量分数(δ)与pH的关系如图2。
A.0 min时,水电离出的 mol/L mol/L |
B.60 min时,溶液中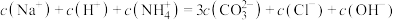 ) ) |
C.60 min~100 min,溶液中, 与 与 的乘积在减小 的乘积在减小 |
D.100 min时,向上层清液中滴加 溶液,无沉淀生成 溶液,无沉淀生成 |
您最近一年使用:0次
名校
7 .  是三元弱酸。室温下,向
是三元弱酸。室温下,向 的
的 溶液中滴加
溶液中滴加 溶液调节pH。混合溶液中
溶液调节pH。混合溶液中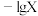 [表示
[表示 、
、 、
、 ]随溶液
]随溶液 的变化如图所示。下列说法不正确的是
的变化如图所示。下列说法不正确的是
 是三元弱酸。室温下,向
是三元弱酸。室温下,向 的
的 溶液中滴加
溶液中滴加 溶液调节pH。混合溶液中
溶液调节pH。混合溶液中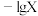 [表示
[表示 、
、 、
、 ]随溶液
]随溶液 的变化如图所示。下列说法不正确的是
的变化如图所示。下列说法不正确的是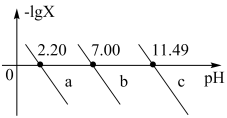
A.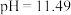 时, 时,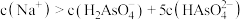 |
B.溶液中存在关系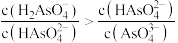 |
C.随着 的增大, 的增大, 保持不变 保持不变 |
D.常温下, 的 的 的数量级为 的数量级为 |
您最近一年使用:0次
8 . 常温下,用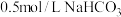 溶液滴定
溶液滴定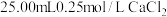 溶液,测得混合溶液的
溶液,测得混合溶液的 随滴加
随滴加 溶液体积的变化如下图所示,当滴加
溶液体积的变化如下图所示,当滴加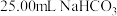 溶液时,出现较为明显的白色沉淀[已知:
溶液时,出现较为明显的白色沉淀[已知: 、
、 ,
,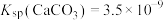 、
、 ]。
]。
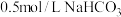 溶液滴定
溶液滴定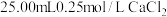 溶液,测得混合溶液的
溶液,测得混合溶液的 随滴加
随滴加 溶液体积的变化如下图所示,当滴加
溶液体积的变化如下图所示,当滴加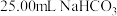 溶液时,出现较为明显的白色沉淀[已知:
溶液时,出现较为明显的白色沉淀[已知: 、
、 ,
,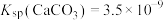 、
、 ]。
]。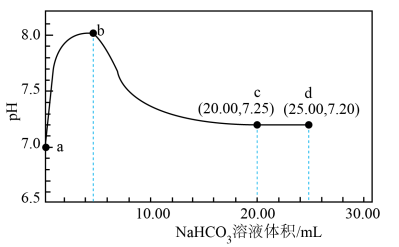
A. 点到 点到 点,混合溶液中水的电离程度增大 点,混合溶液中水的电离程度增大 |
B. 点混合溶液中: 点混合溶液中: |
C. 点混合溶液中: 点混合溶液中: |
D.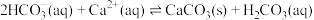 的 的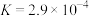 |
您最近一年使用:0次
名校
解题方法
9 . 水在生命演化中起到了重要的作用,下列关于水的说法正确的是
A.由于电负性 ,所以水中H元素化合价为-1,O化合价为+2 ,所以水中H元素化合价为-1,O化合价为+2 |
B.由于 能电离出 能电离出 和 和 ,所以 ,所以 属于强电解质 属于强电解质 |
| C.当外界温度高或体内产热多时,水的蒸发及出汗可帮助散热 |
| D.喝蒸馏水比喝矿泉水更有利于身体健康 |
您最近一年使用:0次
名校
10 . 下列说法正确的是
A.常温下,用pH计测得0.1 mol/L的 溶液的 溶液的 ,则该温度下, ,则该温度下, |
B.已知25℃时某一元弱酸HA的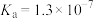 ,向HA溶液中加入NaOH溶液至恰好完全反应,则反应过程中某时刻可能存在: ,向HA溶液中加入NaOH溶液至恰好完全反应,则反应过程中某时刻可能存在: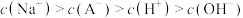 |
| C.将0.1 mol/L的NaOH水溶液,从常温升高到70℃,溶液的pH不变 |
D.1000 mL  的新制氯水中, 的新制氯水中,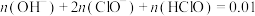 mol mol |
您最近一年使用:0次
2024-06-14更新
|
51次组卷
|
2卷引用:安徽省江南十校2023-2024学年高二下学期5月阶段联考化学B试题



