1 . 回答下列问题
Ⅰ.一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示。
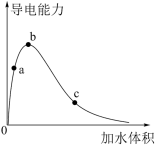
(1)a、b、c三点溶液的pH大小关系:___________ 。
(2)a、b、c三点CH3COOH的电离程度大小关系:___________ 。
(3)a、b、c三点溶液用1 mol·L-1NaOH溶液中和,消耗NaOH溶液体积大小关系:___________ 。
Ⅱ.锌粉与稀硫酸反应产生氢气的体积时间关系如下图所示,选择正确的选项填空。
A. B.
B. 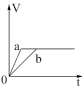 C.
C. 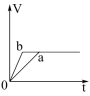 D.
D. 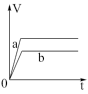
(4)将等质量的两份锌粉a、b分别加入过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是___________ 。
(5)将过量的两份锌粉a、b分别加入定量的稀硫酸,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是___________ 。
(6)将(5)中的CuSO4溶液改成CH3COONa溶液,其他条件不变,则图象是___________ 。
Ⅰ.一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示。

(1)a、b、c三点溶液的pH大小关系:
(2)a、b、c三点CH3COOH的电离程度大小关系:
(3)a、b、c三点溶液用1 mol·L-1NaOH溶液中和,消耗NaOH溶液体积大小关系:
Ⅱ.锌粉与稀硫酸反应产生氢气的体积时间关系如下图所示,选择正确的选项填空。
A.
 B.
B.  C.
C.  D.
D. 
(4)将等质量的两份锌粉a、b分别加入过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是
(5)将过量的两份锌粉a、b分别加入定量的稀硫酸,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是
(6)将(5)中的CuSO4溶液改成CH3COONa溶液,其他条件不变,则图象是
您最近一年使用:0次
20-21高一上·全国·课时练习
解题方法
2 . 下列物质中,属于电解质的是_______ ,属于非电解质的是_______ ,属于强电解质的是_______ ,属于弱电解质的是_______ 。
①氨气; ②氨水; ③盐酸; ④氢氧化钾; ⑤冰醋酸; ⑥氯化钠; ⑦醋酸铵; ⑧二氧化碳; ⑨氯化钠溶液。
①氨气; ②氨水; ③盐酸; ④氢氧化钾; ⑤冰醋酸; ⑥氯化钠; ⑦醋酸铵; ⑧二氧化碳; ⑨氯化钠溶液。
您最近一年使用:0次
名校
解题方法
3 . 按要求回答下列问题
(1)一定温度下,现有a.盐酸,b.硫酸,c.醋酸三种酸
①当三种酸体积相同,物质的量浓度相同时,使其恰好完全中和所需NaOH的物质的量由大到小的顺序是_______ (用a、b、c表示)
②当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是_______ (用a、b、c表示)
③当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为_______ (用a、b、c表示)
(2)现用中和滴定法测定某烧碱溶液的浓度,有关数据记录如表:
①用_______ 式滴定管盛装 盐酸标准液。如图表示第二次滴定前后50mL滴定管中液面的位置。
盐酸标准液。如图表示第二次滴定前后50mL滴定管中液面的位置。
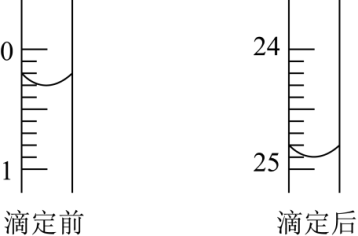
该次滴定所用标准盐酸体积为_______ mL。
②现实验室中有石蕊和酚酞两种指示剂,该实验应选用_______ 作指示剂。
③根据所给数据,该烧碱样品的物质的量浓度为_______ 。
④若操作过程中滴加盐酸速度过快,未充分振荡,刚看到溶液变色,就立刻停止滴定,则会造成测定结果_______ (填“偏低”“偏高”或“无影响”)。
(1)一定温度下,现有a.盐酸,b.硫酸,c.醋酸三种酸
①当三种酸体积相同,物质的量浓度相同时,使其恰好完全中和所需NaOH的物质的量由大到小的顺序是
②当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是
③当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为
(2)现用中和滴定法测定某烧碱溶液的浓度,有关数据记录如表:
| 滴定序号 | 待测液体积 | 所消耗盐酸标准液的体积 | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | 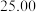 | 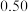 |  |  |
| 2 | 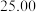 |  |  |  |
| 3 | 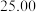 |  |  |  |
 盐酸标准液。如图表示第二次滴定前后50mL滴定管中液面的位置。
盐酸标准液。如图表示第二次滴定前后50mL滴定管中液面的位置。
该次滴定所用标准盐酸体积为
②现实验室中有石蕊和酚酞两种指示剂,该实验应选用
③根据所给数据,该烧碱样品的物质的量浓度为
④若操作过程中滴加盐酸速度过快,未充分振荡,刚看到溶液变色,就立刻停止滴定,则会造成测定结果
您最近一年使用:0次
2021-09-08更新
|
2384次组卷
|
9卷引用:3.2.3 酸碱中和滴定(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
(已下线)3.2.3 酸碱中和滴定(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)辽宁省辽河油田第二高级中学2021-2022学年高二上学期开学考试化学试题(已下线)第3章 水溶液中的离子平衡(提分小卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)河北饶阳中学2021-2022学年高二上学期第一阶段考试化学试题内蒙古乌兰察布市2021-2022学年高二上学期期末考试化学试题新疆乌鲁木齐市第四中学2021-2022学年高二上学期期末考试化学试题(已下线)第三章 水溶液中的离子反应与平衡(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)湖北省武汉海淀外国语实验学校2022-2023学年高二上学期10月月考化学试题(已下线)专题突破卷09 水溶液中的离子反应与平衡 ?-2024年高考化学一轮复习考点通关卷(新教材新高考)
4 . 判断下列溶液的导电性强弱。
(1)①0.1mol·L—1盐酸溶液;②0.1mol·L—1醋酸溶液;③0.1mol·L—1CaCl2溶液___________
(2)①0.00001mol·L—1盐酸溶液;②0.1mol·L—1醋酸溶液;③BaSO4水溶液___________
(1)①0.1mol·L—1盐酸溶液;②0.1mol·L—1醋酸溶液;③0.1mol·L—1CaCl2溶液
(2)①0.00001mol·L—1盐酸溶液;②0.1mol·L—1醋酸溶液;③BaSO4水溶液
您最近一年使用:0次
5 . 下列溶液中存在哪些微粒?请写出微粒符号。
(1)KClO3溶液___________
(2)氯水___________
(3)漂白粉溶液___________
(4)CH3COOH溶液___________
(1)KClO3溶液
(2)氯水
(3)漂白粉溶液
(4)CH3COOH溶液
您最近一年使用:0次
21-22高一·全国·课时练习
解题方法
6 . 有下列物质: ①H2SO4 ②H2CO3 ③Ca(OH)2 ④NH3·H2O ⑤NaHCO3 ⑥BaSO4
(1)其中,属于强电解质的有___________ ,属于弱电解质的有___________ 。
(2)写出上述电解质的电离方程式___________ 。
(1)其中,属于强电解质的有
(2)写出上述电解质的电离方程式
您最近一年使用:0次
7 . 电离常数
(1)表达式
一元弱酸: ,
,
_______ 。
一元弱碱: ,
,
_______ 。
(2)意义:电离常数表征了弱电解质的_______ ,根据相同温度下电离常数的大小可判断_______ 。
(3)影响因素:电离平衡常数受_______ 影响,与溶液浓度无关,温度_______ ,电离平衡常数一定。
(1)表达式
一元弱酸:
 ,
,
一元弱碱:
 ,
,
(2)意义:电离常数表征了弱电解质的
(3)影响因素:电离平衡常数受
您最近一年使用:0次
21-22高一·全国·课时练习
解题方法
8 . 写出下列电解质的电离方程式。
(1)HNO3=___________
(2)Ca(OH)2=___________
(3)KNO3=___________
(4)HCl=___________
(5)(NH4)2SO4=___________
(1)HNO3=
(2)Ca(OH)2=
(3)KNO3=
(4)HCl=
(5)(NH4)2SO4=
您最近一年使用:0次
名校
解题方法
9 . 某酸H2A在水中的电离方程式是:H2A=H++HA-,HA- H++A2-回答下列问题:
H++A2-回答下列问题:
(1)Na2A溶液显___________ (填“酸性”“中性”或“碱性”),用离子方程式表示其原因___________ 。
(2)在0.1 mol·L-1的Na2A溶液中,下列微粒浓度关系式正确的是___________。
(3)常温下,已知0.1 mol·L-1NaHA溶液的pH=2,则0.1 mol·L-1H2A溶液中c(H+)可能___________ (填“>”、“<”或“=”)0.11 mol·L-1;理由是___________ 。
 H++A2-回答下列问题:
H++A2-回答下列问题:(1)Na2A溶液显
(2)在0.1 mol·L-1的Na2A溶液中,下列微粒浓度关系式正确的是___________。
| A.c(A2-)+c(HA-)+c(H2A)=0.1 mol·L-1 | B.c(OH-)=c(H+)+c(HA-)+2c(H2A) |
| C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) | D.c(Na+)>c(A2-)>c(HA-)>c(OH-)>c(H+) |
您最近一年使用:0次
2021-08-24更新
|
430次组卷
|
4卷引用:3.3.1 盐溶液的酸碱性及其原因(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
(已下线)3.3.1 盐溶液的酸碱性及其原因(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)吉林省延边第二中学2020-2021学年高二上学期第二次考试月考化学试题上海行知中学2021-2022学年高二上学期期中考试化学试题吉林省汪清县第六中学2021-2022学年高二12月月考化学试题
名校
10 . Ⅰ.按要求作答。
(1)写出H2CO3在水溶液中的电离方程式:___________ 。
(2)写出FeCl3溶液发生水解的离子方程式:___________ 。
(3)写出Na2CO3溶液的电荷守恒:___________ 。
(4)写出NaHCO3溶液的质子守恒:___________ 。
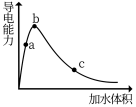
Ⅱ.在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况如图所示,回答下列问题。
(5)“O”点时液体不能导电,说明醋酸中___________ 离子键(填“含有”或“不含”)。
(6)a、b、c三点醋酸电离程度由大到小的顺序为___________ ;a、b、c三点对应的溶液中c(H+)最大的是___________ 。
(7)若实验测得c点处溶液中c(CH3COOH)=0.1mol·L-1,c(CH3COO-)=0.001mol·L-1,则该条件下CH3COOH的电离常数Ka=___________ 。
(8)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是___________。
(1)写出H2CO3在水溶液中的电离方程式:
(2)写出FeCl3溶液发生水解的离子方程式:
(3)写出Na2CO3溶液的电荷守恒:
(4)写出NaHCO3溶液的质子守恒:
Ⅱ.在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况如图所示,回答下列问题。

(5)“O”点时液体不能导电,说明醋酸中
(6)a、b、c三点醋酸电离程度由大到小的顺序为
(7)若实验测得c点处溶液中c(CH3COOH)=0.1mol·L-1,c(CH3COO-)=0.001mol·L-1,则该条件下CH3COOH的电离常数Ka=
(8)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是___________。
| A.c(H+) | B.H+个数 |
| C.CH3COOH分子数 | D. |
您最近一年使用:0次



