1 . 水是生命的源泉、工业的血液、城市的命脉。河水是主要的饮用水源,污染物通过饮用水可宵接毒害人体,也可通过食物链和灌溉农田间接危及健康。请回答下列问题:
(1)纯水在100℃时,pH=6,该温度下1mol·L-1的NaOH溶液中,由水电离出的c(OH-)=_____ mol·L-1。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为___________ 。
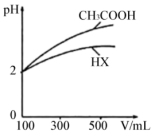
(3)体积均为100mLpH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则相同温度时,HX的电离平衡常数___________ (填“大于”或“小于”或“等于”)CH3COOH的电离平衡常数,理由是___________ 。
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
①25℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三种溶液的pH由大到小的顺序为___________ 。
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为___________ 。
(5)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=___________ mol·L-1(填精确值)。
(1)纯水在100℃时,pH=6,该温度下1mol·L-1的NaOH溶液中,由水电离出的c(OH-)=
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为
(3)体积均为100mLpH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则相同温度时,HX的电离平衡常数

(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为
(5)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=
您最近一年使用:0次
2021-12-25更新
|
358次组卷
|
7卷引用:3.2.1 水的电离 溶液的酸碱性与pH 练习-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)
(已下线)3.2.1 水的电离 溶液的酸碱性与pH 练习-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)河南省洛阳市2019-2020学年高二上学期期末考试化学试题山东省2021-2022学年高二12月“山东学情”联考(鲁科版)化学试题江西省赣州市信丰中学2021-2022学年高二下学期A+班段考化学试题江西省吉安市2021-2022学年高二上学期期末教学质量检测化学试题甘肃省白银市白银区大成学校2022-2023学年高二下学期开学考试(上期末)化学试题四川省江油市太白中学2023-2024学年高二下学期开学考试化学试题
名校
2 . 研究弱电解质的电离,有重要的实际意义。
Ⅰ.有机酸醋酸
(1)保持温度不变,向醋酸溶液中通入一定量的氨气,下列量将变小的是___________。
(2)将0.1 mol∙L−1CH3COOH溶液加水稀释,c(CH3COO-)/c(CH3COOH)的比值将___________ (填“变大”、“不变”或“变小”)。
Ⅱ.对比弱酸酸性相对强弱
(3)某些弱酸在25℃时的电离常数如下:
①下列反应可以发生的是___________ (填字母)。
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.NaHCO3+HCN=NaCN+H2O+CO2↑
②将20mL 1 mol∙L−1 CH3COOH溶液和20mL 1 mol∙L−1HSCN溶液分别与20mL 1 mol∙L−1 NaHCO3溶液混合,画出产生的CO2气体体积(V)随时间(t)的变化关系图,并注明对应酸的化学式 ___________ 。

Ⅰ.有机酸醋酸
(1)保持温度不变,向醋酸溶液中通入一定量的氨气,下列量将变小的是___________。
| A.c(CH3COO-) | B.c(H+) |
| C.c(OH-) | D.CH3COOH电离平衡常数 |
Ⅱ.对比弱酸酸性相对强弱
(3)某些弱酸在25℃时的电离常数如下:
| 化学式 | CH3COOH | HSCN | HCN | HClO | H2CO3 |
| 电离常数 |  | 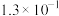 |  |  | 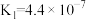 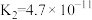 |
①下列反应可以发生的是
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.NaHCO3+HCN=NaCN+H2O+CO2↑
②将20mL 1 mol∙L−1 CH3COOH溶液和20mL 1 mol∙L−1HSCN溶液分别与20mL 1 mol∙L−1 NaHCO3溶液混合,画出产生的CO2气体体积(V)随时间(t)的变化关系图,并注明

您最近一年使用:0次
2021-12-24更新
|
649次组卷
|
3卷引用:3.1.2 电离平衡常数-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)
(已下线)3.1.2 电离平衡常数-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)北京师范大学附属中学2021-2022学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市三立高级中学2021-2022学年高二下学期开学考试化学试题
21-22高二·全国·课时练习
解题方法
3 . 请回答下列问题:
(1)AlCl3水溶液呈___________ 性,原因是___________ (用离子方程式表示,下同),___________ (填“促进”或“抑制”)水的电离。
(2)常温下,有两种溶液:0.1mol·L-1CH3COOH溶液;0.1mol·L-1CH3COONa溶液。
①0.1mol·L-1CH3COONa溶液呈___________ (填“酸”“碱”或“中”)性。其原因是___________ (用离子方程式和适当的叙述说明)。
②下列说法正确的是___________ (填序号)。
A.两种溶液中c(CH3COO﹣)都等于0.1mol·L-1
B.两种溶液中c(CH3COO﹣)都小于0.1mol·L-1
C.CH3COOH溶液中c(CH3COO﹣)小于CH3COONa溶液中c(CH3COO﹣)
(1)AlCl3水溶液呈
(2)常温下,有两种溶液:0.1mol·L-1CH3COOH溶液;0.1mol·L-1CH3COONa溶液。
①0.1mol·L-1CH3COONa溶液呈
②下列说法正确的是
A.两种溶液中c(CH3COO﹣)都等于0.1mol·L-1
B.两种溶液中c(CH3COO﹣)都小于0.1mol·L-1
C.CH3COOH溶液中c(CH3COO﹣)小于CH3COONa溶液中c(CH3COO﹣)
您最近一年使用:0次
名校
解题方法
4 . 如图所示,一定温度下,冰醋酸加水稀释过程中溶液的导电能力曲线图,请回答。

(1)写出醋酸的电离方程式:___________ 。
(2)“O”点为什么不导电___________ 。
(3)a、b、c三点的氢离子浓度由小到大的顺序为___________
(4)a、b、c三点中,醋酸的电离程度最大的一点是___________
(5)若使c点溶液中的c(CH3COO-)提高,在如下措施中,可选择___________
A.加热 B.加很稀的NaOH溶液 C.加固体KOH D.加水
E.加固体CH3COONa F.加Zn粒 G.加MgO固体 H.加Na2CO3固体
(6)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是___________

(1)写出醋酸的电离方程式:
(2)“O”点为什么不导电
(3)a、b、c三点的氢离子浓度由小到大的顺序为
(4)a、b、c三点中,醋酸的电离程度最大的一点是
(5)若使c点溶液中的c(CH3COO-)提高,在如下措施中,可选择
A.加热 B.加很稀的NaOH溶液 C.加固体KOH D.加水
E.加固体CH3COONa F.加Zn粒 G.加MgO固体 H.加Na2CO3固体
(6)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是___________
| A.c(H+) | B.H+个数 | C.CH3COOH分子数 | D. |
您最近一年使用:0次
5 . 25℃时,三种酸的电离平衡常数如下:
回答下列问题:
(1)25℃时,等浓度的三种溶液,酸性最强的是_________ ,一般情况下,当温度升高时,
_________ (填“增大”、“减小”或“不变”);
(2)室温下,某溶液中存在着 CH3COOH(aq)+ (aq)
(aq) CH3COO-(aq)+H2CO3(aq),该反应的平衡常数K=
CH3COO-(aq)+H2CO3(aq),该反应的平衡常数K=___________ 。(用Ka、K1或K2表示)
(3)用蒸馏水稀释 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是________ (填序号)。
a. b.
b. c.
c.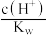 d.
d.
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=___________ (填准确数值)
(5)向次氯酸钠溶液中通入少量二氧化碳的离子方程式_____________ 。
| 化学式 |  | H2CO3 |  |
| 电离平衡常数 | Ka =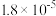 |  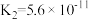 | 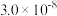 |
(1)25℃时,等浓度的三种溶液,酸性最强的是

(2)室温下,某溶液中存在着 CH3COOH(aq)+
 (aq)
(aq) CH3COO-(aq)+H2CO3(aq),该反应的平衡常数K=
CH3COO-(aq)+H2CO3(aq),该反应的平衡常数K=(3)用蒸馏水稀释
 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是a.
 b.
b. c.
c.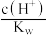 d.
d.
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=
(5)向次氯酸钠溶液中通入少量二氧化碳的离子方程式
您最近一年使用:0次
2021-12-03更新
|
338次组卷
|
5卷引用:3.1.2 电离平衡常数-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)
(已下线)3.1.2 电离平衡常数-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(平行班)化学试题广东省佛山市顺德区第一中学2022-2023学年高二上学期期中考试化学试题(已下线)【2022】【高二上】【期中考】【高中化学】60(已下线)【2022】【高二化学】【期中考】-179
解题方法
6 . 体积相同、pH相同的HCl溶液和CH3COOH溶液分别与NaOH溶液中和时,二者所消耗NaOH的物质的量的关系是___________ ,理由是___________ 。
您最近一年使用:0次
7 . 在氨水中存在的粒子有___________ ;在氯水中存在的粒子有___________ 。
您最近一年使用:0次
名校
8 . 在25℃时对氨水进行如下操作。请填写下列空白。
(1)若向氨水中加入少量硫酸铵固体,则溶液中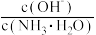 将
将___________ (填“增大”“减小”或“不变”)。
(2)若向氨水中加入稀硫酸,使氨水恰好被中和,写出反应的离子方程式:___________ ;所得溶液的pH___________ 7(填“>”“<”或“=”),用离子方程式表示其原因:___________ 。
(3)若向氨水中加入稀硫酸至溶液的 ,此时溶液中
,此时溶液中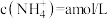 ,则
,则
___________ 。
(1)若向氨水中加入少量硫酸铵固体,则溶液中
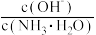 将
将(2)若向氨水中加入稀硫酸,使氨水恰好被中和,写出反应的离子方程式:
(3)若向氨水中加入稀硫酸至溶液的
 ,此时溶液中
,此时溶液中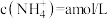 ,则
,则
您最近一年使用:0次
2021-12-02更新
|
1598次组卷
|
3卷引用:人教2019版选择性必修一第三章 水溶液中的离子反应与平衡 复习与提高
人教2019版选择性必修一第三章 水溶液中的离子反应与平衡 复习与提高(已下线)3.3.4 溶液中的粒子浓度(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)黑龙江省哈尔滨市第三十二中学校2021-2022学年高二下学期期中考试化学试题
9 . 已知25℃时, 的
的 。
。
(1)当向醋酸中加入一定量的盐酸时, 的电离常数是否发生变化?为什么?
的电离常数是否发生变化?为什么?___________
(2)若初始时醋酸中 的浓度为0.010mol/L,则达到电离平衡时溶液中
的浓度为0.010mol/L,则达到电离平衡时溶液中 是多少?
是多少?___________
 的
的 。
。(1)当向醋酸中加入一定量的盐酸时,
 的电离常数是否发生变化?为什么?
的电离常数是否发生变化?为什么?(2)若初始时醋酸中
 的浓度为0.010mol/L,则达到电离平衡时溶液中
的浓度为0.010mol/L,则达到电离平衡时溶液中 是多少?
是多少?
您最近一年使用:0次
10 . 判断下列说法是否正确,并说明理由。
(1)强电解质溶液的导电能力一定比弱电解质溶液的强___________ 。
(2)中和等体积、等物质的量浓度的盐酸和醋酸,盐酸所需氢氧化钠的物质的量多于醋酸___________ 。
(3)将NaOH溶液和氨水各稀释一倍,两者的 均减少到原来的
均减少到原来的
___________ 。
(4)如果盐酸中溶质的浓度是醋酸中溶质浓度的2倍,则盐酸中的 也是醋酸的2倍
也是醋酸的2倍___________ 。
(5)物质的量浓度相同的磷酸钠溶液和磷酸中所含 的浓度相同
的浓度相同___________ 。
(1)强电解质溶液的导电能力一定比弱电解质溶液的强
(2)中和等体积、等物质的量浓度的盐酸和醋酸,盐酸所需氢氧化钠的物质的量多于醋酸
(3)将NaOH溶液和氨水各稀释一倍,两者的
 均减少到原来的
均减少到原来的
(4)如果盐酸中溶质的浓度是醋酸中溶质浓度的2倍,则盐酸中的
 也是醋酸的2倍
也是醋酸的2倍(5)物质的量浓度相同的磷酸钠溶液和磷酸中所含
 的浓度相同
的浓度相同
您最近一年使用:0次



