名校
1 . 以菱镁矿(主要成分为 ,还含有
,还含有 、
、 和
和 等杂质)为原料制取高纯
等杂质)为原料制取高纯 的流程如图所示。下列说法错误的是
的流程如图所示。下列说法错误的是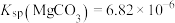 ,
,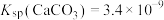
下列说法错误的是
 ,还含有
,还含有 、
、 和
和 等杂质)为原料制取高纯
等杂质)为原料制取高纯 的流程如图所示。下列说法错误的是
的流程如图所示。下列说法错误的是
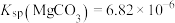 ,
,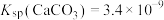
下列说法错误的是
| A.为提高“酸浸”速率,可采取矿石粉碎、搅拌等措施 |
B.“浸渣”为 ,“滤渣”为 ,“滤渣”为 、 、 |
C.“浓缩、部分脱水”时,可能有 沉淀生成 沉淀生成 |
| D.该流程涉及复分解反应、化合反应、分解反应和置换反应 |
您最近一年使用:0次
名校
解题方法
2 . 稀土元素铈及其化合物在生产生活中有重要用途,如汽车尾气用稀土/钯三效催化剂处理,不仅可以降低催化剂的成本,还可以提高催化效能。以氟碳铈矿(主要成分为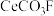 )为原料制备
)为原料制备 的一种工艺流程如图:
的一种工艺流程如图: ,滤渣2的主要成分是
,滤渣2的主要成分是 ;
; 、
、 (a、b均大于0)。
(a、b均大于0)。
②当前工艺条件下,部分金属阳离子开始沉淀和完全沉淀(离子浓度小于 )时的pH如下表:
)时的pH如下表:
回答下列问题:
(1)写出一条提高焙烧效率的方法:_______ 。
(2)加入盐酸和 进行浸取时有污染环境的气体产生,该气体为
进行浸取时有污染环境的气体产生,该气体为_______ (填化学式);操作1和操作2的名称为_______ 。
(3)调节滤液1的pH的范围为_______ ;滤渣3的主要成分为_______ (填化学式)。
(4) 有强氧化性,含
有强氧化性,含 的溶液可吸收雾霾中的NO,生成
的溶液可吸收雾霾中的NO,生成 、
、 (二者物质的量之比为1:1),该反应的离子方程式为
(二者物质的量之比为1:1),该反应的离子方程式为_______ 。
(5)滤渣1经KCl溶液充分浸取后,测得反应体系中 的物质的量浓度为
的物质的量浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为_______  (用含a、b的式子表示)。
(用含a、b的式子表示)。
(6)在空气中焙烧 的反应方程式为
的反应方程式为_______ 。
(7)某研究小组利用硫化锌锂电池,在酸性环境下电解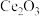 制
制 的装置如图所示。阴极的电极反应式为
的装置如图所示。阴极的电极反应式为_______ ,随着电解反应的进行,为使电解液成分稳定,应不断补充_______ (填化学式)。
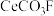 )为原料制备
)为原料制备 的一种工艺流程如图:
的一种工艺流程如图:
 ,滤渣2的主要成分是
,滤渣2的主要成分是 ;
; 、
、 (a、b均大于0)。
(a、b均大于0)。②当前工艺条件下,部分金属阳离子开始沉淀和完全沉淀(离子浓度小于
 )时的pH如下表:
)时的pH如下表:| 金属阳离子 |  |  |
| 开始沉淀时的pH | 1.3 | 7.7 |
| 完全沉淀时的pH | 3.1 | 9.2 |
(1)写出一条提高焙烧效率的方法:
(2)加入盐酸和
 进行浸取时有污染环境的气体产生,该气体为
进行浸取时有污染环境的气体产生,该气体为(3)调节滤液1的pH的范围为
(4)
 有强氧化性,含
有强氧化性,含 的溶液可吸收雾霾中的NO,生成
的溶液可吸收雾霾中的NO,生成 、
、 (二者物质的量之比为1:1),该反应的离子方程式为
(二者物质的量之比为1:1),该反应的离子方程式为(5)滤渣1经KCl溶液充分浸取后,测得反应体系中
 的物质的量浓度为
的物质的量浓度为 ,则
,则 的物质的量浓度为
的物质的量浓度为 (用含a、b的式子表示)。
(用含a、b的式子表示)。(6)在空气中焙烧
 的反应方程式为
的反应方程式为(7)某研究小组利用硫化锌锂电池,在酸性环境下电解
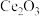 制
制 的装置如图所示。阴极的电极反应式为
的装置如图所示。阴极的电极反应式为
您最近一年使用:0次
昨日更新
|
77次组卷
|
2卷引用:河北省保定市名校协作体2024届高三下学期三模化学试题
3 . 以天青石 (主要成分: 和炭粉焙烧后的水浸液为原料制备
和炭粉焙烧后的水浸液为原料制备  的流程如图所示。
的流程如图所示。 其中。
其中。  约为
约为  。
。
ii.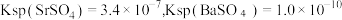 。
。
iii. Sr、Ba分别位于第5、6周期 A族。
A族。
下列说法错误的是
 和炭粉焙烧后的水浸液为原料制备
和炭粉焙烧后的水浸液为原料制备  的流程如图所示。
的流程如图所示。
 其中。
其中。  约为
约为  。
。ii.
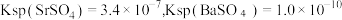 。
。iii. Sr、Ba分别位于第5、6周期
 A族。
A族。下列说法错误的是
A.“焙烧”烟气中可能含有CO和 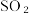 |
| B.“沉钡”后的滤液呈酸性 |
C.“沉钡”过程若  降到 降到  滤渣中混有 滤渣中混有  |
| D.硫酸锶的熔点高于硫酸钡 |
您最近一年使用:0次
4 . 根据下列实验操作和现象所得出的结论错误的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向5 mL浓度均为0.10 mol·L 的KCl和KI混合溶液中滴加几滴 的KCl和KI混合溶液中滴加几滴 溶液,产生黄色沉淀 溶液,产生黄色沉淀 | 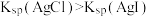 |
| B | 向 溶液中加入过量的KI溶液,充分反应后,再滴入几滴KSCN溶液,溶液变红 溶液中加入过量的KI溶液,充分反应后,再滴入几滴KSCN溶液,溶液变红 |  与KI的反应为可逆反应 与KI的反应为可逆反应 |
| C | 向新制氯水中滴加几滴紫色石蕊溶液,溶液先变红后褪色 | 新制氯水显酸性且具有漂白性 |
| D | 向盛有2 mL新制的银氨溶液的试管中加入1 mL 10%葡萄糖溶液,振荡后将试管放在热水浴中温热,试管壁上出现银镜 | 葡萄糖具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
昨日更新
|
32次组卷
|
2卷引用:2024届河北省承德市部分示范高中高三下学期三模化学试题
名校
5 . 由废旧铜包钢线缆[含Fe、Cu和少量 、碳]回收铜,并制备磷酸亚铁锂,有望代替传统的锂离子电池正极材料。其工艺流程如图所示。
、碳]回收铜,并制备磷酸亚铁锂,有望代替传统的锂离子电池正极材料。其工艺流程如图所示。
(1)常温下进行“酸溶”时,稀硝酸不宜用浓硝酸代替,原因为_______ (写一条)。
(2)滤渣1的主要成分为_______ (填名称)。滤渣2主要成分_______ (填化学式)。
(3)写出用 溶液通过湿法制备Cu的离子反应方程式:
溶液通过湿法制备Cu的离子反应方程式:_______ 。
(4)若滤液2中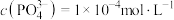 ,则“转化”过程调pH不能高于
,则“转化”过程调pH不能高于_______ {已知:常温下,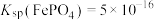 、
、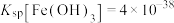 、
、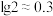 。忽略溶液体积变化}。
。忽略溶液体积变化}。
(5)“焙烧”反应的化学方程式为_______ ;该工序需在氩气氛围中进行的原因为_______ 。
(6)上述工艺中可以循环利用的物质为_______ (填化学式)。
 、碳]回收铜,并制备磷酸亚铁锂,有望代替传统的锂离子电池正极材料。其工艺流程如图所示。
、碳]回收铜,并制备磷酸亚铁锂,有望代替传统的锂离子电池正极材料。其工艺流程如图所示。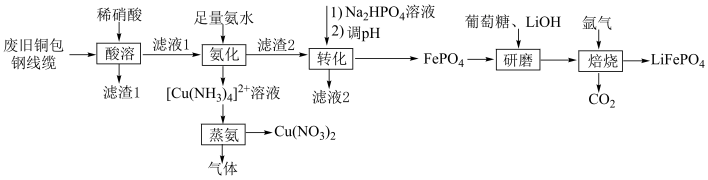
(1)常温下进行“酸溶”时,稀硝酸不宜用浓硝酸代替,原因为
(2)滤渣1的主要成分为
(3)写出用
 溶液通过湿法制备Cu的离子反应方程式:
溶液通过湿法制备Cu的离子反应方程式:(4)若滤液2中
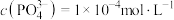 ,则“转化”过程调pH不能高于
,则“转化”过程调pH不能高于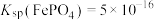 、
、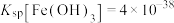 、
、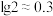 。忽略溶液体积变化}。
。忽略溶液体积变化}。(5)“焙烧”反应的化学方程式为
(6)上述工艺中可以循环利用的物质为
您最近一年使用:0次
6 . 废钼催化剂中钼、钴、镍等有价金属作为二次资源可加以回收利用。一种从废钼催化剂(主要成分为 、
、 ,含少量CoO、CoS、NiO、
,含少量CoO、CoS、NiO、 等)中回收有价金属的工艺流程如下:
等)中回收有价金属的工艺流程如下: ,
,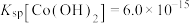 。
。
②当溶液中剩余金属离子的浓度 时,视为已沉淀完全。
时,视为已沉淀完全。
③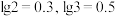 。
。
回答下列问题:
(1)基态Mo原子的价层电子排布式为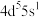 ,则Mo在元素周期表中的位置为
,则Mo在元素周期表中的位置为_______ 。
(2)“焙烧”时先将废钼催化剂磨成粉末,然后采取如图所示的“多层逆流焙烧”,其目的是_______ 。“焙烧”时生成的气体A的主要成分为_______ (写化学式)。 转化为
转化为 。“碱浸”时,
。“碱浸”时, 参与反应的离子方程式为
参与反应的离子方程式为_______ 。
(4)“除铁”时,若溶液中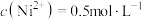 、
、 、
、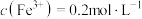 ,加入适量NaOH溶液调节pH(溶液体积变化忽略不计),可以使
,加入适量NaOH溶液调节pH(溶液体积变化忽略不计),可以使 沉淀完全,则调节pH的范围为
沉淀完全,则调节pH的范围为_______ 。
(5)若除铁后所得滤液中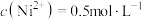 ,“沉镍”后所得滤液中
,“沉镍”后所得滤液中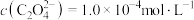 ,则沉镍率=
,则沉镍率=_______ [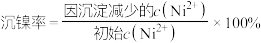 ,计算过程中不考虑溶液体积变化]。
,计算过程中不考虑溶液体积变化]。
(6)在空气中加热18.3g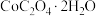 ,其热重曲线如图所示。a点对应固体的成分是
,其热重曲线如图所示。a点对应固体的成分是_______ (填化学式,下同);b、c点对应固体均为钴的氧化物,则b、c点对应固体的成分分别是_______ 、_______ 。
 、
、 ,含少量CoO、CoS、NiO、
,含少量CoO、CoS、NiO、 等)中回收有价金属的工艺流程如下:
等)中回收有价金属的工艺流程如下: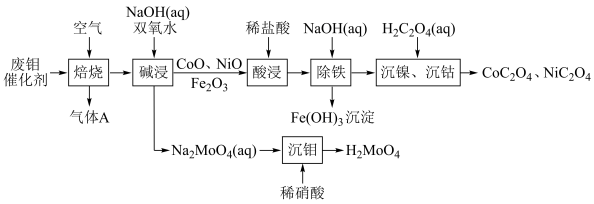
 ,
,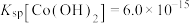 。
。②当溶液中剩余金属离子的浓度
 时,视为已沉淀完全。
时,视为已沉淀完全。③
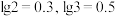 。
。回答下列问题:
(1)基态Mo原子的价层电子排布式为
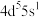 ,则Mo在元素周期表中的位置为
,则Mo在元素周期表中的位置为(2)“焙烧”时先将废钼催化剂磨成粉末,然后采取如图所示的“多层逆流焙烧”,其目的是
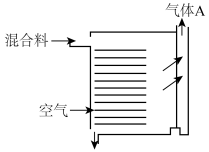
 转化为
转化为 。“碱浸”时,
。“碱浸”时, 参与反应的离子方程式为
参与反应的离子方程式为(4)“除铁”时,若溶液中
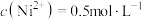 、
、 、
、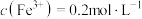 ,加入适量NaOH溶液调节pH(溶液体积变化忽略不计),可以使
,加入适量NaOH溶液调节pH(溶液体积变化忽略不计),可以使 沉淀完全,则调节pH的范围为
沉淀完全,则调节pH的范围为(5)若除铁后所得滤液中
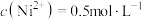 ,“沉镍”后所得滤液中
,“沉镍”后所得滤液中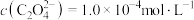 ,则沉镍率=
,则沉镍率=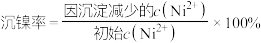 ,计算过程中不考虑溶液体积变化]。
,计算过程中不考虑溶液体积变化]。(6)在空气中加热18.3g
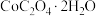 ,其热重曲线如图所示。a点对应固体的成分是
,其热重曲线如图所示。a点对应固体的成分是
您最近一年使用:0次
名校
解题方法
7 . 下列实验操作所得的现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向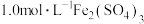 溶液中加入铜粉 溶液中加入铜粉 | 溶液变蓝 | 金属铁比铜活泼 |
B | 常温下分别向稀硝酸和浓硝酸中加入铁粉 | 稀硝酸中产生无色气体,浓硝酸中无明显现象 | 稀硝酸的氧化性比浓硝酸强 |
C | 分别向两支盛有2mL相同浓度的银氨溶液的试管中滴入2滴相同浓度的 和 和 溶液 溶液 | 一支中无明显现象,另一支试管中产生黄色沉淀 | 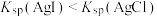 |
D | 向盛有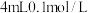 酸性高锰酸钾溶液的两支试管中,分别加入 酸性高锰酸钾溶液的两支试管中,分别加入 草酸溶液和 草酸溶液和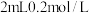 草酸溶液 草酸溶液 | 加入 草酸溶液的试管中溶液褪色更快 草酸溶液的试管中溶液褪色更快 | 其他条件相同时,反应物浓度越大,反应速率越快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下列实验操作、现象、结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向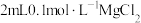 溶液中加入 溶液中加入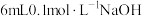 溶液,出现白色沉淀后,继续滴入几滴 溶液,出现白色沉淀后,继续滴入几滴 浓溶液,静置 浓溶液,静置 | 出现红褐色沉淀 | 同温下,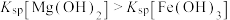 |
B | 分别向等物质的量浓度、等体积的KCl溶液和KI溶液中滴加2滴 稀溶液,充分振荡后静置 稀溶液,充分振荡后静置 | KCl溶液中无白色沉淀,KI溶液中有黄色沉淀 |  结合微粒的能力: 结合微粒的能力: |
C | 向某溶液中先滴加氯水,后滴加KSCN溶液 | 溶液显红色 | 原溶液中一定含有 |
D | 在淀粉溶液中滴入稀硫酸,加热一段时间,冷却后加入氢氧化钠溶液至溶液呈碱性,再滴加碘水 | 溶液未变蓝色 | 证明淀粉已水解完全 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 25℃时,PbR(R2-为 或
或 )的沉淀溶解平衡关系如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法错误的是
)的沉淀溶解平衡关系如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法错误的是
 或
或 )的沉淀溶解平衡关系如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法错误的是
)的沉淀溶解平衡关系如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法错误的是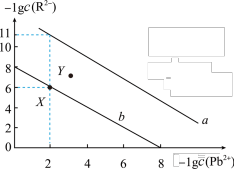
| A.b表示PbSO4的沉淀溶解平衡曲线 |
| B.Y点溶液是PbSO4的不饱和溶液 |
| C.X点对应的溶液中加入少量Pb(NO3)2固体,可转化为Y点对应的溶液 |
D.当PbSO4和PbCO3沉淀共存时,溶液中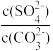 =1×105 =1×105 |
您最近一年使用:0次
10 . “一勤天下无难事”。下列劳动项目所用的化学知识正确的是
| 选项 | 劳动项目 | 化学知识 |
| A | 医疗消毒:用苯酚水溶液进行环境消毒 | 苯酚有强氧化性 |
| B | 家务劳动:用醋酸去除热水壶中的水垢 | 醋酸能溶解硫酸钙 |
| C | 工业劳作:向工业废水中加入FeS除去废水中的Cu2+ | FeS水解显碱性 |
| D | 家庭卫生:用“管道通”(含烧碱和铝粒)清通管道 | 使用过程中产生大量气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



