2024高三下·全国·专题练习
名校
1 . 利用废镍电池的金属电极芯(主要成分为Co、Ni,还含少量Fe、Al等)生产醋酸钴晶体、硫酸镍晶体的工艺流程如下

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
(1)用硫酸浸取金属电极芯时,提高浸取率的方法有___________ (写出一种合理方法即可)。
(2)沉淀A的主要成分是Fe(OH)3、___________ ,“浸出液”调节pH的范围为___________ ,调节pH选用的试剂可以是___________ (填字母)。
a.铁 b.氨水 c.碳酸钠溶液 d.稀硫酸
(3)“母液1”中加入NaClO反应的离子方程式为___________ 。
(4)向Co(OH)3中加入H2SO4-H2O2混合液,H2O2的作用是___________ 。
(5)“母液3”中应控制Na2CO3用量使终点pH为8.5为宜,此时c(Co2+)小于___________ mol·L-1;为防止生成Co(OH)2 沉淀,可用NH4HCO3代替Na2CO3制得CoCO3,写出该反应的离子方程式:___________ {已知:Ksp[Co(OH)2]=2×10-15};
(6)由“母液4”获取NiSO4·7H2O的操作是___________ 、___________ 、过滤、洗涤。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Co(OH)3 | Al(OH)3 | Ni(OH)2 |
| 开始沉淀pH | 2.2 | 7.4 | 7.6 | 0.1 | 4.0 | 7.6 |
| 完全沉淀pH | 3.2 | 8.9 | 9.2 | 1.1 | 5.2 | 9.2 |
(1)用硫酸浸取金属电极芯时,提高浸取率的方法有
(2)沉淀A的主要成分是Fe(OH)3、
a.铁 b.氨水 c.碳酸钠溶液 d.稀硫酸
(3)“母液1”中加入NaClO反应的离子方程式为
(4)向Co(OH)3中加入H2SO4-H2O2混合液,H2O2的作用是
(5)“母液3”中应控制Na2CO3用量使终点pH为8.5为宜,此时c(Co2+)小于
(6)由“母液4”获取NiSO4·7H2O的操作是
您最近一年使用:0次
名校
2 . 根据下列实验操作和现象所得到的实验结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向 溶液中加入 溶液中加入 溶液,有白色沉淀生成 溶液,有白色沉淀生成 |  与 与 发生了双水解反应 发生了双水解反应 |
| B | 向NaOH固体中加入少量稀盐酸,测得温度高于室温 | 盐酸与NaOH反应为放热反应 |
| C | 室温下,测得相同浓度的NaX和NaY溶液的pH分别为8和9 | 酸性: |
| D | 向等浓度的NaCl、KI的混合溶液中滴加少量 溶液,得到黄色沉淀 溶液,得到黄色沉淀 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-17更新
|
128次组卷
|
3卷引用:湖南省长沙麓山国际实验学校2023-2024学年高二下学期第一次学情检测化学试卷
名校
3 . 化学与生活密切相关。下列说法正确的是
| A.高锰酸钾溶液、“84”消毒液、酒精均具有强氧化性,可用于杀菌消毒 |
B.纯碱溶液可去油污,是由于 水解使溶液显碱性 水解使溶液显碱性 |
C.石灰石可减少煤燃烧的 排放,是由于石灰石可将 排放,是由于石灰石可将 转化为 转化为 |
D.用FeS作沉淀剂,可除去废水中的 和 和 |
您最近一年使用:0次
2023-12-26更新
|
205次组卷
|
2卷引用:湖南省常德市临澧县第一中学2023-2024学年高二下学期入学考试化学试题
名校
解题方法
4 . 国家速滑馆又称为“冰丝带”,所用的碲化镉(CdTe)发电玻璃被誉为“挂在墙上的油田”。一种以镉废渣(含 及少量
及少量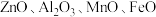 杂质)为原料制备镉的工艺流程如图所示,下列说法错误的是
杂质)为原料制备镉的工艺流程如图所示,下列说法错误的是
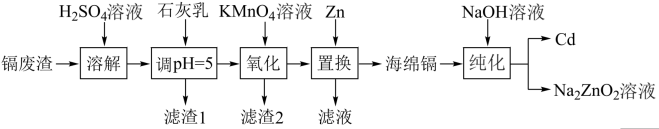
已知:部分金属阳离子以氢氧化物形式沉淀时溶液的 如下表所示:
如下表所示:
 及少量
及少量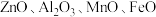 杂质)为原料制备镉的工艺流程如图所示,下列说法错误的是
杂质)为原料制备镉的工艺流程如图所示,下列说法错误的是
已知:部分金属阳离子以氢氧化物形式沉淀时溶液的
 如下表所示:
如下表所示:| 金属阳离子 |  |  |  |
开始沉淀时的 | 2.7 | 6.3 | 3.4 |
完全沉淀时的 | 3.2 | 8.3 | 5.0 |
A.滤渣1的主要成分是 |
B. 置换之后的滤液主要成分是 置换之后的滤液主要成分是 和 和 |
C.“纯化”过程中发生的反应为 |
| D.该工艺用到的主要分离操作是过滤 |
您最近一年使用:0次
2023-11-23更新
|
576次组卷
|
4卷引用:湖南省长沙市周南教育集团2023-2024学年高二下学期入学考试化学试题
名校
5 . 综合利用粉煤灰既有利于环境保护,又有利于资源节约。某种粉煤灰(主要含Al2O3、Fe2O3、CaCO3等)的铝、铁分离工艺流程如下:

(1)“酸浸”时Fe2O3发生反应的离子方程式为___________ 。
(2)当硫酸浓度大于9.2molL1时,铝、铁的浸出率下降。可能原因是___________ 。
(3)有关金属离子以氢氧化物沉淀时离子浓度随pH变化如图所示。“还原”操作加入的试剂为___________ 。“沉铝”过程中加入氨水调pH的范围是___________ ,“沉铝”反应的方程式为___________ 。

(4)“再生”过程中,[Fe(NO)2]2在微生物的作用下与C6H12O6发生反应,生成N2与CO2的物质的量之比为___________ 。

(1)“酸浸”时Fe2O3发生反应的离子方程式为
(2)当硫酸浓度大于9.2molL1时,铝、铁的浸出率下降。可能原因是
(3)有关金属离子以氢氧化物沉淀时离子浓度随pH变化如图所示。“还原”操作加入的试剂为

(4)“再生”过程中,[Fe(NO)2]2在微生物的作用下与C6H12O6发生反应,生成N2与CO2的物质的量之比为
您最近一年使用:0次
2023-09-06更新
|
112次组卷
|
2卷引用:湖南省长沙麓山国际实验学校2023-2024学年高二上学期入学考试化学试题
6 . 金属镓有“电子工业脊梁”的美誉,镓与铝的化学性质类似。从刚玉渣(含钛、镓的低硅铁合金,还含有少量氧化铝)回收镓的流程如图所示:

溶液中金属离子开始沉淀利和完全沉淀的 pH 如下表所示:
请回答下列问题。
(1)“酸浸”过程中禁止出现明火加热,原因是___________ 。
(2)“结晶”过程中得到 FeSO4·7H2O 的具体操作为___________ 、过滤、洗涤、干燥。
(3)“中和沉淀”的目的是分离出______ (填化学式),该过程中 pH 应调节的范围为___________ 。
(4)下列说法中不正确的是___________ (填字母)。
A.为提高浸出率,可将刚玉渣研磨
B.“结晶”过程中得到的 FeSO4·7H2O 可作为净水剂
C. “碱浸”过程中可用氨水代替 NaOH 溶液
(5)“碳酸化”过程中不能通入过量 CO2的原因为___________ (用离子方程式表示)。
(6)GaN 具有优异的光电性能。工业上常采用在 1100℃条件下,利用 Ga 与NH3 反应可制备 GaN,该过程的化学方程式为___________ 。

溶液中金属离子开始沉淀利和完全沉淀的 pH 如下表所示:
| 金属离子 | Ga3 | Al3 | Fe3 | Fe2 |
| 开始沉淀时c 0.01mol L1的 pH | 4.5 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时c 1.0 105 mol L1 的 pH | 5.5 | 4.7 | 3.2 | 9.0 |
(1)“酸浸”过程中禁止出现明火加热,原因是
(2)“结晶”过程中得到 FeSO4·7H2O 的具体操作为
(3)“中和沉淀”的目的是分离出
(4)下列说法中不正确的是
A.为提高浸出率,可将刚玉渣研磨
B.“结晶”过程中得到的 FeSO4·7H2O 可作为净水剂
C. “碱浸”过程中可用氨水代替 NaOH 溶液
(5)“碳酸化”过程中不能通入过量 CO2的原因为
(6)GaN 具有优异的光电性能。工业上常采用在 1100℃条件下,利用 Ga 与NH3 反应可制备 GaN,该过程的化学方程式为
您最近一年使用:0次
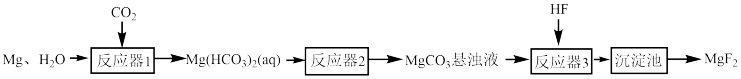
7 . 氟化镁可用于制造陶瓷、玻璃,还可用作铝金属的助熔剂、光学仪器中镜头及滤光器的涂层等。用纯净的Mg制备MgF2的流程如图所示:
下列说法错误的是
| 物质 | MgF2 | MgCO3 |
| 溶度积(Ksp) | 6.4×10-9 | 2.4×10-5 |
| A.反应器1中需通入过量的CO2 |
| B.反应器2中需适当升高温度 |
C.沉淀池的上层清液中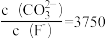 |
| D.从沉淀池中获取纯净MgF2的操作是过滤、洗涤、干燥 |
您最近一年使用:0次
2023-08-31更新
|
390次组卷
|
3卷引用:湖南省部分学校2023-2024学年高三8月开学考试化学试题
名校
解题方法
8 . 铜阳极泥分银渣含有铅、锡、钡以及金、银等有价值的金属元素,具有较高的综合利用价值,其中锡主要以 形式存在,铅、钡主要以硫酸盐的形式存在。分银渣分离的工艺流程如图,请回答下列问题:
形式存在,铅、钡主要以硫酸盐的形式存在。分银渣分离的工艺流程如图,请回答下列问题:
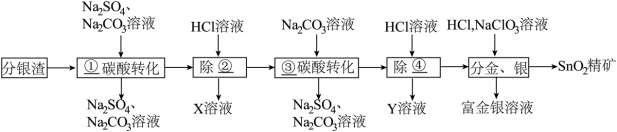
已知:
①常温下,部分碳酸盐、硫酸盐的溶度积常数如下表:
② 不溶于水,也难溶于酸和碱。
不溶于水,也难溶于酸和碱。
(1)已知Sn与C同主族,则基态Sn原子的价层电子轨道表示式为________ 。
(2)请根据提供的数据判断分银渣分离的工艺流程中,②应该填入的元素名称分别为________ ;Y溶液的溶质为________ 。
(3)工艺流程中钡碳酸转化的原理为________ (用离子方程式表示),使 转化成
转化成 ,需要使
,需要使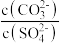 最少等于
最少等于________ 。
(4)加入HCl、 溶液可使Au、Ag转化成
溶液可使Au、Ag转化成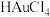 、
、 ,写出Au转化成
,写出Au转化成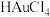 的离子方程式:
的离子方程式:________ 。
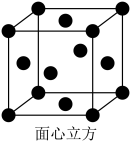
(5)由金的X射线衍射图像可知,其晶胞属于面心立方晶胞(如图)。若金原子的半径为rcm,金的密度为 ,金原子的摩尔质量为
,金原子的摩尔质量为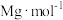 ,则阿伏加德罗常数(
,则阿伏加德罗常数( )的计算表达式
)的计算表达式
___________ (用含r、 、M的代数式表示)。
、M的代数式表示)。
 形式存在,铅、钡主要以硫酸盐的形式存在。分银渣分离的工艺流程如图,请回答下列问题:
形式存在,铅、钡主要以硫酸盐的形式存在。分银渣分离的工艺流程如图,请回答下列问题:
已知:
①常温下,部分碳酸盐、硫酸盐的溶度积常数如下表:
| 盐 |  |  |  |  |
 | 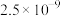 | 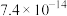 | 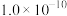 |  |
 不溶于水,也难溶于酸和碱。
不溶于水,也难溶于酸和碱。(1)已知Sn与C同主族,则基态Sn原子的价层电子轨道表示式为
(2)请根据提供的数据判断分银渣分离的工艺流程中,②应该填入的元素名称分别为
(3)工艺流程中钡碳酸转化的原理为
 转化成
转化成 ,需要使
,需要使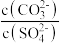 最少等于
最少等于(4)加入HCl、
 溶液可使Au、Ag转化成
溶液可使Au、Ag转化成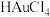 、
、 ,写出Au转化成
,写出Au转化成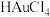 的离子方程式:
的离子方程式:(5)由金的X射线衍射图像可知,其晶胞属于面心立方晶胞(如图)。若金原子的半径为rcm,金的密度为
 ,金原子的摩尔质量为
,金原子的摩尔质量为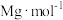 ,则阿伏加德罗常数(
,则阿伏加德罗常数( )的计算表达式
)的计算表达式
 、M的代数式表示)。
、M的代数式表示)。
您最近一年使用:0次
名校
9 . 铅铬黄是一种颜料,主要成分是铬酸铅 (摩尔质量323g/mol)。现以
(摩尔质量323g/mol)。现以 和
和 等为原料制备该物质,并测定产物纯度。
等为原料制备该物质,并测定产物纯度。

回答下列问题:
(1)已知 不溶于水,具有两性。第①步所得绿色溶液中的有色离子是
不溶于水,具有两性。第①步所得绿色溶液中的有色离子是___________ 。
(2)第②步生成了 ,写出该步骤的离子方程式
,写出该步骤的离子方程式___________ 。为了使 反应充分而不剩余,以下方案中最合理的是
反应充分而不剩余,以下方案中最合理的是___________ (填序号)。
A.首先加热绿色溶液,然后将一定量 浓溶液滴入其中
浓溶液滴入其中
B.首先加热 浓溶液,然后转入热的绿色溶液中
浓溶液,然后转入热的绿色溶液中
C.首先将一定量 浓溶液滴入绿色溶液中,然后加热煮沸
浓溶液滴入绿色溶液中,然后加热煮沸
(3)第③步调节pH=5的目的是为了将 转化为
转化为___________ (填写离子符号),并且防止在碱性条件下___________ 形成沉淀。
(4)由于铬酸铅的溶解度比重铬酸铅的小的多,在第④步中逐滴滴加 溶液后,产生
溶液后,产生 黄色沉淀,此时为了提高铅铬黄的产率,可补加少最NaOH溶液,请用化学平衡移动原理加以解释:
黄色沉淀,此时为了提高铅铬黄的产率,可补加少最NaOH溶液,请用化学平衡移动原理加以解释:___________ 。
 (摩尔质量323g/mol)。现以
(摩尔质量323g/mol)。现以 和
和 等为原料制备该物质,并测定产物纯度。
等为原料制备该物质,并测定产物纯度。
回答下列问题:
(1)已知
 不溶于水,具有两性。第①步所得绿色溶液中的有色离子是
不溶于水,具有两性。第①步所得绿色溶液中的有色离子是(2)第②步生成了
 ,写出该步骤的离子方程式
,写出该步骤的离子方程式 反应充分而不剩余,以下方案中最合理的是
反应充分而不剩余,以下方案中最合理的是A.首先加热绿色溶液,然后将一定量
 浓溶液滴入其中
浓溶液滴入其中B.首先加热
 浓溶液,然后转入热的绿色溶液中
浓溶液,然后转入热的绿色溶液中C.首先将一定量
 浓溶液滴入绿色溶液中,然后加热煮沸
浓溶液滴入绿色溶液中,然后加热煮沸(3)第③步调节pH=5的目的是为了将
 转化为
转化为(4)由于铬酸铅的溶解度比重铬酸铅的小的多,在第④步中逐滴滴加
 溶液后,产生
溶液后,产生 黄色沉淀,此时为了提高铅铬黄的产率,可补加少最NaOH溶液,请用化学平衡移动原理加以解释:
黄色沉淀,此时为了提高铅铬黄的产率,可补加少最NaOH溶液,请用化学平衡移动原理加以解释:
您最近一年使用:0次
名校
解题方法
10 . 下列实验探究方案不能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 将二氧化硫气体通入碘和淀粉的混合溶液中,观察溶液颜色的变化 | 探究还原性: |
| B | 向盛有 溶液的试管中滴加几滴 溶液的试管中滴加几滴 溶液。振荡,观察颜色的变化 溶液。振荡,观察颜色的变化 | 探究 是否变质 是否变质 |
| C | 加热溴乙烷和氢氧化钠-乙醇混合溶液,将产生的气体通入高锰酸钾溶液中。观察溶液颜色的变化 | 探究溴乙烷在此条件下发生的是取代反应还是消去反应 |
| D | 向盛有等浓度的NaCl和KI混合溶液的试管中滴加几滴 溶液,振荡,观察沉淀颜色 溶液,振荡,观察沉淀颜色 | 证明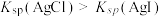 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-06更新
|
429次组卷
|
3卷引用:湖南省岳阳县一中2023-2024学年高三开学考试化学试题



