1 . 回答下列问题:
(1)25℃时,CH3COOH的电离平衡常数为:K=1.8×10-5,H3PO3的电离平衡常数为:K1=8.3×10-3、K2=5.6×10-6;则:
①写出CH3COOH的电离方程式:___________
②25℃时,0.02mol/L的CH3COOH溶液的电离度约为______ %。
③往Na2HPO3溶液中滴加足量CH3COOH溶液的离子反应方程式为:____________
(2)①某课外活动小组为了探究BaSO4的溶解度,分别将足量BaSO4加入下列物质中:
a.5 mL水 b.40mL 0. 2 mol·L-1的Ba(OH)2溶液
c.20mL 0.5 mol·L-1的Na2SO4溶液 d.40mL 0.1 mol·L-1的H2SO4溶液中
溶解BaSO4后形成的溶液中,Ba2+的浓度由大到小的顺序为_____ (填字母)。
A.b>a>c>d B.b>a>d>c C.a>d>c>b D.a>b>d>c
②已知298K时,Ksp(BaSO4)=1.1×10-10,此时,溶液b中加入BaSO4固体后,c( )为
)为______________ mol·L-1。
(3)新型高效的乙烷燃料电池采用铂为电极材料,两电极上分别通入C2H6和O2 ,电解质溶液为KOH溶液。
①请写出乙烷燃料电池的负极反应式:_______________ 。
②利用此乙烷燃料电池给铅蓄电池充电,若充电过程中有3.0g乙烷完全反应,且不考虑能量损耗,则此充电过程消耗的O2在标况下的体积为_________ L(保留3位有效数字)、铅蓄电池的阳极质量减小________ g(保留3位有效数字)。
(1)25℃时,CH3COOH的电离平衡常数为:K=1.8×10-5,H3PO3的电离平衡常数为:K1=8.3×10-3、K2=5.6×10-6;则:
①写出CH3COOH的电离方程式:
②25℃时,0.02mol/L的CH3COOH溶液的电离度约为
③往Na2HPO3溶液中滴加足量CH3COOH溶液的离子反应方程式为:
(2)①某课外活动小组为了探究BaSO4的溶解度,分别将足量BaSO4加入下列物质中:
a.5 mL水 b.40mL 0. 2 mol·L-1的Ba(OH)2溶液
c.20mL 0.5 mol·L-1的Na2SO4溶液 d.40mL 0.1 mol·L-1的H2SO4溶液中
溶解BaSO4后形成的溶液中,Ba2+的浓度由大到小的顺序为
A.b>a>c>d B.b>a>d>c C.a>d>c>b D.a>b>d>c
②已知298K时,Ksp(BaSO4)=1.1×10-10,此时,溶液b中加入BaSO4固体后,c(
 )为
)为(3)新型高效的乙烷燃料电池采用铂为电极材料,两电极上分别通入C2H6和O2 ,电解质溶液为KOH溶液。
①请写出乙烷燃料电池的负极反应式:
②利用此乙烷燃料电池给铅蓄电池充电,若充电过程中有3.0g乙烷完全反应,且不考虑能量损耗,则此充电过程消耗的O2在标况下的体积为
您最近一年使用:0次
2 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属 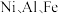 及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体
及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体 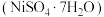 :
: 如表所示:
如表所示:
回答下列问题:
(1)“滤液②”中除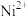 外还含有的金属离子
外还含有的金属离子___________ ;
(2)“转化”中可替代 的物质是
的物质是___________ (不能引入新的杂质离子);
由表格中的数据可求得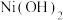 的
的 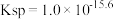 。如果“转化”后的溶液中
。如果“转化”后的溶液中 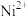 浓度为
浓度为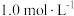 ,则除去杂质金属阳离子时“调
,则除去杂质金属阳离子时“调 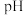 ”应控制的
”应控制的  范围是
范围是___________ 。
(3)硫酸镍在强碱溶液中用 氧化,可沉淀出能用作镍镉电池正极材料的
氧化,可沉淀出能用作镍镉电池正极材料的 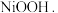 写出该反应的离子方程式
写出该反应的离子方程式___________ 。
(4)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是___________ 。
(5)第Ⅷ族元素单质及其化合物在工业生产和科研领域有重要的用途。
①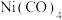 (该物质是配位化合物,且
(该物质是配位化合物,且  的结构式为
的结构式为  )常用作制备高纯镍粉,其熔点为
)常用作制备高纯镍粉,其熔点为 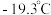 ,沸点为
,沸点为 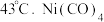 中
中  键和
键和  键的数目之比为
键的数目之比为___________ 。
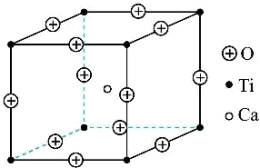
②在高温超导领域中,有一种化合物叫钙钛矿,其晶胞如图所示,在该晶胞中氧、钙、钛的粒子个数比是___________ 。
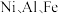 及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体
及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体 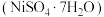 :
:
 如表所示:
如表所示:| 金属离子 | 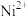 |  | 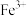 | 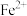 |
开始沉淀时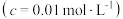 的  | 7.2 | 3.7 | 2.2 | 7.5 |
完全沉淀时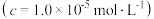 的  | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“滤液②”中除
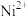 外还含有的金属离子
外还含有的金属离子(2)“转化”中可替代
 的物质是
的物质是由表格中的数据可求得
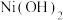 的
的 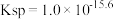 。如果“转化”后的溶液中
。如果“转化”后的溶液中 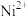 浓度为
浓度为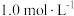 ,则除去杂质金属阳离子时“调
,则除去杂质金属阳离子时“调 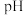 ”应控制的
”应控制的  范围是
范围是(3)硫酸镍在强碱溶液中用
 氧化,可沉淀出能用作镍镉电池正极材料的
氧化,可沉淀出能用作镍镉电池正极材料的 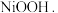 写出该反应的离子方程式
写出该反应的离子方程式(4)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
(5)第Ⅷ族元素单质及其化合物在工业生产和科研领域有重要的用途。
①
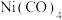 (该物质是配位化合物,且
(该物质是配位化合物,且  的结构式为
的结构式为  )常用作制备高纯镍粉,其熔点为
)常用作制备高纯镍粉,其熔点为 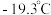 ,沸点为
,沸点为 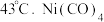 中
中  键和
键和  键的数目之比为
键的数目之比为②在高温超导领域中,有一种化合物叫钙钛矿,其晶胞如图所示,在该晶胞中氧、钙、钛的粒子个数比是
您最近一年使用:0次
名校
解题方法
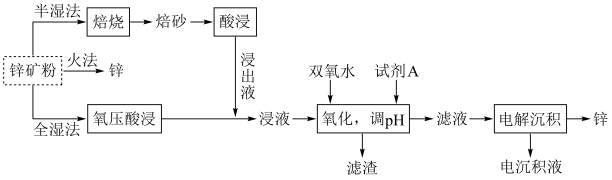
3 . 锌及锌合金(如黄铜)广泛应用于生产、生活。某小组拟以锌矿(主要成分是ZnS,含少量FeS等杂质)为原料采用多种方法冶炼锌,流程如图。回答下列问题:
已知:① 是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
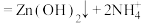 ,
,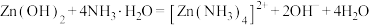 。
。
②常温下,几种金属离子转化成氢氧化物沉淀的pH如表:
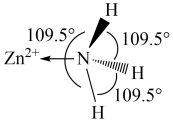
(1)已知 的部分结构如图所示,
的部分结构如图所示, 中
中 采用
采用 杂化,则
杂化,则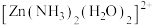 有
有_____ 种结构。 分子中的
分子中的 键角比
键角比 中的小的原因是
中的小的原因是_______ 。
(2)明代宋应星著的《天工开物》中有关“升炼倭铅”的记载:“每炉甘石十斤,装载入一泥罐内,封裹泥固,∙∙∙∙∙∙然后,逐层用煤炭饼垫盛,其底铺薪,发火煅红∙∙∙∙∙∙冷定,毁罐取出。∙∙∙∙∙∙即倭铅也。”(炉甘石主要成分是 ,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的
,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的_______ (填标号,下同)。从环保的角度来看,这三种方法中,最佳方法是_______ 。
a.半湿法 b.火法 c.全湿法
(3)“氧压酸浸”是在稀硫酸中加入锌矿粉,并在加压下通入 ,除生成
,除生成 外,还能回收非金属单质。ZnS参与反应的离子方程式为
外,还能回收非金属单质。ZnS参与反应的离子方程式为_________ 。
(4)“氧化,调pH”时试剂A不宜选择NaOH溶液,也不宜选择氨水,原因是________ 。
(5)“电解沉积”(以惰性材料为电极)时阳极的电极反应式为________ 。航母外壳常镶嵌一些锌块,这种保护航母的方法叫_______ 。
(6)通常认为离子浓度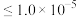 mol⋅L
mol⋅L 时表示该离子已完全除尽。根据表格数据计算
时表示该离子已完全除尽。根据表格数据计算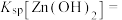
_____ 。

已知:①
 是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
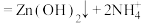 ,
,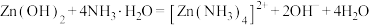 。
。②常温下,几种金属离子转化成氢氧化物沉淀的pH如表:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
 | 6.5 | 9.7 |
 | 5.4 | 8.0 |
 | 2.3 | 4.1 |
(1)已知
 的部分结构如图所示,
的部分结构如图所示, 中
中 采用
采用 杂化,则
杂化,则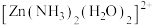 有
有 分子中的
分子中的 键角比
键角比 中的小的原因是
中的小的原因是
(2)明代宋应星著的《天工开物》中有关“升炼倭铅”的记载:“每炉甘石十斤,装载入一泥罐内,封裹泥固,∙∙∙∙∙∙然后,逐层用煤炭饼垫盛,其底铺薪,发火煅红∙∙∙∙∙∙冷定,毁罐取出。∙∙∙∙∙∙即倭铅也。”(炉甘石主要成分是
 ,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的
,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的a.半湿法 b.火法 c.全湿法
(3)“氧压酸浸”是在稀硫酸中加入锌矿粉,并在加压下通入
 ,除生成
,除生成 外,还能回收非金属单质。ZnS参与反应的离子方程式为
外,还能回收非金属单质。ZnS参与反应的离子方程式为(4)“氧化,调pH”时试剂A不宜选择NaOH溶液,也不宜选择氨水,原因是
(5)“电解沉积”(以惰性材料为电极)时阳极的电极反应式为
(6)通常认为离子浓度
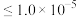 mol⋅L
mol⋅L 时表示该离子已完全除尽。根据表格数据计算
时表示该离子已完全除尽。根据表格数据计算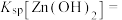
您最近一年使用:0次
2024-02-25更新
|
155次组卷
|
3卷引用:湖南省张家界市2023-2024学年高三上学期期末联考化学试题
名校
解题方法
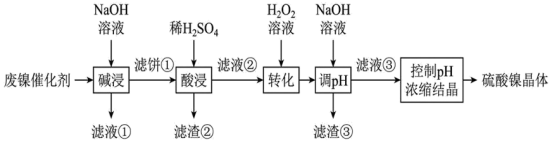
4 . 金属镍广泛应用于制造记忆合金、储氢合金以及用作加氢反应的催化剂,是重要的战略物资,但资源匮乏。某废镍催化剂主要含有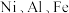 的氧化物及少量不溶性杂质,采用如下工艺流程回收其中的镍制备硫酸镍晶体
的氧化物及少量不溶性杂质,采用如下工艺流程回收其中的镍制备硫酸镍晶体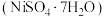 :
:

已知:① 等溶于
等溶于 溶液生成的酸根离子为
溶液生成的酸根离子为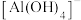 ,不是
,不是 ;
;
②溶液中金属离子开始沉淀和完全沉淀的 如下表所示:
如下表所示:
(1) 的原子序数为
的原子序数为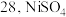 中
中 的简化电子排布式为
的简化电子排布式为_____ 。
(2)“碱浸”时发生反应的离子方程式为_____ 。
(3)滤渣③的主要成分为_____ 。
(4)利用已知②的表格数据,计算 的
的
_____ 。如果“转化”后的溶液中 浓度为
浓度为 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是_____ 。
(5)硫酸镍在强碱性溶液中用 氧化,可沉淀出能用作镍镉电池正极材料的
氧化,可沉淀出能用作镍镉电池正极材料的 。以
。以 溶液为介质的镍镉电池正极反应式可能为
溶液为介质的镍镉电池正极反应式可能为_____ 。
(6)将分离出硫酸镍晶体后的母液收集、并入滤液③进行循环使用,这么做的意义为_____ 。
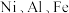 的氧化物及少量不溶性杂质,采用如下工艺流程回收其中的镍制备硫酸镍晶体
的氧化物及少量不溶性杂质,采用如下工艺流程回收其中的镍制备硫酸镍晶体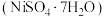 :
:
已知:①
 等溶于
等溶于 溶液生成的酸根离子为
溶液生成的酸根离子为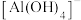 ,不是
,不是 ;
;②溶液中金属离子开始沉淀和完全沉淀的
 如下表所示:
如下表所示:| 金属离子 |  |  |  |  |
开始沉淀时 的 的 | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时 的 的 | 8.7 | 4.7 | 3.2 | 9.0 |
(1)
 的原子序数为
的原子序数为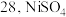 中
中 的简化电子排布式为
的简化电子排布式为(2)“碱浸”时发生反应的离子方程式为
(3)滤渣③的主要成分为
(4)利用已知②的表格数据,计算
 的
的
 浓度为
浓度为 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是(5)硫酸镍在强碱性溶液中用
 氧化,可沉淀出能用作镍镉电池正极材料的
氧化,可沉淀出能用作镍镉电池正极材料的 。以
。以 溶液为介质的镍镉电池正极反应式可能为
溶液为介质的镍镉电池正极反应式可能为(6)将分离出硫酸镍晶体后的母液收集、并入滤液③进行循环使用,这么做的意义为
您最近一年使用:0次
名校
5 . 某温度下,分别向 的
的 和
和 溶液中滴加
溶液中滴加 溶液,滴加过程中
溶液,滴加过程中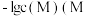 为
为 或
或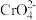 与
与 溶液体积
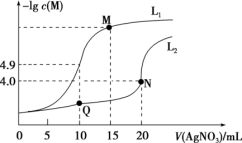
溶液体积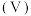 的变化关系如图所示(忽略溶液体积变化)。下列说法
的变化关系如图所示(忽略溶液体积变化)。下列说法不正确 的是
 的
的 和
和 溶液中滴加
溶液中滴加 溶液,滴加过程中
溶液,滴加过程中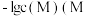 为
为 或
或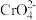 与
与 溶液体积
溶液体积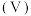 的变化关系如图所示(忽略溶液体积变化)。下列说法
的变化关系如图所示(忽略溶液体积变化)。下列说法
A.曲线 表示 表示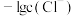 与 与 的变化关系 的变化关系 |
B. 点溶液中: 点溶液中: |
C.该温度下, 的数量级为 的数量级为 |
D.相同实验条件,若改为 的 的 和 和 溶液,曲线 溶液,曲线 中 中 点移到 点移到 点 点 |
您最近一年使用:0次
名校
解题方法
6 . 下列方案设计或现象和结论均完全正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 比较CH3COONa与NaClO酸性 | 室温下,用pH试纸分别测定室温下,用pH试纸分别测定 | NaClO溶液pH较大,则酸性:CH3COOH>HClO |
| B | 探究侯氏制碱法 | 向饱和食盐水中先通入二氧化碳至饱和后,再通入过量氨气 | 溶液变浑浊,析出NaHCO3 |
| C | 比较AgCl、AgI的Ksp大小 | 向5mL0.1mol/LAgNO3溶液中先加入4滴0.1mol/LNaCl溶液,再加入4滴0.1mol/LKI溶液 | 若先产生白色沉淀,后变为黄色沉淀,则AgI的Ksp较小 |
| D | 探究Na2SO3是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入BaCl2溶液 | 若有白色沉淀产生,则样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 根据下列实验操作和实验现象,得出相应实验结论错误的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 向AgCl悬浊液中加入少量KI固体 | 沉淀由白色转化为黄色 |  |
| B | 向2mL0.1mol·L-1的FeCl3溶液中加入足量铁粉,振荡,加1滴KSCN溶液 | 黄色逐渐消失,加KSCN溶液颜色不变 | 还原性: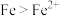 |
| C | 测定不同浓度NaHCO3溶液与Na2CO3溶液的pH | 后者pH更大 |  的水解程度小于 的水解程度小于 |
| D | 向滴有酚酞的Na2SO3溶液中加入少量BaCl2固体 | 生成白色沉淀,且红色逐渐变浅 | Na2SO3溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 硫化汞(HgS)是一种难溶于水的红色颜料,其在水中的沉淀溶解平衡曲线如图所示(已知: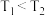 ),下列关于沉淀溶解平衡的说法错误的是
),下列关于沉淀溶解平衡的说法错误的是

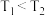 ),下列关于沉淀溶解平衡的说法错误的是
),下列关于沉淀溶解平衡的说法错误的是
A.图中a点对应的是 温度下HgS的不饱和溶液 温度下HgS的不饱和溶液 |
B.图中p、q点对应的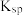 的关系为 的关系为 |
C.向m点对应的溶液中加入少量 固体,HgS的Ksp减小 固体,HgS的Ksp减小 |
| D.升高温度,溶度积增大,可实现由p点向q点的移动 |
您最近一年使用:0次
名校
9 . 下列应用或现象主要体现的是沉淀溶解平衡原理的有
①热纯碱溶液洗涤油污的能力
②误将钡盐[ 、
、 ]当作食盐食用后,用0.5%的
]当作食盐食用后,用0.5%的 溶液解毒
溶液解毒
③溶洞的形成
④碳酸钡不能作“钡餐”而硫酸钡能
⑤泡沫灭火器灭火
①热纯碱溶液洗涤油污的能力
②误将钡盐[
 、
、 ]当作食盐食用后,用0.5%的
]当作食盐食用后,用0.5%的 溶液解毒
溶液解毒③溶洞的形成
④碳酸钡不能作“钡餐”而硫酸钡能
⑤泡沫灭火器灭火
| A.仅②③④ | B.仅①②③ | C.仅③④⑤ | D.全部 |
您最近一年使用:0次
2024-02-14更新
|
43次组卷
|
2卷引用:湖南省 邵阳市第二中学2023-2024学年高二上学期1月期末化学试题
10 . 绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是


A.图中 和 和 可分别表示 可分别表示 温度下 温度下 饱和溶液中 饱和溶液中 与 与 的浓度 的浓度 |
B.图中各点对应的 的关系为 的关系为 |
C.向 点的溶液中加入少量 点的溶液中加入少量 固体,溶液组成由 固体,溶液组成由 沿 沿 线向 线向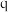 方向移动 方向移动 |
D.温度降低时,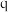 点的饱和溶液的组成由 点的饱和溶液的组成由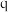 沿 沿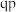 线向 线向 方向移动 方向移动 |
您最近一年使用:0次



