名校
1 . 铊(Tl)广泛用于电子、军工、航天、化工、治金、通讯等方面,一种以红铊矿(主要成分是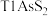 ,含少量
,含少量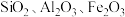 ,等杂质)为原料制备金属铊的流程如图所示。
,等杂质)为原料制备金属铊的流程如图所示。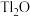 )膜,而失去金属光泽变得灰暗。
)膜,而失去金属光泽变得灰暗。
②TlCl难溶于水,而 溶于水。
溶于水。
③溶液中金属离子开始沉淀和完全沉淀的 如下表所示:
如下表所示:
回答下列问题:
(1) 中三元素的基态原子含有未成对电子数最多的元素是
中三元素的基态原子含有未成对电子数最多的元素是_______ 。(填元素符号)
(2)“焙烧1”中, 最终转化为
最终转化为 ﹔
﹔ 和
和 也转化为相应的硫酸盐。其中,
也转化为相应的硫酸盐。其中, 转化为
转化为 分如下两步完成。请写出第二步反应的化学方程式。
分如下两步完成。请写出第二步反应的化学方程式。
第一步( 与
与 反应):
反应):
第二步:_______ 。
(3)滤渣的成分 属于共价晶体,晶体中每个最小环含有
属于共价晶体,晶体中每个最小环含有_______ 个原子。
(4)“沉铊”步骤中,需要加入过量 ,其原因是
,其原因是_______ 。(用化学用语和简要的文字解释)
(5)向“沉铊”后的滤液中加入生石灰至 时才能外排,此时滤液中的
时才能外排,此时滤液中的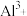 浓度为
浓度为_______  。(指数允许是小数)
。(指数允许是小数)
(6)“焙烧2”中发生的反应为 。则“置换”步骤中发生反应的离子方程式为
。则“置换”步骤中发生反应的离子方程式为_______ 。
(7)所得产品高纯铊应保存在_______ 中。
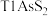 ,含少量
,含少量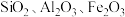 ,等杂质)为原料制备金属铊的流程如图所示。
,等杂质)为原料制备金属铊的流程如图所示。
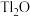 )膜,而失去金属光泽变得灰暗。
)膜,而失去金属光泽变得灰暗。②TlCl难溶于水,而
 溶于水。
溶于水。③溶液中金属离子开始沉淀和完全沉淀的
 如下表所示:
如下表所示:| 金属离子 |  |  |
开始沉淀的 | 2.2 | 3.5 |
沉淀完全( )的 )的 | 3.2 | 4.7 |
(1)
 中三元素的基态原子含有未成对电子数最多的元素是
中三元素的基态原子含有未成对电子数最多的元素是(2)“焙烧1”中,
 最终转化为
最终转化为 ﹔
﹔ 和
和 也转化为相应的硫酸盐。其中,
也转化为相应的硫酸盐。其中, 转化为
转化为 分如下两步完成。请写出第二步反应的化学方程式。
分如下两步完成。请写出第二步反应的化学方程式。第一步(
 与
与 反应):
反应):
第二步:
(3)滤渣的成分
 属于共价晶体,晶体中每个最小环含有
属于共价晶体,晶体中每个最小环含有(4)“沉铊”步骤中,需要加入过量
 ,其原因是
,其原因是(5)向“沉铊”后的滤液中加入生石灰至
 时才能外排,此时滤液中的
时才能外排,此时滤液中的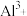 浓度为
浓度为 。(指数允许是小数)
。(指数允许是小数)(6)“焙烧2”中发生的反应为
 。则“置换”步骤中发生反应的离子方程式为
。则“置换”步骤中发生反应的离子方程式为(7)所得产品高纯铊应保存在
您最近一年使用:0次
名校
2 . 钒的用途十分广泛,有金属“维生素”之称。以含钒石煤(主要成分是V2O3、V2O4,含有的杂质有SiO2、FeS2及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
②Ksp(CaCO3)=2.8×10-9,Ksp(CaSiO3)=2.5×10-8,Ksp[Ca(VO3)2]远大于Ksp(CaCO3)。
回答下列问题:
(1)写出Cr3+的核外电子排布式为________ 。
(2)为了提高“焙烧”效率,可采取的措施有______ 。
(3)“焙烧”时,V2O3、V2O4都转化为Ca(VO3)2,写出V2O4转化为Ca(VO3)2的化学方程式:_____ 。
(4)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有______ ;“水浸”加入过量Na2CO3不能使CaSiO3完全转化为CaCO3,原因是_______ 。(列式计算平衡常数分析该反应进行的趋势,一般认为,K>105时反应进行较完全,K<105时反应难以进行)
(5)“离子交换”与“洗脱”可表示为[RCl4]+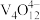
 [R-V4O12]+4Cl- ([RCl4]为强碱性阴离子交换树脂,
[R-V4O12]+4Cl- ([RCl4]为强碱性阴离子交换树脂,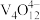 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用_____ 。
(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是____ (填字母)。
A.铝热反应制锰 B.电解熔融氯化钠制钠 C.氧化汞分解制汞

| 金属离子 | Fe3+ | Mg2+ | Al3+ | Mn2+ |
| 开始沉淀时的pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀时的pH | 3.2 | 9.0 | 4.7 | 10.1 |
回答下列问题:
(1)写出Cr3+的核外电子排布式为
(2)为了提高“焙烧”效率,可采取的措施有
(3)“焙烧”时,V2O3、V2O4都转化为Ca(VO3)2,写出V2O4转化为Ca(VO3)2的化学方程式:
(4)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有
(5)“离子交换”与“洗脱”可表示为[RCl4]+
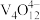
 [R-V4O12]+4Cl- ([RCl4]为强碱性阴离子交换树脂,
[R-V4O12]+4Cl- ([RCl4]为强碱性阴离子交换树脂,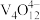 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是
A.铝热反应制锰 B.电解熔融氯化钠制钠 C.氧化汞分解制汞
您最近一年使用:0次
名校
3 . 绿矾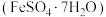 主要用于净水、照相制版及治疗缺铁性贫血等。工业上利用生活废铁(主要成分为
主要用于净水、照相制版及治疗缺铁性贫血等。工业上利用生活废铁(主要成分为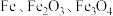 ,以及少量
,以及少量 等)制备绿矾的一种工艺流程如下:
等)制备绿矾的一种工艺流程如下:
(1)“焙烧”的目的是______ 。
(2)提高“酸溶”反应速率的措施是______ (任写一条)。“反应”时发生反应的离子方程式为______ 。
(3)隔绝空气的目的是______ ;一系列操作包括______ 、干燥。
(4)“酸溶”后,若溶液中 为
为 ,为了减少损失,常温下必须控制溶液的
,为了减少损失,常温下必须控制溶液的 小于
小于______  已知:
已知: 。
。
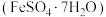 主要用于净水、照相制版及治疗缺铁性贫血等。工业上利用生活废铁(主要成分为
主要用于净水、照相制版及治疗缺铁性贫血等。工业上利用生活废铁(主要成分为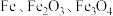 ,以及少量
,以及少量 等)制备绿矾的一种工艺流程如下:
等)制备绿矾的一种工艺流程如下: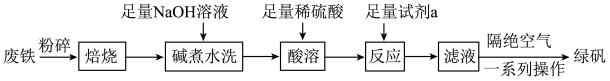
(1)“焙烧”的目的是
(2)提高“酸溶”反应速率的措施是
(3)隔绝空气的目的是
(4)“酸溶”后,若溶液中
 为
为 ,为了减少损失,常温下必须控制溶液的
,为了减少损失,常温下必须控制溶液的 小于
小于 已知:
已知: 。
。
您最近一年使用:0次
4 . 回答下列问题:
(1)某温度下,向含有AgCl固体的AgCl饱和溶液中加入少量稀盐酸,则AgCl的溶解度______ (填增大,减小或不变,下同),Ksp______ ,c(Ag+)______ 。
(2)现有25℃0.1mol/L的氨水。请回答以下问题:
①若向氨水中加入氯化铵固体,此时溶液中NH3•H2O电离程度_______ (填“增大”、“减小”或“不变”);此时溶液中水的离子积约等于_______ 。
②若向氨水中加入稀硫酸,使其恰好中和,写出离子方程式:______ 所得溶液的pH______ 7(填“>”“=”或“<”),用离子方程式表示其原因:______ 。
(1)某温度下,向含有AgCl固体的AgCl饱和溶液中加入少量稀盐酸,则AgCl的溶解度
(2)现有25℃0.1mol/L的氨水。请回答以下问题:
①若向氨水中加入氯化铵固体,此时溶液中NH3•H2O电离程度
②若向氨水中加入稀硫酸,使其恰好中和,写出离子方程式:
您最近一年使用:0次
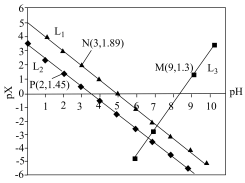
5 . 室温下,向Mg(NO3)2溶液、HF溶液、CH3CH2COOH溶液中分别滴加NaOH溶液,测得溶液中pH与pX[pX=-lgX,X代表 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是
已知:
 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是已知:

A. 代表的是pH与 代表的是pH与 的关系 的关系 |
B. 的 的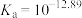 |
C.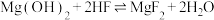 的 的 |
| D.含相同浓度NaF、HF的混合溶液的pH>7 |
您最近一年使用:0次
2024-04-01更新
|
452次组卷
|
5卷引用:湖南省邵阳市第二中学2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
6 . 按如下工艺流程以废旧锌锰干电池的外壳锌皮(含有少量Fe、ZnCl2、MnO2等杂质)为原料制取皓矾(ZnSO4·7H2O)。
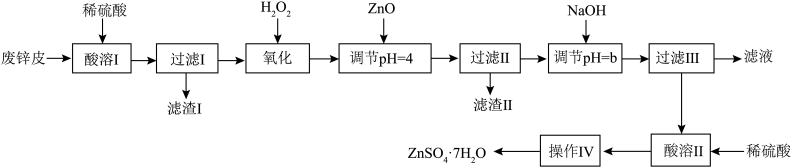
已知:①Ksp[Zn(OH)2]=1.0×10-17,当pH≥12.0时,Zn(OH)2开始转化为 而溶解。
而溶解。
②金属氢氧化物沉淀的pH:
请回答下列问题:
(1)“酸溶I”时,为了提高酸溶速率,可采取的措施有:___________ (任答两点),“滤渣I”的主要成分是___________ 。
(2)“氧化”时,酸性滤液中加入H2O2反应的离子方程式为___________ ,可用NaNO2代替H2O2,但缺点是___________ 。
(3)常温下,加入NaOH调pH=b,b的取值范围是___________ ,若“滤液”的pH=6,则溶液中残留的c(Zn2+)=___________ mol/L。
(4)“操作Ⅳ”的具体操作是___________ ,过滤,洗涤,干燥。

已知:①Ksp[Zn(OH)2]=1.0×10-17,当pH≥12.0时,Zn(OH)2开始转化为
 而溶解。
而溶解。②金属氢氧化物沉淀的pH:
| 氢氧化物 | 开始沉淀的pH | 完全沉淀的pH |
| Zn(OH)2 | 5.7 | 8.0 |
| Fe(OH)3 | 2.7 | 3.7 |
(1)“酸溶I”时,为了提高酸溶速率,可采取的措施有:
(2)“氧化”时,酸性滤液中加入H2O2反应的离子方程式为
(3)常温下,加入NaOH调pH=b,b的取值范围是
(4)“操作Ⅳ”的具体操作是
您最近一年使用:0次
名校
解题方法
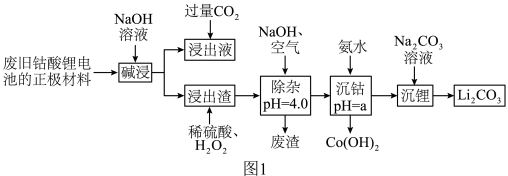
7 . 废旧钴酸锂电池的正极材料主要含有难溶于水的LiCoO2及少量Al、Fe、炭黑等,常用如图1所示的一种工艺分离并回收其中的金属钴和锂。
②相关金属离子形成氢氧化物沉淀的pH如下表:
回答下列问题:
(1)LiCoO2中元素Co的化合价为___________ 。
(2)为提高碱浸率,可采取的措施有___________ (答出一条即可)。
(3)碱浸时的离子反应方程式为___________ 。
(4)沉钴的离子方程式为___________ 。
(5)加氨水控制沉钴的pH,当a≥___________ 时,此时溶液中c(Co2+)≤10-5mol⋅L-1,即认为“沉钴”完全。
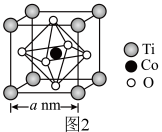
(6)钴的氢氧化物加热至290℃时可以完全脱水,所得产物可用于合成钛酸钴。钛酸钴的晶胞结构如图2所示,则该晶体化学式为___________ 。___________ molAgCl,该配合物中Co3+的配位数为___________ 。
②相关金属离子形成氢氧化物沉淀的pH如下表:
| 金属阳离子 | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀的pH | 4.2 | 2.7 | 7.6 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.6 |
(1)LiCoO2中元素Co的化合价为
(2)为提高碱浸率,可采取的措施有
(3)碱浸时的离子反应方程式为
(4)沉钴的离子方程式为
(5)加氨水控制沉钴的pH,当a≥
(6)钴的氢氧化物加热至290℃时可以完全脱水,所得产物可用于合成钛酸钴。钛酸钴的晶胞结构如图2所示,则该晶体化学式为
您最近一年使用:0次
2024-03-17更新
|
141次组卷
|
2卷引用:湖南省雅礼教育集团2023-2024学年高二下学期期中考试化学试题
名校
8 . 常温下,向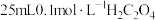 溶液中滴加
溶液中滴加 溶液,溶液中
溶液,溶液中 、
、 、
、 的分布系数
的分布系数 随
随 的变化如图所示(忽略反应过程中温度变化)。已知:
的变化如图所示(忽略反应过程中温度变化)。已知: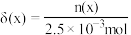 常温下,
常温下,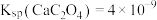 。下列说法错误的是
。下列说法错误的是
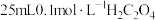 溶液中滴加
溶液中滴加 溶液,溶液中
溶液,溶液中 、
、 、
、 的分布系数
的分布系数 随
随 的变化如图所示(忽略反应过程中温度变化)。已知:
的变化如图所示(忽略反应过程中温度变化)。已知: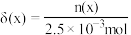 常温下,
常温下,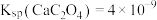 。下列说法错误的是
。下列说法错误的是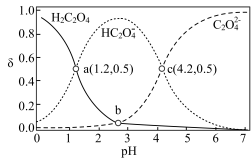
A.常温下,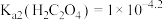 |
B.b、c点对应的溶液中均存在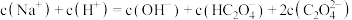 |
C. 时, 时,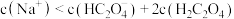 |
D.若等浓度、等体积的 溶液与 溶液与 溶液混合后产生沉淀,则上层清液中 溶液混合后产生沉淀,则上层清液中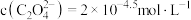 |
您最近一年使用:0次
2024-01-06更新
|
441次组卷
|
3卷引用:湖南省石门县第一中学2023-2024学年高二上学期期中考试化学试题
名校
9 . 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr2O (橙红色)、CrO
(橙红色)、CrO (黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,K2Cr2O7溶液中存在如下平衡:Cr2O
(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,K2Cr2O7溶液中存在如下平衡:Cr2O +H2O⇌2CrO
+H2O⇌2CrO +2H+
+2H+
回答下列问题:
(1)探究外界因素对该平衡的影响。取三支相同(标号1,2,3)试管盛有相同体积K2Cr2O7溶液进行实验,完成表格中的填空。
(2)利用(1)中所得溶液A、B探究pH对K2Cr2O7溶液的氧化性强弱的影响。完成表格中的填空。
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl−,利用Ag+与CrO 生成砖红色沉淀,指示到达滴定终点。滴定终点时,溶液中c(Ag+)=2.0×10−5 mol·L−1时,此时溶液中c(CrO
生成砖红色沉淀,指示到达滴定终点。滴定终点时,溶液中c(Ag+)=2.0×10−5 mol·L−1时,此时溶液中c(CrO )等于
)等于_______ mol·L−1.[已知Ksp(Ag2CrO4)=2.0×10−12 ]
 (橙红色)、CrO
(橙红色)、CrO (黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,K2Cr2O7溶液中存在如下平衡:Cr2O
(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,K2Cr2O7溶液中存在如下平衡:Cr2O +H2O⇌2CrO
+H2O⇌2CrO +2H+
+2H+回答下列问题:
(1)探究外界因素对该平衡的影响。取三支相同(标号1,2,3)试管盛有相同体积K2Cr2O7溶液进行实验,完成表格中的填空。
| 实验操作 | 实验现象 | 实验结论 |
| 向试管1中加入几滴浓NaOH溶液,得溶液A | ①溶液变为 | 其他条件不变时,减小生成物浓度,平衡向正反应方向移动 |
| 向试管2中加入几滴较浓H2SO4溶液,得溶液B | ②溶液变为 | ③其他条件不变时, |
| 向试管2中加入FeSO4,再加入适量NaOH溶液 | ④先形成蓝紫色溶液,加入NaOH溶液后产生沉淀的成分为Fe(OH)3和 | K2Cr2O7溶液具有氧化性 |
| 实验操作 | 实验现象 | 实验结论 |
| 向上述溶液A、B中分别加入相同量甲醇溶液 | 溶液A无明显现象,溶液B形成蓝紫色溶液,产生CO2 | ① ②B中反应的离子方程式: |
 生成砖红色沉淀,指示到达滴定终点。滴定终点时,溶液中c(Ag+)=2.0×10−5 mol·L−1时,此时溶液中c(CrO
生成砖红色沉淀,指示到达滴定终点。滴定终点时,溶液中c(Ag+)=2.0×10−5 mol·L−1时,此时溶液中c(CrO )等于
)等于
您最近一年使用:0次
名校
解题方法
10 . 根据下列实验操作和现象所得到的结论错误的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将少量HA滴入Na2CO3溶液中 | 未产生明显气泡 | 酸性:HA<H2CO3 |
| B | 向盛有同体积、同浓度的H2O2溶液的两支试管中分别滴加等体积的0.1 mol·L−1和0.2 mol·L−1 HI溶液 | 后者出现棕黄色时间短 | 其他条件不变时,一般浓度越大,该反应化学反应速率越快 |
| C | 将装有相同质量NO2和N2O4的混合气的两支烧瓶分别置于热水、冰水中 | 浸泡在热水中的烧瓶红棕色更深 | 2NO2(g)⇌ N2O4(g)H<0 |
| D | 向盛有2 mL 0.1 mol·L−1 NaCl溶液滴加5滴等浓度AgNO3溶液,出现白色沉淀,静置,滴入少量稀NaI溶液 | 出现黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



