2023·湖南·高考真题
1 . 聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
①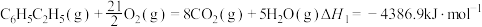
②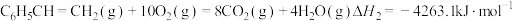
③
计算反应④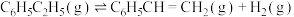 的
的
_______  ;
;
(2)在某温度、 下,向反应器中充入
下,向反应器中充入 气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入
气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入_______  水蒸气作为稀释气(计算时忽略副反应);
水蒸气作为稀释气(计算时忽略副反应);
(3)在 、
、 下,以水蒸气作稀释气。
下,以水蒸气作稀释气。 作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
⑤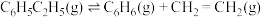
⑥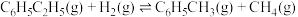
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S( )随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是
)随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是_______ ,理由是_______ ; 的描述错误的是_______;
的描述错误的是_______;
Ⅱ.苯乙烯的聚合
苯乙烯聚合有多种方法,其中一种方法的关键步骤是某 (Ⅰ)的配合物促进
(Ⅰ)的配合物促进 (引发剂,X表示卤素)生成自由基
(引发剂,X表示卤素)生成自由基 ,实现苯乙烯可控聚合。
,实现苯乙烯可控聚合。
(5)引发剂 中活性最高的是
中活性最高的是_______ ;
(6)室温下,① 在配体L的水溶液中形成
在配体L的水溶液中形成 ,其反应平衡常数为K;②
,其反应平衡常数为K;② 在水中的溶度积常数为
在水中的溶度积常数为 。由此可知,
。由此可知, 在配体L的水溶液中溶解反应的平衡常数为
在配体L的水溶液中溶解反应的平衡常数为_______ (所有方程式中计量系数关系均为最简整数比)。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
①
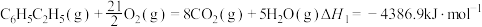
②
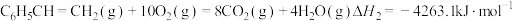
③

计算反应④
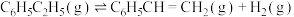 的
的
 ;
;(2)在某温度、
 下,向反应器中充入
下,向反应器中充入 气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入
气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入 水蒸气作为稀释气(计算时忽略副反应);
水蒸气作为稀释气(计算时忽略副反应);(3)在
 、
、 下,以水蒸气作稀释气。
下,以水蒸气作稀释气。 作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:⑤
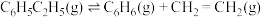
⑥
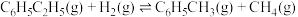
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S(
 )随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是
)随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是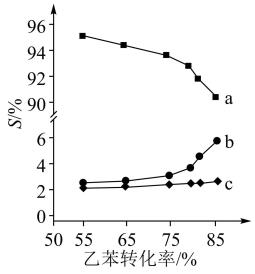
 的描述错误的是_______;
的描述错误的是_______;A.X射线衍射技术可测定 晶体结构 晶体结构 |
B. 可改变乙苯平衡转化率 可改变乙苯平衡转化率 |
C. 降低了乙苯脱氢反应的活化能 降低了乙苯脱氢反应的活化能 |
D.改变 颗粒大小不影响反应速率 颗粒大小不影响反应速率 |
Ⅱ.苯乙烯的聚合
苯乙烯聚合有多种方法,其中一种方法的关键步骤是某
 (Ⅰ)的配合物促进
(Ⅰ)的配合物促进 (引发剂,X表示卤素)生成自由基
(引发剂,X表示卤素)生成自由基 ,实现苯乙烯可控聚合。
,实现苯乙烯可控聚合。(5)引发剂
 中活性最高的是
中活性最高的是(6)室温下,①
 在配体L的水溶液中形成
在配体L的水溶液中形成 ,其反应平衡常数为K;②
,其反应平衡常数为K;② 在水中的溶度积常数为
在水中的溶度积常数为 。由此可知,
。由此可知, 在配体L的水溶液中溶解反应的平衡常数为
在配体L的水溶液中溶解反应的平衡常数为
您最近一年使用:0次
2023-06-16更新
|
7306次组卷
|
9卷引用:2023年湖南卷高考真题变式题(原理综合题)
(已下线)2023年湖南卷高考真题变式题(原理综合题)2023年高考湖南卷化学真题(已下线)专题17 原理综合题(已下线)专题14 化学反应原理综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)湖南省长沙市麓山国际实验学校2023-2024学年高三上学期第一次月考化学试题(已下线)压轴题13 化学反应原理综合题(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用) 浙江省义乌中学2024届高三上学期首考适应性考试化学试题湖北省沙市中学2023-2024学年高三下学期3月月考化学试题
2023·湖南·高考真题
真题
名校
2 . 处理某铜冶金污水(含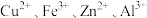 )的部分流程如下:
)的部分流程如下: 如下表所示:
如下表所示:
②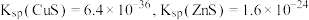 。
。
下列说法错误的是
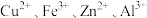 )的部分流程如下:
)的部分流程如下: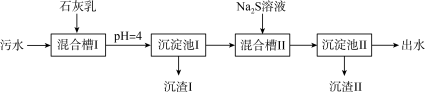
 如下表所示:
如下表所示:| 物质 |  |  |  |  |
开始沉淀 | 1.9 | 4.2 | 6.2 | 3.5 |
完全沉淀 | 3.2 | 6.7 | 8.2 | 4.6 |
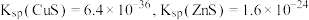 。
。下列说法错误的是
A.“沉渣Ⅰ”中含有 和 和 |
B. 溶液呈碱性,其主要原因是 溶液呈碱性,其主要原因是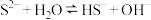 |
C.“沉淀池Ⅱ”中,当 和 和 完全沉淀时,溶液中 完全沉淀时,溶液中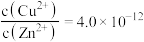 |
| D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水 |
您最近一年使用:0次
2023-06-16更新
|
9264次组卷
|
18卷引用:2023年湖南卷高考真题变式题(选择题6-10)
(已下线)2023年湖南卷高考真题变式题(选择题6-10)2023年高考湖南卷化学真题(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)专题07 无机物的转化 微型工艺流程-2023年高考化学真题题源解密(全国通用)(已下线)选择题11-13(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第32讲难溶电解质的溶解平衡(已下线)难溶电解质的溶解平衡题型15 沉淀溶解平衡及图像分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)安徽省六安第一中学2022-2023学年高二下学期期末考试化学试题浙江省杭州第十四中学2023-2024学年高二上学期 期中考试化学试卷福建省厦门市 第一中学2023-2024上学期高三上学期12月考化学试题江西省宜春市宜丰中学2023-2024学年高三上学期12月月考化学试题(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)10-2023新东方高二上期中考化学2024届河北省部分示范性高中2023-2024学年高三下学期一模化学试题河北省2024届高三下学期3月大数据应用调研联合测评(六)化学试题
22-23高三下·福建厦门·阶段练习
解题方法
3 . 软磁材料 可由阳极渣和黄铁矿
可由阳极渣和黄铁矿 制得。阳极渣的主要成分为
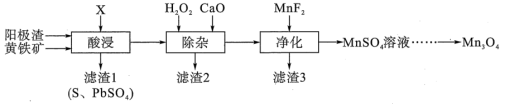
制得。阳极渣的主要成分为 且含有少量Pb、Fe、Cu等元素的化合物。制备流程如下。
且含有少量Pb、Fe、Cu等元素的化合物。制备流程如下。
25℃时,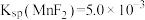 、
、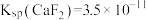 。下列说法错误的是
。下列说法错误的是
 可由阳极渣和黄铁矿
可由阳极渣和黄铁矿 制得。阳极渣的主要成分为
制得。阳极渣的主要成分为 且含有少量Pb、Fe、Cu等元素的化合物。制备流程如下。
且含有少量Pb、Fe、Cu等元素的化合物。制备流程如下。
25℃时,
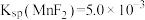 、
、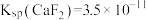 。下列说法错误的是
。下列说法错误的是| A.X可为稀硫酸 |
B.滤渣2成分是 和 和 |
C.“净化”发生的反应为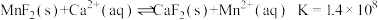 |
D.利用 替代CaO可优化该流程 替代CaO可优化该流程 |
您最近一年使用:0次
22-23高二下·广东肇庆·期中
4 . 镍(Ni)及其化合物广泛应用于电池、电镀和催化剂等领域,一种以电镀废渣(除含镍外,还含有 、
、 、
、 等)为原料获得
等)为原料获得 的流程如图:
的流程如图:
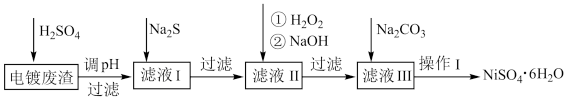
(1) 的VSEPR模型为
的VSEPR模型为_______ 。
(2)加入 的目的是
的目的是_______ [已知: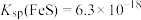 ,
,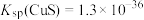 ,
,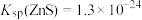 ,
, ]
]
(3) 为
为_______ (填“极性”或“非极性”)分子,写出 与“滤液Ⅱ”反应的离子方程式:
与“滤液Ⅱ”反应的离子方程式:_______ 。
(4)向“滤液Ⅱ”中加入NaOH调节pH在一定范围内可生成氢氧化铁沉淀。已知常温下 的
的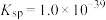 ,若要使溶液中
,若要使溶液中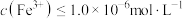 ,则应该控制溶液pH不小于
,则应该控制溶液pH不小于_______ 。
(5)硫酸镍与硫酸铜类似,向硫酸镍中加入足量氨水可以形成 蓝色溶液。在
蓝色溶液。在 中,提供孤对电子的原子是
中,提供孤对电子的原子是_______ , 分子的空间结构为
分子的空间结构为_______ , 的核外电子排布式为
的核外电子排布式为_______ 。
 、
、 、
、 等)为原料获得
等)为原料获得 的流程如图:
的流程如图:
(1)
 的VSEPR模型为
的VSEPR模型为(2)加入
 的目的是
的目的是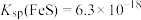 ,
,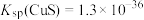 ,
,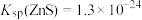 ,
, ]
](3)
 为
为 与“滤液Ⅱ”反应的离子方程式:
与“滤液Ⅱ”反应的离子方程式:(4)向“滤液Ⅱ”中加入NaOH调节pH在一定范围内可生成氢氧化铁沉淀。已知常温下
 的
的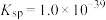 ,若要使溶液中
,若要使溶液中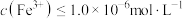 ,则应该控制溶液pH不小于
,则应该控制溶液pH不小于(5)硫酸镍与硫酸铜类似,向硫酸镍中加入足量氨水可以形成
 蓝色溶液。在
蓝色溶液。在 中,提供孤对电子的原子是
中,提供孤对电子的原子是 分子的空间结构为
分子的空间结构为 的核外电子排布式为
的核外电子排布式为
您最近一年使用:0次
2023·全国·模拟预测
名校
5 . 从砷化镓废料(主要成分为GaAs、 ,
, 和
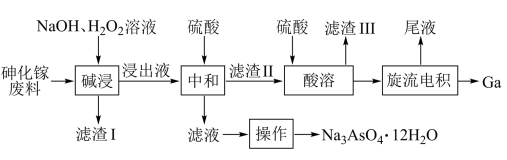
和 )中回收镓和砷的工艺流程如图所示。
)中回收镓和砷的工艺流程如图所示。
已知:① 是两性氢氧化物,25℃时,
是两性氢氧化物,25℃时, 的溶度积
的溶度积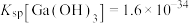 ,电离常数
,电离常数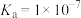 ;②溶液中微粒的浓度不大于
;②溶液中微粒的浓度不大于 时,可认为该微粒沉淀完全。下列说法错误的是
时,可认为该微粒沉淀完全。下列说法错误的是
 ,
, 和
和 )中回收镓和砷的工艺流程如图所示。
)中回收镓和砷的工艺流程如图所示。
已知:①
 是两性氢氧化物,25℃时,
是两性氢氧化物,25℃时, 的溶度积
的溶度积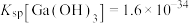 ,电离常数
,电离常数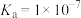 ;②溶液中微粒的浓度不大于
;②溶液中微粒的浓度不大于 时,可认为该微粒沉淀完全。下列说法错误的是
时,可认为该微粒沉淀完全。下列说法错误的是| A.“碱浸”时,温度不能过高也不能过低 |
B.“碱浸”时,GaAs发生反应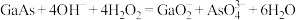 |
| C.为提高镓的回收率,加硫酸中和时,pH的最大值是5 |
| D.“旋流电积”所得“尾液”可循环利用 |
您最近一年使用:0次
22-23高二下·云南玉溪·阶段练习
名校
6 . 电镀行业中废水处理后产生的含重金属污泥废弃物称为电镀污泥,被列入国家危险废物名单中的第十七类危险废物。工业上可利用某电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等重金属,其利用回收流程如下:
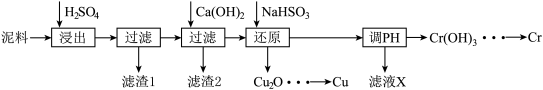
已知①部分物质沉淀的pH如下:
②CaSO4的溶解度:20℃:0.260g 80℃:0.228g
(1)①基态铬的价层电子排布式___________ 。
②已知高温时,Cu2O比CuO稳定,原因是___________ 。
(2)除铁等相关操作:
①加入石灰乳调节pH应满足要求是___________ 。
②将浊液加热到80℃,趁热过滤。滤渣Ⅱ的主要成分是___________ (填化学式)。
(3)还原步骤中生成Cu2O固体的离子反应方程式___________ 。
(4)当离子浓度≤1×10−5 mol∙L−1时认为沉淀完全,则表格中a的值是___________ 。(已知:T=25℃,Ksp[Cr(OH)3]=6.3×10−31,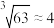 ,lg2=0.3)
,lg2=0.3)
(5)将铬块加入到稀盐酸或稀硫酸中,可观察到铬逐渐溶解,同时放出氢气。但若将铬块加稀硝酸中,却看不到明显现象。由此推测,出现该现象的可能原因是___________ 。

已知①部分物质沉淀的pH如下:
| Fe3+ | Cu2+ | Cr3+ | |
| 开始沉淀的pH | 2.1 | 4.7 | 4.3 |
| 恰好完全沉淀的pH | 3.2 | 6.7 | a |
(1)①基态铬的价层电子排布式
②已知高温时,Cu2O比CuO稳定,原因是
(2)除铁等相关操作:
①加入石灰乳调节pH应满足要求是
②将浊液加热到80℃,趁热过滤。滤渣Ⅱ的主要成分是
(3)还原步骤中生成Cu2O固体的离子反应方程式
(4)当离子浓度≤1×10−5 mol∙L−1时认为沉淀完全,则表格中a的值是
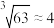 ,lg2=0.3)
,lg2=0.3)(5)将铬块加入到稀盐酸或稀硫酸中,可观察到铬逐渐溶解,同时放出氢气。但若将铬块加稀硝酸中,却看不到明显现象。由此推测,出现该现象的可能原因是
您最近一年使用:0次
7 . 钒铬还原渣是钠化提钒过程的固体废弃物,其主要成分为VO2∙xH2O、Cr(OH)3及少量的SiO2。一种初步分离钒铬还原渣中钒铬并获得Na2Cr2O7的工艺流程如图。
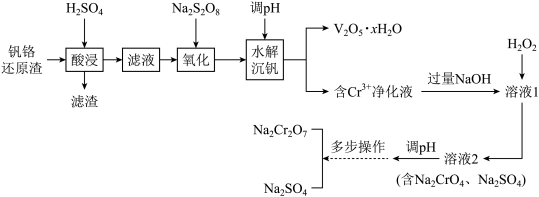
已知:①“酸浸”后为VO2∙xH2O转化为VO2+;
②Cr(OH)3的Ksp近似为1×10-31;下列说法正确的是

已知:①“酸浸”后为VO2∙xH2O转化为VO2+;
②Cr(OH)3的Ksp近似为1×10-31;下列说法正确的是
| A.滤渣的成分为H2SiO3 |
B.“氧化”生成 发生反应的离子方程式为2VO2++ 发生反应的离子方程式为2VO2++ +2H2O=2 +2H2O=2 +2 +2 +4H+ +4H+ |
| C.若“含Cr3+净化液”中c(Cr3+)=0.1mol/L,则“水解沉钒”调pH应不超过10 |
D.“溶液1”中含 ,加入H2O2后发生反应的离子方程式为2 ,加入H2O2后发生反应的离子方程式为2 +3H2O2+2OH-=2 +3H2O2+2OH-=2 +2H++2H2O +2H++2H2O |
您最近一年使用:0次
8 . 铁、镍及其化合物有广泛的用途。某矿渣的主要成分为NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,以下是从该矿渣中回收NiSO4的工艺流程:
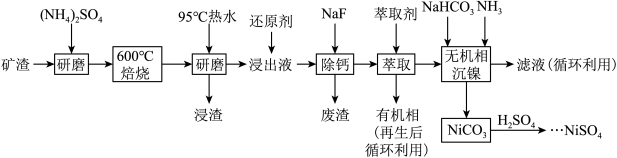
已知:①(NH4)2SO4在350℃以上会分解生成NH3和H2SO4;NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3;
②Ksp(CaF2)=4.0×10-11。
则下列说法错误的是

已知:①(NH4)2SO4在350℃以上会分解生成NH3和H2SO4;NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3;
②Ksp(CaF2)=4.0×10-11。
则下列说法错误的是
| A.(NH4)2SO4的作用是将金属元素转化为可溶性硫酸盐,便于浸出 |
| B.“浸渣”的成分为Fe(OH)3和SiO2 |
C.沉镍过程中的离子方程式:Ni2++HCO +NH3=NiCO3↓+NH +NH3=NiCO3↓+NH |
| D.“浸出液”中c(Ca2+)=1.0×10-3mol•L-1,当除钙率达到99%时,溶液中c(F-)=2.0×10-3mol•L-1 |
您最近一年使用:0次
2023-03-03更新
|
597次组卷
|
3卷引用:2023年湖南卷高考真题变式题(选择题6-10)
2023·黑龙江大庆·一模
解题方法
9 . 我国科学家开发催化剂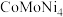 来提高
来提高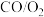 燃料电池的性能。某小组以含镍废料(主要含
燃料电池的性能。某小组以含镍废料(主要含 、
、 ,以及少量
,以及少量 、
、 、
、 、
、 、
、 、
、 和
和 等)为原料提取镍的流程如下:
等)为原料提取镍的流程如下:
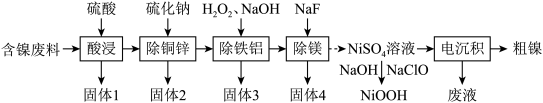
已知常温下部分难溶物的 如表所示:
如表所示:
请回答下列问题:
(1)“酸浸”中产生了一种还原性气体,它是_______ (填化学式);“除铁铝”中双氧水的作用是_______ 。
(2)“固体2”中除 、
、 外,还可能含硫单质等物质,生成硫单质的离子方程式为
外,还可能含硫单质等物质,生成硫单质的离子方程式为_______ 。
(3)为提高原料利用率,“电沉积”得到的“废液”可以循环用于_______ (填名称)工序。
(4)常温下,在“除铁铝”中,当滤液中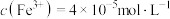 时,其
时,其
_______ 。
(5)可以通过电解法提纯镍,粗镍作_______ (填“阳”或“阴”)极,阴极的电极反应式为_______ 。
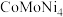 来提高
来提高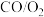 燃料电池的性能。某小组以含镍废料(主要含
燃料电池的性能。某小组以含镍废料(主要含 、
、 ,以及少量
,以及少量 、
、 、
、 、
、 、
、 、
、 和
和 等)为原料提取镍的流程如下:
等)为原料提取镍的流程如下:
已知常温下部分难溶物的
 如表所示:
如表所示:| 物质 |  |  |  |  |  |  |  |
 |  | 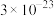 | 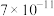 | 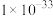 | 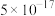 | 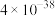 | 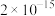 |
(1)“酸浸”中产生了一种还原性气体,它是
(2)“固体2”中除
 、
、 外,还可能含硫单质等物质,生成硫单质的离子方程式为
外,还可能含硫单质等物质,生成硫单质的离子方程式为(3)为提高原料利用率,“电沉积”得到的“废液”可以循环用于
(4)常温下,在“除铁铝”中,当滤液中
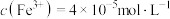 时,其
时,其
(5)可以通过电解法提纯镍,粗镍作
您最近一年使用:0次
22-23高二下·湖北孝感·开学考试
名校
解题方法
10 . 镍、铬等属于宝贵的金属资源。一种回收电化学废渣中铬镍的工艺流程如下:
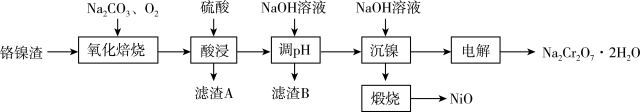
已知:
①铬镍渣中含有 、
、 、
、 、
、 、
、 等;
等;
②25℃时,部分物质的溶度积表:
③
回答下列问题:
(1)“氧化焙烧”时, 发生的化学方程式
发生的化学方程式_______ 。
(2)“酸浸”使用强力搅拌器搅拌的目的是_______ ,滤渣A主要是_______ (填化学式)。
(3)“调 ”时,若
”时,若 至少为
至少为_______ 时, 沉淀完全。(
沉淀完全。( )
)
(4)“沉镍”后,“煅烧”的化学方程式为_______ 。
(5)已知“电解”操作中的装置如下图所示。
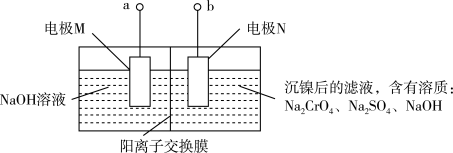
①a接电源的_______ (填“正”或“负”)极。
②电极N上的电极反应式为_______ 。

已知:
①铬镍渣中含有
 、
、 、
、 、
、 、
、 等;
等;②25℃时,部分物质的溶度积表:
| 物质 |  |  |  |  |
 | 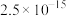 | 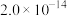 | 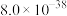 | 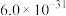 |

回答下列问题:
(1)“氧化焙烧”时,
 发生的化学方程式
发生的化学方程式(2)“酸浸”使用强力搅拌器搅拌的目的是
(3)“调
 ”时,若
”时,若 至少为
至少为 沉淀完全。(
沉淀完全。( )
)(4)“沉镍”后,“煅烧”的化学方程式为
(5)已知“电解”操作中的装置如下图所示。

①a接电源的
②电极N上的电极反应式为
您最近一年使用:0次
2023-02-02更新
|
207次组卷
|
3卷引用:2023年湖南卷高考真题变式题(工业流程题)
(已下线)2023年湖南卷高考真题变式题(工业流程题)湖北省孝感市部分学校2022-2023学年高二下学期收心考试(开学考试)化学试题安徽省淮北市第一中学2022-2023学年高二下学期第二次月考化学试题



