名校
解题方法
1 . 常温下,已知:
下列判断正确的是
| 物质 | CH3COOH | H2CO3 | CaCO3 |
| 平衡常数 | K=1.8×10-5 | Ka1=4.3×10-7,Ka2=5.6×10-11 | Ksp=2.8×10-9 |
A.向 溶液中滴入酚酞,溶液变红,原因是 溶液中滴入酚酞,溶液变红,原因是 |
B.常温时, 与 与 混合溶液的 混合溶液的 ,则 ,则 |
C. 溶液中, 溶液中, |
D. 的 的 溶液与 溶液与 溶液等体积混合出现沉淀,则 溶液等体积混合出现沉淀,则 溶液的浓度一定是 溶液的浓度一定是 (假设混合溶液体积为两溶液体积之和) (假设混合溶液体积为两溶液体积之和) |
您最近一年使用:0次
2023-02-15更新
|
347次组卷
|
18卷引用:湖南省益阳市2022-2023学年高二上学期期末质量检测化学试题
湖南省益阳市2022-2023学年高二上学期期末质量检测化学试题黑龙江省大庆实验中学2020-2021学年高二上学期期末考试化学试题福建省仙游一中、莆田二中、莆田四中2020-2021学年高二上学期期末联考化学试题四川省巴中市恩阳区2022-2023学年高二上学期1月期末化学试题山西省康杰中学2017-2018学年高二上学期期中考试化学试题(已下线)2017-2018学年上学期期末复习备考之精准复习模拟题高二化学选修4(C卷)【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期期中考试化学试题湖北省随州市第一中学2018-2019学年高二下学期期中考试化学试题辽宁省丹东市凤城市第一中学2019-2020学年高二上学期12月月考化学试题湖北省黄冈市黄梅国际育才高级中学2019-2020学年高二上学期期中考试化学试题山东省邹城市第一中学2020-2021学年高二上学期期中质量检测化学试题江西省景德镇一中2020-2021学年高二上学期期中考试化学(2班)试题山西省怀仁市第一中学云东校区2020-2021学年高二上学期第三次月考化学试题江苏省镇江市第一中学2020-2021学年高二下学期4月分阶段测化学试题(已下线)综合复习与测试(2)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)四川省自贡市田家柄中学教育集团2021-2022学年高二下学期入学考试化学试题(已下线)2023年高考浙江卷化学真题(6月)变式题(选择题11-16)上海市控江中学2023-2024学年高二上学期等级班阶段测验卷二 化学试题
解题方法
2 .  是常用于治疗胃酸过多的药剂的主要成分之一、在实验室中,向含有
是常用于治疗胃酸过多的药剂的主要成分之一、在实验室中,向含有 固体的悬浊液中滴加少许浓盐酸(忽略体积和温度变化),下列数值变小的是
固体的悬浊液中滴加少许浓盐酸(忽略体积和温度变化),下列数值变小的是
 是常用于治疗胃酸过多的药剂的主要成分之一、在实验室中,向含有
是常用于治疗胃酸过多的药剂的主要成分之一、在实验室中,向含有 固体的悬浊液中滴加少许浓盐酸(忽略体积和温度变化),下列数值变小的是
固体的悬浊液中滴加少许浓盐酸(忽略体积和温度变化),下列数值变小的是A. | B.c( ) ) | C.c( ) ) | D.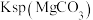 |
您最近一年使用:0次
解题方法
3 . 化学学习离不开实验。下列实验操作正确且能达到实验目的的是
| 选项 | 操作 | 目的 |
| A | 向乙醇中加入生石灰,然后蒸馏 | 除去乙醇中混有的少量水 |
| B | 室温下,用pH试纸测量NaClO溶液的pH | 证明HClO是弱酸 |
| C | 加入NaOH溶液,振荡、静置 | 除去乙酸乙酯中混有的乙酸 |
| D | 向2mL0.1mol•L-1AgNO3溶液中滴加2滴0.1mol•L-1NaCl溶液出现白色沉淀,再滴加2滴相同浓度的NaI溶液,振荡,出现黄色沉淀 | 证明Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-14更新
|
143次组卷
|
2卷引用:湖南省娄底市涟源市2023-2024学年高二上学期1月期末考试化学试题
名校
解题方法
4 . 下列实验方案中能达到相应实验目的的是
| A | B | C | D | |
| 方案 |  | 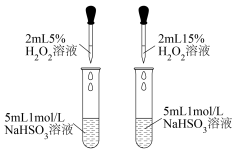 |  取铁电极附近溶液滴加铁氰化钾 |  将NO2球分别浸泡在冷水和热水中 |
| 目的 | 证明 比 比 更难溶 更难溶 | 探究浓度对化学反应速率的影响 | 证明 能在该条件下发生析氢腐蚀 能在该条件下发生析氢腐蚀 | 探究温度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-14更新
|
279次组卷
|
2卷引用:湖南省长沙市实验中学2022-2023学年高二上学期期末考试化学试题
名校
5 . 下列说法中,正确的是
| A.难溶电解质达到沉淀溶解平衡时,保持温度不变增加难溶电解质的量,平衡向溶解方向移动 |
| B.难溶电解质都是弱电解质 |
C.在白色 沉淀上滴加 沉淀上滴加 溶液,沉淀变黑,说明 溶液,沉淀变黑,说明 比 比 更难溶于水 更难溶于水 |
D. 在水中的溶解度大于在饱和 在水中的溶解度大于在饱和 溶液中的溶解度 溶液中的溶解度 |
您最近一年使用:0次
6 . 已知如下物质的溶度积常数: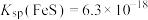 ,
,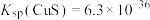 。下列说法正确的是
。下列说法正确的是
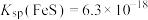 ,
, 。下列说法正确的是
。下列说法正确的是| A.同温度下,CuS的溶解度大于FeS的溶解度 |
B.同温度下,向饱和FeS溶液中加入少量 固体后, 固体后,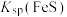 变小 变小 |
C.向含有等物质的量的 和 和 的混合溶液中逐滴加入 的混合溶液中逐滴加入 溶液,最先出现的沉淀是FeS 溶液,最先出现的沉淀是FeS |
D.除去工业废水中的 ,可以选用FeS作沉淀剂 ,可以选用FeS作沉淀剂 |
您最近一年使用:0次
2023-02-14更新
|
451次组卷
|
24卷引用:2015-2016学年湖南省衡阳八中高二上学期期末化学试卷
2015-2016学年湖南省衡阳八中高二上学期期末化学试卷(已下线)2010年广东省东莞市高二第二学期期末考试化学A卷(已下线)2011-2012学年福建师大附中高二上学期期末考试化学试卷2014-2015甘肃省高台县一中高二上学期期末考试化学试卷黑龙江省大庆十中2018-2019学年高二上学期期末考试化学试题甘肃省张掖市2019—2020学年高二上学期期末学业水平质量检测化学试题黑龙江省牡丹江市穆棱市第一中学2019-2020学年高二上学期期末考试化学试题陕西省安康市2020-2021学年高二上学期期末化学试题甘肃省天水市一中2020-2021学年高二上学期第二学段(期末)考试化学试题贵州省贵阳市普通中学2021-2022学年高三上学期期末考试化学试题辽宁省锦州市渤海大学附属高级中学2022-2023学年高二上学期期末考试化学试题(已下线)专题08 沉淀溶解平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)2015-2016学年山东省平度市高二上学期直升班抽考化学试卷2015-2016学年山东省青岛市平度市高二上学期教学质检化学试卷陕西省榆林市第二中学2019-2020学年高二上学期第二次月考化学试题(已下线)易错17 难溶电解质的溶解平衡及应用-备战2021年高考化学一轮复习易错题安徽省六安市新安中学2020-2021学年高二下学期入学考试(重点班)化学试题广西梧州市蒙山中学2020-2021学年高二下学期4月月考化学试题黑龙江省鹤岗市第一中学2021-2022学年高二上学期期中考试化学试题第四节 沉淀溶解平衡 第1课时 难溶电解质的沉淀溶解平衡四川省雅安中学2022-2023学年高二下学期期中考试化学试题第2课时 沉淀溶解平衡的应用北京市育才学校2023-2024学年高一上学期化学期中试题北京市育才学校2023-2024学年高二上学期期中考试化学试题
7 . 由下列实验操作和现象得出的结论一定正确的是
| 选项 | 实验操作和现象 | 实验结论 |
 | 向 溶液中滴加少量硫酸酸化的 溶液中滴加少量硫酸酸化的 溶液,溶液变为棕黄色后迅速出现大量气泡 溶液,溶液变为棕黄色后迅速出现大量气泡 |  催化 催化 发生分解反 发生分解反应生成氧气 |
 | 用 计测定 计测定 和 和 饱和溶液的 饱和溶液的 值,前者 值,前者 小 小 |  酸性强于 酸性强于 |
 | 向盛有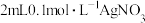 溶液的试管中滴加5滴 溶液的试管中滴加5滴 溶液,产生白色沉淀;再往试管中滴加5滴0.1 溶液,产生白色沉淀;再往试管中滴加5滴0.1 溶液,出现黄色沉淀 溶液,出现黄色沉淀 |  |
 | 等体积 的 的 和 和 两种酸, 两种酸, 稀释10倍, 稀释10倍, 稀释100倍后, 稀释100倍后, 依然相同 依然相同 | 酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 已知25℃时,Ksp(AgCl)=1.8×10-10。下列叙述正确的是
| A.25℃时,向饱和AgCl水溶液中加入盐酸,Ksp值变大 |
| B.25℃时,AgCl在饱和NaCl溶液中的溶解度比在纯水中的小 |
| C.将固体AgCl加入到KI溶液中,部分AgCl转化为AgI,说明AgCl溶解度小于AgI |
| D.AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-) |
您最近一年使用:0次
名校
9 . 现有一瓶市售白醋,化学课外兴趣小组欲用酸碱滴定法测定其含酸量(设其中的酸均为乙酸)。请你参与他们的实验并回答有关问题:选择酚酞作指示剂,用标准 溶液测定白醋中醋酸的浓度,以检测白醋是否符合国家标准。测定过程如图所示:
溶液测定白醋中醋酸的浓度,以检测白醋是否符合国家标准。测定过程如图所示:

已知:国家标准规定酿造白醋中醋酸含量不得低于 。
。
(1)①滴定达到终点时的现象是滴入半滴标准 溶液后
溶液后_______ 。
②某次实验滴定开始和结束时,碱式滴定管中的液面如图所示:

已知实验所用标准 溶液的浓度为
溶液的浓度为 ,根据上述滴定结果可知该白醋
,根据上述滴定结果可知该白醋_______ (填“符合”或“不符合”国家标准。
③下列操作中,可能使所测白醋中醋酸的浓度数值偏低的是_______ (填标号)。
A.碱式滴定管未用标准 溶液润洗就直接注入标准
溶液润洗就直接注入标准 溶液
溶液
B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.滴定过程中摇动锥形瓶时有液滴溅出
D.读取 溶液体积时,开始时仰视读数,滴定结束时俯视读数
溶液体积时,开始时仰视读数,滴定结束时俯视读数
E.碱式滴定管在滴定前有气泡,滴定后气泡消失
④该市售白醋的标签上还注明其中含有苯甲酸钠,如要知道在通常状况下醋酸与苯甲酸钠会不会发生离子互换反应,则需要明确的是_______ (填标号)。
a.在通常状况下,相同物质的量浓度的醋酸溶液、苯甲酸钠溶液的
b.在通常状况下,相同物质的量浓度的醋酸溶液、苯甲酸溶液的
c.在通常状况下,醋酸、苯甲酸钠的溶解度
(2)若用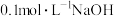 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中
的盐酸和醋酸溶液,得到滴定过程中 随加入
随加入 溶液体积而变化的两条滴定曲线如图所示。
溶液体积而变化的两条滴定曲线如图所示。

①滴定醋酸的曲线是_______ (填“I”或“Ⅱ”)。
② 和
和 的关系:
的关系:
_______  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
(3)在分析化学中,测定含氯的中性溶液中 的含量,以
的含量,以 作指示剂,用
作指示剂,用 溶液滴定。滴定终点的现象是有砖红色沉淀生成,当溶液中
溶液滴定。滴定终点的现象是有砖红色沉淀生成,当溶液中 恰好完全沉淀(浓度为
恰好完全沉淀(浓度为 )时,此时溶液中
)时,此时溶液中
_______  。已知:
。已知: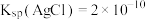 ,
, [
[ (砖红色)]
(砖红色)]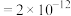 。
。
 溶液测定白醋中醋酸的浓度,以检测白醋是否符合国家标准。测定过程如图所示:
溶液测定白醋中醋酸的浓度,以检测白醋是否符合国家标准。测定过程如图所示:
已知:国家标准规定酿造白醋中醋酸含量不得低于
 。
。(1)①滴定达到终点时的现象是滴入半滴标准
 溶液后
溶液后②某次实验滴定开始和结束时,碱式滴定管中的液面如图所示:

已知实验所用标准
 溶液的浓度为
溶液的浓度为 ,根据上述滴定结果可知该白醋
,根据上述滴定结果可知该白醋③下列操作中,可能使所测白醋中醋酸的浓度数值偏低的是
A.碱式滴定管未用标准
 溶液润洗就直接注入标准
溶液润洗就直接注入标准 溶液
溶液B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.滴定过程中摇动锥形瓶时有液滴溅出
D.读取
 溶液体积时,开始时仰视读数,滴定结束时俯视读数
溶液体积时,开始时仰视读数,滴定结束时俯视读数E.碱式滴定管在滴定前有气泡,滴定后气泡消失
④该市售白醋的标签上还注明其中含有苯甲酸钠,如要知道在通常状况下醋酸与苯甲酸钠会不会发生离子互换反应,则需要明确的是
a.在通常状况下,相同物质的量浓度的醋酸溶液、苯甲酸钠溶液的

b.在通常状况下,相同物质的量浓度的醋酸溶液、苯甲酸溶液的

c.在通常状况下,醋酸、苯甲酸钠的溶解度
(2)若用
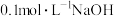 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中
的盐酸和醋酸溶液,得到滴定过程中 随加入
随加入 溶液体积而变化的两条滴定曲线如图所示。
溶液体积而变化的两条滴定曲线如图所示。
①滴定醋酸的曲线是
②
 和
和 的关系:
的关系:
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。(3)在分析化学中,测定含氯的中性溶液中
 的含量,以
的含量,以 作指示剂,用
作指示剂,用 溶液滴定。滴定终点的现象是有砖红色沉淀生成,当溶液中
溶液滴定。滴定终点的现象是有砖红色沉淀生成,当溶液中 恰好完全沉淀(浓度为
恰好完全沉淀(浓度为 )时,此时溶液中
)时,此时溶液中
 。已知:
。已知: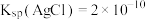 ,
, [
[ (砖红色)]
(砖红色)]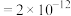 。
。
您最近一年使用:0次
10 . 弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。回答下列问题:
(1)已知 在水中存在以下平衡:
在水中存在以下平衡: ,
, ,
, 溶液显
溶液显_______ (填“酸性”、“碱性”、“中性”);等体积等物质的量浓度的 和
和 溶液混合后,所得溶液中离子浓度由大到小顺序是
溶液混合后,所得溶液中离子浓度由大到小顺序是_______ 。
(2) 时,次氯酸的
时,次氯酸的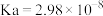 ;亚硫酸的
;亚硫酸的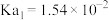 、
、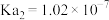 。将少量的
。将少量的 通入
通入 溶液中反应的离子方程式为
溶液中反应的离子方程式为_______ 。
(3)常温下,向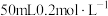 的氨水中逐滴加入
的氨水中逐滴加入 的盐酸,所得溶液的
的盐酸,所得溶液的 、溶液中
、溶液中 和
和 的物质的量分数与加入盐酸的体积的关系如下图所示。
的物质的量分数与加入盐酸的体积的关系如下图所示。

① 的电离常数为
的电离常数为_______ 。
②当加入盐酸的体积为 时,溶液中
时,溶液中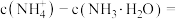
_______  (用计算式表示)。
(用计算式表示)。
(4) 溶液与
溶液与 溶液反应会生成
溶液反应会生成 沉淀。已知:常温下
沉淀。已知:常温下 ,
, ,则
,则 转化为
转化为 的平衡常数
的平衡常数
_______ 。
(1)已知
 在水中存在以下平衡:
在水中存在以下平衡: ,
, ,
, 溶液显
溶液显 和
和 溶液混合后,所得溶液中离子浓度由大到小顺序是
溶液混合后,所得溶液中离子浓度由大到小顺序是(2)
 时,次氯酸的
时,次氯酸的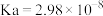 ;亚硫酸的
;亚硫酸的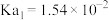 、
、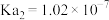 。将少量的
。将少量的 通入
通入 溶液中反应的离子方程式为
溶液中反应的离子方程式为(3)常温下,向
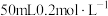 的氨水中逐滴加入
的氨水中逐滴加入 的盐酸,所得溶液的
的盐酸,所得溶液的 、溶液中
、溶液中 和
和 的物质的量分数与加入盐酸的体积的关系如下图所示。
的物质的量分数与加入盐酸的体积的关系如下图所示。
①
 的电离常数为
的电离常数为②当加入盐酸的体积为
 时,溶液中
时,溶液中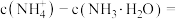
 (用计算式表示)。
(用计算式表示)。(4)
 溶液与
溶液与 溶液反应会生成
溶液反应会生成 沉淀。已知:常温下
沉淀。已知:常温下 ,
, ,则
,则 转化为
转化为 的平衡常数
的平衡常数
您最近一年使用:0次



