名校
1 . 莫尔法是用 作指示剂,用
作指示剂,用 标准溶液测定
标准溶液测定 (或
(或 )浓度的方法。现用莫尔法测定亚硝酰氯样品中NOCl的纯度,实验步骤如下:
)浓度的方法。现用莫尔法测定亚硝酰氯样品中NOCl的纯度,实验步骤如下:
步骤1:配制 溶液。
溶液。
步骤2:标定 溶液。准确称取
溶液。准确称取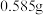 干燥的NaCl固体于烧杯中,用蒸馏水溶解后,转移至
干燥的NaCl固体于烧杯中,用蒸馏水溶解后,转移至 容量瓶中,并洗涤再转移、定容、摇匀。取3份所配NaCl溶液,每份
容量瓶中,并洗涤再转移、定容、摇匀。取3份所配NaCl溶液,每份 ,分别置于锥形瓶中,加
,分别置于锥形瓶中,加 水、适量
水、适量 溶液,在不断摇动下用
溶液,在不断摇动下用 溶液滴定至终点[
溶液滴定至终点[ (砖红色)]。实验测得三次滴定消耗
(砖红色)]。实验测得三次滴定消耗 溶液体积的平均值为
溶液体积的平均值为 。
。
步骤3:测定亚硝酰氯样品中NOCl的纯度。取 样品,溶于蒸馏水(与水发生反应生成一种氯化物和两种氮的氧化物,其中一种呈红棕色),配成
样品,溶于蒸馏水(与水发生反应生成一种氯化物和两种氮的氧化物,其中一种呈红棕色),配成 溶液,准确量取
溶液,准确量取 溶液于锥形瓶中;加入适量
溶液于锥形瓶中;加入适量 溶液作指示剂,用上述
溶液作指示剂,用上述 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液的体积为
标准溶液的体积为 。
。
根据上述实验原理,下列说法正确的是
 作指示剂,用
作指示剂,用 标准溶液测定
标准溶液测定 (或
(或 )浓度的方法。现用莫尔法测定亚硝酰氯样品中NOCl的纯度,实验步骤如下:
)浓度的方法。现用莫尔法测定亚硝酰氯样品中NOCl的纯度,实验步骤如下:步骤1:配制
 溶液。
溶液。步骤2:标定
 溶液。准确称取
溶液。准确称取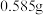 干燥的NaCl固体于烧杯中,用蒸馏水溶解后,转移至
干燥的NaCl固体于烧杯中,用蒸馏水溶解后,转移至 容量瓶中,并洗涤再转移、定容、摇匀。取3份所配NaCl溶液,每份
容量瓶中,并洗涤再转移、定容、摇匀。取3份所配NaCl溶液,每份 ,分别置于锥形瓶中,加
,分别置于锥形瓶中,加 水、适量
水、适量 溶液,在不断摇动下用
溶液,在不断摇动下用 溶液滴定至终点[
溶液滴定至终点[ (砖红色)]。实验测得三次滴定消耗
(砖红色)]。实验测得三次滴定消耗 溶液体积的平均值为
溶液体积的平均值为 。
。步骤3:测定亚硝酰氯样品中NOCl的纯度。取
 样品,溶于蒸馏水(与水发生反应生成一种氯化物和两种氮的氧化物,其中一种呈红棕色),配成
样品,溶于蒸馏水(与水发生反应生成一种氯化物和两种氮的氧化物,其中一种呈红棕色),配成 溶液,准确量取
溶液,准确量取 溶液于锥形瓶中;加入适量
溶液于锥形瓶中;加入适量 溶液作指示剂,用上述
溶液作指示剂,用上述 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液的体积为
标准溶液的体积为 。
。根据上述实验原理,下列说法正确的是
| A.步骤2中,若称量NaCl固体前没有干燥,则测定样品中NClO纯度偏低 |
| B.整个实验过程中,滴定管尖嘴不可触碰锥形瓶内壁 |
| C.滴入最后半滴标准液时,沉淀颜色变为砖红色即停止滴定 |
| D.步骤3中,若滴定终点时俯视读数,则测定结果偏低 |
您最近一年使用:0次
解题方法
2 . 水果中维生素 (摩尔质量为
(摩尔质量为 )的含量可用化学实验方法测定。酸性条件下,向含维生素
)的含量可用化学实验方法测定。酸性条件下,向含维生素 的淀粉
的淀粉 溶液中加入
溶液中加入 溶液,当
溶液,当 溶液刚刚加入时,
溶液刚刚加入时, 会与
会与 迅速发生氧化还原反应生成
迅速发生氧化还原反应生成 ;然后生成的
;然后生成的 会与维生素
会与维生素 发生反应(二者以物质的量之比
发生反应(二者以物质的量之比 反应),
反应), 被迅速消耗;当溶液中的维生素
被迅速消耗;当溶液中的维生素 全部反应后,
全部反应后, 与
与 继续反应生成的
继续反应生成的 会使淀粉变蓝色。实验步骤如下:
会使淀粉变蓝色。实验步骤如下:
(1)称取 水果样品,切碎研磨,取其汁配成
水果样品,切碎研磨,取其汁配成 溶液待用;
溶液待用;
(2)取 该溶液于锥形瓶中,向其中加入适量盐酸和过量淀粉
该溶液于锥形瓶中,向其中加入适量盐酸和过量淀粉 溶液;
溶液;
(3)向滴定管中装入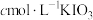 标准溶液,记录滴定管读数为
标准溶液,记录滴定管读数为 ;
;
(4)用滴定管向锥形瓶中逐滴加入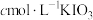 标准溶液至终点,记录滴定管读数为
标准溶液至终点,记录滴定管读数为 。
。
水果样品中维生素 的含量为
的含量为
 (摩尔质量为
(摩尔质量为 )的含量可用化学实验方法测定。酸性条件下,向含维生素
)的含量可用化学实验方法测定。酸性条件下,向含维生素 的淀粉
的淀粉 溶液中加入
溶液中加入 溶液,当
溶液,当 溶液刚刚加入时,
溶液刚刚加入时, 会与
会与 迅速发生氧化还原反应生成
迅速发生氧化还原反应生成 ;然后生成的
;然后生成的 会与维生素
会与维生素 发生反应(二者以物质的量之比
发生反应(二者以物质的量之比 反应),
反应), 被迅速消耗;当溶液中的维生素
被迅速消耗;当溶液中的维生素 全部反应后,
全部反应后, 与
与 继续反应生成的
继续反应生成的 会使淀粉变蓝色。实验步骤如下:
会使淀粉变蓝色。实验步骤如下:(1)称取
 水果样品,切碎研磨,取其汁配成
水果样品,切碎研磨,取其汁配成 溶液待用;
溶液待用;(2)取
 该溶液于锥形瓶中,向其中加入适量盐酸和过量淀粉
该溶液于锥形瓶中,向其中加入适量盐酸和过量淀粉 溶液;
溶液;(3)向滴定管中装入
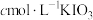 标准溶液,记录滴定管读数为
标准溶液,记录滴定管读数为 ;
;(4)用滴定管向锥形瓶中逐滴加入
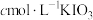 标准溶液至终点,记录滴定管读数为
标准溶液至终点,记录滴定管读数为 。
。水果样品中维生素
 的含量为
的含量为A. | B. |
C. | D. |
您最近一年使用:0次
3 . 可逆反应有一定的反应限度,平衡常数的大小能反映化学反应进行的程度。为测定可逆反应 的平衡常数K,实验步骤如下。
的平衡常数K,实验步骤如下。
I.一定温度下,将0.01mol/L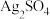 溶液与0.04mol/L
溶液与0.04mol/L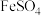 溶液等体积混合。
溶液等体积混合。
Ⅱ.待实验I中反应达到平衡状态时,取V mL上层清液,用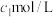
 标准溶液进行滴定,达到终点时,消耗
标准溶液进行滴定,达到终点时,消耗 标准溶液
标准溶液
 。
。
已知: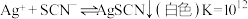
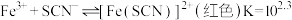
下列操作使测定的K值偏小的是
 的平衡常数K,实验步骤如下。
的平衡常数K,实验步骤如下。I.一定温度下,将0.01mol/L
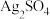 溶液与0.04mol/L
溶液与0.04mol/L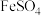 溶液等体积混合。
溶液等体积混合。Ⅱ.待实验I中反应达到平衡状态时,取V mL上层清液,用
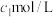
 标准溶液进行滴定,达到终点时,消耗
标准溶液进行滴定,达到终点时,消耗 标准溶液
标准溶液
 。
。已知:
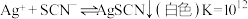
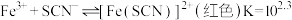
下列操作使测定的K值偏小的是
| A.取实验Ⅰ的浊液测定 |
| B.滴定过程中振荡剧烈,有待测液溅出 |
| C.滴定前滴定管尖嘴内无气泡,滴定后尖嘴内有气泡 |
| D.达到终点时最后半滴标准液用蒸馏水冲入锥形瓶 |
您最近一年使用:0次
名校
4 . 硼酸 在水溶液中存在电离平衡:
在水溶液中存在电离平衡: 。用
。用 溶液分别滴定体积均为
溶液分别滴定体积均为 的
的 硼酸溶液、
硼酸溶液、 硼酸和甘露醇混合溶液,滴定过程中硼酸溶液
硼酸和甘露醇混合溶液,滴定过程中硼酸溶液 ,混合溶液的
,混合溶液的 随加入的
随加入的 溶液体积的变化如图。
溶液体积的变化如图。
 在水溶液中存在电离平衡:
在水溶液中存在电离平衡: 。用
。用 溶液分别滴定体积均为
溶液分别滴定体积均为 的
的 硼酸溶液、
硼酸溶液、 硼酸和甘露醇混合溶液,滴定过程中硼酸溶液
硼酸和甘露醇混合溶液,滴定过程中硼酸溶液 ,混合溶液的
,混合溶液的 随加入的
随加入的 溶液体积的变化如图。
溶液体积的变化如图。
已知:
| A.加入甘露醇不利于硼酸的准确滴定 |
B.从 滴定到 滴定到 ,混合溶液的 ,混合溶液的 比硼酸溶液的 比硼酸溶液的 大 大 |
C.P点: |
D.W点: |
您最近一年使用:0次
名校
5 . 某工厂废液中含有大量的 、
、 及少量的
及少量的 、
、 ,利用该废液制备
,利用该废液制备 的流程如下:
的流程如下:
称取m g产品溶解于大量较浓盐酸中,在 氛围下用适量还原剂恰好将
氛围下用适量还原剂恰好将 还原为
还原为 ,用
,用 的
的 标准液滴定,终点时消耗标准液V mL。
标准液滴定,终点时消耗标准液V mL。
已知:①氧化性 ;
;
②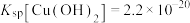 ,
, ;
;
③当溶液中离子浓度小于等于 时,可认为该离子沉淀完全。
时,可认为该离子沉淀完全。
根据上述产品含量测定的实验原理,下列说法错误的是
 、
、 及少量的
及少量的 、
、 ,利用该废液制备
,利用该废液制备 的流程如下:
的流程如下: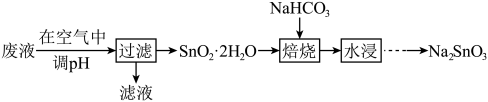
称取m g产品溶解于大量较浓盐酸中,在
 氛围下用适量还原剂恰好将
氛围下用适量还原剂恰好将 还原为
还原为 ,用
,用 的
的 标准液滴定,终点时消耗标准液V mL。
标准液滴定,终点时消耗标准液V mL。已知:①氧化性
 ;
;②
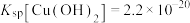 ,
, ;
;③当溶液中离子浓度小于等于
 时,可认为该离子沉淀完全。
时,可认为该离子沉淀完全。根据上述产品含量测定的实验原理,下列说法错误的是
A.实验室配制 溶液时需加入盐酸和锡粉 溶液时需加入盐酸和锡粉 |
| B.若加入的还原剂不足,则测定结果偏小 |
C.滴定时选用淀粉作指示剂,产生 的离子方程式: 的离子方程式: |
D.则产品中Sn的质量分数为 % % |
您最近一年使用:0次
名校
6 . 为检测某品牌银耳中添加剂亚硫酸盐的含量,取 银耳样品和
银耳样品和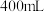 蒸馏水放入三颈瓶中;取
蒸馏水放入三颈瓶中;取 碘标准溶液和
碘标准溶液和 淀粉溶液加入锥形瓶中,并加入适量蒸馏水搅拌,部分装置如图。向三颈瓶中通氮气,再加入过量磷酸,加热并保持微沸,同时用
淀粉溶液加入锥形瓶中,并加入适量蒸馏水搅拌,部分装置如图。向三颈瓶中通氮气,再加入过量磷酸,加热并保持微沸,同时用 碘标准溶液滴定,至终点时滴定消耗了
碘标准溶液滴定,至终点时滴定消耗了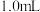 碘标准液。另做空白实验,消耗
碘标准液。另做空白实验,消耗 碘标准溶液。下列说法正确的是
碘标准溶液。下列说法正确的是
 银耳样品和
银耳样品和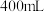 蒸馏水放入三颈瓶中;取
蒸馏水放入三颈瓶中;取 碘标准溶液和
碘标准溶液和 淀粉溶液加入锥形瓶中,并加入适量蒸馏水搅拌,部分装置如图。向三颈瓶中通氮气,再加入过量磷酸,加热并保持微沸,同时用
淀粉溶液加入锥形瓶中,并加入适量蒸馏水搅拌,部分装置如图。向三颈瓶中通氮气,再加入过量磷酸,加热并保持微沸,同时用 碘标准溶液滴定,至终点时滴定消耗了
碘标准溶液滴定,至终点时滴定消耗了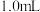 碘标准液。另做空白实验,消耗
碘标准液。另做空白实验,消耗 碘标准溶液。下列说法正确的是
碘标准溶液。下列说法正确的是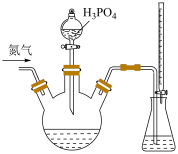
A.选择的三颈瓶规格为 |
| B.滴定终点溶液变为蓝色,读数时应双手上下持滴定管 |
| C.“不通氮气”或者“先加磷酸再通氮气”,这两种做法都会使测定结果偏高 |
D.银耳样品中亚硫酸盐的百分含量(以 质量计)为 质量计)为 |
您最近一年使用:0次
2024-02-06更新
|
344次组卷
|
3卷引用:山东省威海市2023-2024学年高三上学期期末考试化学试题
7 . 一定条件下,利用浓溴水与苯酚反应,可测定工业废水中苯酚的含量(其他杂质不与浓溴水反应)。实验步骤如下:
①用酸式滴定管准确量取20.00mL待测废水于100mL锥形瓶中;
②向锥形瓶中迅速加入过量的 浓溴水,塞紧瓶塞,振荡;
浓溴水,塞紧瓶塞,振荡;
③打开瓶塞,向锥形瓶中迅速加入过量的 溶液,塞紧瓶塞,振荡;
溶液,塞紧瓶塞,振荡;
④滴入2~3滴指示剂,再用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 ,发生反应:
,发生反应: ;
;
⑤待测废水换为蒸馏水进行空白实验,重复上述步骤,消耗 溶液
溶液 。
。
废水中苯酚含量( )表达式正确的是
)表达式正确的是
①用酸式滴定管准确量取20.00mL待测废水于100mL锥形瓶中;
②向锥形瓶中迅速加入过量的
 浓溴水,塞紧瓶塞,振荡;
浓溴水,塞紧瓶塞,振荡;③打开瓶塞,向锥形瓶中迅速加入过量的
 溶液,塞紧瓶塞,振荡;
溶液,塞紧瓶塞,振荡;④滴入2~3滴指示剂,再用
 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 ,发生反应:
,发生反应: ;
;⑤待测废水换为蒸馏水进行空白实验,重复上述步骤,消耗
 溶液
溶液 。
。废水中苯酚含量(
 )表达式正确的是
)表达式正确的是A.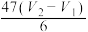 | B. | C.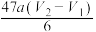 | D. |
您最近一年使用:0次
解题方法
8 . 草酸亚铁晶体(FeC2O4·2H20,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对草酸亚铁晶体样品(含FeSO4杂质)的纯度进行测定。步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250 mL溶液;
步骤2:取上述溶液25.00 mL,用c mol/L KMnO4标准液滴定至终点,消耗标准液V1 mL;
步骡3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4再用c mol/L KMnO4标准溶液滴定至终点,消耗标准液V2 mL。
下列关于该实验的叙述,错误的是
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250 mL溶液;
步骤2:取上述溶液25.00 mL,用c mol/L KMnO4标准液滴定至终点,消耗标准液V1 mL;
步骡3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4再用c mol/L KMnO4标准溶液滴定至终点,消耗标准液V2 mL。
下列关于该实验的叙述,错误的是
| A.步骤3中加入锌粉的目的为将Fe3+还原为Fe2+ |
B.草酸亚铁晶体样品的纯度为 |
| C.量取25.00 mL样品溶液,初始时平视最后仰视读数,将导致测定结果偏高 |
| D.为便于滴定终点的判断,滴定前必须往体系中加入指示剂 |
您最近一年使用:0次
2020·浙江·模拟预测
9 . 室温下,向20.00mL0.1000mol•L-1盐酸中滴加0.1000mol•L-1NaOH溶液,溶液的pH随NaOH溶液体积的变化如图。已知lg5≈0.7。下列说法不正确的是
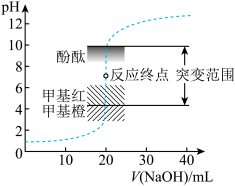
| A.NaOH与盐酸恰好完全反应时,pH=7 |
| B.选择变色范围在pH突变范围内的指示剂,可减小实验误差 |
| C.选择甲基红指示反应终点,误差比甲基橙的大 |
| D.V(NaOH)=30.00mL时,pH≈12.3 |
您最近一年使用:0次
2023-10-21更新
|
877次组卷
|
51卷引用:山东省济南市大学城实验高级中学2021届高三1月阶段性考试化学试题
山东省济南市大学城实验高级中学2021届高三1月阶段性考试化学试题(已下线)浙江省2020年1月选考(学考)化学试题2020年浙江省高考化学试卷(1月选考)浙江省丽水市松阳县第二中学2019-2020学年高二4月线上教学检测化学试题广东省化州市第一中学2019-2020学年高二4月线上统一测试化学试题江苏省启东中学2020-2021学年高二上学期第一次月考化学试题湖南省怀化市2020-2021学年高二上学期10月联考化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP409】【化学】(已下线)【浙江新东方】99(已下线)小题必刷31 酸碱中和滴定及拓展应用——2021年高考化学一轮复习小题必刷(通用版本)(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)广西贵港市覃塘区覃塘高级中学2020-2021学年高二下学期3月月考化学试题浙江省杭州市长征中学2020-2021学年高二下学期第二学期阶段性练习化学试题选择性必修1(SJ)专题3专题培优专练选择性必修1 专题3素养检测(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时41 酸碱中和滴定及拓展应用-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题3.2.2 酸碱中和滴定和pH的计算(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)湖北省麻城市实验高级中学2021-2022学年高二上学期9月月考化学(B卷)试卷内蒙古鄂尔多斯市第一中学2021-2022学年高二上学期第一次月考化学试题(已下线)3.2.2 酸碱中和滴定和pH的计算-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)专题14.水溶液中的离子平衡-十年(2012-2021)高考化学真题分项汇编(浙江专用)安徽师范大学附属中学2021-2022学年高二上学期期中考查化学试题浙江省浙北G2(湖州中学、嘉兴一中)2021-2022学年高二上学期期中联考化学试题(已下线)专题25 水的电离和溶液的酸碱性(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)内蒙古霍林郭勒市第一中学2021-2022学年高二上学期期中考试化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题18 酸碱混合图像为载体考查离子平衡-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)专题4 滴定终点专练(已下线)考点27 水的电离和溶液的pH-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第31练 水的电离和溶液的pH-2023年高考化学一轮复习小题多维练(全国通用)陕西省汉中中学2021-2022学年高二上学期第四次月考化学试题(已下线)第24讲 水的电离和溶液的pH(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第22讲 水的电离与溶液的pH(讲)-2023年高考化学一轮复习讲练测(新教材新高考)湖南省株洲市五雅中学2022-2023学年高二上学期11月期中考试化学试题 广西钦州市2022-2023学年高二上学期第2次教学质量监测化学试卷(已下线)题型133 酸碱中和滴定实验及误差分析(已下线)第八章 水溶液中的离子反应与平衡 第48练 酸碱中和反应及中和滴定上海市华东政法大学附属中学2022-2023学年高二下学期期中考试(等级考)化学试题(已下线)第12讲 酸碱中和滴定和氧化还原反应滴定-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)作业(十六) 酸碱中和滴定(已下线)考点27 水的电离与溶液的pH(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第3讲 酸碱中和滴定河北省衡水市第二中学2023-2024学年高三上学期学科素养评估(三调)化学试题【定心卷】3.2.3 酸碱中和滴定随堂练习-人教版2023-2024学年选择性必修1江苏省无锡市锡东高级中学2023-2024学年高二下学期期中考试化学试题天津市和平区2023-2024学年高三下学期第二次质量调查化学试卷
名校
解题方法
10 . 25℃时,向浓度均为 的NaOH和氨水的混合溶液中逐滴加入
的NaOH和氨水的混合溶液中逐滴加入 的盐酸(
的盐酸( 的
的 ;用
;用 的盐酸滴定等浓度的NaOH溶液,滴定终点的pH突跃范围9.7~4.3)。下列说法
的盐酸滴定等浓度的NaOH溶液,滴定终点的pH突跃范围9.7~4.3)。下列说法不正确 的是
 的NaOH和氨水的混合溶液中逐滴加入
的NaOH和氨水的混合溶液中逐滴加入 的盐酸(
的盐酸( 的
的 ;用
;用 的盐酸滴定等浓度的NaOH溶液,滴定终点的pH突跃范围9.7~4.3)。下列说法
的盐酸滴定等浓度的NaOH溶液,滴定终点的pH突跃范围9.7~4.3)。下列说法| A.恰好中和时,溶液呈酸性 |
B.滴定过程中, |
C.滴加盐酸接近pH=9.7的过程中,发生反应的离子方程式为: |
D.中性时, |
您最近一年使用:0次
2023-07-29更新
|
286次组卷
|
5卷引用:山东省济宁市嘉祥县第一中学2023-2024学年高二上学期12月月考化学试题
山东省济宁市嘉祥县第一中学2023-2024学年高二上学期12月月考化学试题山东省济南市历城第二中学2023-2024学年高二上学期期末化学模拟试题河南省郑州市2022-2023学年高二上学期期末化学试题(已下线)题型02 溶液中粒子浓度大小比较-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)河南省焦作市博爱县第一中学2023-2024学年高二下学期开学化学试题



