名校
1 . 下列实验操作规范且能达到相应实验目的的是
|
|
|
|
| A | B | C | D |
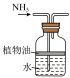
| A.制备氨水 |
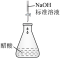
| B.测定醋酸浓度 |
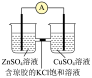
| C.验证锌与硫酸铜反应过程中有电子转移 |
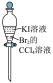
D.除去 中的 中的 |
您最近一年使用:0次
名校
解题方法
2 . 滴定是中学阶段重要的实验之一,请回答下列问题。
用0.1mol·L-1NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol·L-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。

(1)滴定醋酸的曲线是___________ (填“Ⅰ”或“Ⅱ”),可选用的滴定终点指示剂为___________ 。
(2)滴定开始前,三种溶液中由水电离出的c(H+)最大的是___________ 。
(3)V1和V2的关系:V1___________ V2(填“>”、“=”或“<”)。
(4)M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是___________ 。
(5)硫代硫酸钠晶体(Na2S2O3·5H2O,M=248g·mol-1)可用作定影剂,还原剂。利用K2Cr2O7,标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①称取1.2000g硫代硫酸钠晶体样品配成100mL溶液。
②取0.00950mol·L-1的K2Cr2O7标准溶液20.00mL,硫酸酸化后加入过量KI,发生反应: 。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:
。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应: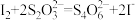 。加入淀粉溶液作为指示剂,继续滴定,当溶液
。加入淀粉溶液作为指示剂,继续滴定,当溶液___________ ,即为终点。平行滴定3次,样品溶液的平均用量为24.80mL,则样品纯度为___________ 。
用0.1mol·L-1NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol·L-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。

(1)滴定醋酸的曲线是
(2)滴定开始前,三种溶液中由水电离出的c(H+)最大的是
(3)V1和V2的关系:V1
(4)M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是
(5)硫代硫酸钠晶体(Na2S2O3·5H2O,M=248g·mol-1)可用作定影剂,还原剂。利用K2Cr2O7,标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①称取1.2000g硫代硫酸钠晶体样品配成100mL溶液。
②取0.00950mol·L-1的K2Cr2O7标准溶液20.00mL,硫酸酸化后加入过量KI,发生反应:
 。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:
。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应: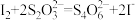 。加入淀粉溶液作为指示剂,继续滴定,当溶液
。加入淀粉溶液作为指示剂,继续滴定,当溶液
您最近一年使用:0次
名校
3 . 某学习小组用 标准溶液来测定未知物质的量浓度的盐酸时,选择酚酞作指示剂.请回答下列问题:
标准溶液来测定未知物质的量浓度的盐酸时,选择酚酞作指示剂.请回答下列问题:
(1)盛装 标准溶液的仪器名称为
标准溶液的仪器名称为___________________ ,若滴定开始和结束时,该仪器中溶液读数如图所示,所用 标准溶液的体积为
标准溶液的体积为_______________  .
.

(2)下列操作会使所测结果偏高的是_______________ (填字母).
A.滴定前用蒸馏水冲洗锥形瓶
B.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定过程中不慎将数滴碱液滴在锥形瓶外
D.碱式滴定管在滴定前有气泡,滴定后气泡消失
E.读取 体积时,开始仰视读数,滴定结束时俯视读数
体积时,开始仰视读数,滴定结束时俯视读数
(3)用 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液
的盐酸和醋酸溶液,得到滴定过程中溶液 随加入
随加入 溶液体积而变化的两条滴定曲线.
溶液体积而变化的两条滴定曲线.

①滴定醋酸的曲线是_______________ (填“Ⅰ”或“Ⅱ”).
② 和
和 的关系:
的关系:
________  (填“>”、“=”或“<”).
(填“>”、“=”或“<”).
③M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是________________________________ .
(4)氧化还原滴定法是氧化还原反应为基础的一种滴定分析方法,某同学用 的酸性
的酸性 标准溶液滴定某试样中过氧化氢的含量,反应原理为
标准溶液滴定某试样中过氧化氢的含量,反应原理为

①到达滴定终点时的现象为________________________________
②用滴定管量取 试样置于锥形瓶中,重复滴定四次,每次消耗的酸性标准
试样置于锥形瓶中,重复滴定四次,每次消耗的酸性标准 溶液的体积如表所示:测试样中过氧化氢的浓度为
溶液的体积如表所示:测试样中过氧化氢的浓度为________________  .
.
 标准溶液来测定未知物质的量浓度的盐酸时,选择酚酞作指示剂.请回答下列问题:
标准溶液来测定未知物质的量浓度的盐酸时,选择酚酞作指示剂.请回答下列问题:(1)盛装
 标准溶液的仪器名称为
标准溶液的仪器名称为 标准溶液的体积为
标准溶液的体积为 .
.
(2)下列操作会使所测结果偏高的是
A.滴定前用蒸馏水冲洗锥形瓶
B.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定过程中不慎将数滴碱液滴在锥形瓶外
D.碱式滴定管在滴定前有气泡,滴定后气泡消失
E.读取
 体积时,开始仰视读数,滴定结束时俯视读数
体积时,开始仰视读数,滴定结束时俯视读数(3)用
 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液
的盐酸和醋酸溶液,得到滴定过程中溶液 随加入
随加入 溶液体积而变化的两条滴定曲线.
溶液体积而变化的两条滴定曲线.
①滴定醋酸的曲线是
②
 和
和 的关系:
的关系:
 (填“>”、“=”或“<”).
(填“>”、“=”或“<”).③M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是
(4)氧化还原滴定法是氧化还原反应为基础的一种滴定分析方法,某同学用
 的酸性
的酸性 标准溶液滴定某试样中过氧化氢的含量,反应原理为
标准溶液滴定某试样中过氧化氢的含量,反应原理为
①到达滴定终点时的现象为
②用滴定管量取
 试样置于锥形瓶中,重复滴定四次,每次消耗的酸性标准
试样置于锥形瓶中,重复滴定四次,每次消耗的酸性标准 溶液的体积如表所示:测试样中过氧化氢的浓度为
溶液的体积如表所示:测试样中过氧化氢的浓度为 .
.第一次 | 第二次 | 第三次 | 第四次 | |
体积 | 17.04 | 18.00 | 17.00 | 16.96 |
您最近一年使用:0次
2024-02-01更新
|
81次组卷
|
2卷引用:安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题
2020·浙江·模拟预测
4 . 室温下,向20.00mL0.1000mol•L-1盐酸中滴加0.1000mol•L-1NaOH溶液,溶液的pH随NaOH溶液体积的变化如图。已知lg5≈0.7。下列说法不正确的是
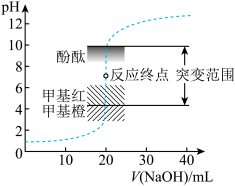
| A.NaOH与盐酸恰好完全反应时,pH=7 |
| B.选择变色范围在pH突变范围内的指示剂,可减小实验误差 |
| C.选择甲基红指示反应终点,误差比甲基橙的大 |
| D.V(NaOH)=30.00mL时,pH≈12.3 |
您最近一年使用:0次
2023-10-21更新
|
877次组卷
|
51卷引用:安徽师范大学附属中学2021-2022学年高二上学期期中考查化学试题
安徽师范大学附属中学2021-2022学年高二上学期期中考查化学试题(已下线)浙江省2020年1月选考(学考)化学试题2020年浙江省高考化学试卷(1月选考)浙江省丽水市松阳县第二中学2019-2020学年高二4月线上教学检测化学试题广东省化州市第一中学2019-2020学年高二4月线上统一测试化学试题江苏省启东中学2020-2021学年高二上学期第一次月考化学试题湖南省怀化市2020-2021学年高二上学期10月联考化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP409】【化学】(已下线)【浙江新东方】99(已下线)小题必刷31 酸碱中和滴定及拓展应用——2021年高考化学一轮复习小题必刷(通用版本)山东省济南市大学城实验高级中学2021届高三1月阶段性考试化学试题(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)广西贵港市覃塘区覃塘高级中学2020-2021学年高二下学期3月月考化学试题浙江省杭州市长征中学2020-2021学年高二下学期第二学期阶段性练习化学试题选择性必修1(SJ)专题3专题培优专练选择性必修1 专题3素养检测(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时41 酸碱中和滴定及拓展应用-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题3.2.2 酸碱中和滴定和pH的计算(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)湖北省麻城市实验高级中学2021-2022学年高二上学期9月月考化学(B卷)试卷内蒙古鄂尔多斯市第一中学2021-2022学年高二上学期第一次月考化学试题(已下线)3.2.2 酸碱中和滴定和pH的计算-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)专题14.水溶液中的离子平衡-十年(2012-2021)高考化学真题分项汇编(浙江专用)浙江省浙北G2(湖州中学、嘉兴一中)2021-2022学年高二上学期期中联考化学试题(已下线)专题25 水的电离和溶液的酸碱性(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)内蒙古霍林郭勒市第一中学2021-2022学年高二上学期期中考试化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题18 酸碱混合图像为载体考查离子平衡-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)专题4 滴定终点专练(已下线)考点27 水的电离和溶液的pH-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第31练 水的电离和溶液的pH-2023年高考化学一轮复习小题多维练(全国通用)陕西省汉中中学2021-2022学年高二上学期第四次月考化学试题(已下线)第24讲 水的电离和溶液的pH(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第22讲 水的电离与溶液的pH(讲)-2023年高考化学一轮复习讲练测(新教材新高考)湖南省株洲市五雅中学2022-2023学年高二上学期11月期中考试化学试题 广西钦州市2022-2023学年高二上学期第2次教学质量监测化学试卷(已下线)题型133 酸碱中和滴定实验及误差分析(已下线)第八章 水溶液中的离子反应与平衡 第48练 酸碱中和反应及中和滴定上海市华东政法大学附属中学2022-2023学年高二下学期期中考试(等级考)化学试题(已下线)第12讲 酸碱中和滴定和氧化还原反应滴定-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)作业(十六) 酸碱中和滴定(已下线)考点27 水的电离与溶液的pH(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第3讲 酸碱中和滴定河北省衡水市第二中学2023-2024学年高三上学期学科素养评估(三调)化学试题【定心卷】3.2.3 酸碱中和滴定随堂练习-人教版2023-2024学年选择性必修1江苏省无锡市锡东高级中学2023-2024学年高二下学期期中考试化学试题天津市和平区2023-2024学年高三下学期第二次质量调查化学试卷
名校
解题方法
5 . 298K时,在20.0mL0.10mol·L-1氨水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10mol·L-1氨水的电离度为1.32%,下列有关叙述不正确 的是
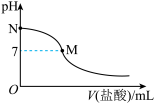
| A.该滴定过程应该选择甲基橙作为指示剂 |
| B.N点处的溶液中12<pH<14 |
C.M点处的溶液中c(NH )=c(Cl-)>c(H+)=c(OH-) )=c(Cl-)>c(H+)=c(OH-) |
D.过M点后的所得溶液中可存在如下离子浓度大小关系:c(Cl-)>c(H+)>c(NH )>c(OH-) )>c(OH-) |
您最近一年使用:0次
2023-09-24更新
|
60次组卷
|
2卷引用:安徽省无为襄安中学2022-2023学年高二下学期开学考试化学试题
名校
解题方法
6 . 常温下,用 的
的 溶液分别滴定
溶液分别滴定 的
的 溶液和
溶液和 的醋酸溶液,滴定曲线如下图。下列有关说法正确的是
的醋酸溶液,滴定曲线如下图。下列有关说法正确的是
 的
的 溶液分别滴定
溶液分别滴定 的
的 溶液和
溶液和 的醋酸溶液,滴定曲线如下图。下列有关说法正确的是
的醋酸溶液,滴定曲线如下图。下列有关说法正确的是
| A.实线表示滴定盐酸的曲线 |
| B.酸的强弱是影响突跃范围大小的重要因素 |
C.ab段的离子反应式是 |
| D.两个体系滴定终点的确定都可用甲基橙作指示剂 |
您最近一年使用:0次
2023-04-16更新
|
384次组卷
|
2卷引用:安徽省池州市第一中学、 池州市第六中学、池州市第八中学2022-2023学年高二下学期4月期中联考化学试题
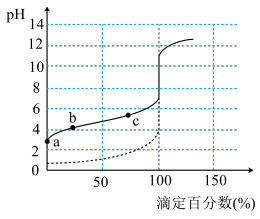
7 . 室温下,用标准液0.01mol·L-1NaOH溶液滴定20.00ml0.01mol·L-1H2C2O4(二元弱酸)溶液,在滴定过程中有关说法正确的是
A.当标准液滴到10.00mL时,溶液中存在[Na+]=[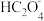 ] ] |
| B.滴定终点时,水电离的氢离子浓度为10-7mol·L-1 |
| C.pH=2的H2C2O4溶液中水电离的[H+]大于0.01mol·L-1NaOH溶液中水电离的[H+] |
D.滴定过程中始终存在[Na+]+[H+]=[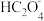 ]+2[ ]+2[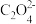 ]+[OH-] ]+[OH-] |
您最近一年使用:0次
2023-04-12更新
|
240次组卷
|
3卷引用:安徽省蚌埠市2022-2023学年高二下学期期末学业水平监测化学试题
解题方法
8 . 用 溶液滴定
溶液滴定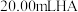 溶液过程中的
溶液过程中的 变化如图所示:
变化如图所示:

下列叙述错误的是
 溶液滴定
溶液滴定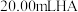 溶液过程中的
溶液过程中的 变化如图所示:
变化如图所示:
下列叙述错误的是
A. 为一元弱酸 为一元弱酸 |
B.初始 溶液中的电离度 溶液中的电离度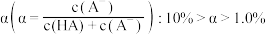 |
C.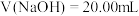 时,混合溶液中有 时,混合溶液中有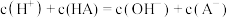 |
D.若使用酚酞作指示剂,会产生系统误差,测得 溶液浓度会偏大 溶液浓度会偏大 |
您最近一年使用:0次
2023-02-24更新
|
1928次组卷
|
7卷引用:安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试理科综合化学试题
安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试理科综合化学试题(已下线)安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试变式题(选择题11-13)(已下线)安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试举一反三(选择题11-13)(已下线)2023四省联考化学学科试卷分析(已下线)素养卷05 电解质溶液中微粒变化图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点09 盘点溶液中的“四大”平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)江西省南昌市2023届高三下学期第三次模拟测试理综化学试题
9 . 三氯化硼(BCl3)用于制备光导纤维和有机硼化物等,其制备原理为B2O3+3C+3Cl2 2BCl3+3CO。某小组据此设计实验制备BCl3并测定其纯度,装置如图所示(部分夹持装置略)。
2BCl3+3CO。某小组据此设计实验制备BCl3并测定其纯度,装置如图所示(部分夹持装置略)。

已知:BCl3的相对分子质量为117.5,熔点为−107.3℃,沸点为12.5℃,极易水解产生H3BO3[或B(OH)3]和HCl。
实验(一):制备BCl3。
(1)水浴R选择_____ (填“热水浴”或“冰水浴”),盛装碱石灰的仪器是_____ (填名称)。
(2)装置F的作用是______ 。
(3)已知装置A中还原产物为Cr3+,其离子方程式为______ 。
实验(二):测定BCl3产品的纯度。
①准确称取wg产品,置于蒸馏水中,完全水解,并配成250mL溶液;
②准确量取25.00mL溶液于锥形瓶中;
③向其中加入V1mLc1 mol∙L−1AgNO3溶液(过量),然后加入3mL硝基苯(常温常压下,密度为1.205 g∙cm−3),振荡;
④向锥形瓶中滴加3滴FeCl3溶液,然后逐滴加入c2 mol∙L−1KSCN标准溶液滴定过量AgNO3溶液,消耗KSCN标准溶液的体积为V2mL。已知:Ksp(AgCl)>Ksp(AgSCN)。
(4)步骤③中加入硝基苯的目的是______ ;滴定终点的现象是______ 。
(5)该产品中BCl3的质量分数为______ %;如果其他操作都正确,仅滴定管没有用KSCN标准溶液润洗,则测得产品中BCl3的质量分数______ (填“偏高”“偏低”或“无影响”)。
 2BCl3+3CO。某小组据此设计实验制备BCl3并测定其纯度,装置如图所示(部分夹持装置略)。
2BCl3+3CO。某小组据此设计实验制备BCl3并测定其纯度,装置如图所示(部分夹持装置略)。
已知:BCl3的相对分子质量为117.5,熔点为−107.3℃,沸点为12.5℃,极易水解产生H3BO3[或B(OH)3]和HCl。
实验(一):制备BCl3。
(1)水浴R选择
(2)装置F的作用是
(3)已知装置A中还原产物为Cr3+,其离子方程式为
实验(二):测定BCl3产品的纯度。
①准确称取wg产品,置于蒸馏水中,完全水解,并配成250mL溶液;
②准确量取25.00mL溶液于锥形瓶中;
③向其中加入V1mLc1 mol∙L−1AgNO3溶液(过量),然后加入3mL硝基苯(常温常压下,密度为1.205 g∙cm−3),振荡;
④向锥形瓶中滴加3滴FeCl3溶液,然后逐滴加入c2 mol∙L−1KSCN标准溶液滴定过量AgNO3溶液,消耗KSCN标准溶液的体积为V2mL。已知:Ksp(AgCl)>Ksp(AgSCN)。
(4)步骤③中加入硝基苯的目的是
(5)该产品中BCl3的质量分数为
您最近一年使用:0次
10 . 青蒿素是高效的抗疟药,为无色针状晶体,易溶于有机溶剂,难溶于水,熔点为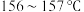 ,温度超过
,温度超过 完全失去药效(已知:乙醚沸点为
完全失去药效(已知:乙醚沸点为 )。从青蒿中提取青蒿素的一种工艺如下:
)。从青蒿中提取青蒿素的一种工艺如下:

索氏提取装置如图所示.实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至装置a,冷凝后滴入滤纸套筒1中,与青蒿粉末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对青蒿粉末的连续萃取。回答下列问题:

(1)装置a的名称为__________ 。
(2)索氏提取的青蒿素位于__________ (填“圆底烧瓶”或“索氏提取器”)中;与常规的萃取相比,索氏提取的优点是__________ 。
(3)提取液蒸馏过程中选用下列哪种装置更好__________ (填字母),原因是__________ 。

(4)粗品提纯的过程可能是__________ (填字母)。
a.加水溶解、蒸发浓缩、冷却结晶
b.加70%的乙醇溶解、水浴加热、冷却结晶、过滤
c.加入乙醚进行萃取分液
(5)青蒿素( )中含有过氧键,与碘化钠反应生成碘单质。为测定产品中青蒿素的纯度,取样品
)中含有过氧键,与碘化钠反应生成碘单质。为测定产品中青蒿素的纯度,取样品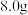 配制成
配制成 溶液,取
溶液,取 加入锥形瓶中,再加入足量的
加入锥形瓶中,再加入足量的 溶液和几滴淀粉溶液,用
溶液和几滴淀粉溶液,用 标准液滴定。(已知:
标准液滴定。(已知: ,M(青蒿素)
,M(青蒿素) )
)
①滴定终点的现象为__________ ;
②三次滴定数据记录如下:
青蒿素的纯度为__________ 。
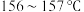 ,温度超过
,温度超过 完全失去药效(已知:乙醚沸点为
完全失去药效(已知:乙醚沸点为 )。从青蒿中提取青蒿素的一种工艺如下:
)。从青蒿中提取青蒿素的一种工艺如下:
索氏提取装置如图所示.实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至装置a,冷凝后滴入滤纸套筒1中,与青蒿粉末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对青蒿粉末的连续萃取。回答下列问题:

(1)装置a的名称为
(2)索氏提取的青蒿素位于
(3)提取液蒸馏过程中选用下列哪种装置更好

(4)粗品提纯的过程可能是
a.加水溶解、蒸发浓缩、冷却结晶
b.加70%的乙醇溶解、水浴加热、冷却结晶、过滤
c.加入乙醚进行萃取分液
(5)青蒿素(
 )中含有过氧键,与碘化钠反应生成碘单质。为测定产品中青蒿素的纯度,取样品
)中含有过氧键,与碘化钠反应生成碘单质。为测定产品中青蒿素的纯度,取样品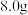 配制成
配制成 溶液,取
溶液,取 加入锥形瓶中,再加入足量的
加入锥形瓶中,再加入足量的 溶液和几滴淀粉溶液,用
溶液和几滴淀粉溶液,用 标准液滴定。(已知:
标准液滴定。(已知: ,M(青蒿素)
,M(青蒿素) )
)①滴定终点的现象为
②三次滴定数据记录如下:
滴定次数 | 待测液体( | 标准液读数( | |
滴定前读数 | 滴定后读数 | ||
第一次 | 25.00 | 1.50 | 41.52 |
第二次 | 25.00 | 3.00 | 42.98 |
第三次 | 25.00 | 4.50 | 41.60 |
青蒿素的纯度为
您最近一年使用:0次