名校
1 . 下表中的物质为化学实验室常用药品:
回答下列问题:
(1)NH4Cl溶液呈弱酸性的原因(用离子方程式表示):_______ ;常温时,0.1mol·L-1的溶液呈碱性的是_______ (填序号)。
(2)标准状况下,5.6LHCl气体完全溶于蒸馏水中,形成2500mL溶液,则该溶液的pH=_______ ;常温时,pH=3的H2SO4溶液中,由水电离出的c水(H+)=_______ mol‧L-1;pH=10的Na2CO3溶液中由水电离出的c水(OH-)=_______ mol‧L-1。
(3)常温时,向CH3COOH溶液中加入少量NH4Cl固体,电离平衡常数Ka_______ (填“增大”“减小”或“不变”。
(4)写出NaHCO3在生活中的一种用途:_______ 。
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 物质 | H2SO4 | CH3COOH | NaHCO3 | Na2CO3 | NH4Cl | NH3·H2O | HCl | NaCl |
(1)NH4Cl溶液呈弱酸性的原因(用离子方程式表示):
(2)标准状况下,5.6LHCl气体完全溶于蒸馏水中,形成2500mL溶液,则该溶液的pH=
(3)常温时,向CH3COOH溶液中加入少量NH4Cl固体,电离平衡常数Ka
(4)写出NaHCO3在生活中的一种用途:
您最近一年使用:0次
2023-02-12更新
|
206次组卷
|
2卷引用:广东省汕头市潮阳区教师发展中心教学研究室 2022-2023学年高二上学期期末质量检测化学试题
2 . NH4Al(SO4)2常作食品加工中的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其原理是_______ (用离子方程式说明)。
(2)配制NH4Al(SO4)2溶液时,通常需加入适量的______ ,减小其水解程度。
(3)相同条件下,0.1mol•L-1NH4Al(SO4)2溶液中的c(NH )
)______ (填“等于”“大于”或“小于”)0.1mol•L-1CH3COONH4溶液中的c(NH )。
)。
(4)下列图像为0.1mol/L的几种电解质溶液的pH随温度变化的曲线。

其中符合0.1mol•L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是______ (填罗马数字),NH4Al(SO4)2溶液的pH随温度变化的原因是______ 。
(5)室温时,向100mL0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图所示。

①试分析图中a、b、c、d四个点,水的电离程度最大的是______ 点。
②在b点,溶液中各离子浓度由大到小的排列顺序是______ 。
(1)NH4Al(SO4)2可作净水剂,其原理是
(2)配制NH4Al(SO4)2溶液时,通常需加入适量的
(3)相同条件下,0.1mol•L-1NH4Al(SO4)2溶液中的c(NH
 )
) )。
)。(4)下列图像为0.1mol/L的几种电解质溶液的pH随温度变化的曲线。

其中符合0.1mol•L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是
(5)室温时,向100mL0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图所示。

①试分析图中a、b、c、d四个点,水的电离程度最大的是
②在b点,溶液中各离子浓度由大到小的排列顺序是
您最近一年使用:0次
2023-04-22更新
|
169次组卷
|
2卷引用:四川省巴中市恩阳区2022-2023学年高二上学期1月期末化学试题
名校
解题方法
3 . 二氧化碳(碳酸)、碳酸氢盐及碳酸盐在生产和生活中有广泛的用途。H2CO3、HClO的电离平衡常数如表:
(1)将少量CO2气体通入NaClO溶液中,反应的离子方程式:______ 。
(2)小苏打(NaHCO3)可用作糕点的发酵剂。NaHCO3溶液是显____ (填“酸”、“碱”或“中”)性,溶液中含碳微粒浓度大小关系为______ 。
(3)泡沫灭火器中存放的物质主要是NaHCO3和A12(SO4)3溶液,使用时,将两物质混合即可产生大量的CO2气体,用平衡移动原理解释灭火原理:_______ 。
(4)25℃时,潮湿的石膏雕像表面会发生反应:CaSO4(s)+CO (aq)
(aq) CaCO3(s)+SO
CaCO3(s)+SO (aq),其平衡常数K=
(aq),其平衡常数K=_______ (填数值)[已知:Ksp(CaSO4)=9.1×10-6,Ksp(CaCO3)=2.8×10-9]。
| 弱酸 | H2CO3 | HClO |
| 电离平衡常数(25℃) | K1=4.2×10-7 K2=4.8×10-11 | K1=3.0×10-8 |
(1)将少量CO2气体通入NaClO溶液中,反应的离子方程式:
(2)小苏打(NaHCO3)可用作糕点的发酵剂。NaHCO3溶液是显
(3)泡沫灭火器中存放的物质主要是NaHCO3和A12(SO4)3溶液,使用时,将两物质混合即可产生大量的CO2气体,用平衡移动原理解释灭火原理:
(4)25℃时,潮湿的石膏雕像表面会发生反应:CaSO4(s)+CO
 (aq)
(aq) CaCO3(s)+SO
CaCO3(s)+SO (aq),其平衡常数K=
(aq),其平衡常数K=
您最近一年使用:0次
解题方法
4 . 砷(As)位于元素周期表的第四行与氮、磷同列。砷有多种化合物,用途广泛。完成下列填空:
(1)写出砷原子核外最外层电子的电子排布式。_______ 。
(2)1个砷的氢化物分子中含_______ 个化学键。
(3)砷化镓(GaAs)和氮化镓(GaN)都是原子间以共价键结合而成的晶体。GaAs熔点为1238°C、GaN熔点为1500°C,GaAs熔点低于GaN的原因是_______ 。
亚砷酸(H3AsO3) 可以用于治疗白血病。25°C,向0.1mol·L-1 H3AsO3溶液中滴加0.1mol·L-1KOH溶液,各种微粒的物质的量分数与溶液pH的关系如图所示。
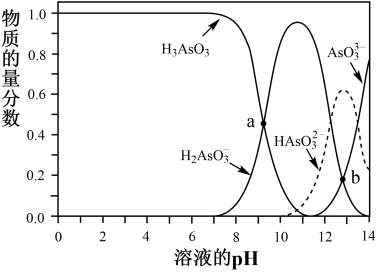
(4)人体血液的pH在7.35~7.45,患者用药后人体中含砷元素的主要微粒是_______ 。
(5)25°C,H2AsO 电离程度小于水解程度,依据是:
电离程度小于水解程度,依据是: _______ 。
(6)以酚酞为指示剂,将KOH溶液滴入H3AsO3溶液中,滴定终点的离子方程式是_______ 。
(7)b点溶液中:c(K+)_______ 2c(HAsO )+4c(AsO
)+4c(AsO ) (选填 “<”“>”或“=”)
) (选填 “<”“>”或“=”)
(1)写出砷原子核外最外层电子的电子排布式。
(2)1个砷的氢化物分子中含
(3)砷化镓(GaAs)和氮化镓(GaN)都是原子间以共价键结合而成的晶体。GaAs熔点为1238°C、GaN熔点为1500°C,GaAs熔点低于GaN的原因是
亚砷酸(H3AsO3) 可以用于治疗白血病。25°C,向0.1mol·L-1 H3AsO3溶液中滴加0.1mol·L-1KOH溶液,各种微粒的物质的量分数与溶液pH的关系如图所示。

(4)人体血液的pH在7.35~7.45,患者用药后人体中含砷元素的主要微粒是
(5)25°C,H2AsO
 电离程度小于水解程度,依据是:
电离程度小于水解程度,依据是: (6)以酚酞为指示剂,将KOH溶液滴入H3AsO3溶液中,滴定终点的离子方程式是
(7)b点溶液中:c(K+)
 )+4c(AsO
)+4c(AsO ) (选填 “<”“>”或“=”)
) (选填 “<”“>”或“=”)
您最近一年使用:0次
名校
解题方法
5 . 钠及其化合物具有广泛的用途。
(1)常温下,浓度均为0.1 mol·L-1的下列五种钠盐溶液的pH如表所示:所给几种钠盐的阴离子,结合氢离子能力最弱的是_______ (填离子符号),根据表中数据判断,将浓度均为0.01 mol·L-1的下列四种酸的溶液分别稀释100倍,pH变化最小的是_______ (填序号)。
A. HCN B. HClO C. CH3COOH D. H2CO3
(2) 浓度均为0.1 mol·L-1的Na2CO3和NaHCO3的混合液,所得溶液中各离子的浓度由大到小的顺序为:_______
(3)已知,常温下几种离子开始沉淀时溶液的pH如表所示:
当向含有相同浓度的Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时,_______ 后沉淀(填离子符号);Ksp[Fe(OH)2]_______ Ksp[Mg(OH)2] (填“>”“=”或“<”)
常温下,要使0.2 mol·L-1的硫酸铜溶液中铜离子沉淀较为完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠溶液使溶液pH=_______ 。(Ksp[Cu(OH)2]=2×10-20)
(1)常温下,浓度均为0.1 mol·L-1的下列五种钠盐溶液的pH如表所示:所给几种钠盐的阴离子,结合氢离子能力最弱的是
A. HCN B. HClO C. CH3COOH D. H2CO3
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
(2) 浓度均为0.1 mol·L-1的Na2CO3和NaHCO3的混合液,所得溶液中各离子的浓度由大到小的顺序为:
(3)已知,常温下几种离子开始沉淀时溶液的pH如表所示:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
当向含有相同浓度的Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时,
常温下,要使0.2 mol·L-1的硫酸铜溶液中铜离子沉淀较为完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠溶液使溶液pH=
您最近一年使用:0次
解题方法
6 . NaCl 是一种基础化工原料,NaOH 也是一种基础化工原料,他们在生产、生活中有广泛的用途。请根据所学知识回答下列问题。
(1)请写出电解饱和食盐水的化学方程式:_______ 。
(2)证明生产产物中的 Cl2 的方法是_______ 。
(3)在电解饱和食盐水所涉及到的物质中,属于强电解质的是______ 。属于弱电解质的是______ 。写出该弱电解质的电离方程式______ 。
(4)电解产生的 Cl2 经过压缩后变成液氯,这是_______ (填“物理”或“化学”)变化,常通过管道进行输送到灌装车间,若管道不慎破裂,常用氨水来检查破裂处,破裂处会观察到大量 NH4Cl 白烟和 N2,请写出化学方程式________ 。
(1)请写出电解饱和食盐水的化学方程式:
(2)证明生产产物中的 Cl2 的方法是
(3)在电解饱和食盐水所涉及到的物质中,属于强电解质的是
(4)电解产生的 Cl2 经过压缩后变成液氯,这是
您最近一年使用:0次
7 . Cl2及其化合物在生产、生活中具有广泛的用途.将氯气溶于水能形成氯气﹣氯水体系.
完成下列填空:
(1)氯原子最外层电子的电子排布式是__ .与电子排布式相比,轨道表示式增加了对核外电子运动状态中__ 描述.
(2)氢、氯、氧三种元素各能形成一种简单阴离子,按离子半径由大到小的顺序排列这些离子__ .
(3)氯气﹣氯水体系中,存在多个含氯元素的平衡关系,请分别用平衡方程式表示:__ .已知HClO的杀菌能力比ClO﹣强,氯处理饮用水时,在夏季的杀菌效果比在冬季差,可能原因是__ (一种原因即可).
(4)在氯水中,下列关系正确的是__ (选填编号).
a c(HClO)+c(ClO﹣)=c(H+)﹣c(OH﹣)
b c(H+)=c(ClO﹣)+c(Cl﹣)+c(OH﹣)
c c(HClO)<c(Cl﹣)
d c(Cl﹣)<c(OH﹣)
(5)ClO2是一种更高效、安全的消毒剂,工业上可用ClO2与水中的MnCl2在常温下反应,生成MnO2和盐酸,以除去水中Mn2+,写出该反应的化学方程式(需配平)__ .有人认为产物MnO2和盐酸会继续反应生成氯气,这种认识对吗?__ (填“对”或“错”),说明理由__ .
完成下列填空:
(1)氯原子最外层电子的电子排布式是
(2)氢、氯、氧三种元素各能形成一种简单阴离子,按离子半径由大到小的顺序排列这些离子
(3)氯气﹣氯水体系中,存在多个含氯元素的平衡关系,请分别用平衡方程式表示:
(4)在氯水中,下列关系正确的是
a c(HClO)+c(ClO﹣)=c(H+)﹣c(OH﹣)
b c(H+)=c(ClO﹣)+c(Cl﹣)+c(OH﹣)
c c(HClO)<c(Cl﹣)
d c(Cl﹣)<c(OH﹣)
(5)ClO2是一种更高效、安全的消毒剂,工业上可用ClO2与水中的MnCl2在常温下反应,生成MnO2和盐酸,以除去水中Mn2+,写出该反应的化学方程式(需配平)
您最近一年使用:0次
8 . 硫及其化合物在工业生产、生活中有重要的用途。
(1)硫原子最外层电子轨道表示式为__________ 。与电子排布式相比,轨道表示式还描述了核外电子运动状态中的______ 和______ 。
(2)S、Cl、N三种元素常见的氢化物中,写出属于非电解质的电子式___________ 。已知PbS与O2在高温时生成铅的氧化物和SO2,化学平衡常数(K)的表达式为:K= 。
。
(3)写出上述反应的化学方程式__________________________ 。在2L高温密闭容器中加入PbS固体和O2,0~5min内气体质量增加1.6g,则5min内SO2的平均反应速率___________________ 。
(4)上述反应达到平衡后,说法正确的是_________ (选填编号)。
a. 速率关系:2v(O2)=3v(SO2)
b. 气体密度随着PbS的质量增加而增大
c. 每生成1.5molO2,同时消耗1molSO2
d. 压缩体积到新平衡,浓度增大的倍数:O2>SO2

(5)向NaOH溶液中缓慢通入SO2至过量,反应过程中某微粒X的物质的量浓度随通入SO2的体积变化如图所示。该微粒X为_________ 。SO2过量时溶液中仍存在微粒X,解释原因。______________________
(1)硫原子最外层电子轨道表示式为
(2)S、Cl、N三种元素常见的氢化物中,写出属于非电解质的电子式
 。
。(3)写出上述反应的化学方程式
(4)上述反应达到平衡后,说法正确的是
a. 速率关系:2v(O2)=3v(SO2)
b. 气体密度随着PbS的质量增加而增大
c. 每生成1.5molO2,同时消耗1molSO2
d. 压缩体积到新平衡,浓度增大的倍数:O2>SO2

(5)向NaOH溶液中缓慢通入SO2至过量,反应过程中某微粒X的物质的量浓度随通入SO2的体积变化如图所示。该微粒X为
您最近一年使用:0次
名校
9 . NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
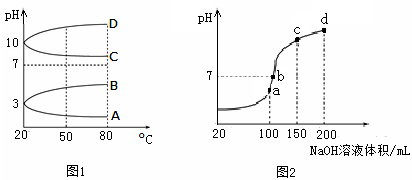
(1)如图1是几种0.1 mol·L-1电解质溶液的pH随温度变化的图象。
①其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是_________ (填写字母);
②20℃时,0.1 mol·L-1NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=______ 。
(2)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是___ 点;在b点,溶液中各离子浓度由大到小的排列顺序是____________ 。

(1)如图1是几种0.1 mol·L-1电解质溶液的pH随温度变化的图象。
①其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是
②20℃时,0.1 mol·L-1NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=
(2)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是
您最近一年使用:0次
10 . 铜、磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)磷的一种化合物叫亚磷酸(H3PO3),已知:
Ⅰ.0.1 mol/L H3PO3溶液的pH=1.7;
Ⅱ.H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ.H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3溶液有黄色沉淀生成.
① 关于H3PO3的说法:
强酸; B.弱酸; C.二元酸;D.三元酸;
E.氧化性酸;F.还原性酸,其中正确的是___________ 。
② 写出H3PO3与少量NaOH溶液反应的离子方程式_________________________ 。
③ Na2HPO3 为__________________ (填“正盐”或“酸式盐”)。
(2)碘化亚铜可作催化剂、饲料添加剂等,是难溶于水的固体.铜可以与氢碘酸发生置换反应得到氢气,试从离子浓度对离子反应方向影响的角度解释此反应能够发生的原因_________________________ ,CuSO4溶液也能使淀粉﹣KI试纸变蓝,用离子方程式说明其原理_____________________________ 。
(3)纳米氧化亚铜是一种具有良好光电效应的材料,工业上制备它的方法之一是:先向KOH溶液中加入一定量的CuSO4溶液,再加入一定量的肼(N2H4),加热并保持反应体系的温度在90℃,反应完全后,分离、洗涤、真空干燥所得到的固体样品.检验反应混合体系内纳米Cu2O已经生成的实验方法的名称是_________ 。
(1)磷的一种化合物叫亚磷酸(H3PO3),已知:
Ⅰ.0.1 mol/L H3PO3溶液的pH=1.7;
Ⅱ.H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ.H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3溶液有黄色沉淀生成.
① 关于H3PO3的说法:
强酸; B.弱酸; C.二元酸;D.三元酸;
E.氧化性酸;F.还原性酸,其中正确的是
② 写出H3PO3与少量NaOH溶液反应的离子方程式
③ Na2HPO3 为
(2)碘化亚铜可作催化剂、饲料添加剂等,是难溶于水的固体.铜可以与氢碘酸发生置换反应得到氢气,试从离子浓度对离子反应方向影响的角度解释此反应能够发生的原因
(3)纳米氧化亚铜是一种具有良好光电效应的材料,工业上制备它的方法之一是:先向KOH溶液中加入一定量的CuSO4溶液,再加入一定量的肼(N2H4),加热并保持反应体系的温度在90℃,反应完全后,分离、洗涤、真空干燥所得到的固体样品.检验反应混合体系内纳米Cu2O已经生成的实验方法的名称是
您最近一年使用:0次



